Acidi e basi 1 Le teorie sugli acidi

Acidi e basi 1. Le teorie sugli acidi e sulle basi 2. Il p. H e la forza degli acidi e delle basi 3. La neutralizzazione: una reazione tra acidi e basi Valitutti, Tifi, Gentile, Esploriamo la chimica © Zanichelli editore 2010 1

1. Le teorie sugli acidi e sulle basi Acidi e basi secondo Arrhenius Gli acidi sono sostanze che, sciolte in acqua, liberano ioni H+ (H 3 O+). Le basi sono sostanze che, sciolte in acqua liberano ioni OH-. HCl(g) H+(aq)+ Cl-(aq) Na. OH(s) Na+(aq)+ OH-(aq) Valitutti, Tifi, Gentile, Esploriamo la chimica © Zanichelli editore 2010 2

1. Le teorie sugli acidi e sulle basi Gli acidi si distinguono in • acidi monoprotici se sono in grado di liberare un solo H+ ; • acidi poliprotici se liberano più ioni H+. Valitutti, Tifi, Gentile, Esploriamo la chimica © Zanichelli editore 2010 3

• Le soluzioni acide sono perciò caratterizzate da un eccesso di ioni H+. • • Le soluzioni basiche sono caratterizzate da un eccesso di ioni OH-. • • Nelle soluzioni neutre le concentrazioni dei due ioni sono uguali.
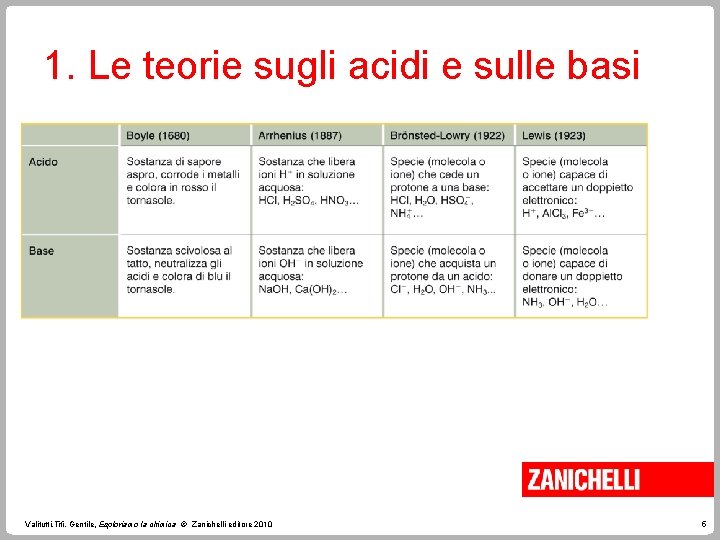
1. Le teorie sugli acidi e sulle basi Valitutti, Tifi, Gentile, Esploriamo la chimica © Zanichelli editore 2010 5
![2. La ionizzazione dell’acqua • Se [H+] > OH- l’ambiente è acido; • Se 2. La ionizzazione dell’acqua • Se [H+] > OH- l’ambiente è acido; • Se](http://slidetodoc.com/presentation_image_h2/8c6787f8f11644c66002569c5b6a2eb1/image-6.jpg)
2. La ionizzazione dell’acqua • Se [H+] > OH- l’ambiente è acido; • Se [H+] = OH- l’ambiente è neutro; • Se [H+] < OH- l’ambiente è basico. Valitutti, Tifi, Gentile, Esploriamo la chimica © Zanichelli editore 2010 6

3. Il p. H e la forza degli acidi e delle basi Il p. H misura il grado di acidità di una sostanza Valitutti, Tifi, Gentile, Esploriamo la chimica © Zanichelli editore 2010 7

3. Il p. H e la forza degli acidi e delle basi Analogamente il p. OH misura il grado di basicità di una sostanza Valitutti, Tifi, Gentile, Esploriamo la chimica © Zanichelli editore 2010 8

3. Il p. H e la forza degli acidi e delle basi Valitutti, Tifi, Gentile, Esploriamo la chimica © Zanichelli editore 2010 9

3. Il p. H e la forza degli acidi e delle basi Gli acidi e le basi, posti in soluzioni acquosa, assumono comportamenti diversi, in base ai quali vengono classificati come forti o deboli. Sono considerati forti quegli acidi e quelle basi che in acqua sono completamente ionizzati. Valitutti, Tifi, Gentile, Esploriamo la chimica © Zanichelli editore 2010 10

3. Il p. H e la forza degli acidi e delle basi Gli acidi si dicono forti se si ionizzano completamente e deboli se non si ionizzano completamente. Valitutti, Tifi, Gentile, Esploriamo la chimica © Zanichelli editore 2010 11

si definiscono acidi forti quegli acidi che in acqua sono completamente dissociati, per i quali è quindi possibile scrivere la seguente reazione: HCl(g) H+(aq)+ Cl-(aq) In soluzione acquosa sono quindi presenti solo gli ioni H+ ed Cl-. Si definiscono basi forti quelle basi che in acqua sono completamente dissociate Na. OH(s) Na+(aq)+ OH-(aq)

3. Il p. H e la forza degli acidi e delle basi Il p. H di una soluzione si misura tramite gli indicatori. Gli indicatori sono sostanze che assumono colorazioni diverse a seconda del p. H della soluzione in cui si trovano. Il punto di passaggio da un colore a un altro è detto punto di viraggio. Valitutti, Tifi, Gentile, Esploriamo la chimica © Zanichelli editore 2010 13

4. La neutralizzazione: una reazione tra acidi e basi Nelle reazioni acido-base di neutralizzazione in cui gli ioni H+ devono uguagliare gli ioni OH–, è più corretto esprimere la concentrazione in normalità e non in molarità. Valitutti, Tifi, Gentile, Esploriamo la chimica © Zanichelli editore 2010 14

4. La neutralizzazione: una reazione tra acidi e basi La neutralizzazione è una reazione fra un acido e una base in quantità equivalenti che porta alla formazione di sale e di acqua, con liberazione di calore. Valitutti, Tifi, Gentile, Esploriamo la chimica © Zanichelli editore 2010 15
- Slides: 15