ACIDI CARBOSSILICI Gli acidi contengono il gruppo carbossile
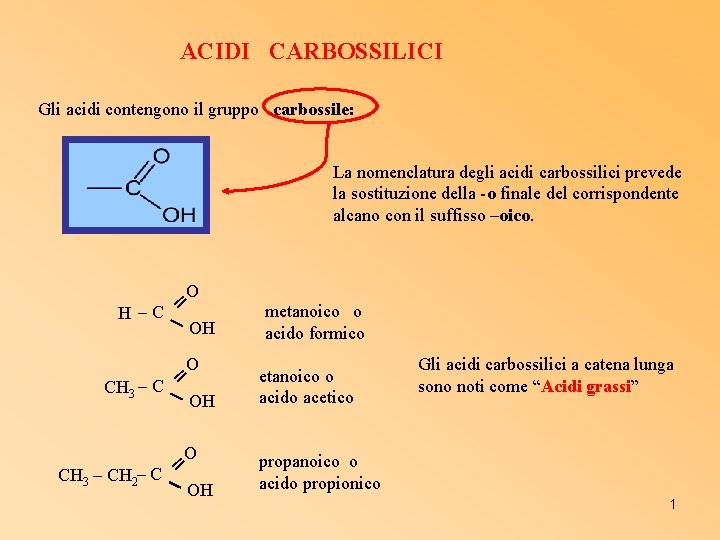
ACIDI CARBOSSILICI Gli acidi contengono il gruppo carbossile: La nomenclatura degli acidi carbossilici prevede la sostituzione della -o finale del corrispondente alcano con il suffisso –oico. O ═ H –C OH O ═ CH 3 – CH 2– C OH metanoico o acido formico etanoico o acido acetico Gli acidi carbossilici a catena lunga sono noti come “Acidi grassi” propanoico o acido propionico 1
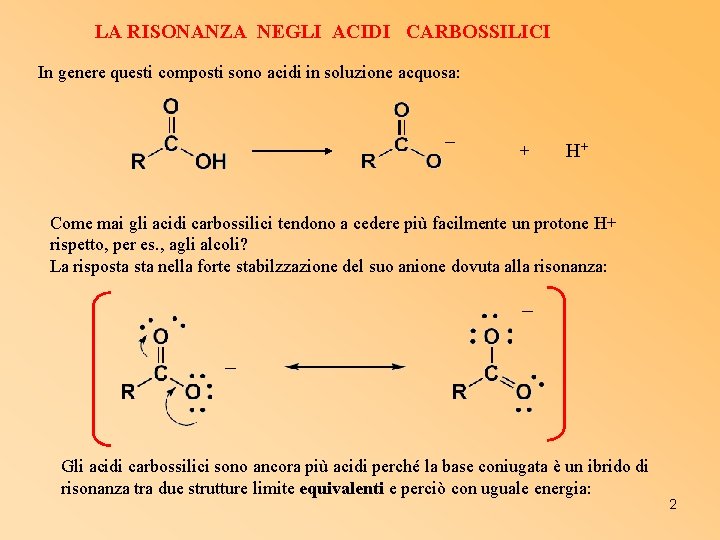
LA RISONANZA NEGLI ACIDI CARBOSSILICI In genere questi composti sono acidi in soluzione acquosa: + H+ Come mai gli acidi carbossilici tendono a cedere più facilmente un protone H+ rispetto, per es. , agli alcoli? La risposta nella forte stabilzzazione del suo anione dovuta alla risonanza: Gli acidi carbossilici sono ancora più acidi perché la base coniugata è un ibrido di risonanza tra due strutture limite equivalenti e perciò con uguale energia: 2
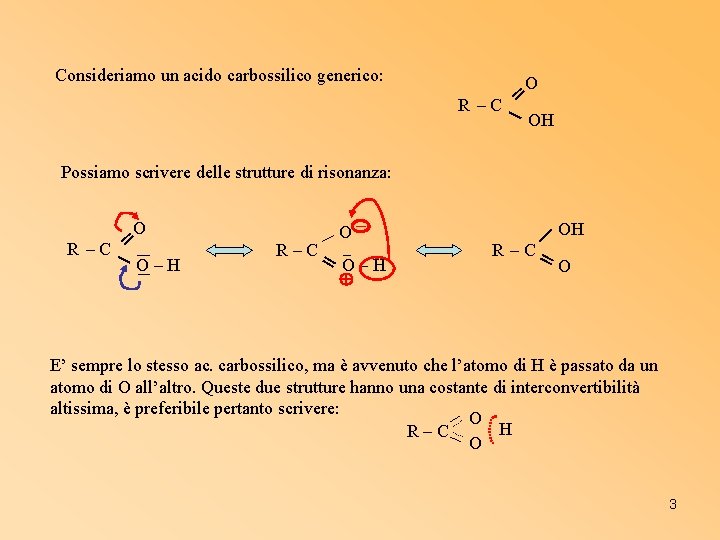
Consideriamo un acido carbossilico generico: O ═ R –C OH Possiamo scrivere delle strutture di risonanza: O ═ R –C O–H R – C═ O─ O–H OH R – C═ O E’ sempre lo stesso ac. carbossilico, ma è avvenuto che l’atomo di H è passato da un atomo di O all’altro. Queste due strutture hanno una costante di interconvertibilità altissima, è preferibile pertanto scrivere: O H R–C O 3

Nel caso dell’anione carbossilato analogamente la carica negativa può saltare da un atomo di O all’altro, per cui scriveremo: O O R–C E’ come se l’atomo di C e quello di O fossero uniti da un legame e mezzo: ─ L’acidità di un acido carbossilico è di media forza, circa 10 volte > rispetto a quella dell’H 2 O: O ═ R –C OH 10 -5 + H 2 O O ═ R –C O─ + H 3 O+ A p. H fisiologico, cioè neutro (intorno a 6) l’acido carbossilico si troverà sotto forma di sale, in quanto si comporta da acido. Se il p. H è < 5 -6 l’acido carbossilico si troverà nella forma indissociata. 4

La formula tipica di un acido carbossilico è: CH 3 – (CH 2)n - COOH Molto importanti sono gli acidi carbossilici a numero pari di atomi di C, da 12 in su (acidi grassi): CH 3 – (CH 2)10 – COOH Acido laurico o dodecanoico CH 3 – (CH 2)12 – COOH Acido miristico o tetradecanoico CH 3 – (CH 2)14 – COOH Acido palmitico o esadecanoico CH 3 – (CH 2)16 – COOH Acido stearico o octadecanoico CH 3 – (CH 2)18 – COOH Acido arachico o ecasanoico Questi acidi sono contenuti in tutti i tipi di olio, in vari rapporti. Gli acidi grassi a numero dispari di atomi di C non sono naturali. Gli acidi grassi sono detti “SATURI” quando presentano solo legami semplici, sono detti “INSATURI” quando nella molecola sono presenti 1 o più doppi legami. 5

L’acido grasso insaturo più importante è l’acido oleico con 18 atomi di C: CH 3 – (CH 2)7 – C 10 H = C 9 H – (CH 2)7 – COOH Il doppio legame si trova tra il C 9 ed il C 10. La catena di atomi di C si conta partendo dal gruppo COOH. Poichè vi è un doppio legame, vi sarà isomeria geometrica. In natura tutti gli acidi grassi sono presenti in forma “cis”. Nel caso dell’acido oleico, il suo isomero trans è l’acido elaidinico. L’acido grasso a 18 atomi di C che contiene 2 doppi legami (diene) entrambi cis, è l’acido linoleico, particolarmente abbondante nell’olio di lino: CH 3 – (CH 2)4 – C 13 H = C 12 H – CH 2 – C 10 H = C 9 H – (CH 2)7 – COOH Nell’olio di lino è presente anche un acido grasso a 18 atomi di C che contiene 3 doppi legami (triene) tutti cis, l’acido linolenico: : CH 3 – (CH 2)4 – C 13 H = C 12 H – CH 2 – C 10 H = C 9 H – CH 2 – C 7 H = C 6 H – (CH 2)4 – COOH NOTA: i doppi legami sono intervallati da atomi di C ibridizzati sp 3 6

NOMENCLATURA DEGLI ACIDI GRASSI Z isomero cis E isomero trans Acido oleico: 9 octa - decenoico cis (Z, 9) 9 octa-decenoico Acido elaidinico: 9 octa - decenoico trans (E, 9) 9 octa-decenoico Acido linoleico: 9, 12 octa - decadienoico cis (Z, 9; Z, 12) 9, 12 octa-diecadienoico Acido linolenico: 6, 9, 12 octa - decatrienoico cis (Z, 6; Z, 9; Z, 12) 6, 9, 12 octa-decatrienoico Man mano che aumenta il n° dei doppi legami, la molecola dell’acido carbossilico tende a ripiegarsi su se stessa, importante caratteristica che troviamo, ad es. , nei lipidi di membrana e che facilita il passaggio dei metaboliti attraverso la membrana stessa. 7
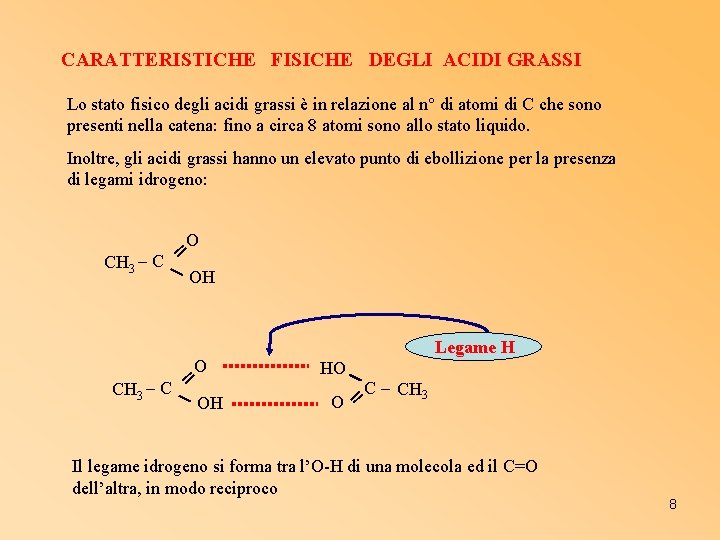
CARATTERISTICHE FISICHE DEGLI ACIDI GRASSI Lo stato fisico degli acidi grassi è in relazione al n° di atomi di C che sono presenti nella catena: fino a circa 8 atomi sono allo stato liquido. Inoltre, gli acidi grassi hanno un elevato punto di ebollizione per la presenza di legami idrogeno: O ═ CH 3 – C OH OH ═O O ═ CH 3 – C OH Legame H C – CH 3 Il legame idrogeno si forma tra l’O-H di una molecola ed il C=O dell’altra, in modo reciproco 8

Gli acidi carbossilici fino ad un certo n° di atomi di C sono solubili in H 2 O. Infatti, in un acido grasso abbiamo due effetti opposti: v COOH effetto idrofilo v Catena carboniosa effetto idrofobo L’uno o l’altro effetto prevalgono a seconda della lunghezza della catena : Ø Fino a 10 -12 atomi di C: solubili Ø Tra 12 e 20 atomi di C: equilibrio dei due effetti, formazione di micelle Ø Oltre i 20 atomi di C: insolubili 9
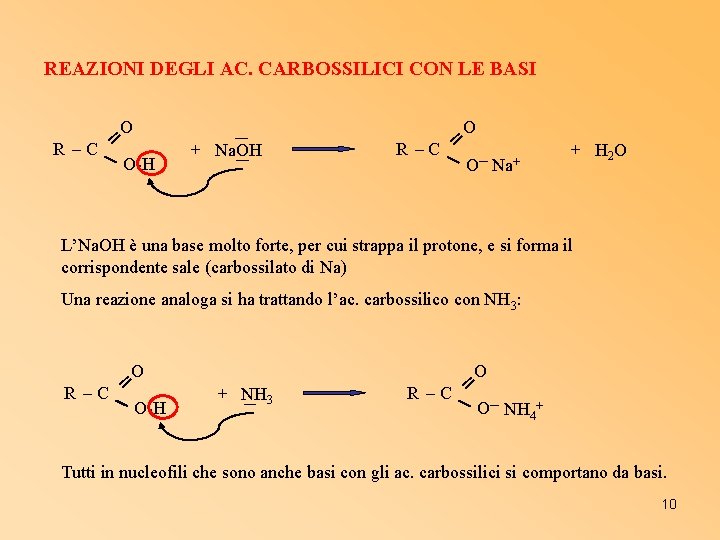
REAZIONI DEGLI AC. CARBOSSILICI CON LE BASI O ═ R –C O-H + Na. OH O ═ R –C O─ Na+ + H 2 O L’Na. OH è una base molto forte, per cui strappa il protone, e si forma il corrispondente sale (carbossilato di Na) Una reazione analoga si ha trattando l’ac. carbossilico con NH 3: O ═ R –C O-H + NH 3 O ═ R –C O─ NH 4+ Tutti in nucleofili che sono anche basi con gli ac. carbossilici si comportano da basi. 10
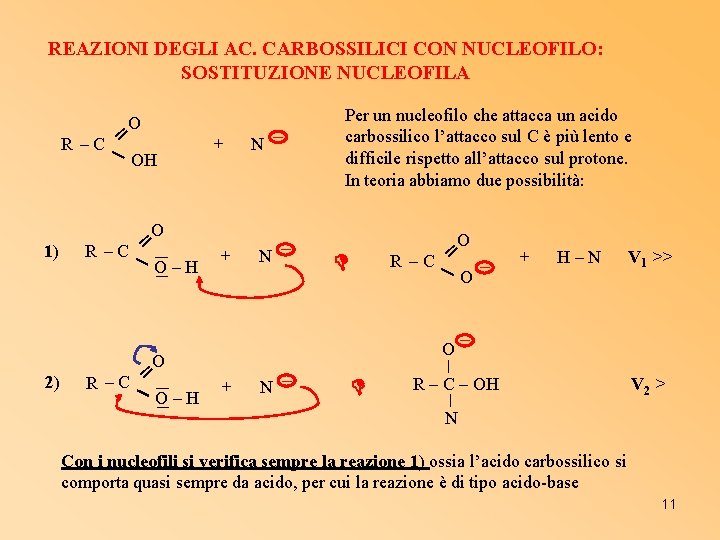
REAZIONI DEGLI AC. CARBOSSILICI CON NUCLEOFILO: SOSTITUZIONE NUCLEOFILA O ═ R –C OH 1) 2) O R –C ═ O–H O ═ R –C O–H + + N N ─ ─ Per un nucleofilo che attacca un acido carbossilico l’attacco sul C è più lento e difficile rispetto all’attacco sul protone. In teoria abbiamo due possibilità: O ═ R –C O O + N ─ ─ + H–N V 1 >> ─ R – C – OH V 2 > N Con i nucleofili si verifica sempre la reazione 1) ossia l’acido carbossilico si comporta quasi sempre da acido, per cui la reazione è di tipo acido-base 11
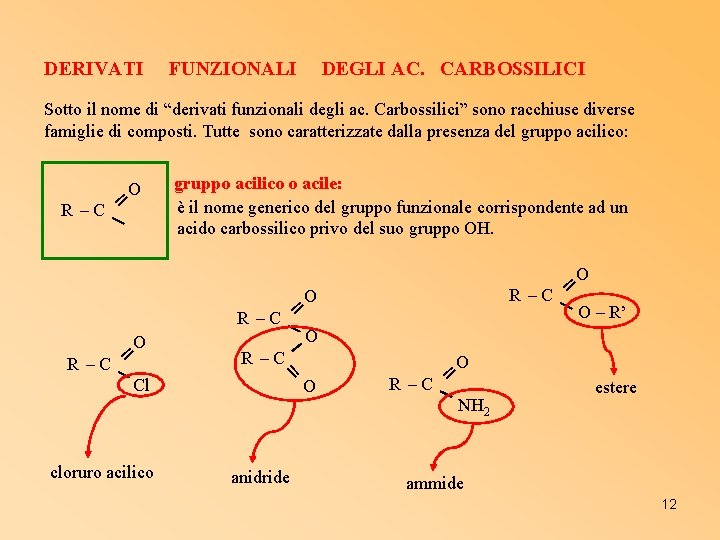
DERIVATI FUNZIONALI DEGLI AC. CARBOSSILICI Sotto il nome di “derivati funzionali degli ac. Carbossilici” sono racchiuse diverse famiglie di composti. Tutte sono caratterizzate dalla presenza del gruppo acilico: O ═ R –C cloruro acilico O ═ R –C O R –C ═ O ═ R –C Cl gruppo acilico o acile: è il nome generico del gruppo funzionale corrispondente ad un acido carbossilico privo del suo gruppo OH. anidride O O R –C ═ O – R’ O R –C ═ NH 2 estere ammide 12

REAZIONI DEGLI AC. CARBOSSILICI CON ALCOL: ESTERIFICAZIONE L’unica reazione possibile tra un acido carbossilico ed un alcol è quella acido-base: O ═ R –C O–H + R’ – O – H O ═ R –C ─ O anione carbossilato + R’ – O – H H alcol protonato L’equilibrio di questa reazione è notevolmente spostato a sinistra, poiché l’alcol protonato è un acido ben più forte dell’acido carbossilico. Se nella reazione aggiungiamo anche solo una goccia di un acido forte, ad es. , H 2 SO 4, avremo invece una reazione molto spedita, detta “Esterificazione”. 13
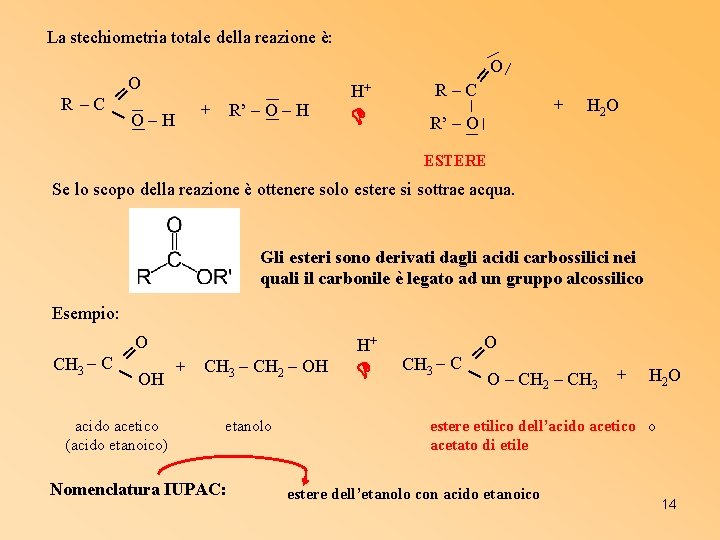
La stechiometria totale della reazione è: ═ O ═ R –C O–H O + R’ – O – H H+ R–C R’ – O + H 2 O ESTERE Se lo scopo della reazione è ottenere solo estere si sottrae acqua. Gli esteri sono derivati dagli acidi carbossilici nei quali il carbonile è legato ad un gruppo alcossilico Esempio: O ═ CH 3 – C + OH acido acetico (acido etanoico) H+ CH 3 – CH 2 – OH etanolo Nomenclatura IUPAC: O ═ CH 3 – C O – CH 2 – CH 3 + H 2 O estere etilico dell’acido acetico o acetato di etile estere dell’etanolo con acido etanoico 14

ALTRE REAZIONI DEGLI ACIDI CARBOSSILICI Abbiamo visto che le reazioni degli acidi carbossilici con nucleofili sono in fondo delle reazioni acido-base, a causa della presenza del protone. Infatti il C risente dell’effetto elettron-attrattore di un O ed elettron-donatore dell’altro O: O ═ R –C O–H Se il protone non ci fosse, potrebbero avvenire altri tipi di reazione. Per togliere il protone trasformo l’acido carbossilico nel corrispondente “cloruro acilico”: cloruro di tionile O R –C ═ O–H + SOCl 2 O ═ R –C Cl + SO 2 + HCl cloruro acilico 15
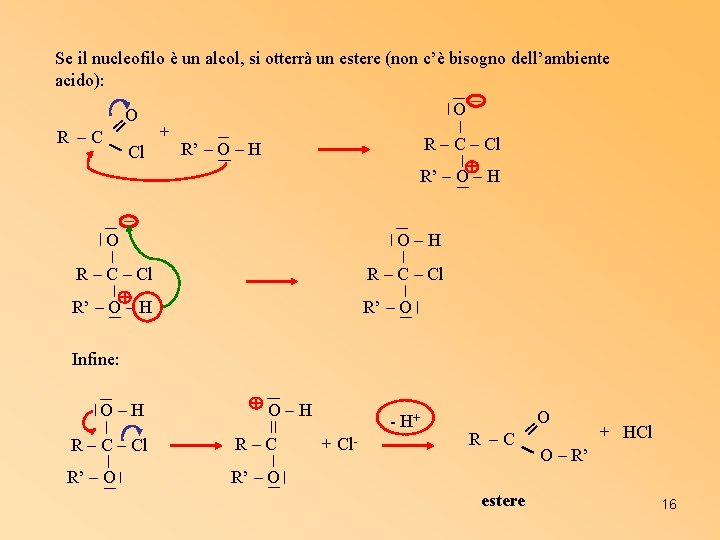
Se il nucleofilo è un alcol, si otterrà un estere (non c’è bisogno dell’ambiente acido): O O ═ + R –C R’ – O – H Cl ─ R – Cl R’ – O – H ─ O O–H R – Cl R’ – O – H R – Cl R’ – O Infine: O–H R – Cl R–C R’ – O - H+ + Cl- O + HCl R –C ═ O – R’ estere 16
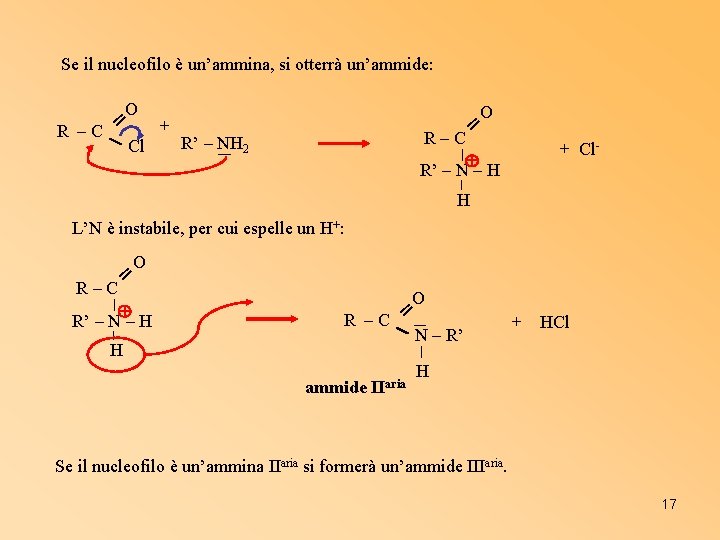
Se il nucleofilo è un’ammina, si otterrà un’ammide: O + R –C ═ R’ – NH 2 Cl O ═ R–C R’ – N – H + Cl- H L’N è instabile, per cui espelle un H+: O ═ R–C R’ – N – H H O ═ R –C N – R’ ammide IIaria + HCl H Se il nucleofilo è un’ammina IIaria si formerà un’ammide IIIaria. 17
- Slides: 17