ACIDES CARBOXYLIQUES ET DERIVES IAcides carboxyliques 1 Dfinition

ACIDES CARBOXYLIQUES ET DERIVES
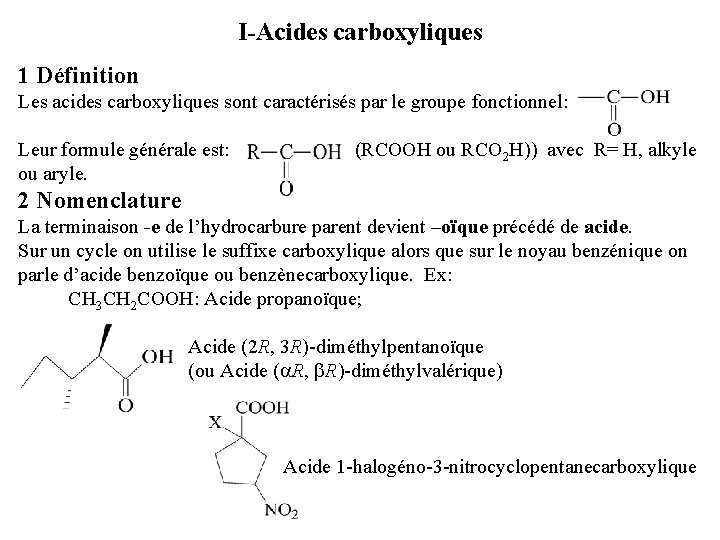
I-Acides carboxyliques 1 Définition Les acides carboxyliques sont caractérisés par le groupe fonctionnel: Leur formule générale est: (RCOOH ou RCO 2 H)) avec R= H, alkyle ou aryle. 2 Nomenclature La terminaison -e de l’hydrocarbure parent devient –oïque précédé de acide. Sur un cycle on utilise le suffixe carboxylique alors que sur le noyau benzénique on parle d’acide benzoïque ou benzènecarboxylique. Ex: CH 3 CH 2 COOH: Acide propanoïque; Acide (2 R, 3 R)-diméthylpentanoïque (ou Acide (a. R, b. R)-diméthylvalérique) Acide 1 -halogéno-3 -nitrocyclopentanecarboxylique
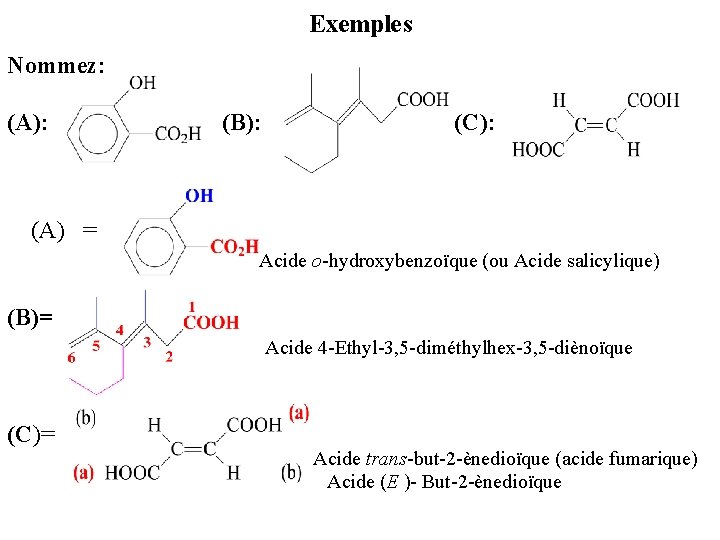
Exemples Nommez: (A): (B): (C): (A) = Acide o-hydroxybenzoïque (ou Acide salicylique) (B)= Acide 4 -Ethyl-3, 5 -diméthylhex-3, 5 -diènoïque (C)= Acide trans-but-2 -ènedioïque (acide fumarique) Acide (E )- But-2 -ènedioïque

Remarques - Noms courants comme acide formique, acide acétique, acide butyrique, acide valérique et acide caproïque (pour des acides de 1 à 6 atomes de carbone). - Les sels adoptent la terminaison –oate à la place de –oïque de l’acide, plus le nom du cation : CH 3 CO 2 Na, éthanoate de sodium. - Groupe prioritaire, il intervient dans le suffixe de l’hydrure fondamental (précédé si nécéssaire de –én ou –yn). Les autres sont cités en préfixe avec leurs positions.

Remarque (suite) La dénomination « carboxylique » peut être aussi employée en série acyclique. La numérotation de la chaine principale, dans ce cas, n’inclut pas le carbone du groupe carboxylique. Pour plus de deux groupes carboxyliques on utilise les suffixes tri, tétra, penta…carboxylique. Dans ce cas les carbones du groupe carboxylique ne font parti de la chaîne principale mais le maximum de groupes lui est rattaché même si elle n’est pas la plus longue.
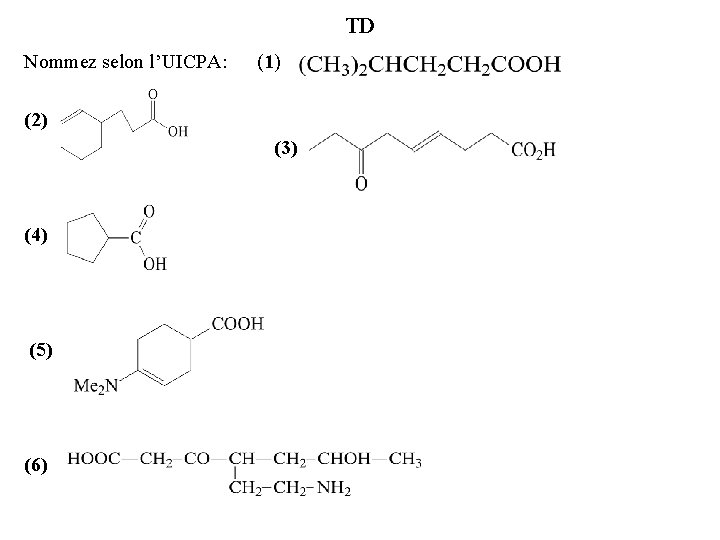
TD Nommez selon l’UICPA: (1) (2) (3) (4) (5) (6)
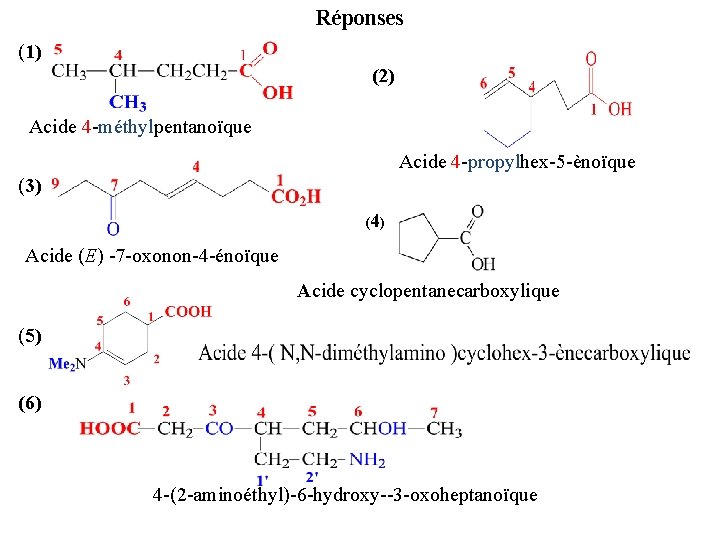
Réponses (1) (2) Acide 4 -méthylpentanoïque Acide 4 -propylhex-5 -ènoïque (3) (4) Acide (E) -7 -oxonon-4 -énoïque Acide cyclopentanecarboxylique (5) (6) 4 -(2 -aminoéthyl)-6 -hydroxy--3 -oxoheptanoïque
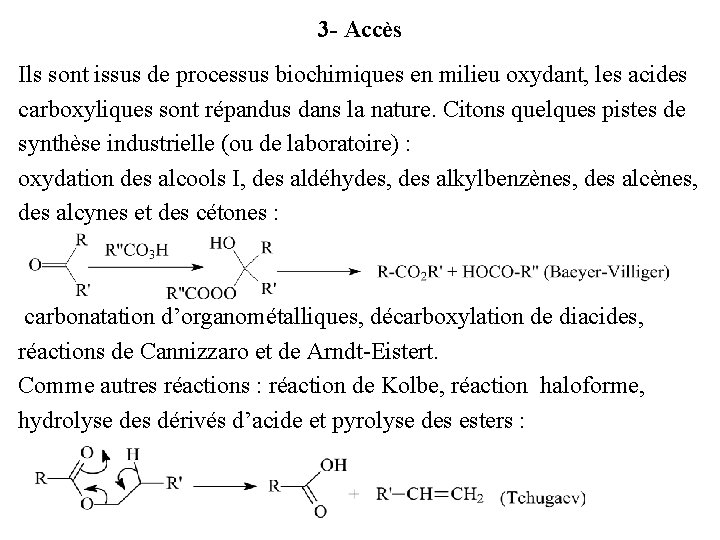
3 - Accès Ils sont issus de processus biochimiques en milieu oxydant, les acides carboxyliques sont répandus dans la nature. Citons quelques pistes de synthèse industrielle (ou de laboratoire) : oxydation des alcools I, des aldéhydes, des alkylbenzènes, des alcènes, des alcynes et des cétones : carbonatation d’organométalliques, décarboxylation de diacides, réactions de Cannizzaro et de Arndt-Eistert. Comme autres réactions : réaction de Kolbe, réaction haloforme, hydrolyse des dérivés d’acide et pyrolyse des esters :

4 -Caractéristiques physiques Ils sont liquides ou solides avec des Teb élevées (liaisons H plus fortes qu’avec les alcools). La solubilité dans l’eau de RCOOH diminue quand R augmente. -Acidité Les substituants électroattracteurs sur R exaltent l’acidité. Cette propriété est utilisée dans la séparation de RCO 2 H par la solution aqueuse de Na. HCO 3 subissant l’acidification par HCl et le test chimique (solubilisation). - Basicité
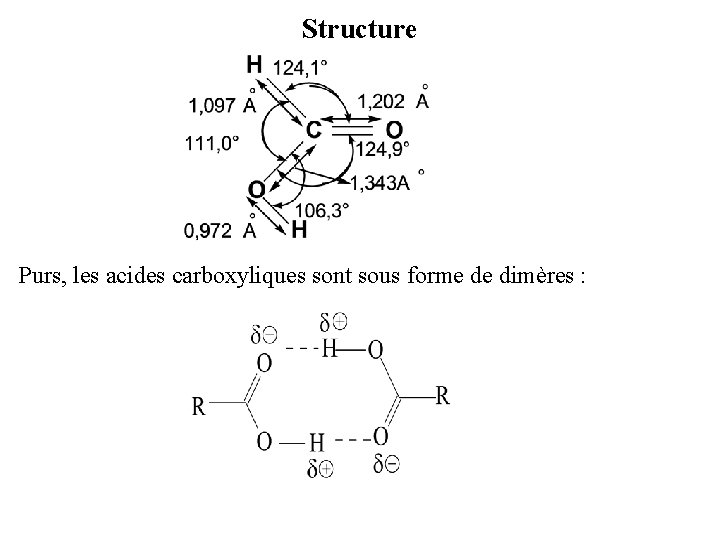
Structure Purs, les acides carboxyliques sont sous forme de dimères :
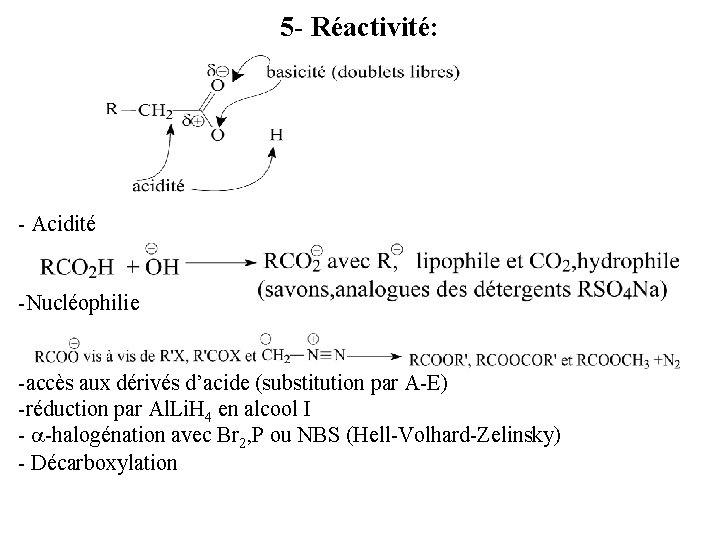
5 - Réactivité: - Acidité -Nucléophilie -accès aux dérivés d’acide (substitution par A-E) -réduction par Al. Li. H 4 en alcool I - a-halogénation avec Br 2, P ou NBS (Hell-Volhard-Zelinsky) - Décarboxylation
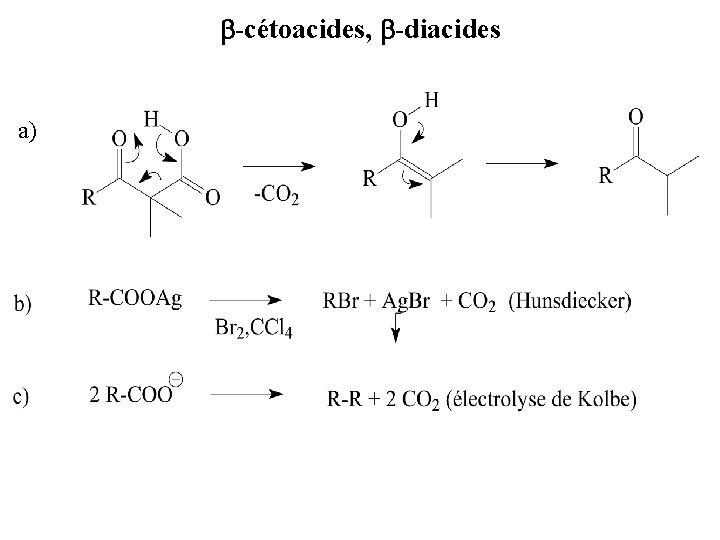
b-cétoacides, b-diacides a)

II-LES DERIVES DES ACIDES CARBOXYLIQUES 1 - Définition Y= X (halogénure d’acyle), OCOR’(anhydride), OR’(ester), NR’R’’(amide) et nitrile. Ces fonctions dérivées régénèrent RCOOH par hydrolyse, ont des H en a labiles et sont siège de substitution par A-E exceptés les nitriles. Si Y= N 3 et NH-NH 2 on a respectivement les azotures d’acyle et hydrazides. acidité/basicité
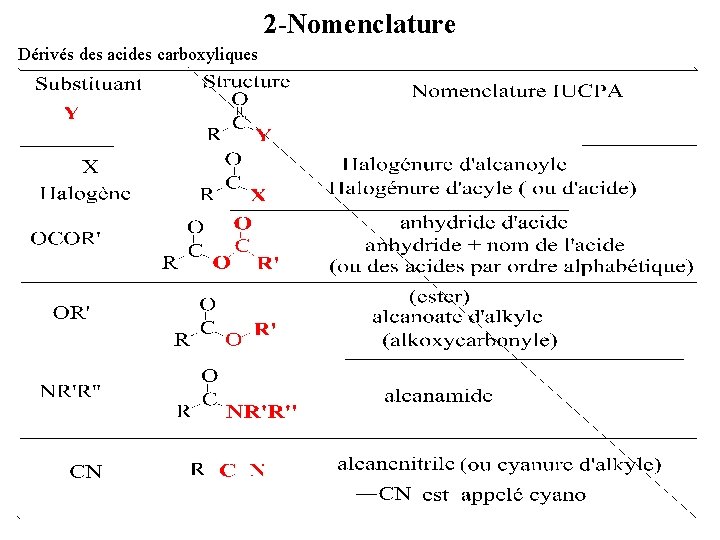
2 -Nomenclature Dérivés des acides carboxyliques
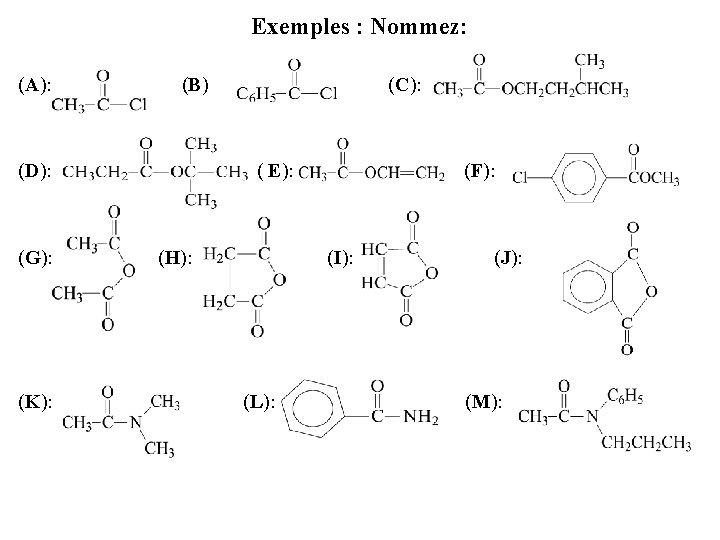
Exemples : Nommez: (A): (B) (C): (D): ( E): (F): (G): (H): (I): (J): (K): (L): (M):
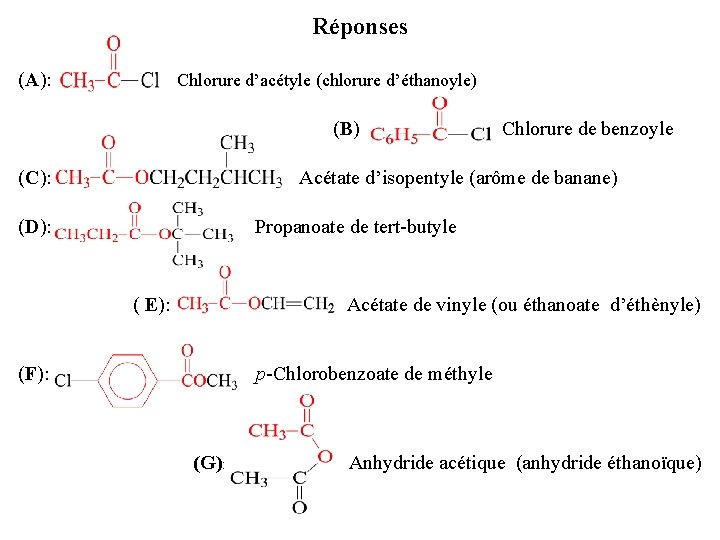
Réponses (A): Chlorure d’acétyle (chlorure d’éthanoyle) (B) Chlorure de benzoyle (C): Acétate d’isopentyle (arôme de banane) (D): Propanoate de tert-butyle ( E): Acétate de vinyle (ou éthanoate d’éthènyle) (F): p-Chlorobenzoate de méthyle (G): Anhydride acétique (anhydride éthanoïque)
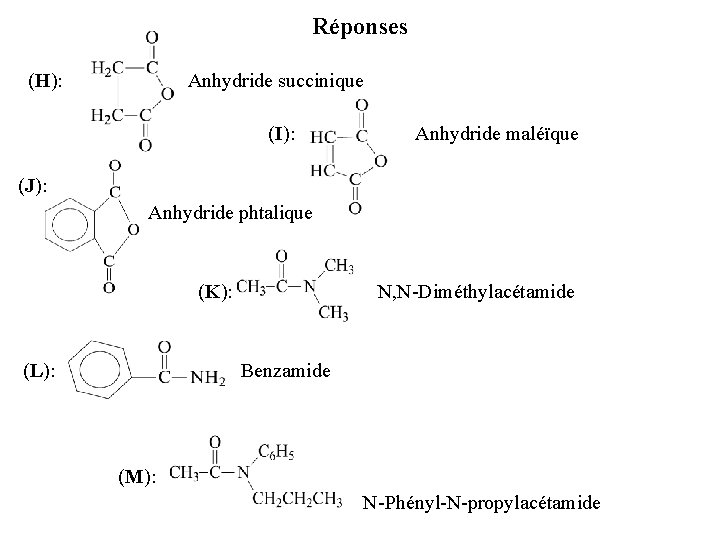
Réponses (H): Anhydride succinique (I): Anhydride maléïque (J): Anhydride phtalique (K): N, N-Diméthylacétamide (L): Benzamide (M): N-Phényl-N-propylacétamide

Remarques: - Les halogénures des acides cycloalcanecarboxyliques sont des halogénures de cycloalcanecarbonyle - L’ester cyclique (lactone) est une oxacycloalcan-2 -one - L’amide cyclique (lactame) est une azacycloalcan-2 -one. - La fonction amide sur un cycle s’exprime en remplaçant la terminaison –carboxylique de l’acide par la terminaison carboxamide

Réactivité Elle suit le caractère meilleur sortant de Y et en meilleure interaction avec CO. L’ordre de réactivité par SN et A-E (inverse de l’ordre de stabilité) est : Les halogénures d’acide : les réactifs nucléophiles variés (OH-, H 2 O, ROH, NH 3) conduisent aux acides et dérivés d’acides. Les organométalliques (R-) et Li. Al. H 4 (H-) permettent d’accéder aux cétones, aux aldéhydes (si Li. Al. H 4 est remplacé par Li. Al. O-t. Bu 3 H ou H 2/Pd) et aux alcools. En présence de cycle benzénique, les SE sont envisageables. Par transposition de Wolff, on peut accéder, via un cétène, à un acide à un carbone de plus (Arndt-Eistert) :
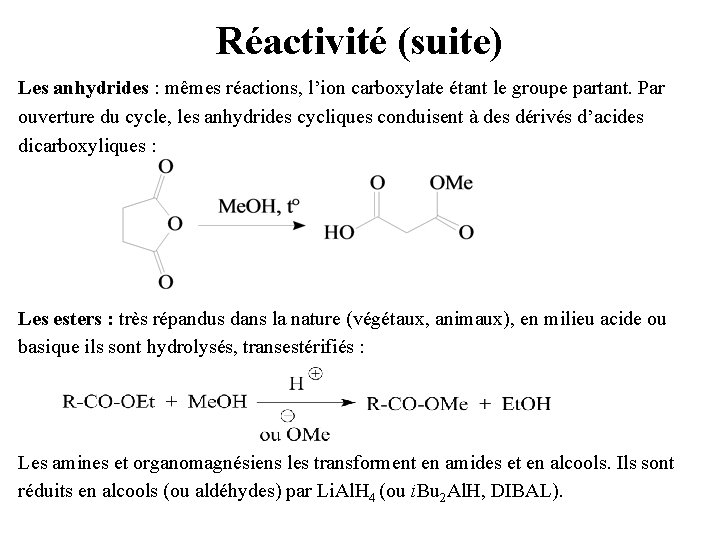
Réactivité (suite) Les anhydrides : mêmes réactions, l’ion carboxylate étant le groupe partant. Par ouverture du cycle, les anhydrides cycliques conduisent à des dérivés d’acides dicarboxyliques : Les esters : très répandus dans la nature (végétaux, animaux), en milieu acide ou basique ils sont hydrolysés, transestérifiés : Les amines et organomagnésiens les transforment en amides et en alcools. Ils sont réduits en alcools (ou aldéhydes) par Li. Al. H 4 (ou i. Bu 2 Al. H, DIBAL).
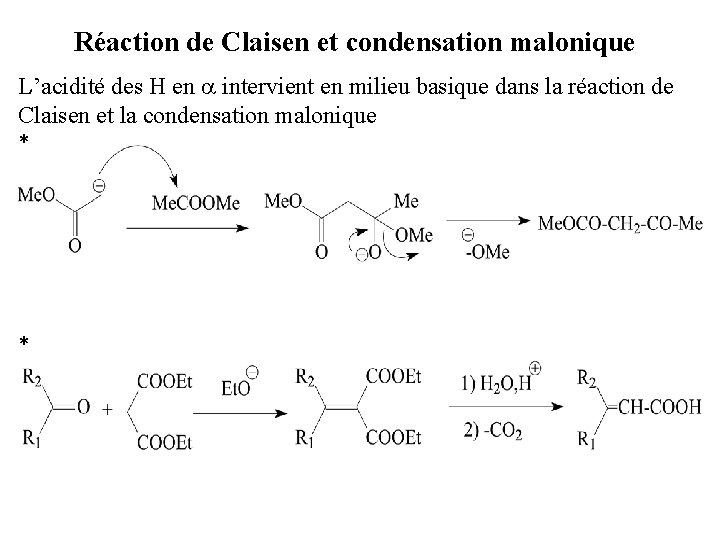
Réaction de Claisen et condensation malonique L’acidité des H en a intervient en milieu basique dans la réaction de Claisen et la condensation malonique * *
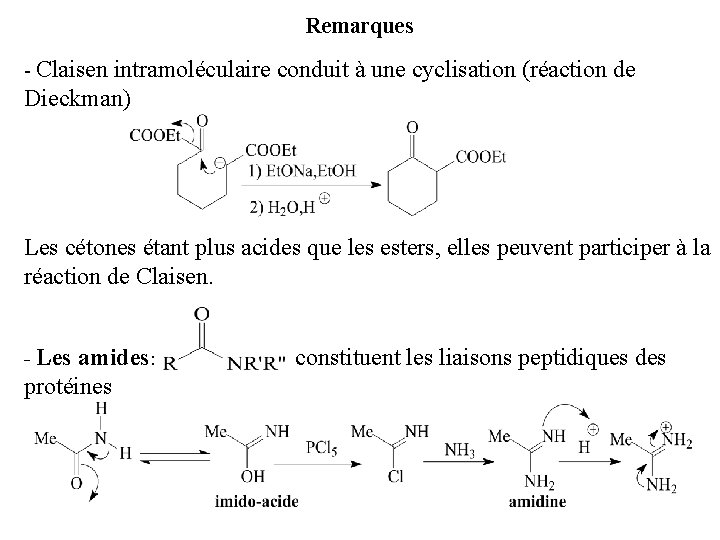
Remarques - Claisen intramoléculaire conduit à une cyclisation (réaction de Dieckman) Les cétones étant plus acides que les esters, elles peuvent participer à la réaction de Claisen. - Les amides: constituent les liaisons peptidiques des protéines

Remarques (suite) La stabilité de l’acide conjugué de l’amidine traduit son caractère de base forte. L’hydrolyse a lieu en milieu acide ou basique à chaud. La réduction par Li. Al. H 4 (ou le DIBAL) conduit à une amine (ou un aldéhyde). En milieu basique, le réarrangement de Hofmann donne une amine. Les amides non substitués ou monosubstitués ont des réactions analogues aux amines. I et II en présence Na. NO 2, HCl. Les imides R-CO-NH-CO-R’ et les acides hydroxamiques R-CO-NH-OH sont des dérivés des amides. - Les nitriles : sont hydrolysés en milieu acide ou basique en acides carboxyliques alors que les organomagnésiens les transforment en cétones (après hydrolyse). La réduction par Li. Al. H 4 (ou H 2/Ni, t°) et le DIBAL conduit respectivement aux amines et aux aldéhydes. En milieu basique, une alkylation est possible :
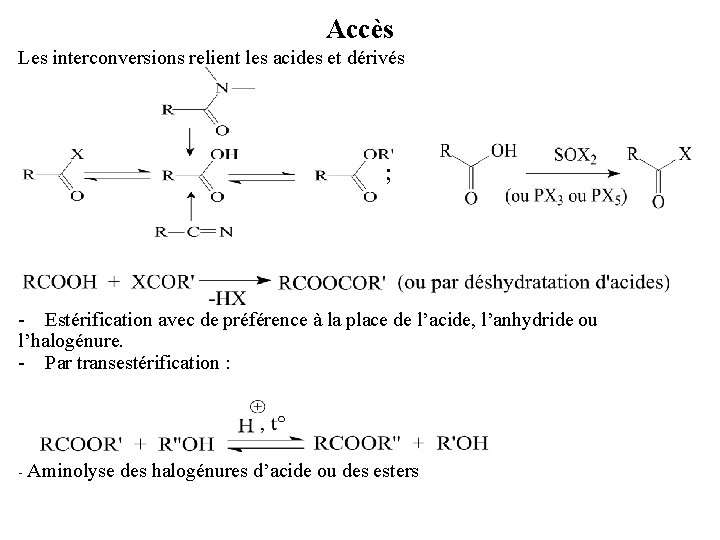
Accès Les interconversions relient les acides et dérivés ; - Estérification avec de préférence à la place de l’acide, l’anhydride ou l’halogénure. - Par transestérification : - Aminolyse des halogénures d’acide ou des esters
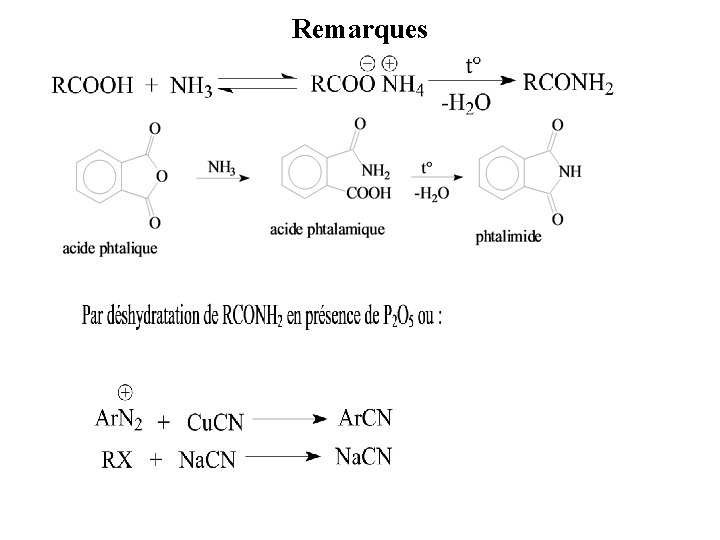
Remarques

Diagnose RCOOH: solution aqueuse tourne au bleu le papier tournesol ; solubles dans une solution aqueuse de Na. OH et de Na. HCO 3 (avec dégagement de CO 2) RCOX: solution aqueuse de Ag. NO 3 donne un précipité de Ag. X RCOOCOR’: soluble à chaud dans la solution aqueuse de Na. OH RCOOR’ et RCONR’R’’: à chaud, dans la solution aqueuse de Na. OH on obtient respectivement RCOO- + R’OH et RCOO- + RNH 2 ou NH 3 RCONH 2: insoluble dans HCl dilué à la différence de RNH 2

Dans la nature et l’industrie L’organisme humain est le siège de transferts d’acyle en permanence : biosynthèse des protéines, graisses, précurseurs des stéroïdes et dégradation de nutriments au niveau cellulaire. Ainsi, en l’absence d’acétylcholine (équivalent biologique des chlorures d’acide), la transmission nerveuse n’est pas assurée: arrêt de toute activité musculaire. On les rencontre dans les phéromones, les fruits, l’urée, les cires… Dans l’industrie pharmaceutique (aspirine, ibuprofène, antibiotiques, vitamine C, …), le textile (nylons, polyesters, polyuréthanes, …), l’agrochimie (fertilisants, insecticides), la cosmétique (savons), les agents de synthèse, les conservateurs et rehausseurs de goût.

TD 1 Donner un nom aux composés suivants : a) C 6 H 5 -CH 2 -COOH b) c) (CH 3 -CH 2 -CH 2 CO)2 O d) CH 3 -CH(CH 3)-CH 2 -CO-NH-CH 2 -CH 3 e) CH 2=CH-CH 2 -O-CO-CH 3 f) C 2 H 5 -O-CO-CO-O-C 2 H 5 Rép a) C 6 H 5 -CH 2 -COOH Phénylacétique b) Acide pent-4 -ynoïque c) (CH 3 -CH 2 -CH 2 CO)2 O Anhydride pentanoïque N-Ethyl-3 -méthylbutanamide ou N-Ethylisovaléramide e) CH 2=CH-CH 2 -O-CO-CH 3 Acétate d’allyle ou (éthanoate de prop-2 -ènyle) f) C 2 H 5 -O-CO-CO-O-C 2 H 5 Ethanedioate de diéthyle (oxalate d’éthyle)
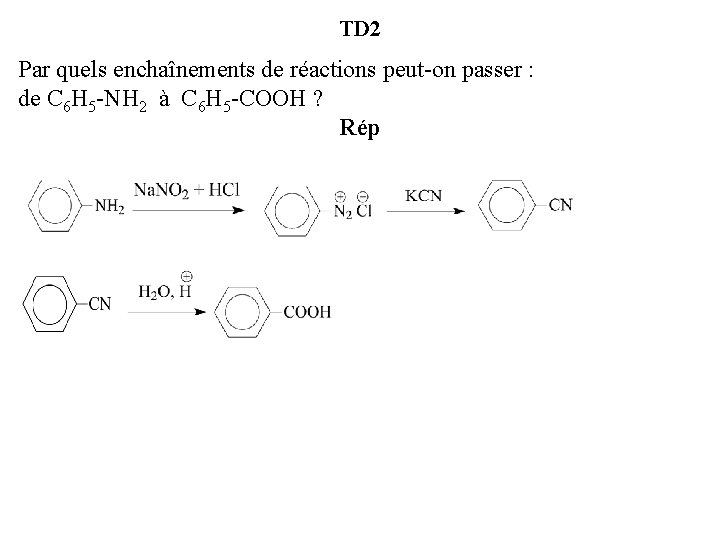
TD 2 Par quels enchaînements de réactions peut-on passer : de C 6 H 5 -NH 2 à C 6 H 5 -COOH ? Rép
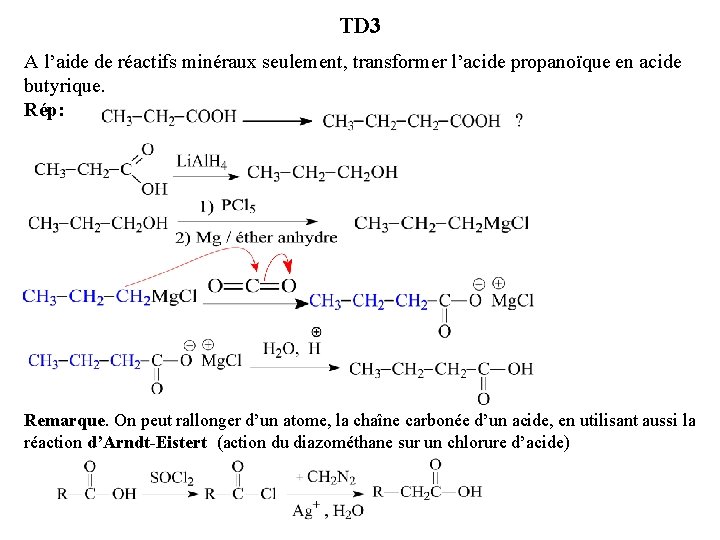
TD 3 A l’aide de réactifs minéraux seulement, transformer l’acide propanoïque en acide butyrique. Rép: Remarque. On peut rallonger d’un atome, la chaîne carbonée d’un acide, en utilisant aussi la réaction d’Arndt-Eistert (action du diazométhane sur un chlorure d’acide)
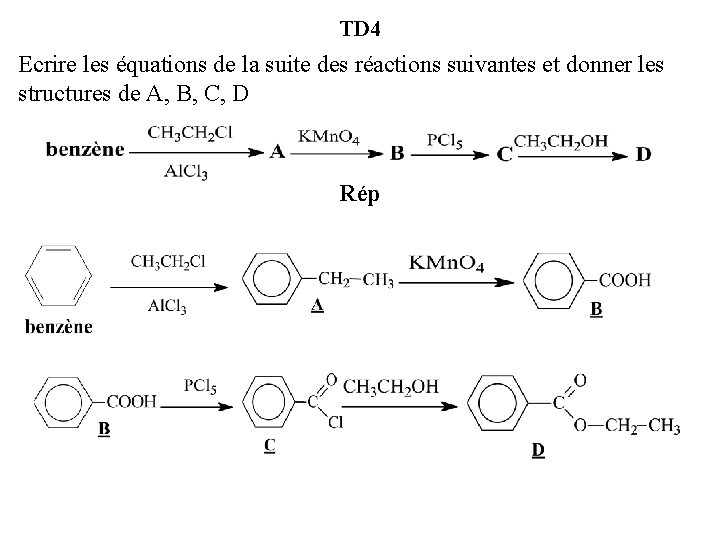
TD 4 Ecrire les équations de la suite des réactions suivantes et donner les structures de A, B, C, D Rép
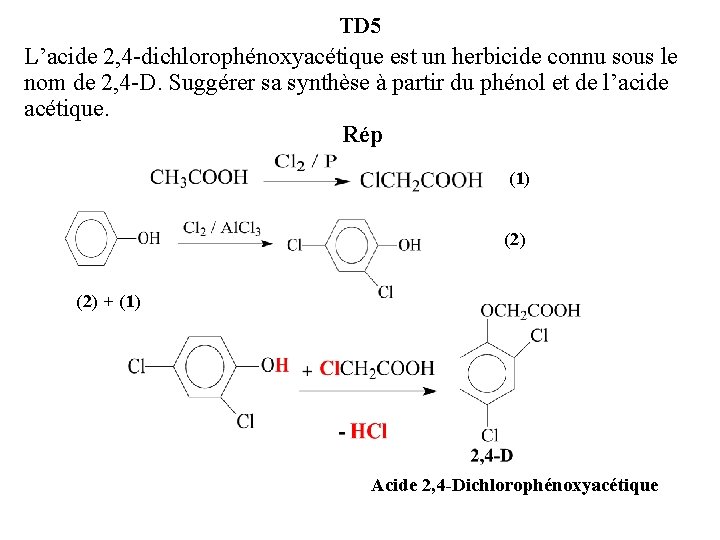
TD 5 L’acide 2, 4 -dichlorophénoxyacétique est un herbicide connu sous le nom de 2, 4 -D. Suggérer sa synthèse à partir du phénol et de l’acide acétique. Rép (1) (2) (2) + (1) Acide 2, 4 -Dichlorophénoxyacétique

EXERCICES 1 - La benzocaïne et la procaïne sont des anesthésiques locaux obtenus à partir du p -nitrotoluène. Identifier les ainsi que les intermédiaires de synthèse (A, B, C, D, A’, B’, et C’) d’après les suites réactionnelles ci-dessous : 2 - Identifier les produits de A à D de la suite réactionnelle : 3 - Comment préparer du 2, 2 -diméthylpropanenitrile à partir de l’acide 2, 2 -diméthylpropanoïque. Que se passera-t-il en essayant
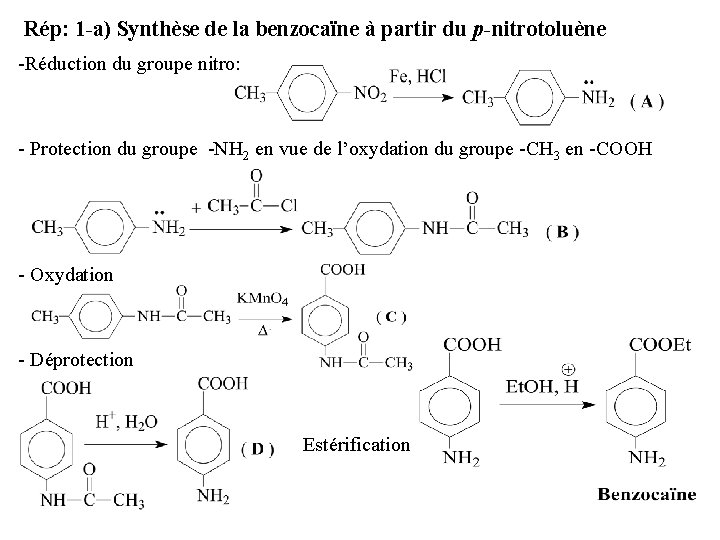
Rép: 1 -a) Synthèse de la benzocaïne à partir du p-nitrotoluène -Réduction du groupe nitro: - Protection du groupe -NH 2 en vue de l’oxydation du groupe -CH 3 en -COOH - Oxydation - Déprotection Estérification
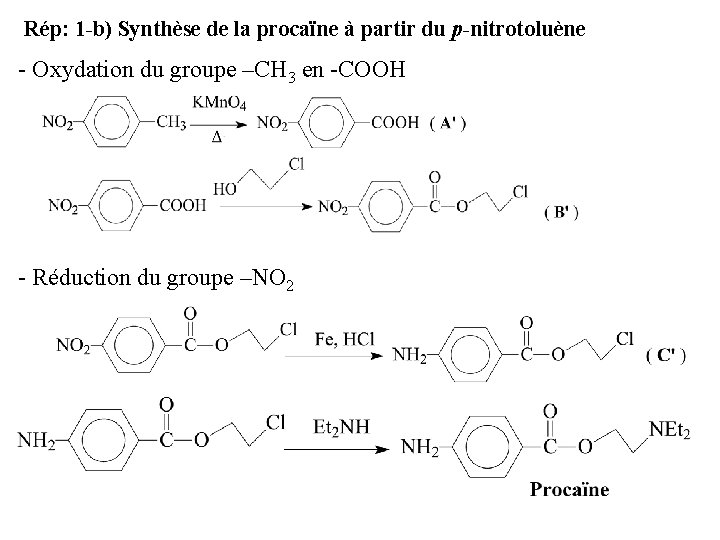
Rép: 1 -b) Synthèse de la procaïne à partir du p-nitrotoluène - Oxydation du groupe –CH 3 en -COOH - Réduction du groupe –NO 2
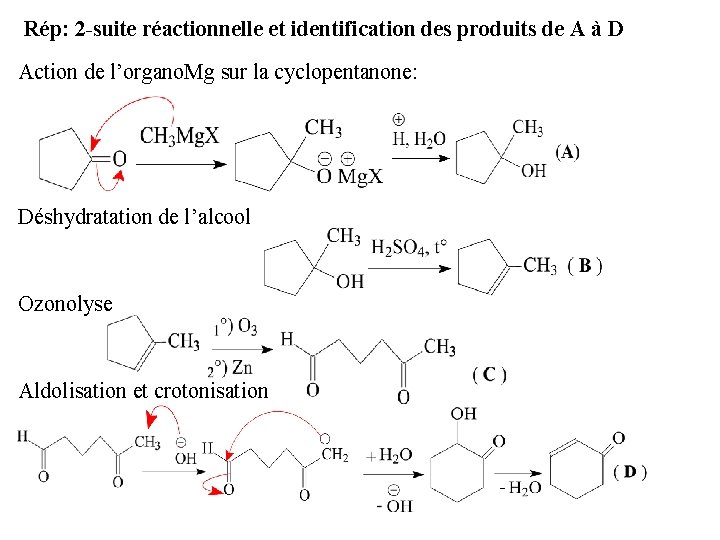
Rép: 2 -suite réactionnelle et identification des produits de A à D Action de l’organo. Mg sur la cyclopentanone: Déshydratation de l’alcool Ozonolyse Aldolisation et crotonisation
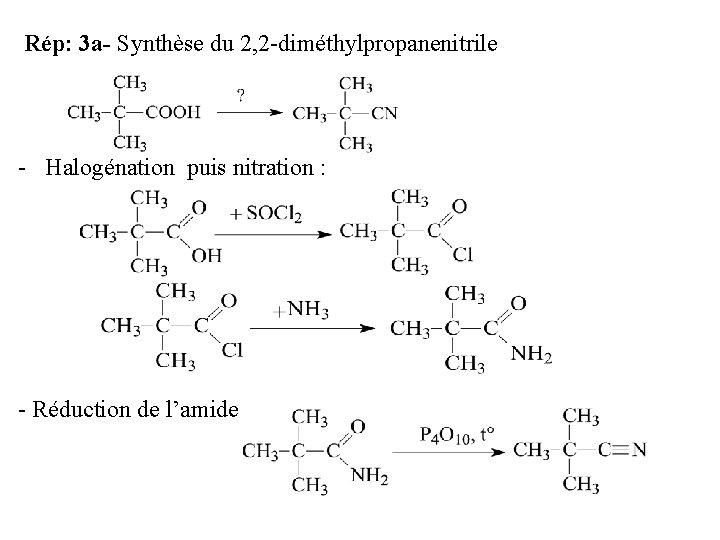
Rép: 3 a- Synthèse du 2, 2 -diméthylpropanenitrile - Halogénation puis nitration : - Réduction de l’amide
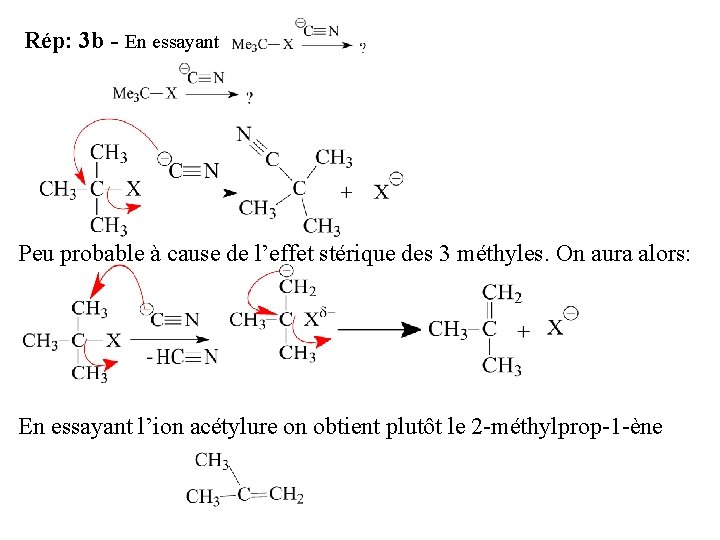
Rép: 3 b - En essayant Peu probable à cause de l’effet stérique des 3 méthyles. On aura alors: En essayant l’ion acétylure on obtient plutôt le 2 -méthylprop-1 -ène

Rép

FIN
- Slides: 40