Aceros Inoxidables 67 50 Materiales Ferrosos y sus

Aceros Inoxidables 67. 50 Materiales Ferrosos y sus aplicaciones

Temas a Desarrollar Origen. n Composición. n Clasificación. n Tipos de corrosión. n Criterios de selección. n

Origen La de aceros inoxidables esinvestigaciones muy amplia y especializada, donde cada aleación fue diseñada para Enfamilia 1904 Leon Guillet, publica sus sobre aleaciones Hierro-Cromo. Desde allí, varios una necesidad especifica de. Alemania la industria. investigadores en Francia, e inglaterra siguieron trabajando en esos estudios. ¿Pero quéagosto se necesita paraentransformar al hierro en acero inoxidable? . El 20 de de 1912, los laboratorios Brown Firth de Sheffield, Harry Brearley intentaba encontrar Cromo una solución a la corrosión y desgaste de los cañones de armas de fuego y obtuvo, entre muchas, una aleación que contenía 0, 24% C y 12, 8% Cr. Para analizarla, una al probeta se dispuso atacarla con ácido nítrico resistencia para observar micro La aleación debecortó contener menosy 10, 5% de Cra para tener una adecuada a lasu oxidación. estructura. para mejor su sorpresa, material resultó ser inmune todos los existe reactivos que utilizó. Cuanto mas. Pero Cr tenga, será suelresistencia a la corrosión. Sinaembargo, un límite superior a la cantidad de Cr que el hierro puede retener. Debido a esto, se necesitan aleantes adicionales que Como él resistir era de tipos Sheffield, pensó que a este nuevo material podría aplicarlo en un producto que en esa permitan específicos de corrosión. región era típico, los cuchillos, ya que en esa época, los cubiertos de mesa debían pulirse cada vez antes de usarlos porque sedel oxidaban. Cuando el Cr supera 10, 5%, la superficie del material cambia de una película activa a pasiva. Esto Fue así que con ayuda del fabricante desarrollaron primero “Rustless mas es, mientras que una capa activa crecelocal, en forma continua lo enque contacto conseelllamó medio corrosivo. Steel” hastayque acuñaron el actual definitivo nombre Steel”. y deja de crecer, aislando al metal base eladelante metal base se consume pory completo, la capa “Stainless pasiva se forma del medio agresivo e impidiendo que el oxigeno entre en contacto con éste. En forma independiente, acerías Krupp Alemania investigaban sobre aleaciones resistentes a laes Esta capa es muy fina, dellas orden de 10 a 100 deátomos se compone principalmente de óxido de Cr, que corrosión, pero en su ycaso añadiendo níquel en gran cantidad, llegando a obtener así un material mucho un compuesto estable no reactivo en un amplio espectro de condiciones. mas resistente a los ácidos, mas blando y fácil de conformar que el desarrollo inglés. Sin embargo, el Cr es también su talón de Aquiles y el Ion Cloro su Némesis. Esto se debe a que el ión Deseestos dos inventos, luegoformando las dos primeras la que serieson 300 solubles y la serie 400. Cl combina con el Cr se de derivaron la capa pasiva clorurosfamilias, de cromo y se desprenden dejando expuesto al hierro base para que reaccione formando oxidos activos. El todas establecimiento definitivo llegó encomo 1924, elcuando Hatfield inventó la aleación 18 -8, la mas De maneras, existen aleantes Mo que. W. H. minimizan esta reacción. utilizada en el mundo hasta hoy.
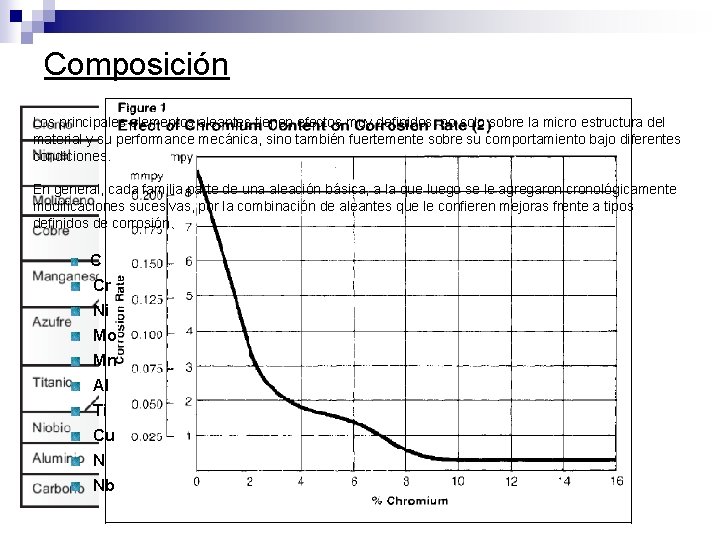
Composición Los principales elementos aleantes tienen efectos muy definidos, no solo sobre la micro estructura del material y su performance mecánica, sino también fuertemente sobre su comportamiento bajo diferentes condiciones. En general, cada familia parte de una aleación básica, a la que luego se le agregaron cronológicamente modificaciones sucesivas, por la combinación de aleantes que le confieren mejoras frente a tipos definidos de corrosión. C Cr Ni Mo Mn Al Ti Cu N Nb
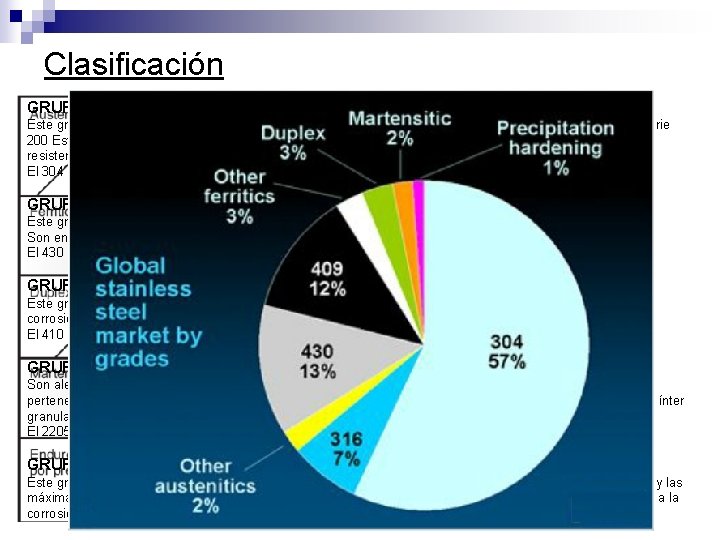
Clasificación GRUPO AUSTENITICO Este grupo contiene Cr y Ni y se identifica como serie 300. Los que reemplazan el Ni por N y Mn son de la serie 200 Estas series tienen características en común. Como ser endurecibles por deformación en frió, tienen una resistencia a la corrosión general excelente, y una ductilidad muy alta. El 304 (18 Cr-8 Ni) y el 316 (16 Cr-10 Ni-2 Mo son los mas utilizados de este grupo. GRUPO FERRITICO Este grupo contiene solo Cr y C limitado, se identifican como serie 400. Son endurecibles por deformación en frío. Su resistencia y ductilidad son intermedias. El 430 (16 Cr) es el mas utilizado de la serie. GRUPO MARTENSITICO Este grupo contiene Cr y alto C y también pertenecen a la serie 400. Son moderadamente resistentes a la corrosión pero logran muy alta dureza y resistencia. El 410 (11, 5 Cr) es el mas utilizado. GRUPO DÚPLEX Son aleaciones con Cr y Mo con suficiente Ni y N para lograr el balance entre Ferrita y Austenita. Algunos pertenecen a la serie 300. El resultado es una combinación de ductilidad, resistencia al picado, a la corrosión ínter granular y SSCC. El 2205 (22 Cr-5 Ni-3 Mo) es el mas conocido. GRUPO ENDURECIBLE POR PRECIPITADO Este grupo contiene Al, Cu y Ti para generar alta resistencia por TT. Tiene alta ductilidad en estado recocido y las máximas resistencias de todos los inoxidables luego del TT, pero manteniendo a la vez excelente resistencia a la corrosión. El 17 -4 PH (17 Cr-4 Ni) es el mas utilizado.
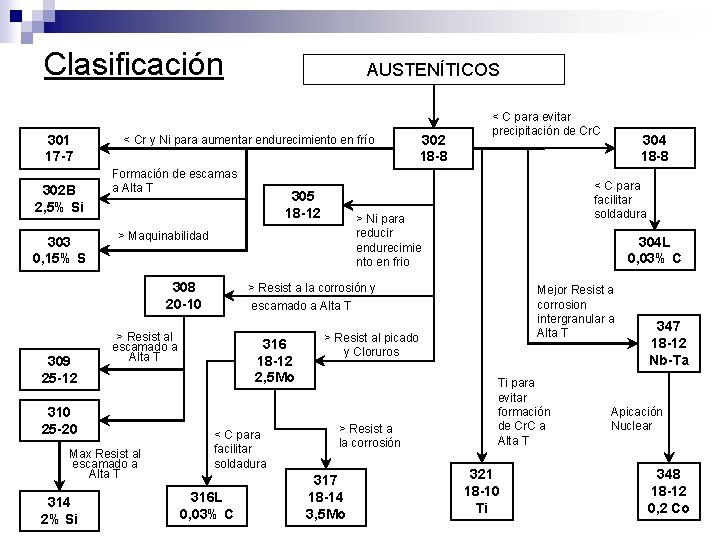
Clasificación 301 17 -7 302 B 2, 5% Si 303 0, 15% S < Cr y Ni para aumentar endurecimiento en frío Formación de escamas a Alta T Max Resist al escamado a Alta T 302 18 -8 < C para evitar precipitación de Cr. C 316 18 -12 2, 5 Mo < C para facilitar soldadura > Ni para reducir endurecimie nto en frio 304 L 0, 03% C 316 L 0, 03% C Mejor Resist a corrosion intergranular a Alta T > Resist al picado y Cloruros > Resist a la corrosión 317 18 -14 3, 5 Mo 304 18 -8 < C para facilitar soldadura > Resist a la corrosión y escamado a Alta T > Resist al escamado a Alta T 310 25 -20 314 2% Si 305 18 -12 > Maquinabilidad 308 20 -10 309 25 -12 AUSTENÍTICOS Ti para evitar formación de Cr. C a Alta T 321 18 -10 Ti 347 18 -12 Nb-Ta Apicación Nuclear 348 18 -12 0, 2 Co
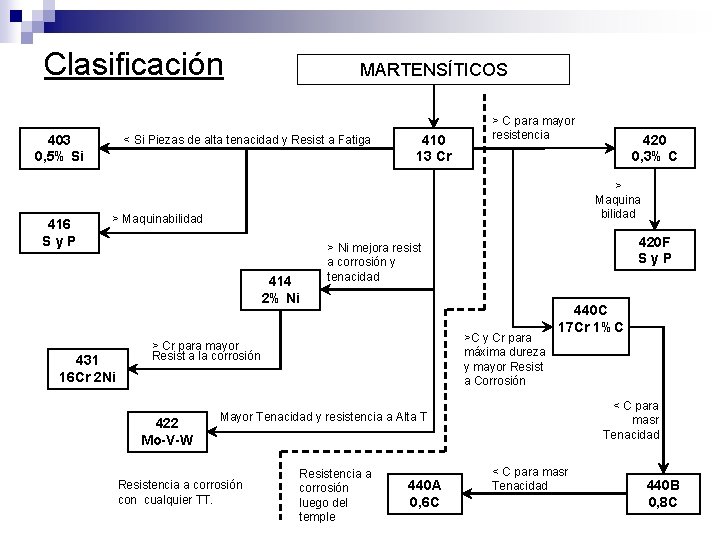
Clasificación 403 0, 5% Si 416 Sy. P MARTENSÍTICOS < Si Piezas de alta tenacidad y Resist a Fatiga 410 13 Cr > C para mayor resistencia > Maquina bilidad > Maquinabilidad 414 2% Ni 431 16 Cr 2 Ni 420 F Sy. P > Ni mejora resist a corrosión y tenacidad >C y Cr para máxima dureza y mayor Resist a Corrosión > Cr para mayor Resist a la corrosión 422 Mo-V-W 420 0, 3% C 440 C 17 Cr 1%C < C para masr Tenacidad Mayor Tenacidad y resistencia a Alta T Resistencia a corrosión con cualquier TT. Resistencia a corrosión luego del temple 440 A 0, 6 C < C para masr Tenacidad 440 B 0, 8 C
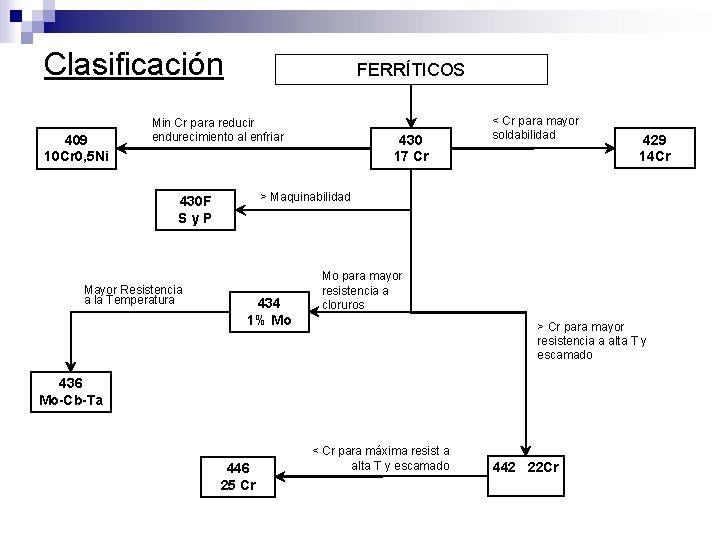
Clasificación 409 10 Cr 0, 5 Ni FERRÍTICOS Min Cr para reducir endurecimiento al enfriar 429 14 Cr > Maquinabilidad 430 F Sy. P Mayor Resistencia a la Temperatura 430 17 Cr < Cr para mayor soldabilidad 434 1% Mo Mo para mayor resistencia a cloruros > Cr para mayor resistencia a alta T y escamado 436 Mo-Cb-Ta 446 25 Cr < Cr para máxima resist a alta T y escamado 442 22 Cr
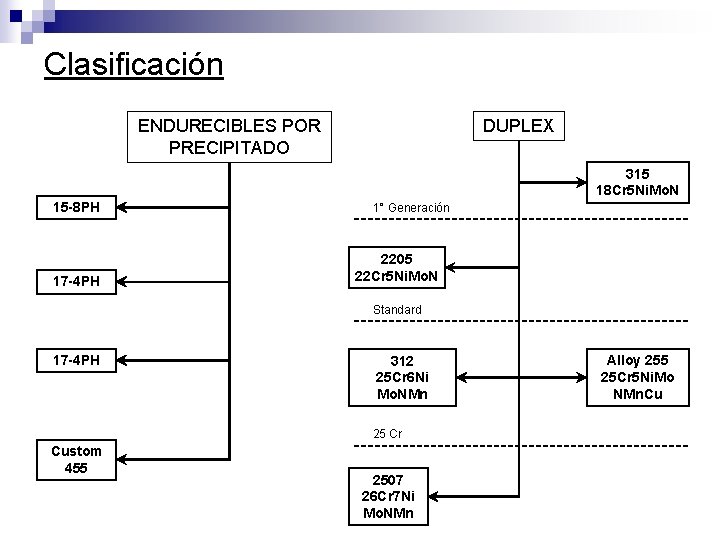
Clasificación DUPLEX ENDURECIBLES POR PRECIPITADO 315 18 Cr 5 Ni. Mo. N 15 -8 PH 17 -4 PH 1° Generación 2205 22 Cr 5 Ni. Mo. N Standard 17 -4 PH 312 25 Cr 6 Ni Mo. NMn 25 Cr Custom 455 2507 26 Cr 7 Ni Mo. NMn Alloy 255 25 Cr 5 Ni. Mo NMn. Cu

Clasificación PROPIEDADES FERRÍTICOS AUSTENITICOS DUPLEX ENDURECIBLES MARTENSÍTICOS POR PRECIPITADO v Ductilidad Gran Ductilidad. intermedia. Intermedia. Alta baja. previo al TT. v Tenacidad Endurecibles Resistencia Alta. intermedia únicamente por deformación en frío. v Endurecibles Excelente resistencia Tenacidad intermedia. por TT deformación TT. –a. Autotemplables. la corrosión en frío. general. v Máxima Buena Baja Endurecibles resistencia pory. TT. dureza. a mecánica temperatura y dureza ambiente. ídem Martensíticos luego del TT. v Magnéticos. No magnéticos. Excelente resistencia a corrosión por cloruros bajo tensión (SCC), intersticial (Crevice), ínter granular y picado (Pitting) hasta temperatura intermedia. v Soldabilidad Excelente soldabilidad. buena Intermedia. pobre. v Susceptibles a formación de Cr 3 C 2 a 475ºC. v Resistencia Excelente resistencia Susceptibles aalaprecipitación corrosión a corrosión general baja de –Cralgunos por C 2 cloruros a 475ºC solohasta bajo después salvotemperaturas tensión 321 de y 347. TT. (SCC), intermedias. intersticial (Crevice) y 3 excelente v Poseen Picado (pitting). transición dúctil-frágil. v Poseen No poseen transición dúctil-frágil. v Magnéticos. Poseen transición dúctil-frágil. v Excelente Inmunes aresistencia la fisuración al por desgaste. Hidrógeno (HIC). v Soldabilidad Susceptibles Intermedia. a precipitación de Cr 3 C 2 a 375ºC v Susceptibles a corrosión por cloruros (CSCC) e intergranular. v Susceptibles a la fisuración por Hidrógeno (HIC). v Excelente tenacidad para trabajo criogénico.

Tipos de corrosión n n n UNIFORME GALVÁNICA PICADO (PITTING) INTERSTICIAL (CREVICE) INTERGRANULAR POR TENSIÓN (SCC) FISURACIÓN INDUCIDA POR HIDRÓGENO (HIC)
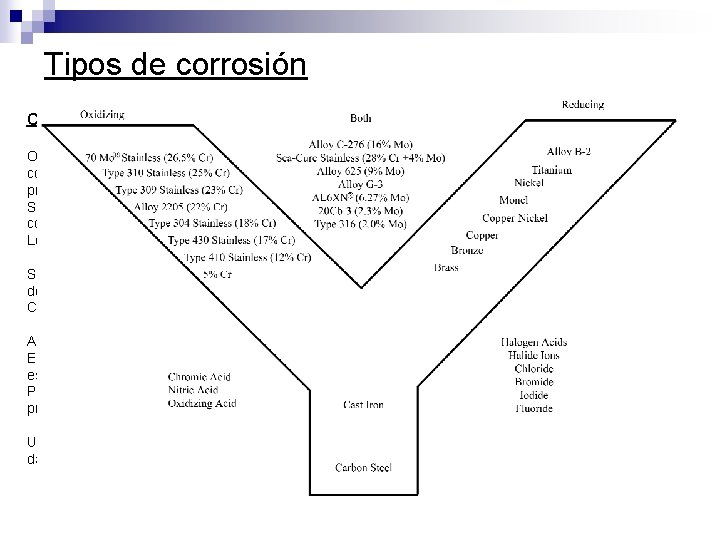
Tipos de corrosión CORROSIÓN UNIFORME Ocurre sobre amplias áreas de la superficie. Es el mecanismo de corrosión mas común para el acero y el cobre. Es la mas fácil de medir y de calcular y el único mecanismo en el cual el incremento de la sección prolonga la vida útil de la pieza. Se mide por tasa de corrosión en mm/y (milímetros por año). Se puede minimizar pintando la superficie y con inspección periódica. Los Inoxidables sufren este tipo de ataque en medios ácidos y básicos, peor no en agua. Se puede prevenir seleccionando el material con mayor resistencia al medio específico. La mejor manera de seleccionar un material para este tipo de corrosión es por medio del uso de las tablas y los gráficos del Corrosion Data Survey de NACE. Algunos aleantes tienen efecto definidos. Por ejemplo: El Cr aumenta la resistencia a la oxidación, por tanto se debe apuntar a aleaciones con alto contenido de este elemento para Ácidos Oxidantes. También otorga gran resistencia a la oxidación por temperatura. Por otra parte, el Ni otorga resistencia a medios reductores y mejora la adherencia de la capa de oxido protector a alta temperatura Utilizando las tablas de corrosión general, se puede determinar la resistencia de una aleación a un medio dado o preseleccionar algunos de un grupo amplio de materiales.

Tipos de corrosión CORROSIÓN GALVÁNICA La corrosión galvánica ocurre cuando dos metales de diferente electrovalencia entran en contacto entre si o a través de un medio conductor. Este tipo de corrosión requiere de la ocurrencia de 3 condiciones: o o o 2 metales de diferente electrovalencia Un camino o circuito para el flujo de electrones Ambos metales sumergidos en un medio conductor. Una variante de la corrosión galvánica ocurre en metales con film de óxido pasivo. Si ésta capa se destruye en un punto aislado, se cierra el circuito al tener áreas activas y pasivas en si mismo, generándose un par interno. Este es el mecanismo detrás de la corrosión intersticial y el picado. Las tablas de serie galvánica dan una idea de afinidad relativa entre distintas aleaciones. En general cuando un ánodo y un cátodo son conectados eléctricamente, el primero será corroído y el segundo no. Sin embargo, existe el Factor de Área, que modifica este comportamiento. Si el ánodo tiene mucha mas superficie que el cátodo, la corrosión será pequeña, pero si el ánodo es mucho mas pequeño que el cátodo, la corrosión será muy rápida.

Tipos de corrosión PICADO (PITTING) Es una forma de corrosión galvánica, en donde el Cr de la capa pasiva es disuelto dejando expuesto al hierro. La diferencia de potencial entre la capa pasiva y el metal activo en un acero austenítico es +0. 78 V. Los cloruros ácidos son los mas reactivos, formando (Cr. Cl 3) soluble. Se forma una cavidad en la superficie donde el hierro se combina con este compuesto para formar Cloruro Férrico, (Fe. Cl 3), una sustancia altamente corrosiva para el acero inoxidable. El Mo y el N, son elementos que reducen el ataque de los cloruros. Para cuantificar los efectos, se desarrolló una ecuación llamada Pitting Resistance Equivalent Number, o N° PREN, donde a mayor valor, mayor resistencia al picado. PREN = %Cr + 3, 3 %Mo + 16 %N El picado es influenciado por 3 factores: o o o Contenido de Cloruros PH Temperatura A mayor temperatura y contenido de Cloruros, mayor reactividad. A menor PH, mayor reactividad. El picado avanza rápidamente una vez que se inicia.

Tipos de corrosión CORROSIÓN INTERSTICIAL (CREVICE) Es otra forma de corrosión galvánica, la cual ocurre cuando el metal base está contacto con un fluido conductor estancado en un intersticio o espacio confinado muy pequeño. La diferencia de concentración del oxigeno en este punto sumado al contacto con no-metales, fomenta aun mas la reacción. Usualmente es la primera forma de corrosión en ocurrir y es predecible cuándo y en que lugar debido a la geometría necesaria. Como el picado, la presencia de cloruros aumenta la tasa de avance. Los factores que modifican la severidad son: o o Temperatura Contenido de aleantes Concentración de Cloruros Espacio o luz del intersticio Se define el "critical crevice corrosion temperature“(CCCT) bajo la cual no se produce el efecto. A mayor temperatura, mayor reactividad, ídem concentración de cloruros. A menor luz entre piezas, mayor reactividad. La mejor solución a este fenómeno es evitar al máximo la geometria que lo produce o seleccionar aleaciones mas resistentes.

Tipos de corrosión CORROSIÓN INTERGRANULAR Los bordes de grano de una micro estructura son puntos de alta concentración de energía, por ende, las reacciones químicas y metalúrgicas usualmente se inician primero en estos puntos. En inoxidables, la reacción mas común es la formación de Cr 3 C 2 por temperatura en los bordes de grano, llamado sensibilización. Este compuesto se forma a expensas del Cr disponible en solución por ende las regiones adyacentes pierden Cr y su % disminuye, creándose una aleación diferente al metal base. Esto genera una diferencia de potencial entre el metal base y el borde de grano con la consecuente corrosión galvanica, actuando los bordes de grano como ánodos. Los carburos se forman al soldar, al hacer T. T. y al calentar para conformar en caliente. Los inoxidables austeníticos son los mas susceptibles a este tipo de corrosión. Para evitarlo se utilizan distintos enfoques: Austeníticos versión bajo carbono para soldar (Grados L). Aleaciones estabilizadas con Ti, Ta y Nb para uso por encima de 427 hasta 900°C por largos períodos. Factores que influyen en formación de carburos: o o o Temperatura (425°C-800°C % de Carbono Tiempo
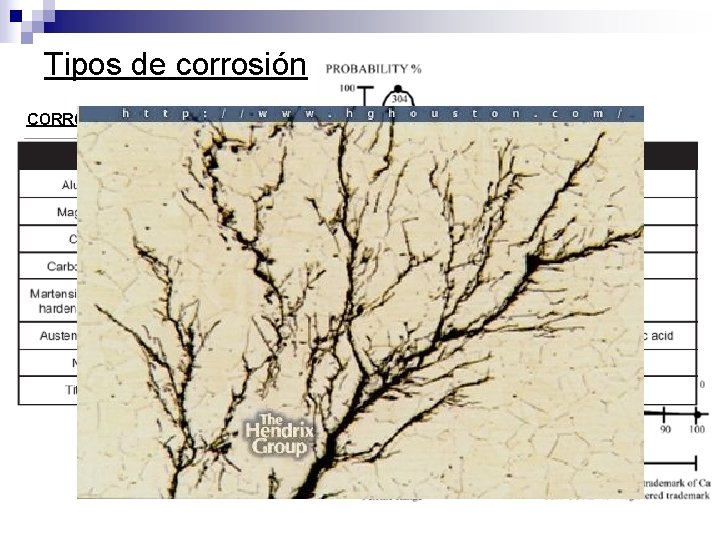
Tipos de corrosión CORROSIÓN POR TENSIÓN (SCC) Es una de las formas comunes, peligrosas y complejas de corrosión. Los Inoxidables que contienen Ni son especialmente susceptibles al SCC inducida por cloruros. La susceptibilidad se da con 5 a 35% Ni y la máxima entre 7 a 20%. Por eso todos los Austeníticos son corroídos por este mecanismo, mientras que los Ferríticos son en gran parte inmunes. Se necesitan 3 factores: o Contenido de Niquel o Tensión de tracción. o Temperatura Con solo una pocas ppm de cloruros con bajo PH, en presencia de oxigeno y por encima del umbral de temperatura, el SCC se iniciará. Las fisuras generadas son intra granulares y muestran un aspecto plumoso.

Tipos de corrosión FISURACION INDUCIDA POR HIDRÓGENO (HIC) Este gas penetra en la estructura causando fisuración, ampollas, porosidad y pérdida de ductilidad. La difusión del H dentro de la estructura es posible gracias a su pequeño diámetro atómico, lo que posibilita que los átomos se alojen dentro de la estructura cristalina, para luego recombinarse en moléculas de H 2, generando presiones extremas que rompen el material y generan fisuras trans granulares. . Los inoxidables ferríticos son particularmente susceptibles a temperatura ambiente, mientras que los Austeníticos se consideran inmunes a este fenómeno por la alta plasticidad de la austenita. Se necesitan 4 factores: o Concentración crítica de Hidrógeno o Tensiones de tracción. o Microestructura susceptible o Temperatura entre -100 y 200°C Por debajo de -100°C no hay difusión suficiente y por encima de 200°C no existe hidrógeno molecular. Se elimina con un T. T. de deshidrogenado a 250°C, ya que por encima de esa temperatura , el H se combina con el C formando Metano y generando descarburación y perdida de resistencia. A su vez, a mayor temperatura la solubilidad del H en el Fe es mayor. Se reduce el efecto, limitando la dureza de la estructura en general hasta 22 HRc.

Tipos de corrosión RESUMEN Galvánica: Por diferencia de electrovalencia entre aleaciones a través de un medio conductor. Picado: Por presencia de cloruros en PH ácido. . Intersticial: Fluido estancado, presencia de oxigeno y cloruros en un espacio confinado muy pequeño. . Intergranular: Formación de Cr 3 C 2 por exposición a temperaturas entre 425 -800°C Bajo tensión: Por contenido de 5% a 35% de Ni, tensiones de tracción y superar umbral de temperatura. Fisuración por hidrógeno: Por presencia de hidrógeno en estructura cristalina entre -100 y 200°C. Escamado: Oxidación por exposición a gases oxidantes a temperaturas mayores a 800°C.

Criterios de selección CORROSIÓN Elegir el acero inoxidable adecuado es esencialmente sopesar 4 factores en orden de importancia: Los ambientes corrosivos se definen con múltiples parámetros: compuestos químicos, concentración, temperatura, velocidad, tiempo. De manera que es complejo definir en forma perfecta el servicio y por ende el material. Sin embargo hay criterios generales: Tipo 304. Sirve al mas amplio rango de aplicaciones. Soporta fluidos orgánicos e inorgánicos salvo a elevadas temperaturas, presencia de cloruros o ácidos concentrados. Tipo 316 Mas resistente a la corrosión general y a cloruros. Tipo 317, Especialmente resistente a cloruros, picado y corrosión intersticial.

Criterios de selección PASOS A SEGUIR Elegir el acero inoxidable adecuado es esencialmente sopesar 4 factores en orden de importancia: 1. Corrosión o Resistencia al calor. Identificar las condiciones de P y T del ambiente y la reactividad de los fluidos involucrados para determinar cuál es el requerimiento mas importante 2. Propiedades mecánicas Considerar la resistencia mecánica que se necesita y a qué temperatura. Determinar la mejor combinación entre Resistencia a la corrosión y resistencia mecánica. 3. Métodos de fabricación-Obtención Analizar los procesos de manufactura necesarios para conformar la pieza, ya que éstos afectarán la decisión de la aleación a elegir. 4. Costo Total. Se deben analizar los costos completos, incluyendo el ciclo de vida y costo de reposición.

¡MUCHAS GRACIAS!
- Slides: 22