Academia Europea de Pacientes sobre Innovacin Teraputica Retos

Academia Europea de Pacientes sobre Innovación Terapéutica Retos éticos y prácticos de la organización de ensayos clínicos en poblaciones de tamaño reducido

Poblaciones de tamaño reducido en ensayos clínicos Academia Europea de Pacientes sobre Innovación Terapéutica § No existe una definición común para las poblaciones de tamaño reducido. El concepto «población de tamaño reducido» hace referencia a un número limitado de pacientes con la enfermedad investigada. § Los conceptos de población de tamaño reducido y población especial coinciden en cierta medida. Las poblaciones de tamaño reducido pueden incluir: Ø enfermedades raras, incluyendo subtipos específicos de enfermedades más comunes Ø niños (pacientes pediátricos) Ø personas de edad avanzada (pacientes de geriatría) 2

Enfermedades raras y ultrarraras Academia Europea de Pacientes sobre Innovación Terapéutica § 30 millones de personas padecen enfermedades raras en la UE. § Las enfermedades raras son las que aparecen en una proporción inferior a 1 de cada 2000 personas. § Las enfermedades ultrarraras aparecen en menos de 1 de cada 2 000 de personas (prevalencia sugerida 1). § Los conocimientos sobre las enfermedades raras son limitados debido a que la investigación es menor (interés y financiación limitados). § Las enfermedades raras pueden presentar variaciones considerables por lo que respecta a la manifestación y el estado. 1 Hennekam, R. C. (2011). Care for patients with ultra-rare disorders. European Journal of Medical Genetics, 54(3), 220 -224. doi: 10. 1016/j. ejmg. 2010. 12. 001 3

Situaciones estándar y no estándar Academia Europea de Pacientes sobre Innovación Terapéutica § En principio, el desarrollo de medicamentos huérfanos y medicamentos para niños se consideran situaciones estándar (es decir, existen directrices para su regulación). § En estos casos, el desarrollo de medicamentos sigue los principios de la medicina basada en la evidencia, al igual que en las enfermedades comunes. § El desarrollo de medicamentos huérfanos y medicamentos para niños puede establecer limitaciones específicas en relación con lo que es posible y razonable. § El desarrollo puede requerir, por lo tanto, soluciones no estándar. 4
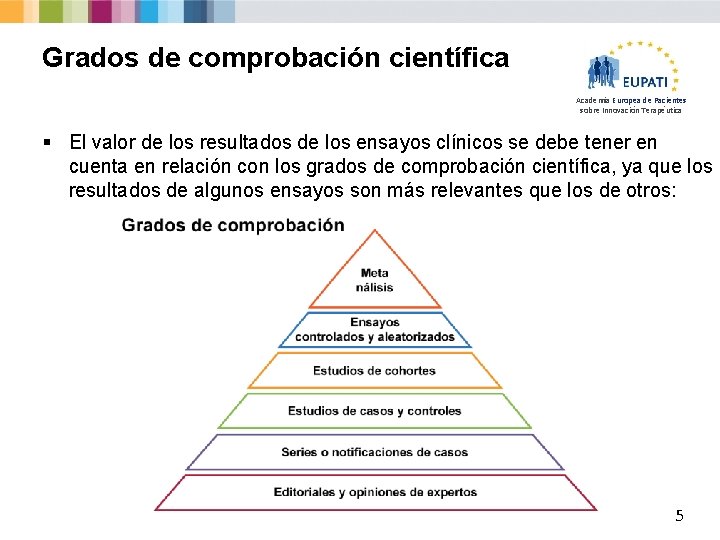
Grados de comprobación científica Academia Europea de Pacientes sobre Innovación Terapéutica § El valor de los resultados de los ensayos clínicos se debe tener en cuenta en relación con los grados de comprobación científica, ya que los resultados de algunos ensayos son más relevantes que los de otros: 5

¿Qué grado de comprobación científica puede obtenerse en estudios con poblaciones de tamaño reducido y niños? Academia Europea de Pacientes sobre Innovación Terapéutica § Preguntas clave: Ø ¿Es posible realizar un ensayo controlado y aleatorizado (ECA)? Ø ¿Es mejor un ECA de tamaño reducido que un estudio de observación de mayor envergadura? Ø ¿Existe riesgo de sesgo? Ø ¿Hasta qué punto será exacto el resultado? Ø ¿Qué comprobación se necesita para la autorización de comercialización inicial? Ø ¿Qué comprobación se necesita tras la comercialización? 6
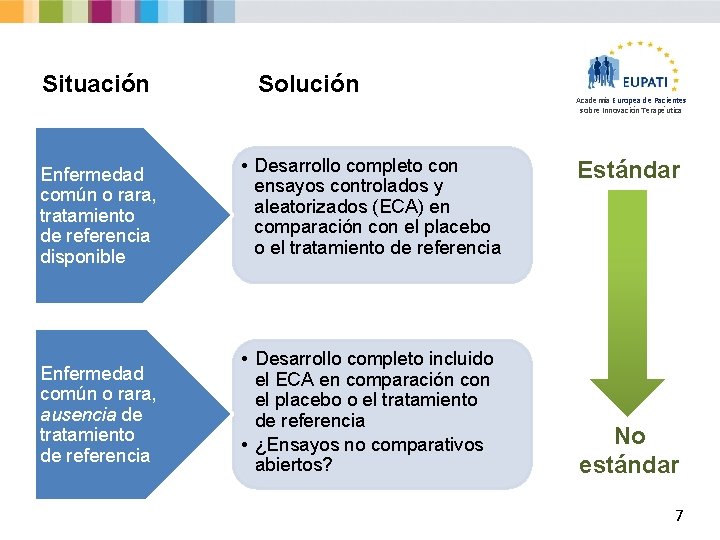
Situación Solución Enfermedad común o rara, tratamiento de referencia disponible • Desarrollo completo con ensayos controlados y aleatorizados (ECA) en comparación con el placebo o el tratamiento de referencia Enfermedad común o rara, ausencia de tratamiento de referencia • Desarrollo completo incluido el ECA en comparación con el placebo o el tratamiento de referencia • ¿Ensayos no comparativos abiertos? Academia Europea de Pacientes sobre Innovación Terapéutica Estándar No estándar 7
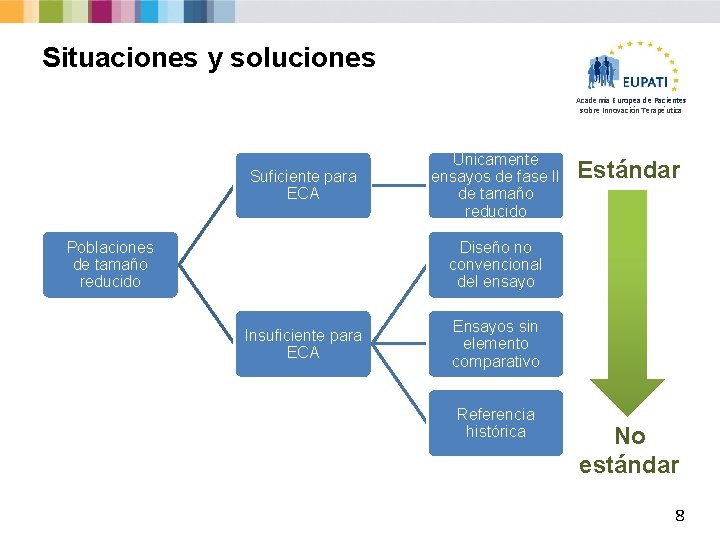
Situaciones y soluciones Academia Europea de Pacientes sobre Innovación Terapéutica Suficiente para ECA Poblaciones de tamaño reducido Únicamente ensayos de fase II de tamaño reducido Estándar Diseño no convencional del ensayo Insuficiente para ECA Ensayos sin elemento comparativo Referencia histórica No estándar 8

Disponibilidad de directrices para estudios en poblaciones de tamaño reducido Academia Europea de Pacientes sobre Innovación Terapéutica El Comité de Medicamentos de Uso Humano (CHMP) ha establecido una serie de directrices para estos estudios: Ø poblaciones de tamaño reducido (http: //www. ema. europa. eu/docs/en_GB/document_library/Scientific_ guideline/2009/09/WC 500003615. pdf) Ø población infantil (http: //www. ema. europa. eu/docs/en_GB/document_library/Scientific_ guideline/2009/09/WC 500002926. pdf) 9

Estudios con poblaciones de tamaño reducido: factores clave (1) Academia Europea de Pacientes sobre Innovación Terapéutica § Recopilación estandarizada de datos: planificada con antelación (prospectivamente), documentada en protocolo y de conformidad con las siguientes normas: Ø maximizar la recogida de información importante Ø mantener en un nivel aceptable la carga participativa del estudio Ø evitar la pérdida de seguimiento § Debe hacerse un buen uso de los modelos animales de la enfermedad. 10

Estudios con poblaciones de tamaño reducido: factores clave (2) Academia Europea de Pacientes sobre Innovación Terapéutica Factores clave: § Comprender el curso natural de la enfermedad y cómo puede cambiar con el tiempo. § Comprender el origen de posibles interpretaciones de datos incorrectas (factores de confusión). § Comprender el origen de la variedad de respuestas a una terapia. 11

Estudios con poblaciones de tamaño reducido: evaluación de la eficacia (1) Academia Europea de Pacientes sobre Innovación Terapéutica § Normalmente, la eficacia se mide en términos de: Ø Curación Ø Supervivencia Ø Tiempo transcurrido hasta la evolución de la enfermedad Ø Supervivencia sin progresión Ø Reversión de disfunción orgánica Ø Estabilización de la enfermedad § La selección del criterio más adecuado es crucial. 12

Estudios con poblaciones de tamaño reducido: evaluación de la eficacia (2) Academia Europea de Pacientes sobre Innovación Terapéutica § ¿Cómo se mide la eficacia? Ø Criterios objetivos de valoración (por ejemplo, índices de supervivencia) Ø Criterios indirectos de valoración (mejoría clínica) Ø Alivio de los síntomas Ø Calidad de vida Ø Biomarcador, valor indirecto desconocido Suele ser necesario tener en cuenta una combinación lógica de medidas que apunten en la misma dirección. 13
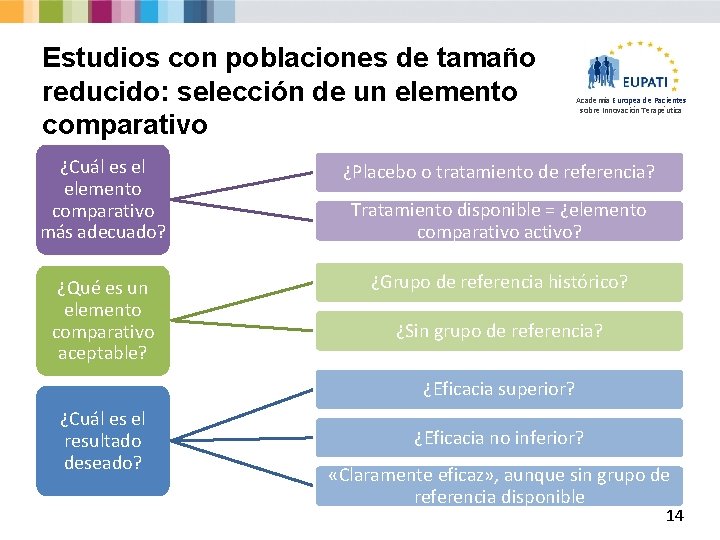
Estudios con poblaciones de tamaño reducido: selección de un elemento comparativo Academia Europea de Pacientes sobre Innovación Terapéutica ¿Cuál es el elemento comparativo más adecuado? ¿Placebo o tratamiento de referencia? ¿Qué es un elemento comparativo aceptable? ¿Grupo de referencia histórico? Tratamiento disponible = ¿elemento comparativo activo? ¿Sin grupo de referencia? ¿Eficacia superior? ¿Cuál es el resultado deseado? ¿Eficacia no inferior? «Claramente eficaz» , aunque sin grupo de referencia disponible 14

Ejemplos de diseños de estudios Academia Europea de Pacientes sobre Innovación Terapéutica § Diseño de adaptación óptimo: Ø La fase II y la fase III se combinan en un estudio. Ø El diseño se adapta mientras continúa el ensayo. Ø Se continúa con los niveles de mejor dosis tras los análisis provisionales. § Estudios secuenciales: Ø Se incluyen pacientes y análisis hasta llegar a una conclusión fiable. Ø El efecto/resultado aparece rápidamente. § Modelado: Ø Efecto de los parámetros. Ø Relación entre la eficacia y los efectos. 15

Problemas prácticos de los pacientes de un ensayo sobre enfermedades raras Academia Europea de Pacientes sobre Innovación Terapéutica § La búsqueda de ensayos relevantes puede ser compleja. § Puede ser necesario recorrer largas distancias para desplazarse hasta el centro del investigador. § Es posible que sea necesaria la reubicación del paciente. § Puede ser necesario el apoyo económico o el acceso al sistema de atención sanitaria. § Necesidad de ayuda con el idioma. § Necesidad de prestaciones/instalaciones educativas para niños. § Reorganización de la vida familiar en general. 16

Privacidad y transparencia Academia Europea de Pacientes sobre Innovación Terapéutica § Se toman todas las medidas necesarias para proteger la privacidad durante los ensayos clínicos. No obstante, esto puede ser difícil en el caso de las enfermedades raras o ultrarraras debido a lo siguiente: Ø Registros de pacientes de menor tamaño (o ausencia de registros). Ø Riesgo de ser identificado en un ensayo clínico. 17

Cuestiones éticas en los ensayos clínicos con enfermedades raras Academia Europea de Pacientes sobre Innovación Terapéutica § Evaluación de beneficios y riesgos en el caso de una enfermedad potencialmente mortal. § A menudo no se dispone de un elemento comparativo conocido eficaz. § Puede que el nuevo tratamiento no esté accesible tras la finalización del ensayo. § No existe ningún proceso establecido para facilitar los resultados del ensayo a los pacientes. 18

Proceso de consentimiento informado Academia Europea de Pacientes sobre Innovación Terapéutica § Puede que los pacientes no puedan otorgar el consentimiento informado por sí mismos y que tengan que confiar en la decisión del representante legal (que quizá no coincida forzosamente con la opinión del propio paciente). § La decisión de participar en el ensayo puede no ser realmente voluntaria, dado que quizá no exista otra alternativa de tratamiento. § El control con placebo es un problema concreto debido a la gravedad de la enfermedad, ya que se requiere que el participante consienta en que posiblemente no reciba tratamiento alguno durante la fase inicial del ensayo. 19

Conclusión Academia Europea de Pacientes sobre Innovación Terapéutica § Se debe encontrar un equilibrio entre lo que es necesario y lo que es posible. § Hay métodos para demostrar la eficacia de los ensayos clínicos con poblaciones de tamaño reducido. § La estrategia de desarrollo para el tratamiento en poblaciones reducidas debería discutirse con antelación con las autoridades regulatorias para el asesoramiento científico y la asistencia con el protocolo. § Los ensayos clínicos sobre enfermedades raras o ultrarraras suponen una serie de retos éticos y organizativos. 20
- Slides: 20