Academia Europea de Pacientes sobre Innovacin Teraputica Cmo

Academia Europea de Pacientes sobre Innovación Terapéutica Cómo se fabrica un fármaco: Los principios básicos del descubrimiento y el desarrollo de fármacos

Resumen Academia Europea de Pacientes sobre Innovación Terapéutica § Más de 12 años y unos costes de más de 1000 millones de euros de media es lo que supone realizar toda la investigación y el desarrollo necesarios para que pueda ponerse un nuevo medicamento a disposición de los pacientes. § El desarrollo de fármacos es una empresa de alto riesgo. Ø Alrededor de un 98 % de los fármacos que se desarrollan no llegan nunca al mercado. Ø El motivo suele ser que, en términos de ventajas y riesgos, la comparación no resulta ventajosa respecto a fármacos de los que ya disponen los pacientes. 2
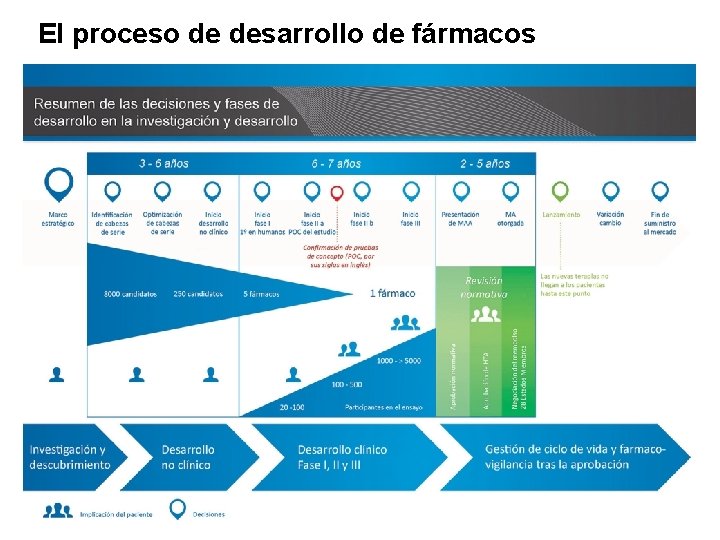
El proceso de desarrollo de fármacos

FASE 1: Descubrimiento (1) Academia Europea de Pacientes sobre Innovación Terapéutica § Investigación previa y determinación de si existe una "necesidad sin cubrir". Ø Científicos universitarios y de la industria farmacéutica trabajan para comprender la enfermedad en la fase de investigación previa. § Una "necesidad sin cubrir" hace referencia a una enfermedad para la que: Ø no hay un medicamento adecuado o Ø hay un medicamento, pero puede tener efectos secundarios inaceptables en algunos pacientes, que por ello no podrán tomarlo. 4

FASE 1: Descubrimiento (2) Academia Europea de Pacientes sobre Innovación Terapéutica § El proceso de investigación y desarrollo requiere múltiples recursos y es muy caro. § Existen muchos casos de necesidades sin cubrir en los que no se están desarrollando nuevos medicamentos. § El proceso de presentación y aprobación normativa debe superarse antes de poder comercializar el medicamento. 5

FASE 1: Descubrimiento (3) Academia Europea de Pacientes sobre Innovación Terapéutica § Cada fase del desarrollo implica acuerdos económicos (inversión) y sobre las personas (recursos) que realizarán el trabajo. Este acuerdo se denomina "decisión de inversión". § Cuando se toma la decisión de inversión, pueden iniciarse las actividades de la siguiente fase de la investigación. Este patrón de "decisión de inversión – actividad – resultados – decisión de inversión" será el que se seguirá durante todo el proceso de desarrollo. 6

FASE 2: Selección de objetivo (1) Academia Europea de Pacientes sobre Innovación Terapéutica § Las enfermedades surgen cuando los procesos corporales normales sufren alteraciones o no funcionan debidamente. § Al desarrollar un fármaco, es importante comprender en detalle (a nivel de células), qué es lo que ha fallado. De esa manera, puede establecerse como objetivo el proceso anormal. § El "objetivo" puede ser: Ø una molécula que se ha producido en exceso y que interfiere con el funcionamiento corporal normal; Ø una molécula que no se produce en cantidades normales o Ø una molécula que tiene una estructura anormal. 7
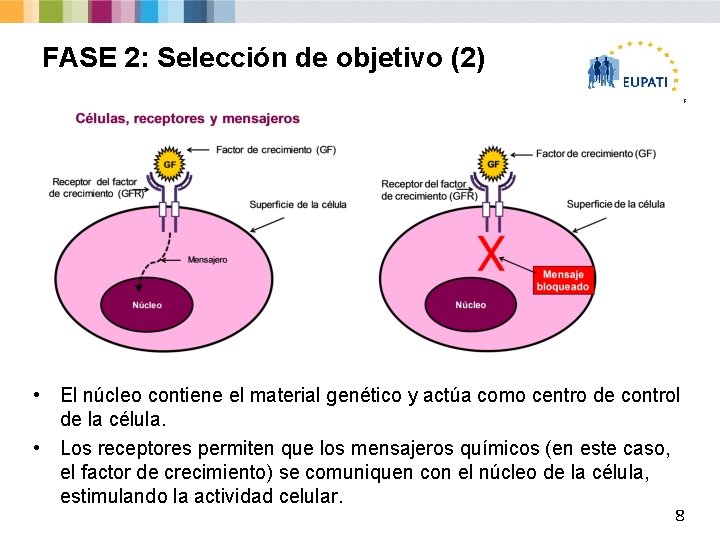
FASE 2: Selección de objetivo (2) Academia Europea de Pacientes sobre Innovación Terapéutica • El núcleo contiene el material genético y actúa como centro de control de la célula. • Los receptores permiten que los mensajeros químicos (en este caso, el factor de crecimiento) se comuniquen con el núcleo de la célula, estimulando la actividad celular. 8

FASE 2: Selección de objetivo (3) Academia Europea de Pacientes sobre Innovación Terapéutica § Ejemplo: cáncer Ø Un mensajero químico se combina con el receptor del factor de crecimiento en la superficie de la célula, generándose un mensaje dentro de la célula. Ø Si las señales se descontrolan, el crecimiento celular lleva al cáncer. Ø El bloqueo del receptor en las células cancerígenas evitará la transmisión del mensaje, así como un crecimiento celular descontrolado. § Si se puede bloquear el receptor en las células cancerígenas, se evitará: Ø que se envíe el mensaje y Ø el crecimiento celular descontrolado. 9

FASE 2: Selección de objetivo (4) Academia Europea de Pacientes sobre Innovación Terapéutica • Los científicos a menudo no pueden decir con exactitud qué anormalidad u objetivo es el responsable de la enfermedad; por lo tanto, puede que los intentos por corregir los objetivos no traten la enfermedad. • De ser así, el proyecto de desarrollo puede estar detrás del objetivo equivocado y acabar fracasando. • Seleccionar el mejor objetivo sobre el que trabajar resulta crucial en un proyecto. 10

FASE 3: Generación de cabezas de serie Academia Europea de Pacientes sobre Innovación Terapéutica § Esta fase consiste en hallar una molécula que interactúe con el objetivo. Se las denomina "cabezas de serie". Ø Las cabezas de serie pueden ser moléculas que se produzcan de forma natural o que se fabriquen de forma química. Ø Las cabezas de serie también pueden ser grandes moléculas o proteínas. Se las denomina "biológicas". § Las pruebas en busca de cabezas de serie se denominan "proceso de cribado". Ø La tecnología robótica denominada "cribado de alto rendimiento" permite someter a prueba millones de moléculas de forma rápida. § Una vez se han generado o hallado las cabezas de serie, puede pasarse al siguiente paso del proceso. 11

FASE 4: Optimización de cabezas de serie (1) Academia Europea de Pacientes sobre Innovación Terapéutica § Puede que una cabeza de serie seleccionada tenga únicamente un efecto débil sobre el objetivo. Entonces los químicos deberán modificar la molécula cabeza de serie seleccionada para aumentar su efecto en el objetivo. Ø Se añaden o eliminan algunos de los elementos de la cabeza de serie original para aumentar su efecto, lo que da como resultado una serie de moléculas ligeramente diferentes. 12
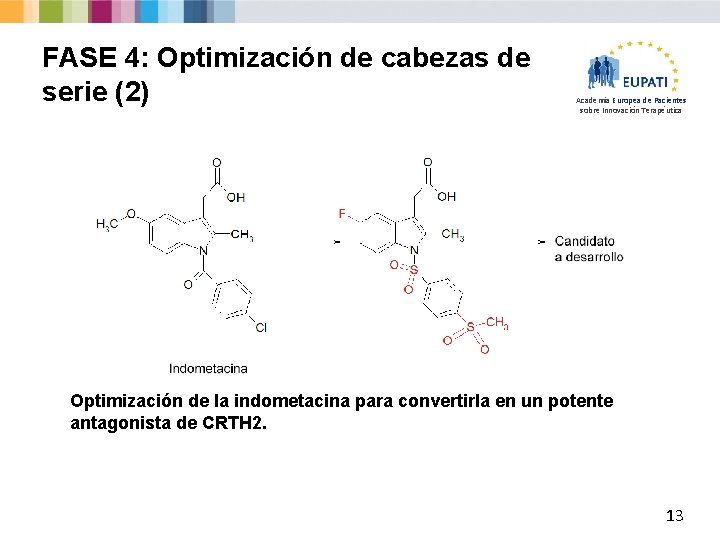
FASE 4: Optimización de cabezas de serie (2) Academia Europea de Pacientes sobre Innovación Terapéutica Optimización de la indometacina para convertirla en un potente antagonista de CRTH 2. 13

FASE 4: Optimización de cabezas de serie (3) Academia Europea de Pacientes sobre Innovación Terapéutica § Estas moléculas modificadas se someten entonces a pruebas para determinar cuál es la estructura más eficaz y mejor tolerada por el organismo (seguridad). § Las moléculas con una mejor eficacia y seguridad pueden someterse entonces a nuevas pruebas en calidad de "fármaco candidato". § Aproximadamente en esta fase, la información científica y técnica sobre el compuesto candidato, como su estructura molecular y sus efectos, suele registrarse, o patentarse, para protegerlo como propiedad intelectual. 14

FASE 5: Pruebas de seguridad no clínicas (1) Academia Europea de Pacientes sobre Innovación Terapéutica § El siguiente paso en el proceso de desarrollo implica pruebas de seguridad en animales que se rigen por normas y reglamentos específicos de Buenas prácticas de laboratorio (BPL). § Estos reglamentos establecen los estudios que deben realizarse y qué tipo de animales debe usarse para obtener información razonable. 15

FASE 5: Pruebas de seguridad no clínicas (2) Academia Europea de Pacientes sobre Innovación Terapéutica § Las BPL y los reglamentos no clínicos requieren la recopilación de información sobe los efectos del fármaco: Ø en el animal en general; Ø en todos los tejidos y órganos del animal (estudios de toxicología sistémica); Ø en la capacidad de los animales para reproducirse y desarrollarse con normalidad (estudios de toxicología de la reproducción); Ø en la piel u ojos (estudios toxicológicos locales); Ø en los cromosomas y genes (estudios de genotoxicidad) y Ø en la aparición de cánceres (estudios carcinogénicos). 16

FASE 5: Pruebas de seguridad no clínicas (3) Academia Europea de Pacientes sobre Innovación Terapéutica 17

FASE 5: Pruebas de seguridad no clínicas (4) Academia Europea de Pacientes sobre Innovación Terapéutica § Estos estudios no solo muestran el perfil de seguridad en animales, sino que también proporcionan información importante sobre: Ø cómo la sustancia accede al organismo (Absorción) Ø distribución por el organismo (Distribución) Ø desintegración de la sustancia por parte del organismo (Metabolismo) Ø cómo abandona el organismo la sustancia (Excreción). § Suele abreviarse como "ADME". § Toda esta información se usa para decidir si el compuesto candidato puede pasar al primer estudio (clínico) en humanos, y de ser así, qué dosis utilizar. 18

FASE 6: Prueba de mecanismo – Estudios clínicos de fase I (1) Academia Europea de Pacientes sobre Innovación Terapéutica § Antes de iniciar un estudio clínico, debe presentarse una solicitud de ensayo clínico (CTA, por sus siglas en inglés). § Se pedirá también la opinión del comité de Ética. § La seguridad es la prioridad número uno; el estudio en humanos no puede empezar hasta que se reciba la aprobación de: Ø el comité de revisión interno de la empresa; Ø el comité de Ética (externo) y Ø la autoridad normativa (externa). 19

FASE 6: Prueba de mecanismo – Estudios clínicos de fase I (2) Academia Europea de Pacientes sobre Innovación Terapéutica § Los estudios en voluntarios (o estudios clínicos de fase I) permiten a los médicos y científicos comprobar si el fármaco es seguro en humanos. Se les denomina estudios de "prueba de mecanismo". Ø Los estudios clínicos de fase I examinan si el fármaco se comporta igual en los humanos que en los animales. § Toda la información procedente del estudio se recopila en un documento denominado formulario de registro de caso (CRF). § Dos elementos muy importantes son: Ø el consentimiento informado (que garantiza que los participantes comprenden qué se va a hacer y aceptan participar en el estudio) y Ø la revisión y opinión del comité de Ética 20

FASE 6: Prueba de mecanismo – Estudios clínicos de fase I (3) Academia Europea de Pacientes sobre Innovación Terapéutica § Dado que la seguridad es prioritaria, el primer estudio clínico se inicia con una sola dosis, muy baja, del fármaco. A continuación se aumenta la dosis. Ø Estos estudios se denominan estudios de dosis única ascendente (SAD, por sus siglas en inglés). Suelen seguirles un estudio de dosis múltiple ascendente (MAD, por sus siglas en inglés) en el que se administran múltiples dosis a cada voluntario. § A continuación se analizan los resultados del estudio y se evalúan todas las mediciones de seguridad, incluyendo: Ø Farmacocinética: lo que el organismo le hace al fármaco. Los niveles del fármaco en sangre pueden medirse para determinar la ADME. Ø Farmacodinámica: lo que el fármaco le hace al organismo (el "efecto"). 21

FASE 7: Prueba de principio: Estudios clínicos de fase II (1) Academia Europea de Pacientes sobre Innovación Terapéutica § Si los resultados del estudio de fase I muestran que es seguro continuar, el siguiente paso es comenzar con los ensayos clínicos en pacientes con la enfermedad que se pretende tratar. § Suele haber dos grupos de tratamiento: Ø un grupo que recibe el fármaco activo y Ø otro que recibe un fármaco que no tiene efectos en el organismo (un "placebo"). § Estos ensayos suelen realizarse en 100 -500 pacientes. Están diseñados para recopilar información sobre el efecto del fármaco en la enfermedad en sí ("prueba de principio"). 22

FASE 7: Prueba de principio: Estudios clínicos de fase II (2) Academia Europea de Pacientes sobre Innovación Terapéutica § Los estudios suelen llevarse a cabo en diversos hospitales y por parte de médicos de hospital denominados investigadores. Realizar ensayos en varias ubicaciones diferentes al mismo tiempo es más complicado que llevar a cabo un ensayo en un único emplazamiento. § Al final de los estudios de fase II, el programa habrá: Ø durado 8, 5 años, de media y Ø costado millones de euros, de media. § De los 10 fármacos que se someten a prueba en la fase I y la fase II, solo dos pasarán, de media, a la siguiente fase. 23

FASE 8: Estudios de confirmación: Estudios clínicos de fase III (1) Academia Europea de Pacientes sobre Innovación Terapéutica § Los ensayos de fase III (estudios de confirmación) pretenden confirmar la eficacia y seguridad de un fármaco en una población de pacientes de gran tamaño. § Toda la información recopilada en las fases anteriores se usa ahora para tomar decisiones importantes como la fórmula final del fármaco y la dosis que se va a poner a prueba. § Los estudios de fase III pueden incluir a miles de pacientes, realizarse en muchos países, requerir una gran cantidad de experiencia para llevarlos a cabo de forma eficaz y, por lo tanto, son muy caros y llevan mucho tiempo. 24

FASE 8: Estudios de confirmación: Estudios clínicos de fase III (1) Academia Europea de Pacientes sobre Innovación Terapéutica § No obstante, es la única forma de obtener una respuesta clara entre la eficacia del fármaco (hasta qué punto funciona) y su seguridad (si se tolera bien). § Más de un 50 % de los fármacos que llegan a la fase III no la superan. El índice global de fracaso de los proyectos (desde la fase de descubrimiento) es de más de un 97 %. § Los ingresos que generen los escasos medicamentos que lleguen a comercializarse deberán cubrir los costes de todos los proyectos (tanto de los que se han concluido con éxito como de los que han fracasado). 25

FASE 9: Presentación normativa (1) Academia Europea de Pacientes sobre Innovación Terapéutica § Si los resultados de los estudios clínicos de fase III muestran una relación riesgo-beneficio aceptable, puede elaborarse una solicitud de autorización de comercialización (MAA, por sus siglas en inglés). § Se recoge toda la información acerca del fármaco (no clínica, clínica y de fabricación) y se organiza con un formato predeterminado denominado "dosier". El dosier se envía a las autoridades normativas (RA, por sus siglas en inglés). § Cuando la RA esté satisfecha con los resultados (relación riesgo-beneficio), aprobará la comercialización del nuevo fármaco. 26

FASE 9: Presentación normativa (2) Academia Europea de Pacientes sobre Innovación Terapéutica § El proceso de revisión suele tardar unos 12 -18 meses. No se permitirá la comercialización del fármaco hasta que las autoridades normativas estén satisfechas y den su aprobación. § Muchos países exigen estudios sobre la relación costeeficacia del nuevo fármaco. Estos documentos respaldarán al gobierno o a las empresas de seguros a través de grupos de Evaluación de tecnologías sanitarias (HTA, por sus siglas en inglés) para tomar una decisión y ofrecer recomendaciones sobre el permiso para que el medicamento se recete y lo pague el sistema de seguros del país. 27

FASE 10: Vigilancia de la seguridad durante y después de la comercialización Academia Europea de Pacientes sobre Innovación Terapéutica § El proceso de marketing implica compartir la información acerca del nuevo fármaco con médicos y otros profesionales sanitarios para que sean conscientes de sus efectos y puedan recetarlo en los casos en los que piensen que puede ayudar a los pacientes. § Sin embargo, todavía es necesario recoger y analizar la información sobre la seguridad del fármaco cuando se usa en la "vida real". Este proceso se denomina "farmacovigilancia". § Tanto los ensayos clínicos como los datos de la vida real recogidos tras la comercialización son necesarios para comprender en su totalidad la relación riesgo-beneficio real. 28

FASE 10: Gestión del ciclo de vida Academia Europea de Pacientes sobre Innovación Terapéutica § Por último, el proceso de desarrollo continuará explorando: Ø Otros usos posibles (indicaciones) para el fármaco. Por ejemplo, si el uso inicial era pacientes con asma, una indicación nueva podría ser para los pacientes con otro tipo de enfermedad pulmonar. Ø Mejores maneras de fabricar y usar el medicamento (nuevas fórmulas). Por ejemplo, una fórmula especial para niños. § Todas estas actividades se conocen como "gestión del ciclo de vida". 29

FASE 10: Otros cambios en el ciclo de vida de un fármaco Academia Europea de Pacientes sobre Innovación Terapéutica § Cuando se lanza al mercado un fármaco, está protegido por una patente. Esto significa que las demás empresas no pueden comercializar un medicamento similar. Al final de la patente o del periodo de protección de datos, otras empresas fabricarán y comercializarán el mismo producto. Cuando esto sucede, el producto se denomina "genérico". § Los fármacos nuevos suelen venderse únicamente con receta. De esa forma, los profesionales de la salud pueden supervisar su uso en los primeros años. Posteriormente, puede que el fármaco pueda adquirirse sin ella. Esto implica un cambio en el estado normativo del fármaco. 30
- Slides: 30