ABSORCIN 2 INGENIERO QUMICO 2003 2004 1 Mtodo

ABSORCIÓN 2º INGENIERO QUÍMICO 2003 -2004 1

►Método de Operación: ●La alimentación es un gas y se introduce por el fondo de la columna al contrario del disolvente líquido que lo hace por la parte superior. ●El gas absorbido y el disolvente salen por el fondo. Los componentes no absorbidos salen por la parte superior en forma gaseosa. ●Al considerar el diseño de la columna de absorción se ha de buscar el mejor contacto entre el gas y el líquido. ●La eficacia de la columna está determinada por el contacto entre las fases. 2
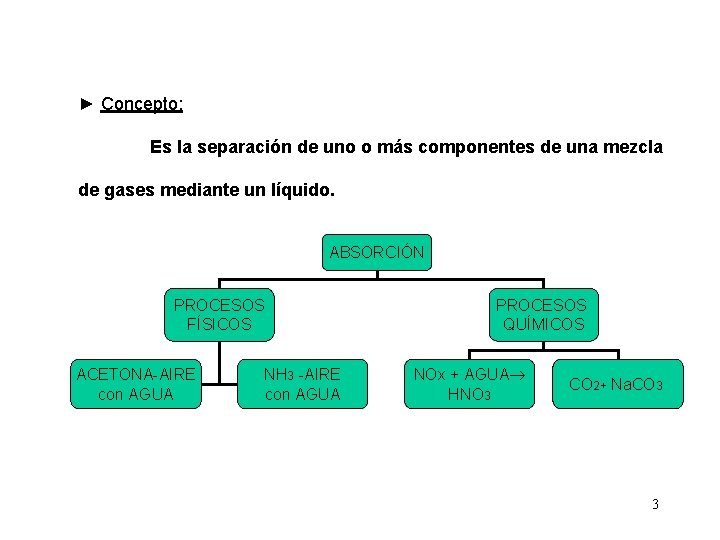
► Concepto: Es la separación de uno o más componentes de una mezcla de gases mediante un líquido. ABSORCIÓN PROCESOS FÍSICOS ACETONA-AIRE con AGUA NH 3 -AIRE con AGUA PROCESOS QUÍMICOS NOx + AGUA HNO 3 CO 2+ Na. CO 3 3
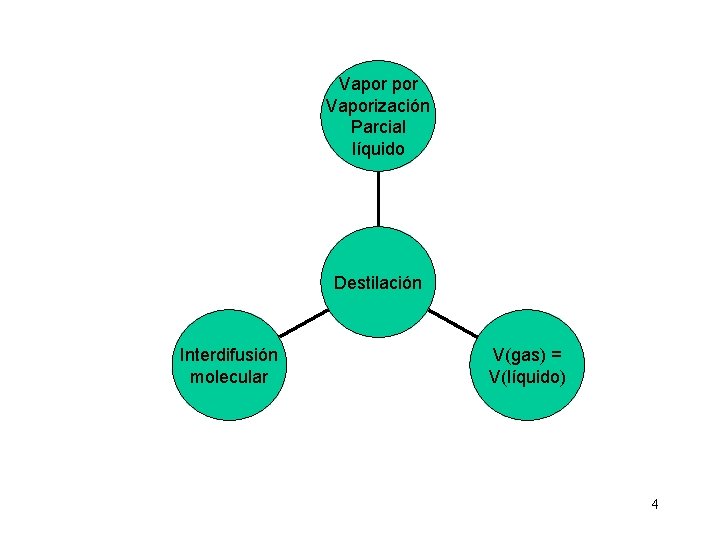
Vaporización Parcial líquido Destilación Interdifusión molecular V(gas) = V(líquido) 4
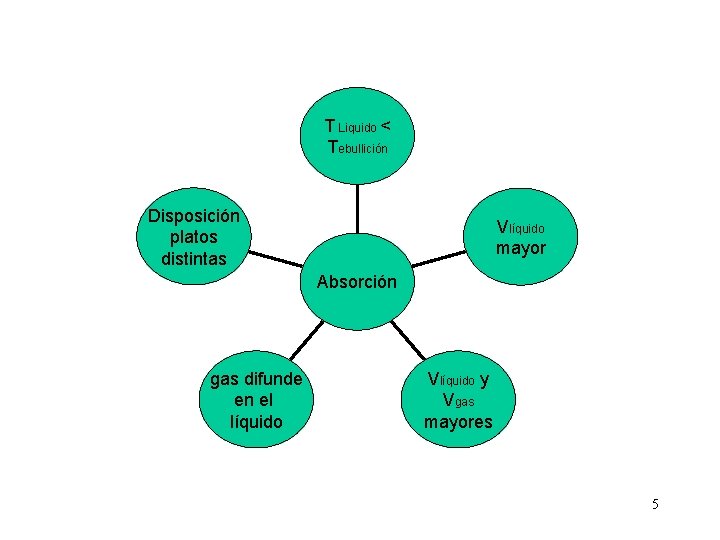
T Liquido < Tebullición Disposición platos distintas Vlíquido mayor Absorción gas difunde en el líquido Vlíquido y Vgas mayores 5
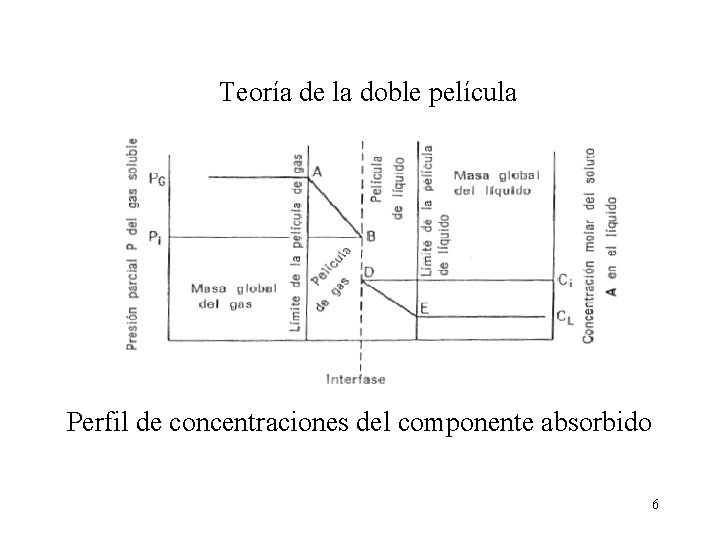
Teoría de la doble película Perfil de concentraciones del componente absorbido 6

Difusión de un gas a través de un gas estancado: N’A = - Dv CT d. CA CB dz Ley de Stefan NA’ = Velocidad global de transferencia de materia: moles/(área tiempo) DV = Difusividad de la fase gaseosa z = Distancia en la dirección de la transferencia de materia CA, , , CB, CT = concentraciones de A, de B y total del gas 7

Integrando: NA’ = k. G(PA 1 -PA 2) k. G = coeficiente de transferencia de masa para la absorción en la película gaseosa. Es una medida directa de la velocidad de absorción por unidad de área de la interfase con una fuerza impulsora igual a la unidad en la diferencia de las presiones parciales. k. G = Dv P R T z. G PBm 8

Difusión en la fase líquida: Para disoluciones diluidas: NA’ = k. L(CA 1 -CA 2) k. L = coeficiente de transferencia de masa para la película líquida. Para disoluciones diluidas: k. L = DL/z. L 9

Velocidad de absorción: En un proceso estacionario la velocidad de transferencia de materia en la película líquida es igual a la velocidad de transferencia en la película de líquido NA ’ = k. G (PG-Pi) = k. L(Ci-CL) PG = presión parcial en la masa del gas CL = concentración en la masa de líquido Pi y Ci = concentraciones en la interfase, en equilibrio 10
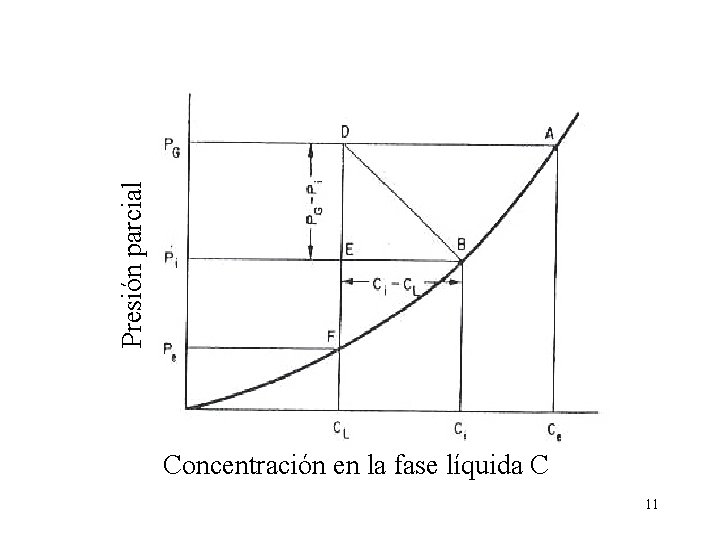
Presión parcial Concentración en la fase líquida C 11

La fuerza impulsora que provoca la transferencia en la fase gaseosa es : PG-Pi = DE La fuerza impulsora que provoca la transferencia en la fase líquida es: Ci-CL = BE 12

Por el punto D se traza una línea de pendiente –k. L/k. G la cual corta a la curva de equilibrio en B Coeficientes globales: NA’ = KG(PG-Pe) = KL(Ce-CL) KG y KL son los coeficientes globales de la fase gaseosa y líquida 13

La relación entre los coeficientes globales y los de película son: H es la constante de la ley de Henry 14

Velocidades en función de las fracciones molares N’A = k”G (y-yi) = K”G (y-ye) N’A = k”L(xi-x) = K”L (xe-x) donde x e y son las fracciones molares del componente soluble A en la fase líquida y en la fase gaseosa 15

k”G , k”L , K”G , K”L son los coeficientes de transferencia en función de las fracciones molares Si m es la pendiente de la curva de equilibrio: 16

Valores de los coeficientes de transferencia : 17
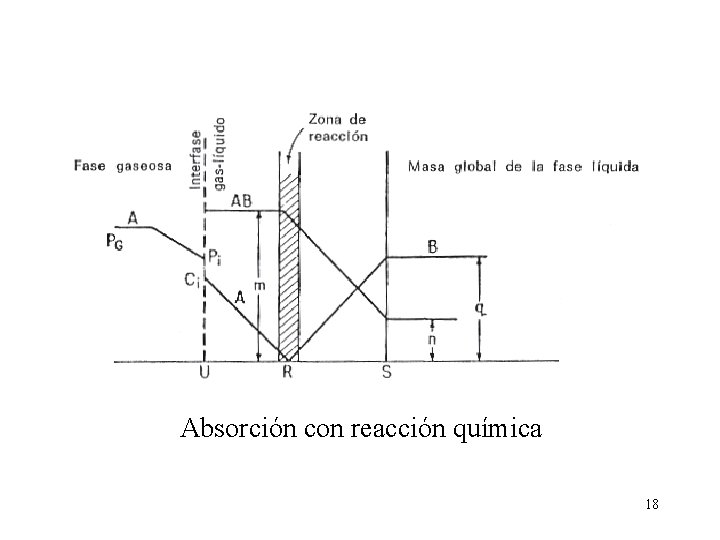
Absorción con reacción química 18
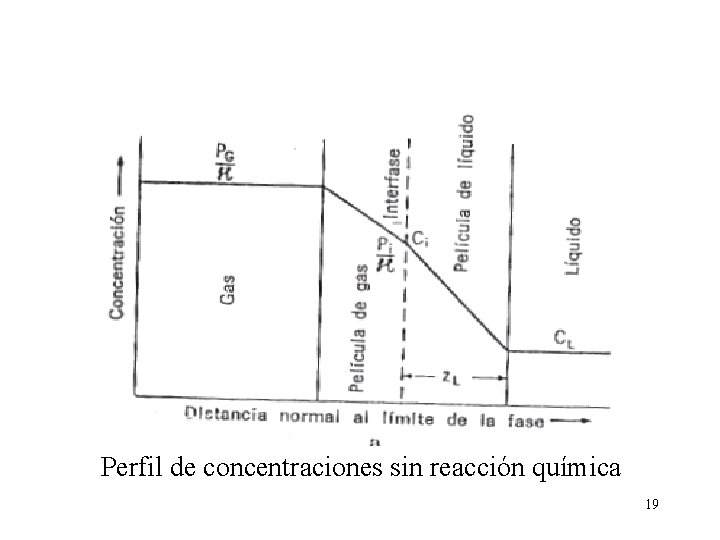
Perfil de concentraciones sin reacción química 19
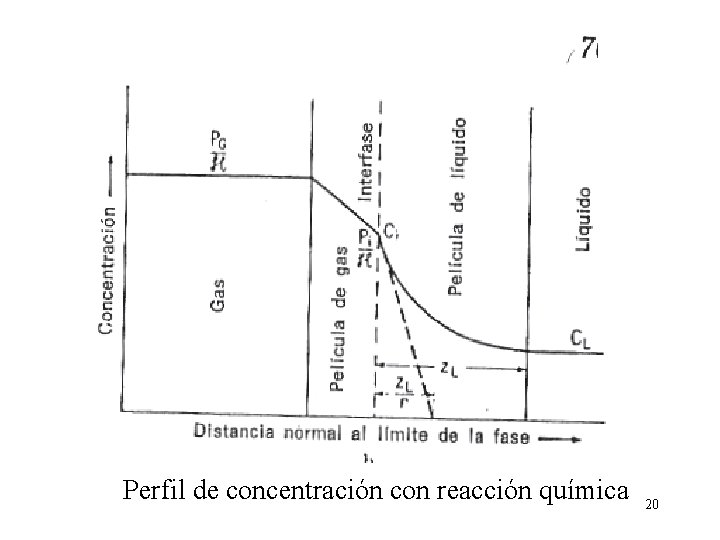
Perfil de concentración con reacción química 20
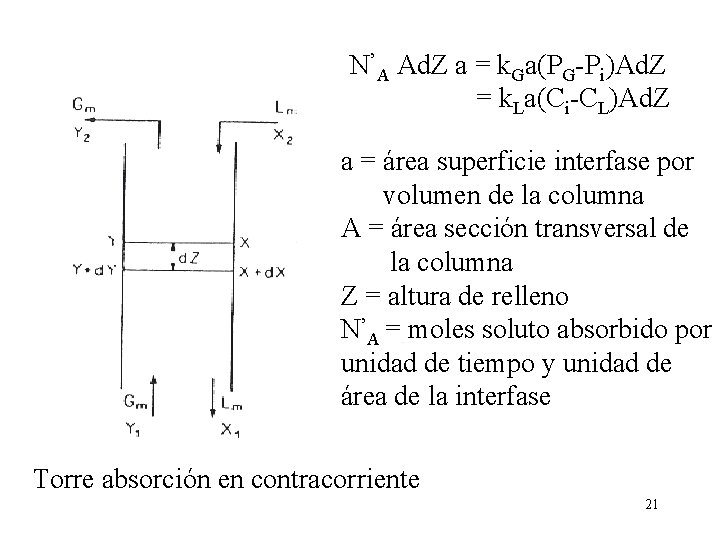
N’A Ad. Z a = k. Ga(PG-Pi)Ad. Z = k. La(Ci-CL)Ad. Z a = área superficie interfase por volumen de la columna A = área sección transversal de la columna Z = altura de relleno N’A = moles soluto absorbido por unidad de tiempo y unidad de área de la interfase Torre absorción en contracorriente 21

Altura de la columna en relación a la película gaseosa: Gm = moles de inertes/(tiempo área columna) Lm = moles líquido libre soluto/(tiempo área columna) Y = moles gas soluto A /moles gas B inerte fase gaseosa X = moles soluto A/ moles disolvente inerte fase líquida 22

Aplicando un balance al elemento dz de la columna los moles de soluto que dejan la fase gaseosa es igual a los moles captados por el líquido A Gm d. Y = A Lmm d. X resultando: Gm A d. Y = N’A a d. V = k. G a (PG-Pi) A d. Z 23

La altura Z de la columna necesaria para conseguir un cambio desde Y 1 en el fondo hasta Y 2 en la parte superior de la columna resulta de la expresión anterior 24

Altura de la columna en relación a la película líquida De forma análoga a la película gaseosa: para concentraciones diluidas con CT y k. L ctes 25

Altura basada en los coeficientes globales Si la fuerza impulsora basada en la concentración del gas es Y-Ye y KG es el coeficiente global del gas para la transferencia, la altura de la torre para concentraciones diluidas es: La segunda expresión se refiere a la concentración en el líquido Para concentraciones diluidas; Y≈ y, las expresiones 26 anteriores son válidas

Línea de operación Se efectúa un balance de materia para el soluto desde el fondo de la columna hasta un plano cualquiera en el que las proporciones molares son X e Y Esta ecuación es la línea de operación que pasa por (X 1, Y 1) y por (X 2, Y 2) representa las condiciones en un punto cualquiera de la columna 27
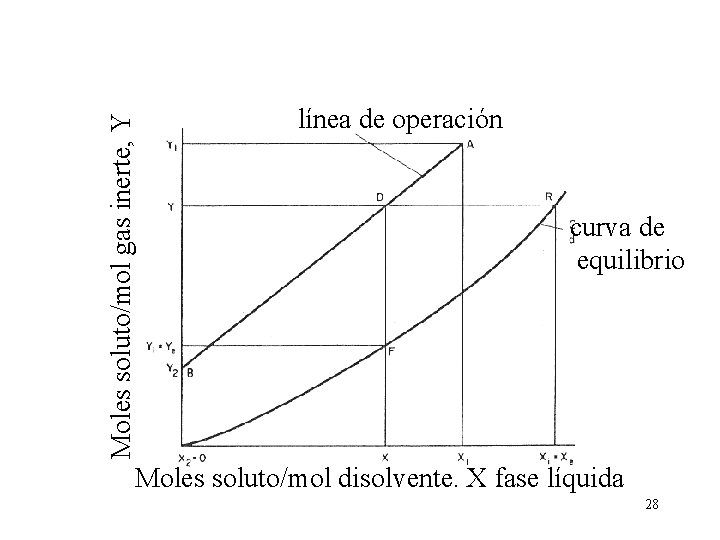
Moles soluto/mol gas inerte, Y línea de operación curva de equilibrio Moles soluto/mol disolvente. X fase líquida 28

En un proceso controlado por la película gaseosa la fuerza impulsora que provoca la transferencia es la distancia DF, siendo Yi = Ye se puede calcular Se dan valores a Y, se obtienen los valores de Yi mediante la curva de equilibrio y luego se obtiene la integral 29

Si el proceso está controlado por la película de líquido, Xi = Xe y la fuerza impulsora Xi-X está dada en el diagrama por el segmento DR. De Igual forma se calcula: Si la curva de equilibrio es una recta ye= mx+c, Para concentraciones bajas: 30

Para disoluciones concentradas 31

Si la pendiente DE permanece constante, es decir, k. L/k. G, fuerza impulsora a través de la fase gas entre DF, fuerza impulsora suponiendo que toda la resistencia se encuentra en la fase gas es constante. Esto permite utilizar indistintamente k. G y k. L 32
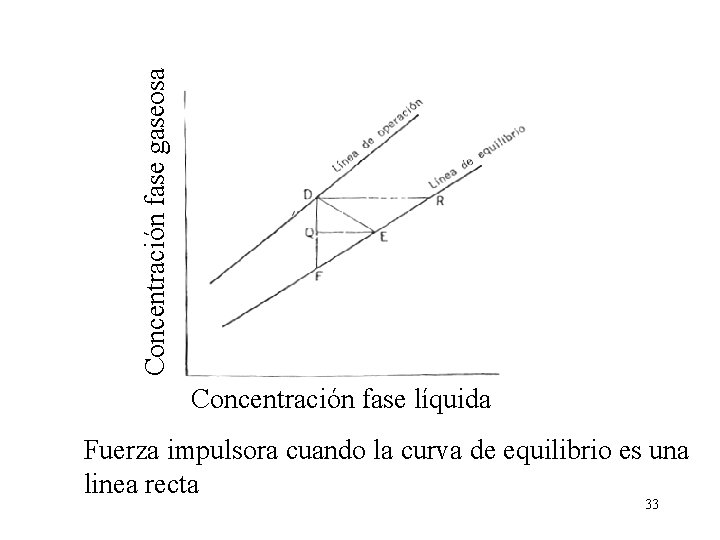
Concentración fase gaseosa Concentración fase líquida Fuerza impulsora cuando la curva de equilibrio es una linea recta 33

Altura de la columna en función de las presiones parciales a altas concentraciones Realizando un balance de materia entre el fondo de la columna y un plano en el que la presión parcial sea PG y la concentración en el líquido sea X 34

Para una pequeña altura d. Z de la columna; 35

Unidad de transferencia el número de unidades globales de transferencia NOG, es un valor integrado de la variación de la composición por unidad de fuerza impulsora y representa la dificultad de separación 36
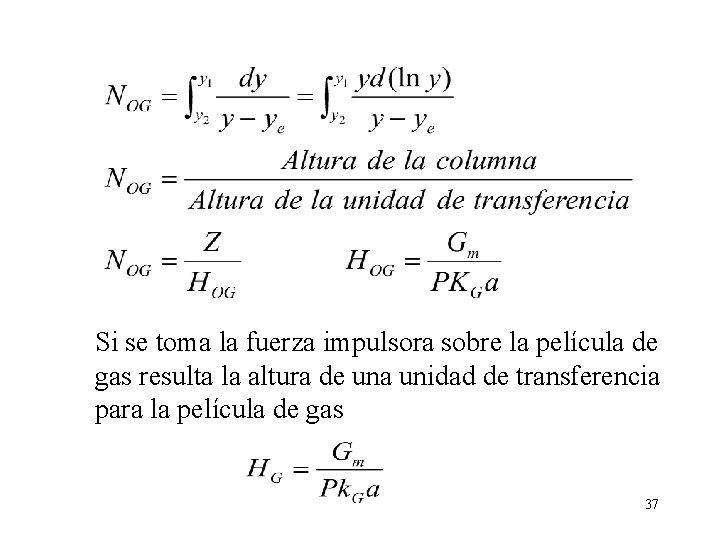
Si se toma la fuerza impulsora sobre la película de gas resulta la altura de una unidad de transferencia para la película de gas 37

De manera análoga se obtiene para la película de líquido, la altura de la unidad global de transferencia para el líquido: La altura para la unidad de transferencia para la película de líquido: CT es la densidad molar media del líquido 38

La relación entre las alturas globales y de película es: Para disoluciones concentradas Donde (1 -y)lm es la diferencia media logarítmica de 1 -yi 39

Velocidad del líquido, del gas y pendiente de la curva de equilibrio A bajas concentraciones coinciden aproximadamente las relaciones molares con las fracciones molares, es decir: x ≈ Xi e y ≈Yi resultando el balance: Siendo x e y las fracciones molares de soluto en las fases líquida y gaseosa y Gm y Lm son los flujos molares del gas y del líquido por unidad de área libre de disolvente. 40

Haciendo un balance entre la parte superior y un plano cualquiera en el que las fracciones molares son x e y: el disolvente que entra está libre de soluto, x 2 = 0 41

Se ha considerado concentraciones bajas así como la aplicación de la ley de Henry, ye = m x esta ecuación está representada gráficamente donde NOG está en función de y 1/y 2 para distintos valores del parámetro m. Gm/Lm 42
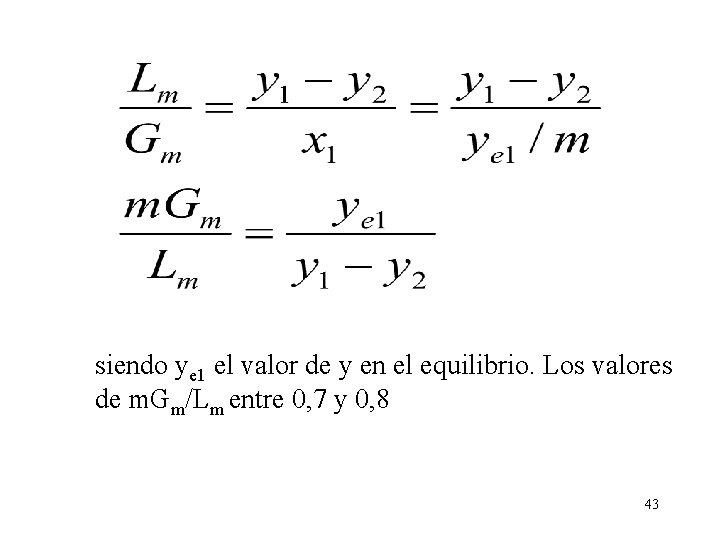
siendo ye 1 el valor de y en el equilibrio. Los valores de m. Gm/Lm entre 0, 7 y 0, 8 43
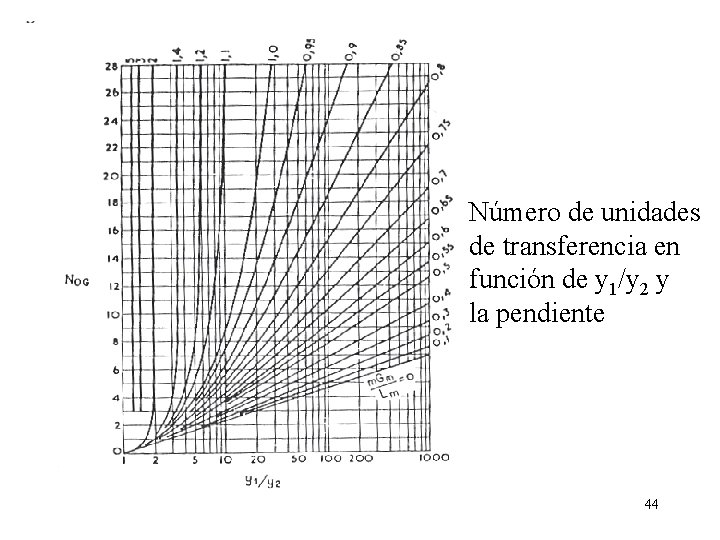
Número de unidades de transferencia en función de y 1/y 2 y la pendiente 44
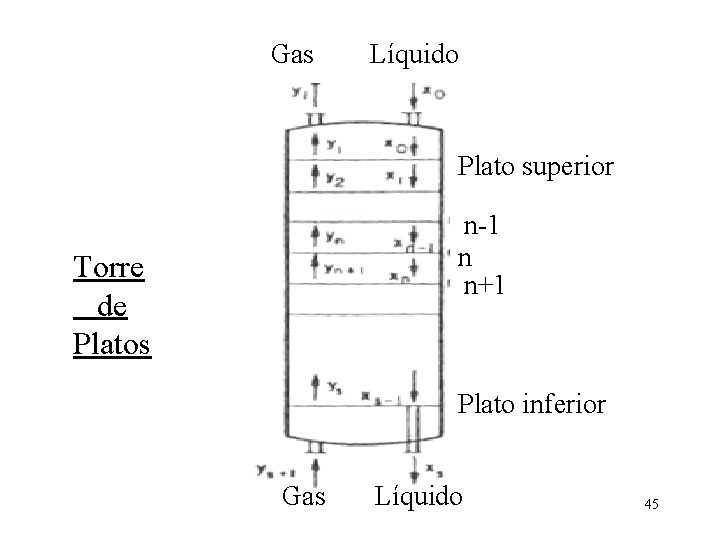
Gas Líquido Plato superior n-1 n n+1 Torre de Platos Plato inferior Gas Líquido 45

Lm = Flujo molar por unidad de área de líquido libre de soluto Gm = Flujo molar de gas inerte por unidad de área n = Plato numerado desde extremo superior hacia abajo x = Fracción molar del componente absorbido en el líquido y = Fracción molar del componente absorbido en el gas 46

Balance de materia para el componente absorbido desde el fondo hasta un plato situado por encima plato n: Gm yn + Lm xs = Gm ys+1 + Lm xn-1 Lm Lm yn = xn-1 + ys+1 xs Gm Gm Recta que pasa por A(xs, ys+1) y B(x 0, y 1) 47
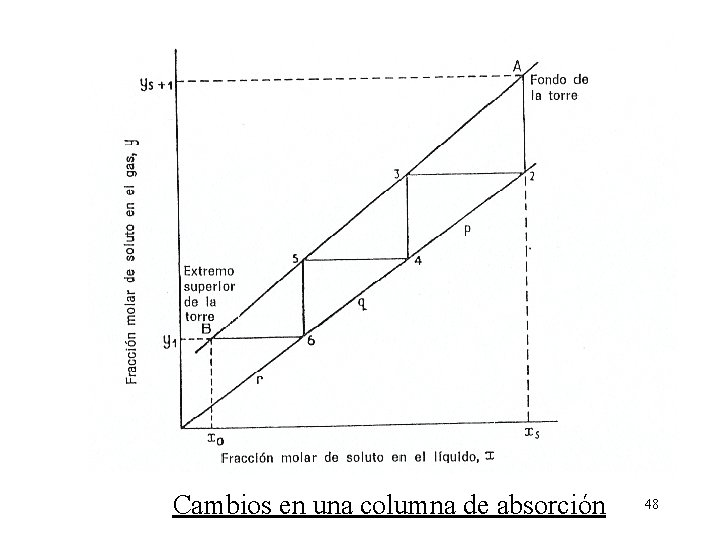
Cambios en una columna de absorción 48

Factor de absorción. Cálculo número de platos Balance de materia sobre el plato n: Lm (xn -xn-1) = Gm (yn+1 - yn) Curva de equilibrio está representada por y = mx para un plato ideal: yn = m xn Lm ( y –y ) = y - y n n-1 n+1 n m. Gm 49

Lm = A = constante = factor de absorción m Gm yn = yn+1 + A yn-1 1+A para el plato superior: y 1 = y 2 + A y 0 1+A 50

Para el plato n: yn= (An -1) yn+1 + An(A-1) y 0 An+1 - 1 Balance entre la parte superior hasta el plato n: A(yn-y 0) = yn+1 – y 1 yn+1 - y 1 An+1 - A = An+1 - 1 yn+1 – y 0 51

yn+1 – y 1 = cambio real en la composición del gas yn+1 – y 0 = cambio máximo posible en la composición del gas Para las concentraciones terminales, y 0 = m x 0 52
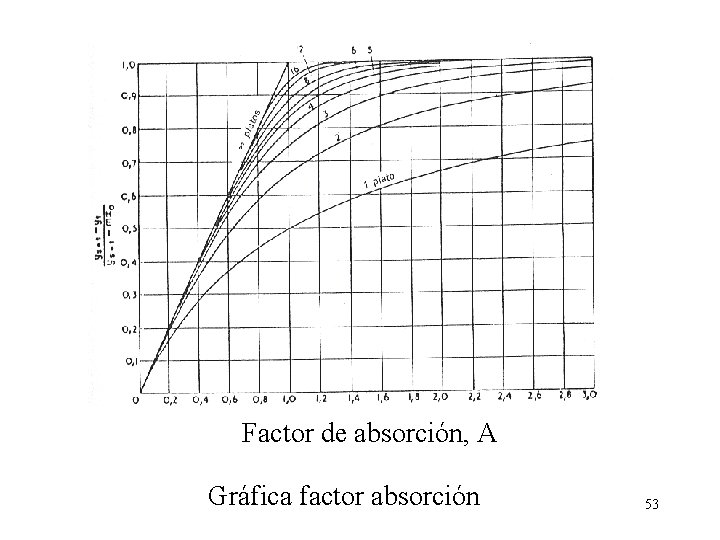
Factor de absorción, A Gráfica factor absorción 53
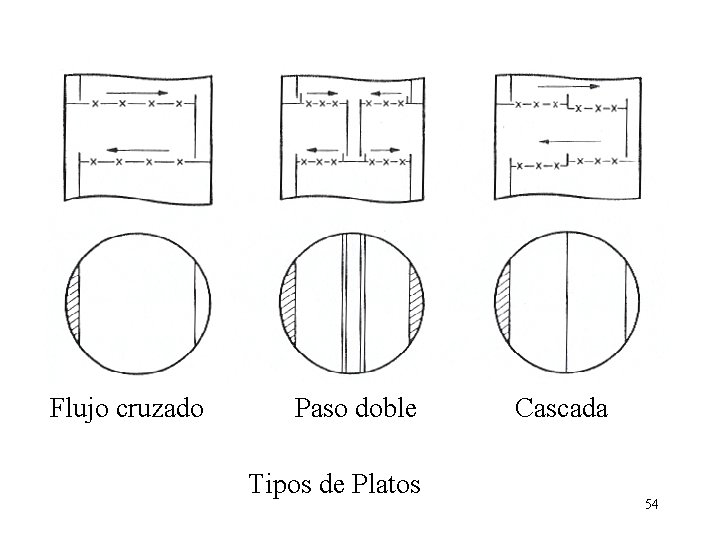
Flujo cruzado Paso doble Tipos de Platos Cascada 54
- Slides: 54