Abrange todos processo qumicos envolvem transferncia de eltrons

Abrange todos processo químicos envolvem transferência de elétrons. que Quando um processo químico ocorre, produzindo transferência de elétrons, é chamado de pilha ou bateria. 1
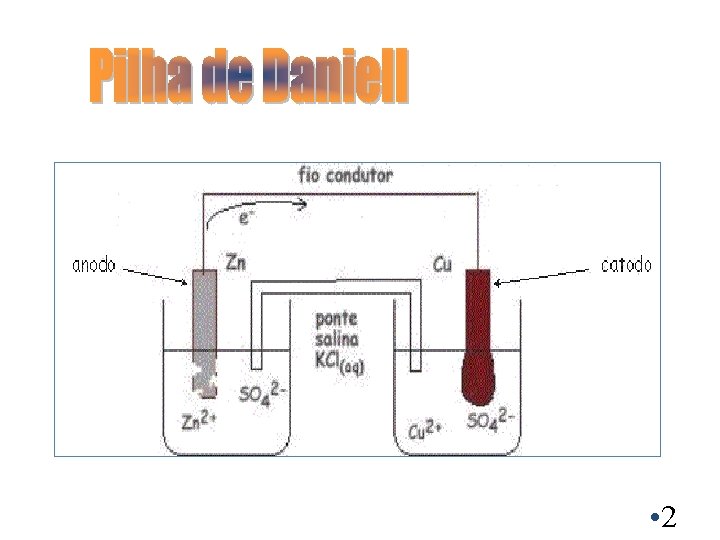
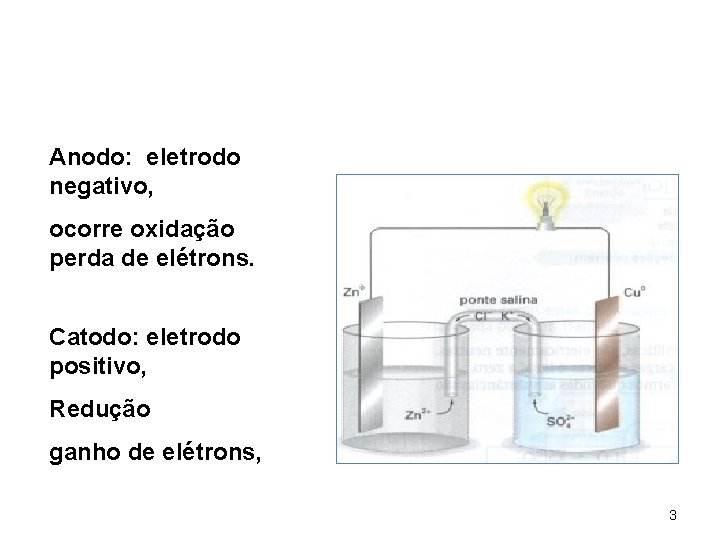
Anodo: eletrodo negativo, ocorre oxidação perda de elétrons. Catodo: eletrodo positivo, Redução ganho de elétrons, 3

Cu 2+ +2 e- --> Cu(s) o íon cobre (Cu 2+) da solução é reduzido por 2 e- que vem da corrente elétrica. Zn(s) --> Zn 2+ + 2 eo zinco é oxidado, formando íon zinco (Zn 2+) e 2 e-. Estes elétrons serão os responsáveis pela geração da corrente elétrica do sistema (pilha). 4

Cu 2+ + 2 e- --> Cu 0 Zn 0 --> Zn 2+ + 2 e_________ Zn 0 + Cu 2+ --> Zn 2+ + Cu 0 Reação global Com o desenvolvimento da reação, ocorrerá formação de cobre metálico, que se depositará na superfície do eletrodo de cobre, já o eletrodo de zinco será corroído, pois o zinco está se transformando em íons que irão para a solução de sulfato de zinco. 5

A pilha de Daniell pode ser escrita por: Zn 0 + Cu 2+(aq) --> Zn 2+(aq) + Cu 0 ou Zn | Zn 2+ || Cu 2+ | Cu onde, || representa a ponte salina 6
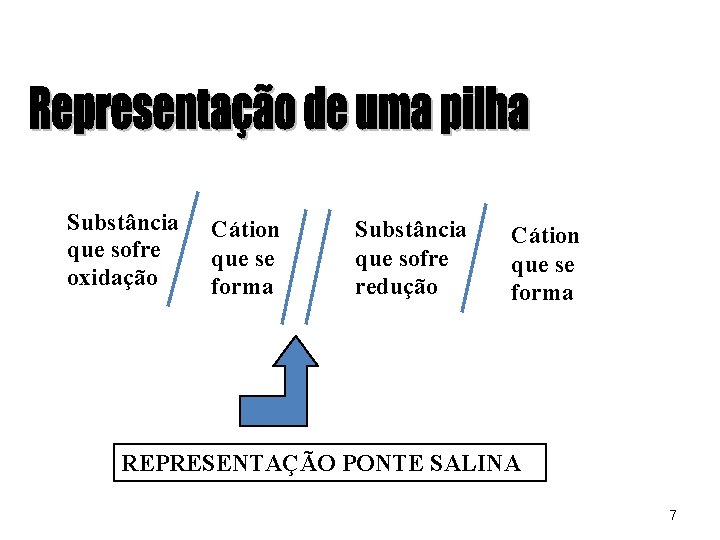
Substância que sofre oxidação Cátion que se forma Substância que sofre redução Cátion que se forma REPRESENTAÇÃO PONTE SALINA 7

ØToda pilha possui um potencial, ou seja, produz uma voltagem, sendo este potencial medido na pilha. Eºoxi=Potencial de oxidação Eºred=Potencial de redução Facilidade da espécie em sofrer oxidação Facilidade da espécie em sofrer redução Znº/Zn+2 Eºoxi=+0, 76 v Zn+2/Znº Eºoxi=-0, 76 v Naº/Na+ Eºoxi=+2, 71 v Na+/Naº Eºoxi=-2, 71 8

ØO potencial da pilha pode ser dado, de uma maneira simplificada por: E = Eoxi- Ered sendo Eoxie Ered, os potenciais padrões de redução de cada semi equação ddp= Eº oxi do metal que perde elétrons - Eº oxi do metal que ganha elétrons ØÉ a partir do potencial de uma pilha, que se sabe se a reação ocorre ou não. 9

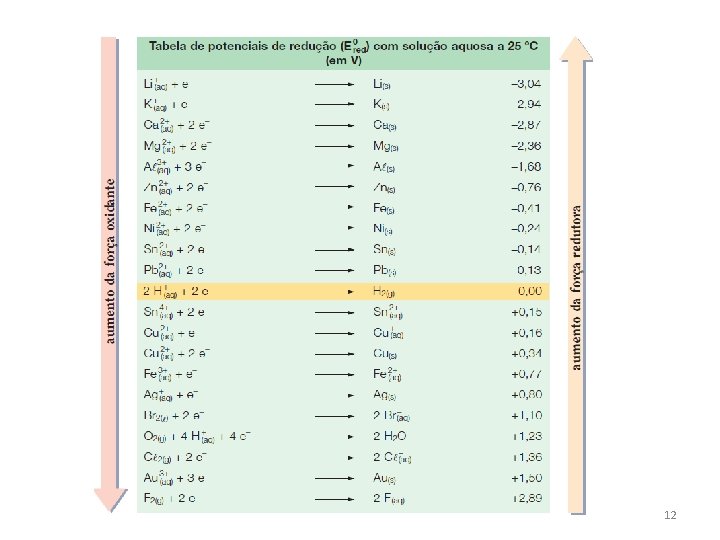
Quando a variação de potencial da pilha, E, é maior que zero a reação é espontânea. Quando o potencial é negativo, a reação não ocorre espontaneamente e quanto maior for o potencial, positivo, maior será a eficiência da pilha. Obs Todo elemento que possui maior Eºoxidação é capaz de deslocar outro de menor potencial. Ex: Fe Eºoxi=+0, 44 e Cu Eºoxi=- 0, 34 O Fe tende a deslocar o Cu. 10

Medidas dos potenciais • Para determinar os Ered e os Eoxi das diversas espécies, foi escolhido como padrão o eletrodo de hidrogênio, que consiste em um fio de platina (Pt) no interior de um tubo de vidro preenchido com gás hidrogênio (H 2)*. O fio de platina está ligado a uma placa de platina em que o H 2(g) fica adsorvido, e a platina não participa da reação. O conjunto está imerso em uma solução ácida, em que a concentração dos íons H+ é 1 mol/L, à pressão de 1 atm. Por convenção, foi atribuído a este eletrodo o valor zero, tanto para seu E°oxi como para o E°red. 11
12

Cálculo da voltagem (ΔE) das pilhas elétrons fluem do eletrodo em que ocorre oxidação (ânodo) para o eletrodo em que ocorre redução (cátodo), através do fio externo. voltímetro: força eletromotriz (fem ou E) valor indicado pelo voltímetro, em volts (V), corresponde à força eletromotriz da pilha. 13

ΔE é medido na chamada condição-padrão, que corresponde a espécies com concentração 1 mol/L e possíveis gases envolvidos com pressão de 1 atmosfera a 25 ºC. Nessas condições, a diferença de potencial da pilha será representada por ΔEº. 14

Eº red = = – 2, 36 V. Mg Eºº Oxid = +0, 24 V. Ni 15

16

17
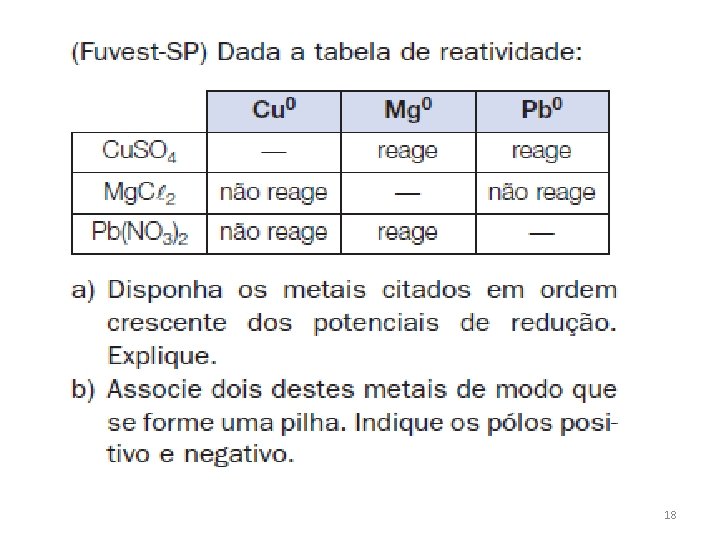
18

(UFRJ) Os quatro frascos apresentados a seguir contêm soluções salinas de mesma concentração molar, a 25 o. C. Em cada frasco, encontra-se uma placa metálica mergulhada na solução. a) Identifique o frasco em que ocorre reação química espontânea e escreva a respectiva equação. b) Sabendo que o frasco III contém 304 gramas de Fe. SO 4 em 2 litros de solução, determine a concentração, em g/L, da solução de Zn. SO 4 no frasco I. 19

1. Com o passar do tempo, objetos de prata geralmente adquirem manchas escuras que são películas de sulfeto de prata (Ag 2 S) formadas na reação da prata compostos que contém enxofre encontrados em vários alimentos. Um dos processos para limpar o objeto escurecido consiste em colocá-lo em um recipiente de alumínio contendo água e detergente e aquecer até a fervura. O detergente retira a gordura do objeto facilitando a reação do alumínio da panela com o sulfeto de prata, regenerando a prata com seu brilho característico. 2 Al + 3 Ag 2 S → Al 2 S 3 + 6 Ag Sobre o assunto relativo ao texto acima, escreva V para as afirmativas verdadeiras ou F para as afirmativas falsas. ( ) A prata ao adquirir manchas escuras sofre oxidação. ( ) Na reação entre alumínio e o sulfeto de prata, o alumínio é o ânodo do processo. ( ) A prata possui maior potencial de oxidação do que o alumínio. ( ) A presença do detergente na água diminui o potencial de oxidação do alumínio. ( ) O alumínio é menos reativo do que a prata. 20

21

(Cefet-MG) Nos processos de transporte subterrâneo, as tubulações de ferro têm barras de magnésio ligadas, conforme o desenho abaixo. 22

4. (FMTM-MG) Considerando a ampla utilização dos metais no mundo moderno, a corrosão do metal ferro é um problema de grande importância nos países industrializados. Estudos realizados sobre o assunto mostram que o contato com certos metais pode retardar, impedir ou acelerar a formação de ferrugem. Considere a ilustração a seguir e os potenciaispadrão de redução fornecidos na tabela 23
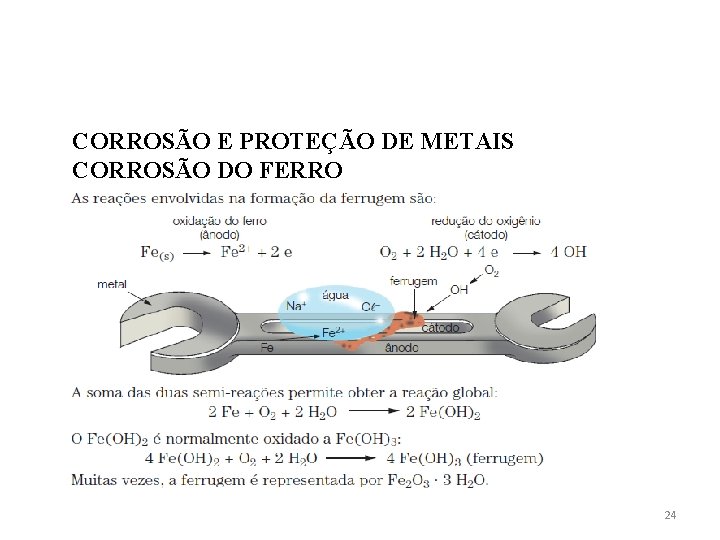
CORROSÃO E PROTEÇÃO DE METAIS CORROSÃO DO FERRO 24
- Slides: 24