ABORDAJE Y TRATAMENTO DEL PACIENTE CON INSUFICIENCIA RENAL

ABORDAJE Y TRATAMENTO DEL PACIENTE CON INSUFICIENCIA RENAL CRONICA Y VIRUS C CRONICO VI Curso Superior Universitario de Nefrología Dr. Martin Barrabino Jefe De La Unidad De Hígado Subjefe del Programa de Trasplante Hepático Hospital Privado Universitario De Córdoba

Declaro tener CONFLICTO DE INTERESES por haber sido sponsoreado en actividades de capacitación científica en cursos, congresos o reuniones , y contratado para realizar tareas de difusión, divulgación científica o investigación clínica por parte de: • • • Gilead Argentina Abbvie Novartis Argentina Gador Merck Argentina Bayer Internacional Sandoz Argentina Pfiser Argentina Bristol Argentina Richmond Sanofi

DESDE EL DESCUBRIMIENTO DEL VIRUS AL PLAN DE ELIMINACION EN 2030 Pan-genotypic era 1989: Identificacion del Virus HCV 1984 1989 1998 2001 “non-A, non-B” hepatitis The IFN era 2016: OMS establece el “DAA revolution” objetivo como estrategia mayor de eliminacion de Early era of DAA’s Salud Publica para el 2030 2011 2013 2014 2015 2016 2017…
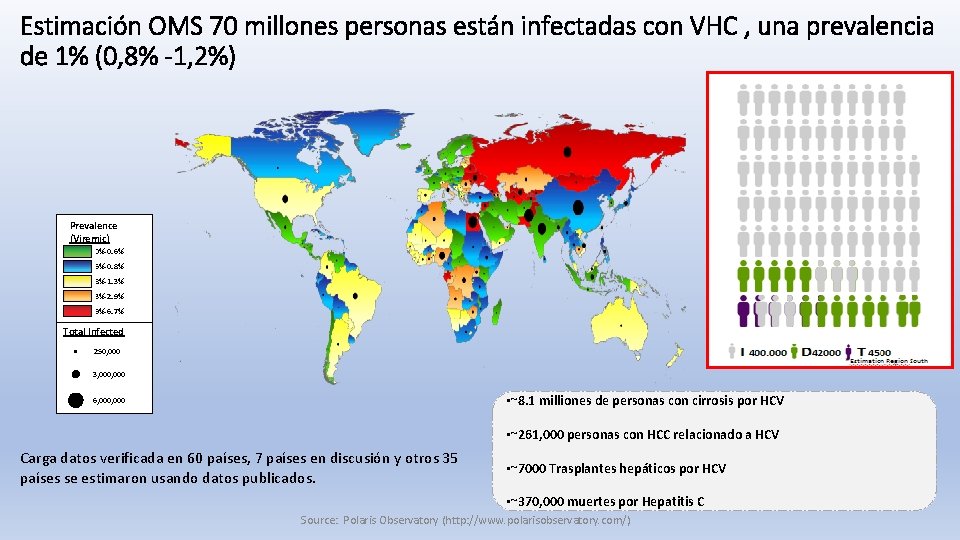
Estimación OMS 70 millones personas están infectadas con VHC , una prevalencia de 1% (0, 8% -1, 2%) Prevalence (Viremic) 0. 0%-0. 6%-0. 8%-1. 3%-2. 9%-6. 7% Total Infected 250, 000 3, 000 • ~8. 1 milliones de personas con cirrosis por HCV 6, 000 • ~261, 000 personas con HCC relacionado a HCV Carga datos verificada en 60 países, 7 países en discusión y otros 35 países se estimaron usando datos publicados. • ~7000 Trasplantes hepáticos por HCV • ~370, 000 muertes por Hepatitis C Source: Polaris Observatory (http: //www. polarisobservatory. com/)

MORTALIDAD EN LATINOAMERICA Sistema Regional de Mortalidad, 2015. Pan American Health Organization. http: //www. paho. org
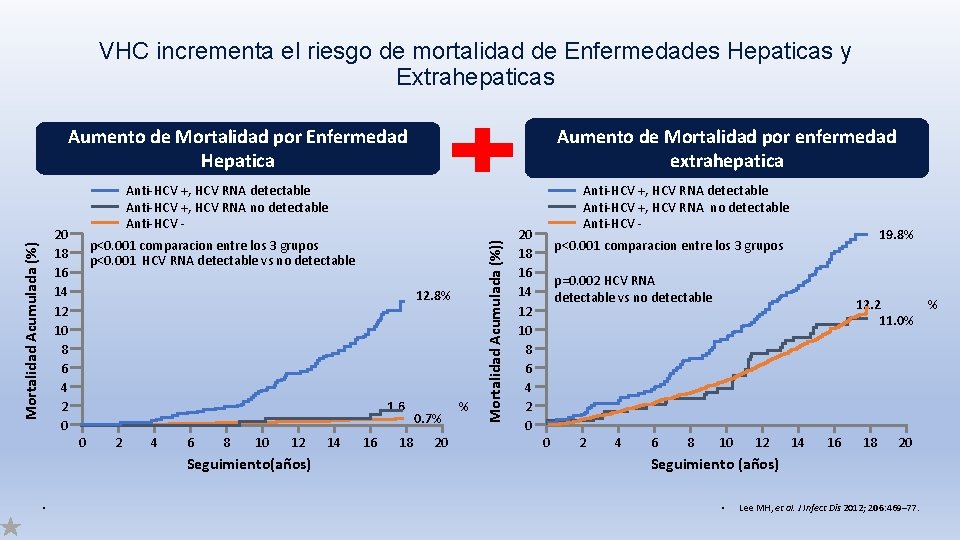
VHC incrementa el riesgo de mortalidad de Enfermedades Hepaticas y Extrahepaticas Aumento de Mortalidad por enfermedad extrahepatica Aumento de Mortalidad por Enfermedad Hepatica p<0. 001 comparacion entre los 3 grupos p<0. 001 HCV RNA detectable vs no detectable 12. 8% 1. 6 0 2 4 6 8 10 12 Seguimiento(años) • 14 16 18 0. 7% 20 % Mortalidad Acumulada (%)) Mortalidad Acumulada (%) 20 18 16 14 12 10 8 6 4 2 0 Anti-HCV +, HCV RNA detectable Anti-HCV +, HCV RNA no detectable Anti-HCV - 19. 8% p<0. 001 comparacion entre los 3 grupos p=0. 002 HCV RNA detectable vs no detectable 0 2 4 6 8 12. 2 % 11. 0% 10 12 14 16 18 20 Seguimiento (años) • Lee MH, et al. J Infect Dis 2012; 206: 469– 77.
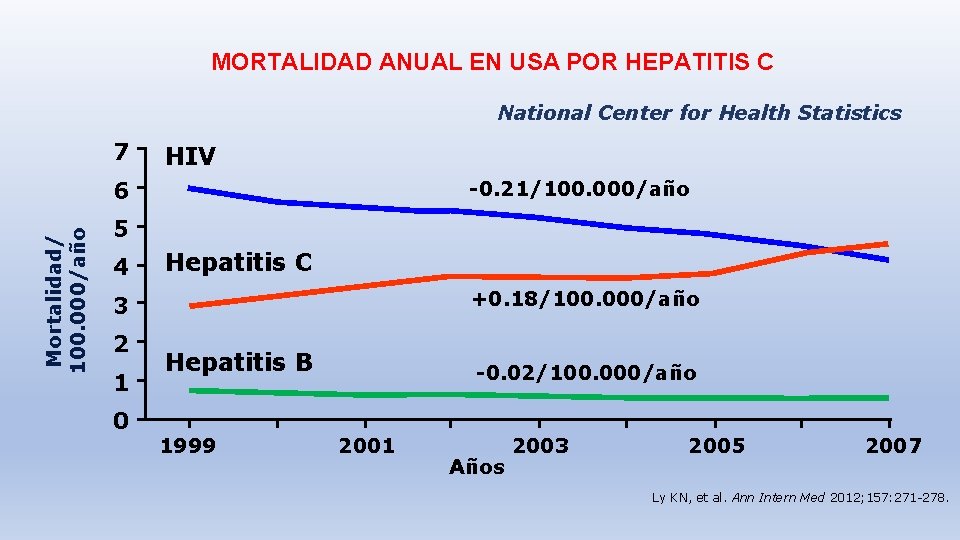
MORTALIDAD ANUAL EN USA POR HEPATITIS C National Center for Health Statistics 7 HIV Mortalidad/ 100. 000/año 6 -0. 21/100. 000/año 5 4 Hepatitis C +0. 18/100. 000/año 3 2 1 0 Hepatitis B 1999 -0. 02/100. 000/año 2001 Años 2003 2005 2007 Ly KN, et al. Ann Intern Med 2012; 157: 271 -278.
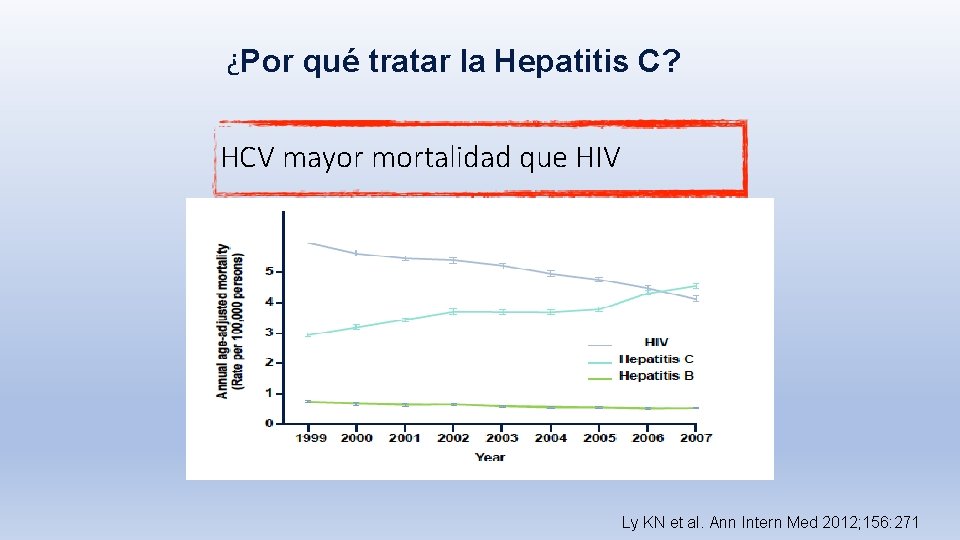
¿Por qué tratar la Hepatitis C? HCV mayor mortalidad que HIV Ly KN et al. Ann Intern Med 2012; 156: 271
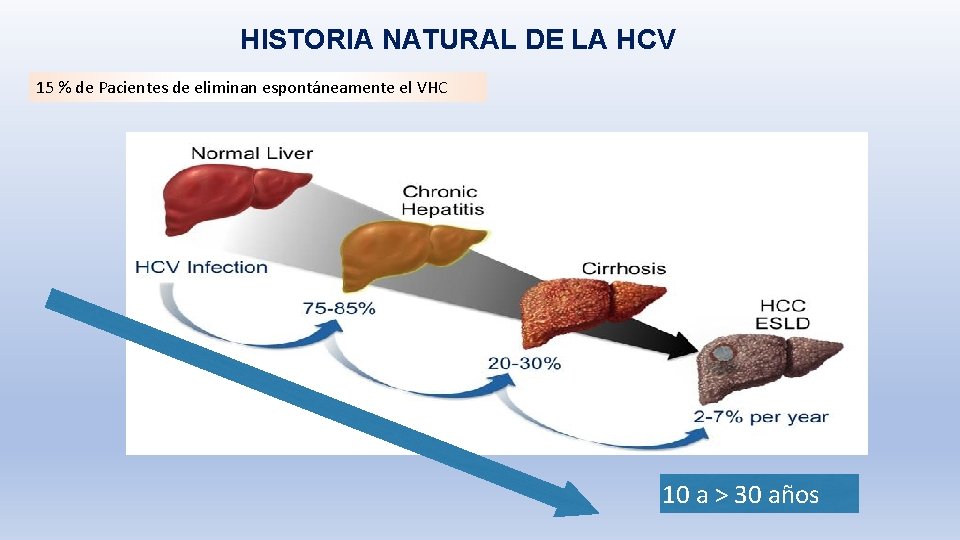
HISTORIA NATURAL DE LA HCV 15 % de Pacientes de eliminan espontáneamente el VHC 10 a > 30 años
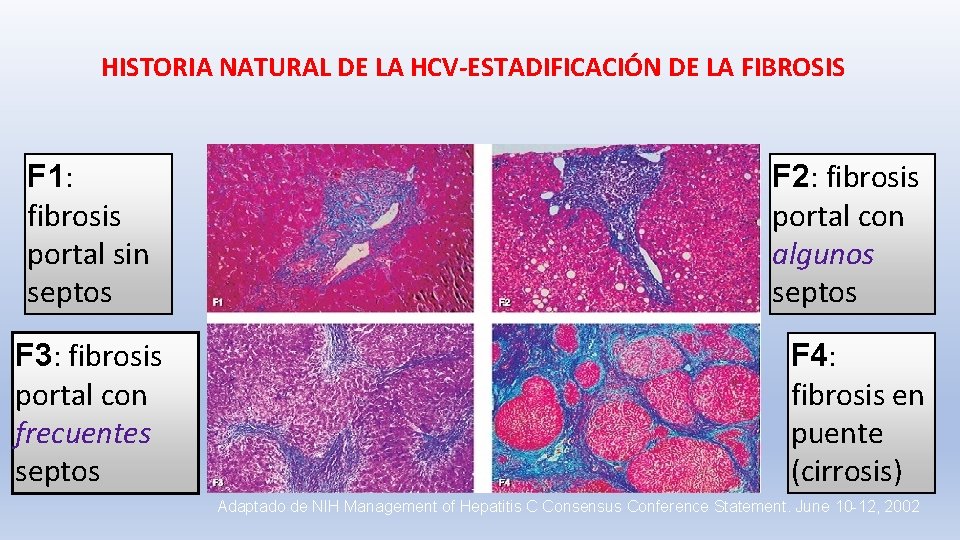
HISTORIA NATURAL DE LA HCV-ESTADIFICACIÓN DE LA FIBROSIS F 1: fibrosis portal sin septos F 3: fibrosis portal con frecuentes septos F 2: fibrosis portal con algunos septos F 4: fibrosis en puente (cirrosis) Adaptado de NIH Management of Hepatitis C Consensus Conference Statement. June 10 -12, 2002
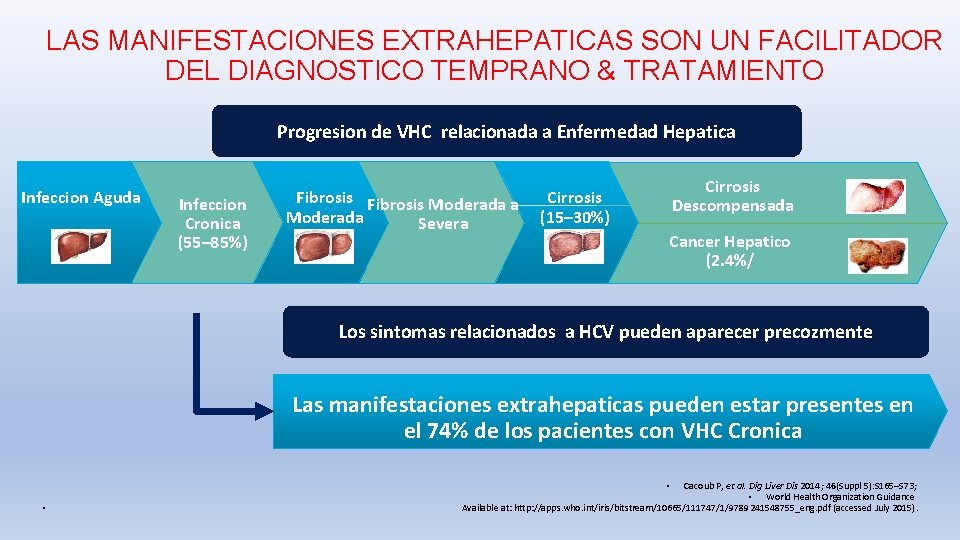
LAS MANIFESTACIONES EXTRAHEPATICAS SON UN FACILITADOR DEL DIAGNOSTICO TEMPRANO & TRATAMIENTO Progresion de VHC relacionada a Enfermedad Hepatica Infeccion Aguda Infeccion Cronica (55– 85%) Fibrosis Moderada a Cirrosis Moderada (15– 30%) Severa Cirrosis Descompensada Cancer Hepatico (2. 4%/ Los sintomas relacionados a HCV pueden aparecer precozmente Las manifestaciones extrahepaticas pueden estar presentes en el 74% de los pacientes con VHC Cronica Cacoub P, et al. Dig Liver Dis 2014; 46(Suppl 5): S 165–S 73; • World Health Organization Guidance Available at: http: //apps. who. int/iris/bitstream/10665/111747/1/9789241548755_eng. pdf (accessed July 2015). • •
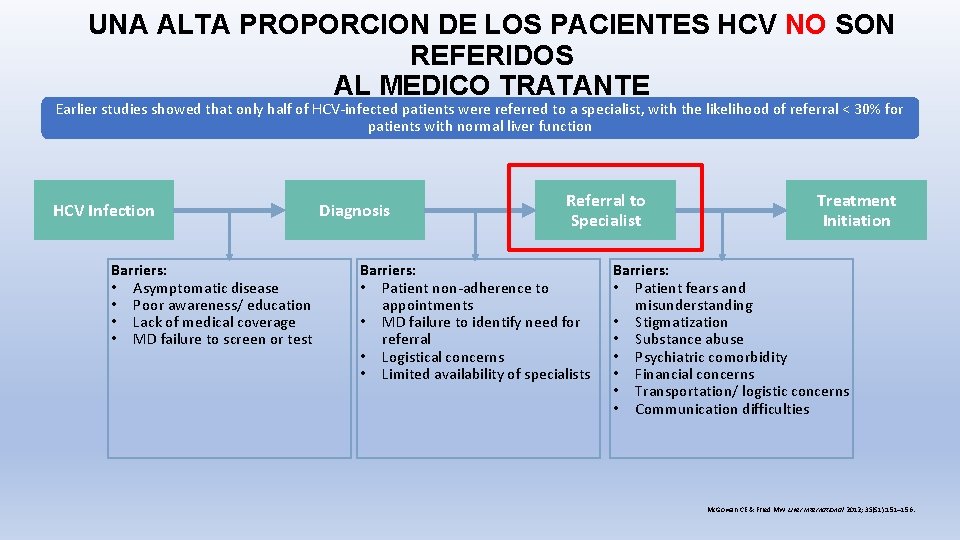
UNA ALTA PROPORCION DE LOS PACIENTES HCV NO SON REFERIDOS AL MEDICO TRATANTE Earlier studies showed that only half of HCV-infected patients were referred to a specialist, with the likelihood of referral < 30% for patients with normal liver function HCV Infection Barriers: • Asymptomatic disease • Poor awareness/ education • Lack of medical coverage • MD failure to screen or test Diagnosis Referral to Specialist Barriers: • Patient non-adherence to appointments • MD failure to identify need for referral • Logistical concerns • Limited availability of specialists Treatment Initiation Barriers: • Patient fears and misunderstanding • Stigmatization • Substance abuse • Psychiatric comorbidity • Financial concerns • Transportation/ logistic concerns • Communication difficulties Mc. Gowan CE & Fried MW Liver International 2012; 35(S 1): 151– 156.

RETRASAR EL TRATAMIENTO IMPONE COSTOS A LAS PERSONAS Y A LOS SISTEMAS DE ATENCIÓN SANITARIA UN ESTUDIO ESTIMÓ UN AHORRO DE £ 27. 804 EN GASTOS (GASTOS POR DISCAPACIDAD Y REDUCCIÓN DE AUSENTISMO LABORAL) MEJORAS EN LA FUNCIÓN HEPÁTICA (EVITA TRASPLANTES) REDUCCIÓN DEL 70% EN RIESGO DE CARCINOMA HEPATOCELULAR (CHC) REDUCCIÓN EN EL RIESGO DE MUERTE UNA ENCUESTA A 5 PAÍSES EUROPEOS ESTIMÓ QUE: • Nuno Solinis, . "Value of Treating All Stages of Chronic Hepatitis C: A Comprehensive Review of Clinical and Economic Evidence 491 -508. Springer. Link. 25 Oct. 2016. • Papatheodoridis, GV, et al. Hepatitis C: The beginning of the end—key elements for successful European and national • Abb. Vie, Argentina
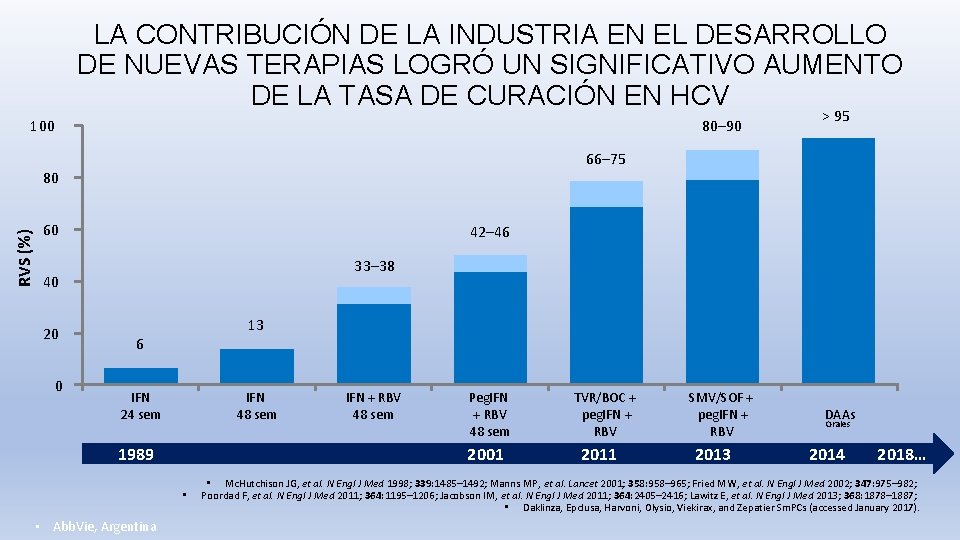
LA CONTRIBUCIÓN DE LA INDUSTRIA EN EL DESARROLLO DE NUEVAS TERAPIAS LOGRÓ UN SIGNIFICATIVO AUMENTO DE LA TASA DE CURACIÓN EN HCV 80– 90 100 66– 75 RVS (%) 80 60 42– 46 33– 38 40 20 0 > 95 13 6 IFN 24 sem IFN 48 sem IFN + RBV 48 sem Peg. IFN + RBV 48 sem TVR/BOC + peg. IFN + RBV SMV/SOF + peg. IFN + RBV DAAs Orales 1989 2001 2013 2014 2018… • • Abb. Vie, Argentina • Mc. Hutchison JG, et al. N Engl J Med 1998; 339: 1485– 1492; Manns MP, et al. Lancet 2001; 358: 958– 965; Fried MW, et al. N Engl J Med 2002; 347: 975– 982; Poordad F, et al. N Engl J Med 2011; 364: 1195– 1206; Jacobson IM, et al. N Engl J Med 2011; 364: 2405– 2416; Lawitz E, et al. N Engl J Med 2013; 368: 1878– 1887; • Daklinza, Epclusa, Harvoni, Olysio, Viekirax, and Zepatier Sm. PCs (accessed January 2017).
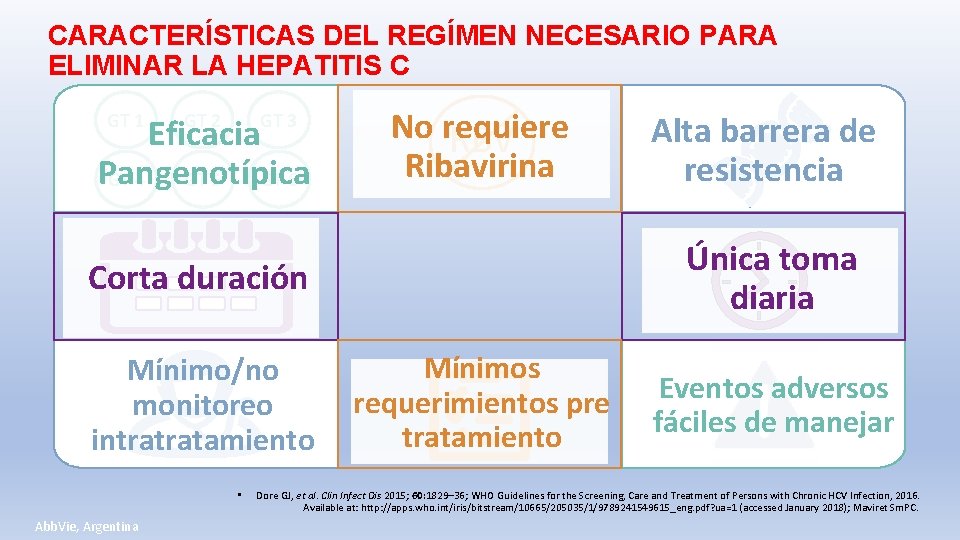
CARACTERÍSTICAS DEL REGÍMEN NECESARIO PARA ELIMINAR LA HEPATITIS C GT 1 GT 2 GT 3 Eficacia Pangenotípica GT 4 GT 5 GT 6 No requiere RBV Ribavirina Única toma diaria Corta duración Mínimo/no monitoreo intratratamiento • Abb. Vie, Argentina Alta barrera de resistencia Mínimos requerimientos pre tratamiento Eventos adversos fáciles de manejar Dore GJ, et al. Clin Infect Dis 2015; 60: 1829– 36; WHO Guidelines for the Screening, Care and Treatment of Persons with Chronic HCV Infection, 2016. Available at: http: //apps. who. int/iris/bitstream/10665/205035/1/9789241549615_eng. pdf? ua=1 (accessed January 2018); Maviret Sm. PC.
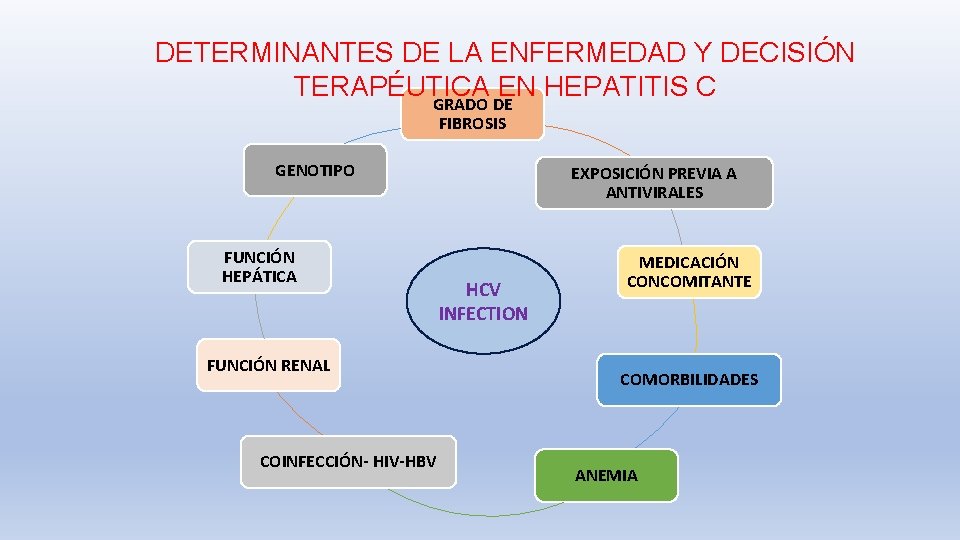
DETERMINANTES DE LA ENFERMEDAD Y DECISIÓN TERAPÉUTICA EN HEPATITIS C GRADO DE FIBROSIS GENOTIPO FUNCIÓN HEPÁTICA FUNCIÓN RENAL COINFECCIÓN- HIV-HBV EXPOSICIÓN PREVIA A ANTIVIRALES HCV INFECTION MEDICACIÓN CONCOMITANTE COMORBILIDADES ANEMIA
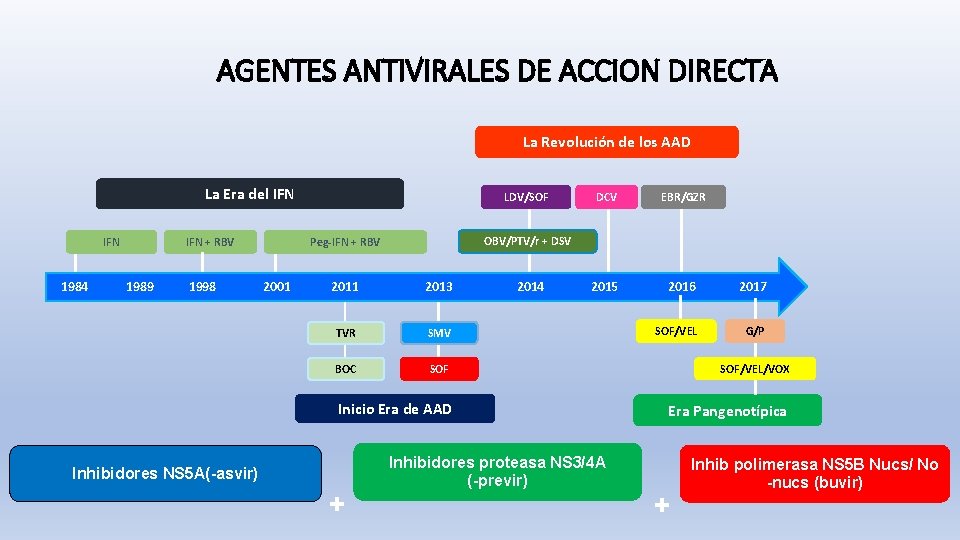
AGENTES ANTIVIRALES DE ACCION DIRECTA La Revolución de los AAD La Era del IFN + RBV IFN 1984 1989 1998 Inhibidores NS 5 A(-asvir) LDV/SOF EBR/GZR 2015 2016 2017 SOF/VEL G/P OBV/PTV/r + DSV Peg-IFN + RBV 2001 DCV 2011 2013 TVR SMV BOC SOF/VEL/VOX Inicio Era de AAD Era Pangenotípica + 2014 Inhibidores proteasa NS 3/4 A (-previr) + Inhib polimerasa NS 5 B Nucs/ No -nucs (buvir)
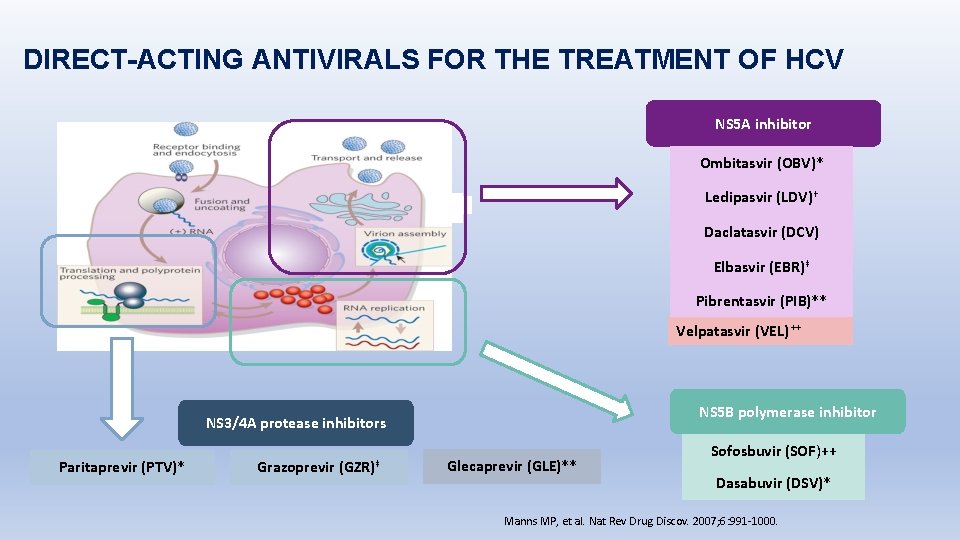
DIRECT-ACTING ANTIVIRALS FOR THE TREATMENT OF HCV NS 5 A inhibitor Ombitasvir (OBV)* Ledipasvir (LDV)† Daclatasvir (DCV) Elbasvir (EBR)‡ Pibrentasvir (PIB)** Velpatasvir (VEL) ++ NS 5 B polymerase inhibitor NS 3/4 A protease inhibitors Paritaprevir (PTV)* Grazoprevir (GZR)‡ Glecaprevir (GLE)** Sofosbuvir (SOF)++ Dasabuvir (DSV)* Manns MP, et al. Nat Rev Drug Discov. 2007; 6: 991 -1000.
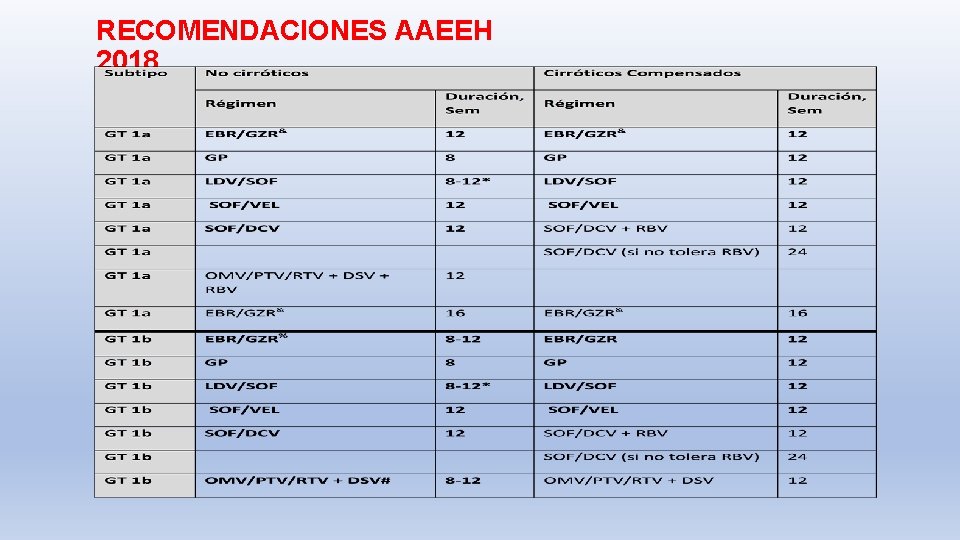
RECOMENDACIONES AAEEH 2018
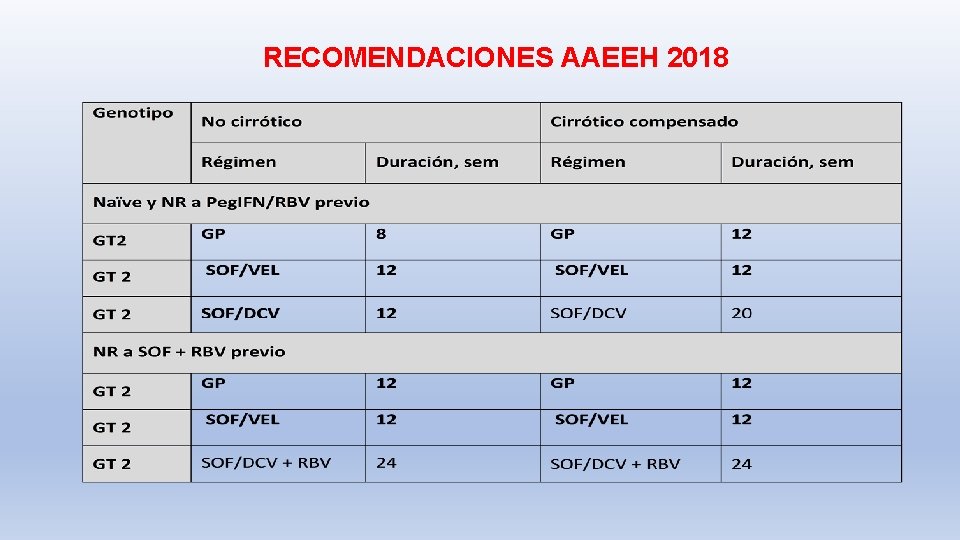
RECOMENDACIONES AAEEH 2018
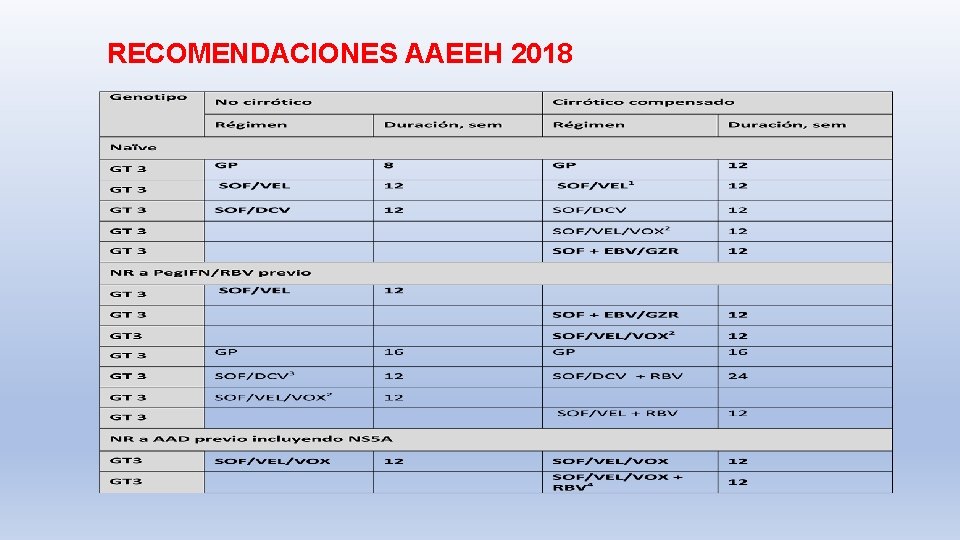
RECOMENDACIONES AAEEH 2018

CAMBIO DE PARADIGMA: LA HEPATITIS C ES UNA ENFERMEDAD SISTÉMICA • Journal of Hepatology 2016 vol. 65 j S 109–S 119 Abb. Vie, Argentina
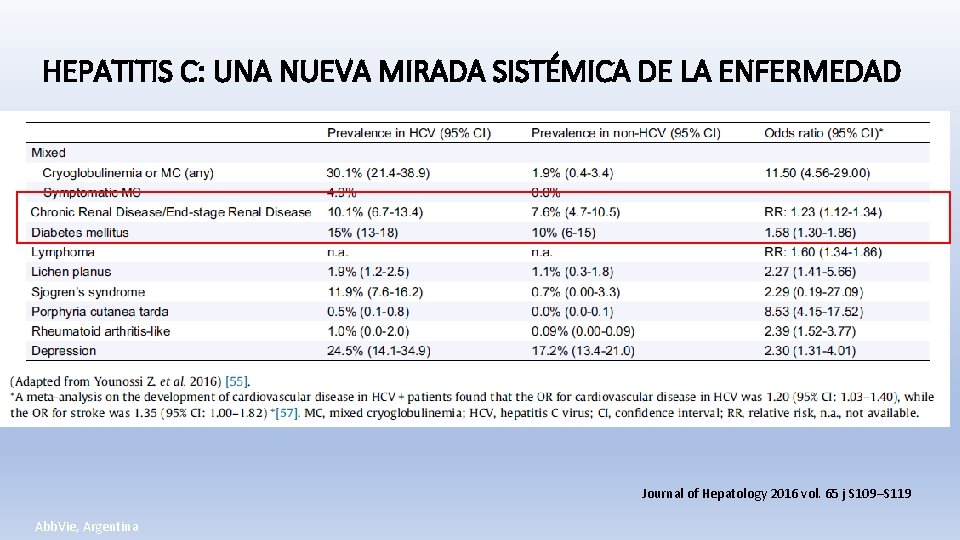
HEPATITIS C: UNA NUEVA MIRADA SISTÉMICA DE LA ENFERMEDAD Journal of Hepatology 2016 vol. 65 j S 109–S 119 Abb. Vie, Argentina

El HCV aumenta 32 veces la muerte de causa hepática El HCV aumenta 2. 4 veces la mortalidad Relación con muerte cardiovascular y ACV, asociado con el síndrome metabólico Analizar este punto es fundamental Journal of Hepatology 2016 vol. 65 j S 109–S 119
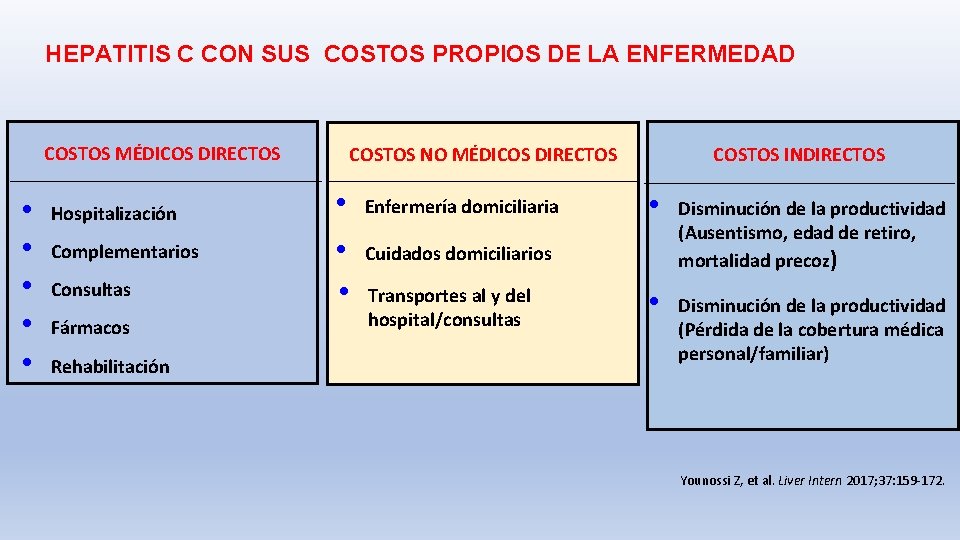
HEPATITIS C CON SUS COSTOS PROPIOS DE LA ENFERMEDAD COSTOS MÉDICOS DIRECTOS • • • Hospitalización Complementarios Consultas Fármacos Rehabilitación COSTOS NO MÉDICOS DIRECTOS • • • Enfermería domiciliaria COSTOS INDIRECTOS • Disminución de la productividad (Ausentismo, edad de retiro, mortalidad precoz) • Disminución de la productividad (Pérdida de la cobertura médica personal/familiar) Cuidados domiciliarios Transportes al y del hospital/consultas Younossi Z, et al. Liver Intern 2017; 37: 159 -172.
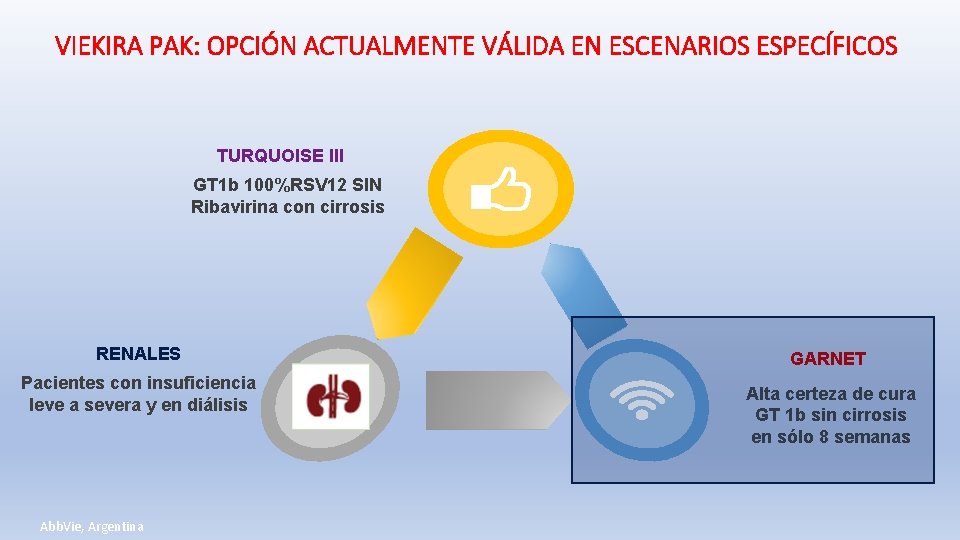
VIEKIRA PAK: OPCIÓN ACTUALMENTE VÁLIDA EN ESCENARIOS ESPECÍFICOS TURQUOISE III GT 1 b 100%RSV 12 SIN Ribavirina con cirrosis RENALES Pacientes con insuficiencia leve a severa y en diálisis Abb. Vie, Argentina GARNET Alta certeza de cura GT 1 b sin cirrosis en sólo 8 semanas
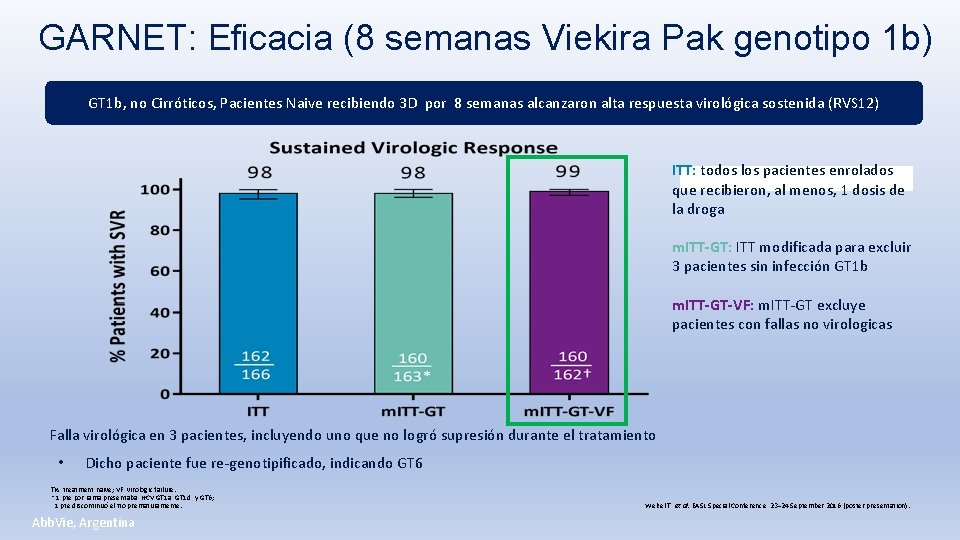
GARNET: Eficacia (8 semanas Viekira Pak genotipo 1 b) GT 1 b, no Cirróticos, Pacientes Naive recibiendo 3 D por 8 semanas alcanzaron alta respuesta virológica sostenida (RVS 12) ITT: todos los pacientes enrolados que recibieron, al menos, 1 dosis de la droga m. ITT-GT: ITT modificada para excluir 3 pacientes sin infección GT 1 b m. ITT-GT-VF: m. ITT-GT excluye pacientes con fallas no virologicas Falla virológica en 3 pacientes, incluyendo uno que no logró supresión durante el tratamiento • Dicho paciente fue re-genotipificado, indicando GT 6 TN, treatment naïve; VF, virologic failure. * 1 pte por rama presentaba HCV GT 1 a, GT 1 d, y GT 6; † 1 pte discontinuó el tto prematuramente. Abb. Vie, Argentina Welzel T, et al. EASL Special Conference, 23– 24 September 2016 (poster presentation).
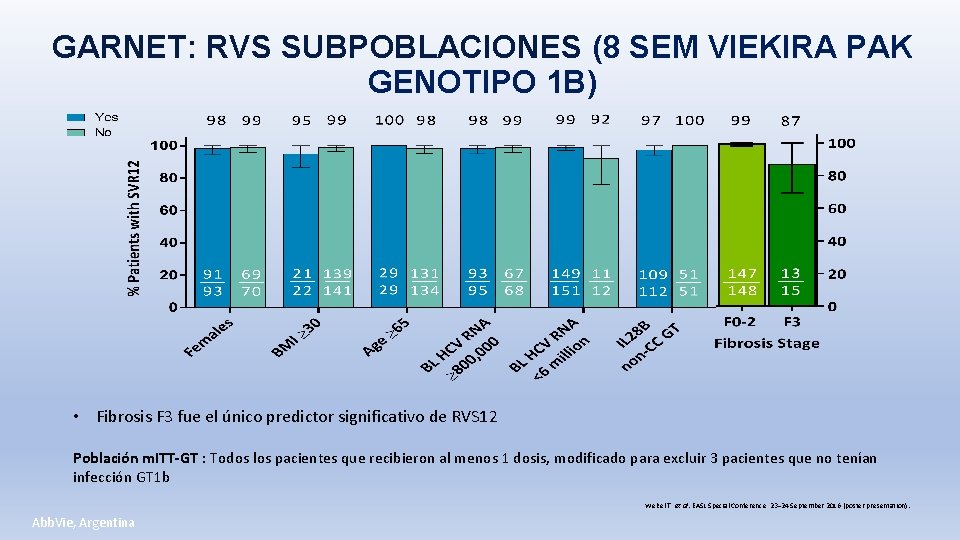
GARNET: RVS SUBPOBLACIONES (8 SEM VIEKIRA PAK GENOTIPO 1 B) • Fibrosis F 3 fue el único predictor significativo de RVS 12 Población m. ITT-GT : Todos los pacientes que recibieron al menos 1 dosis, modificado para excluir 3 pacientes que no tenían infección GT 1 b Welzel T, et al. EASL Special Conference, 23– 24 September 2016 (poster presentation). Abb. Vie, Argentina
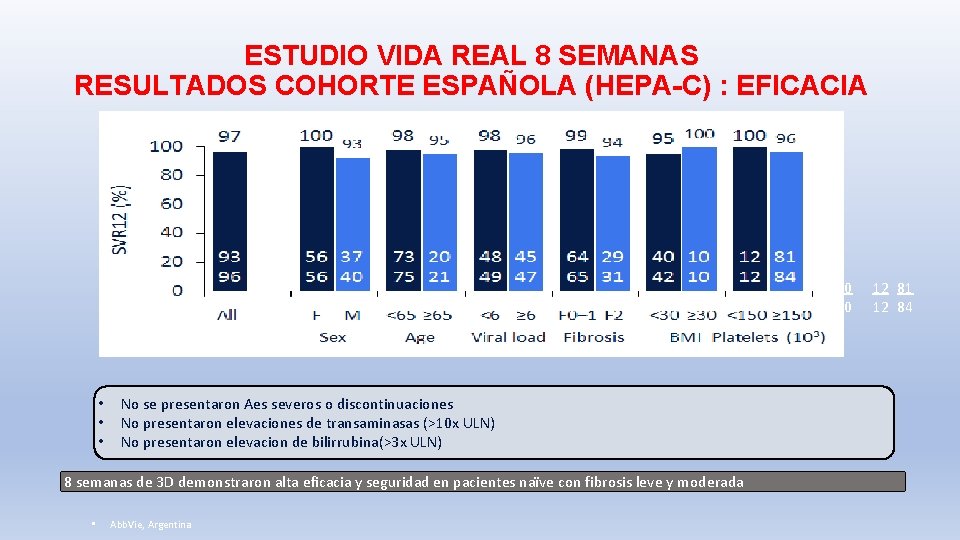
ESTUDIO VIDA REAL 8 SEMANAS RESULTADOS COHORTE ESPAÑOLA (HEPA-C) : EFICACIA 93 96 • • • 56 37 56 40 73 20 75 21 48 45 49 47 No se presentaron Aes severos o discontinuaciones No presentaron elevaciones de transaminasas (>10 x ULN) No presentaron elevacion de bilirrubina(>3 x ULN) 8 semanas de 3 D demonstraron alta eficacia y seguridad en pacientes naïve con fibrosis leve y moderada • Abb. Vie, Argentina 64 29 65 31 40 10 42 10 12 81 12 84

VIEKIRA PAK: OPCIÓN ACTUALMENTE VÁLIDA EN ESCENARIOS ESPECÍFICOS TURQUOISE III GT 1 b 100%RSV 12 SIN Ribavirina con cirrosis RENALES Pacientes con insuficiencia leve a severa y en diálisis Abb. Vie, Argentina GARNET Alta certeza de cura GT 1 b sin cirrosis en sólo 8 semanas
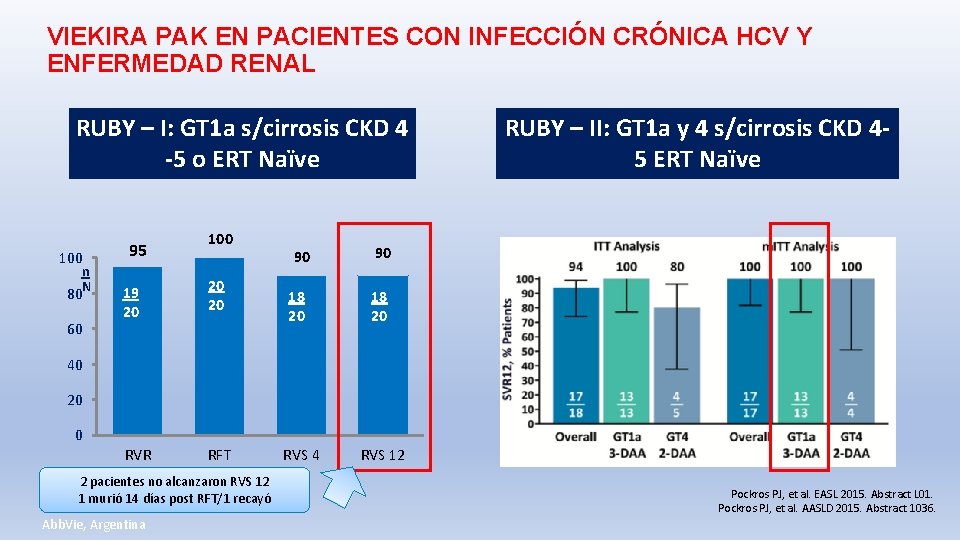
VIEKIRA PAK EN PACIENTES CON INFECCIÓN CRÓNICA HCV Y ENFERMEDAD RENAL RUBY – I: GT 1 a s/cirrosis CKD 4 -5 o ERT Naïve 100 n N 80 60 95 100 19 20 20 20 RVR RFT 90 18 20 RUBY – II: GT 1 a y 4 s/cirrosis CKD 45 ERT Naïve 90 18 20 40 20 0 2 pacientes no alcanzaron RVS 12 1 murió 14 días post RFT/1 recayó Abb. Vie, Argentina RVS 4 RVS 12 Pockros PJ, et al. EASL 2015. Abstract L 01. Pockros PJ, et al. AASLD 2015. Abstract 1036.
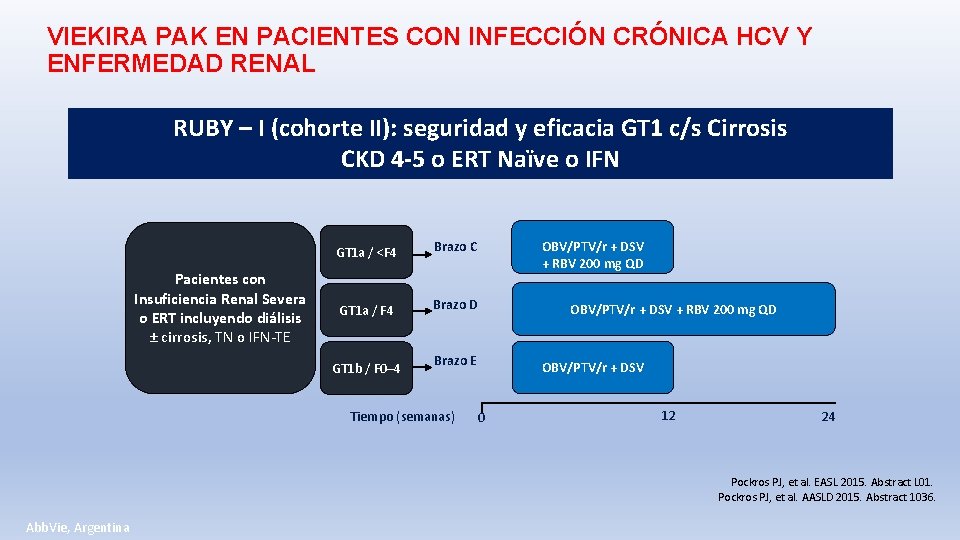
VIEKIRA PAK EN PACIENTES CON INFECCIÓN CRÓNICA HCV Y ENFERMEDAD RENAL RUBY – I (cohorte II): seguridad y eficacia GT 1 c/s Cirrosis CKD 4 -5 o ERT Naïve o IFN Pacientes con Insuficiencia Renal Severa o ERT incluyendo diálisis ± cirrosis, TN o IFN-TE GT 1 a / <F 4 Brazo C GT 1 a / F 4 Brazo D GT 1 b / F 0– 4 OBV/PTV/r + DSV + RBV 200 mg QD Brazo E Tiempo (semanas) OBV/PTV/r + DSV 0 12 24 Pockros PJ, et al. EASL 2015. Abstract L 01. Pockros PJ, et al. AASLD 2015. Abstract 1036. Abb. Vie, Argentina
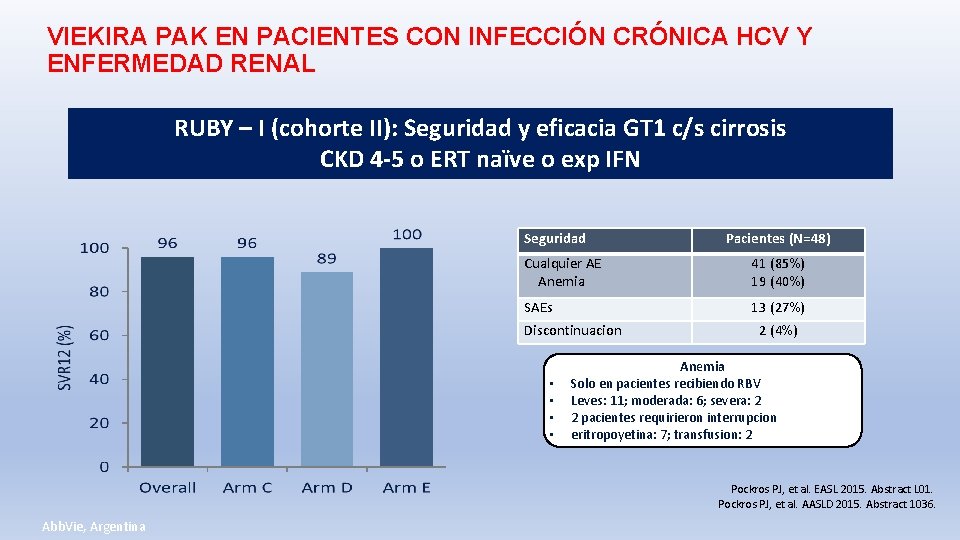
VIEKIRA PAK EN PACIENTES CON INFECCIÓN CRÓNICA HCV Y ENFERMEDAD RENAL RUBY – I (cohorte II): Seguridad y eficacia GT 1 c/s cirrosis CKD 4 -5 o ERT naïve o exp IFN Seguridad Pacientes (N=48) Cualquier AE Anemia 41 (85%) 19 (40%) SAEs 13 (27%) Discontinuacion • • 2 (4%) Anemia Solo en pacientes recibiendo RBV Leves: 11; moderada: 6; severa: 2 2 pacientes requirieron interrupcion eritropoyetina: 7; transfusion: 2 Pockros PJ, et al. EASL 2015. Abstract L 01. Pockros PJ, et al. AASLD 2015. Abstract 1036. Abb. Vie, Argentina
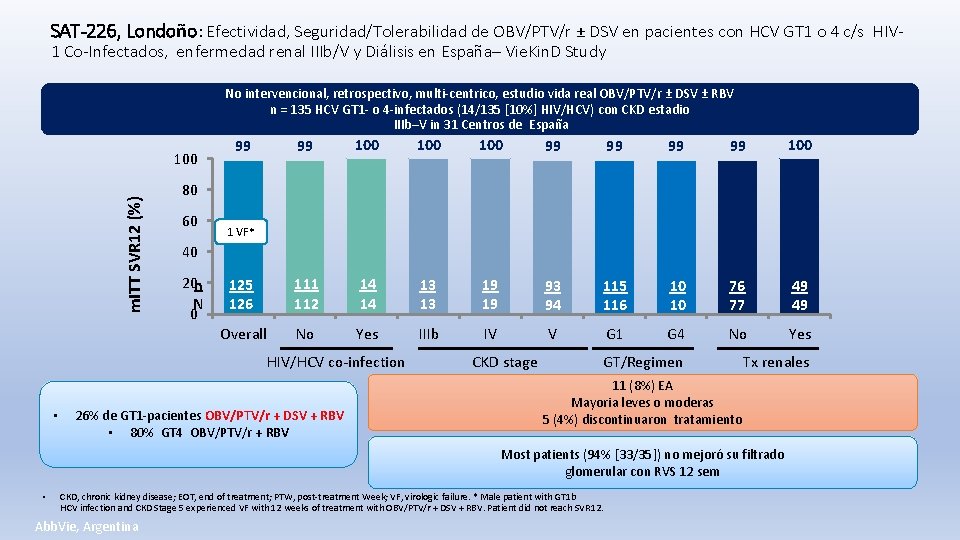
SAT-226, Londoño: Efectividad, Seguridad/Tolerabilidad de OBV/PTV/r ± DSV en pacientes con HCV GT 1 o 4 c/s HIV 1 Co-Infectados, enfermedad renal IIIb/V y Diálisis en España– Vie. Kin. D Study No intervencional, retrospectivo, multi-centrico, estudio vida real OBV/PTV/r ± DSV ± RBV n = 135 HCV GT 1 - o 4 -infectados (14/135 [10%] HIV/HCV) con CKD estadio IIIb–V in 31 Centros de España m. ITT SVR 12 (%) 100 99 100 100 99 99 100 125 126 111 112 14 14 13 13 19 19 93 94 115 116 10 10 76 77 49 49 Overall No Yes IIIb IV V G 1 G 4 No Yes 99 80 60 1 VF* 40 20 n N 0 HIV/HCV co-infection • 26% de GT 1 -pacientes OBV/PTV/r + DSV + RBV • 80% GT 4 OBV/PTV/r + RBV CKD stage GT/Regimen Tx renales 11 (8%) EA Mayoria leves o moderas 5 (4%) discontinuaron tratamiento Most patients (94% [33/35]) no mejoró su filtrado glomerular con RVS 12 sem • CKD, chronic kidney disease; EOT, end of treatment; PTW, post-treatment Week; VF, virologic failure. * Male patient with GT 1 b HCV infection and CKD Stage 5 experienced VF with 12 weeks of treatment with OBV/PTV/r + DSV + RBV. Patient did not reach SVR 12. Abb. Vie, Argentina
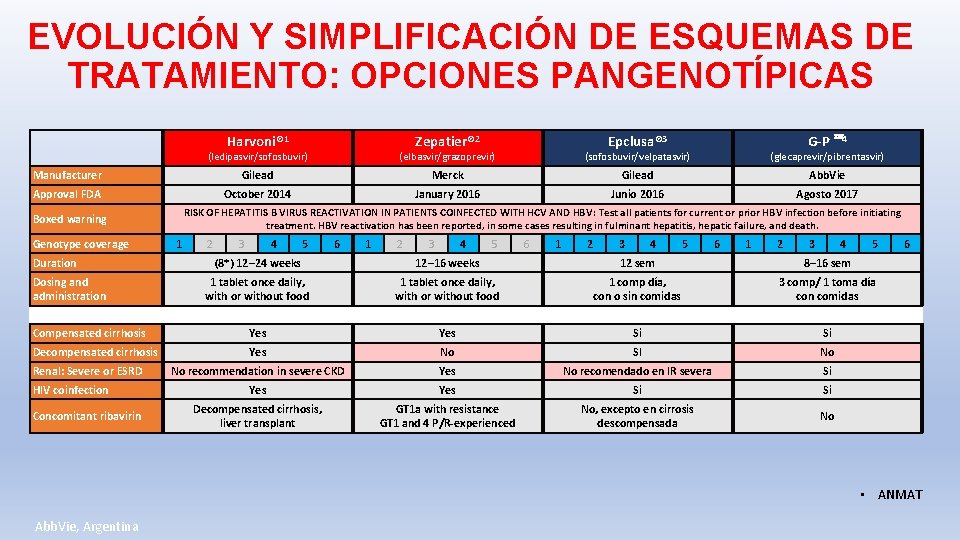
EVOLUCIÓN Y SIMPLIFICACIÓN DE ESQUEMAS DE TRATAMIENTO: OPCIONES PANGENOTÍPICAS Harvoni® 1 Zepatier® 2 G-P 4 Epclusa® 3 (ledipasvir/sofosbuvir) (elbasvir/grazoprevir) (sofosbuvir/velpatasvir) (glecaprevir/pibrentasvir) Manufacturer Gilead Merck Gilead Abb. Vie Approval FDA October 2014 January 2016 Junio 2016 Agosto 2017 RISK OF HEPATITIS B VIRUS REACTIVATION IN PATIENTS COINFECTED WITH HCV AND HBV: Test all patients for current or prior HBV infection before initiating treatment. HBV reactivation has been reported, in some cases resulting in fulminant hepatitis, hepatic failure, and death. Boxed warning Genotype coverage Duration 1 2 3 4 5 6 1 2 3 4 5 (8*) 12– 24 weeks 12– 16 weeks 12 sem 8– 16 sem 1 tablet once daily, with or without food 1 comp día, con o sin comidas 3 comp/ 1 toma día con comidas Compensated cirrhosis Yes Si Si Decompensated cirrhosis Yes No SI No No recommendation in severe CKD Yes No recomendado en IR severa Si Yes Si Si Decompensated cirrhosis, liver transplant GT 1 a with resistance GT 1 and 4 P/R-experienced No, excepto en cirrosis descompensada No Dosing and administration Renal: Severe or ESRD HIV coinfection Concomitant ribavirin 6 • ANMAT Abb. Vie, Argentina

Características del producto Glecaprevir/Pibrentasvir (G/P) Glecaprevir (GLE) Inhibidor pangenotípico de la proteasa NS 3/4 A Pibrentasvir (PIB) Glecaprevir (100 mg) Pibrentasvir (40 mg) Inhibidor pangenotípico de NS 5 A • Alta barrera a la resistencia • La potencia de GLE y PIB se conserva frente a la mayoría de sustituciones individuales de aminoácidos asociadas con resistencia a otros inhibidores de NS 5 A e inhibidores de la proteasa NS 3/4 A, incluida la mutación Y 93 H. • G/P experimenta una excreción renal mínima (<1 %). No se prevé ningún ajuste de la dosis de G/P en pacientes con insuficiencia renal leve, moderada o severa, incluidos aquellos en diálisis. • No se prevé ningún requisito de monitoreo de la función hepática durante el tratamiento, excepto en pacientes con infección concomitante por VHB. Abb. Vie, Argentina
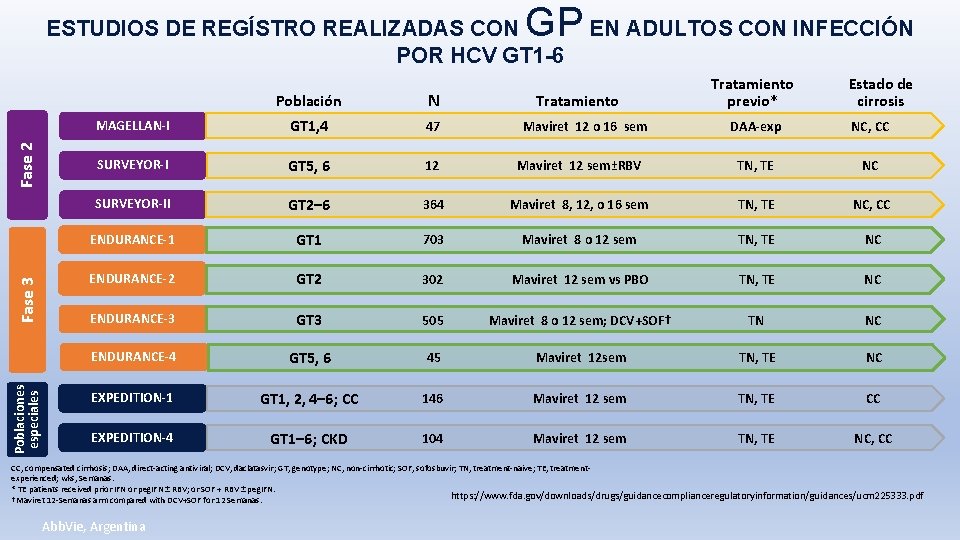
GP EN ADULTOS CON INFECCIÓN Poblaciones especiales Fase 3 Fase 2 ESTUDIOS DE REGÍSTRO REALIZADAS CON POR HCV GT 1 -6 Población N MAGELLAN-I GT 1, 4 47 SURVEYOR-I GT 5, 6 12 SURVEYOR-II GT 2– 6 ENDURANCE-1 Tratamiento previo* Estado de cirrosis DAA-exp NC, CC Maviret 12 sem±RBV TN, TE NC 364 Maviret 8, 12, o 16 sem TN, TE NC, CC GT 1 703 Maviret 8 o 12 sem TN, TE NC ENDURANCE-2 GT 2 302 Maviret 12 sem vs PBO TN, TE NC ENDURANCE-3 GT 3 505 Maviret 8 o 12 sem; DCV+SOF† TN NC ENDURANCE-4 GT 5, 6 45 Maviret 12 sem TN, TE NC EXPEDITION-1 GT 1, 2, 4– 6; CC 146 Maviret 12 sem TN, TE CC EXPEDITION-4 GT 1– 6; CKD 104 Maviret 12 sem TN, TE NC, CC Maviret 12 o 16 sem CC, compensated cirrhosis; DAA, direct-acting antiviral; DCV, daclatasvir; GT, genotype; NC, non-cirrhotic; SOF, sofosbuvir; TN, treatment-naive; TE, treatmentexperienced; wks, Semanas. * TE patients received prior IFN or peg. IFN ± RBV; or SOF + RBV ± peg. IFN. https: //www. fda. gov/downloads/drugs/guidancecomplianceregulatoryinformation/guidances/ucm 225333. pdf †Maviret 12 -Semanas arm compared with DCV+SOF for 12 Semanas. Abb. Vie, Argentina
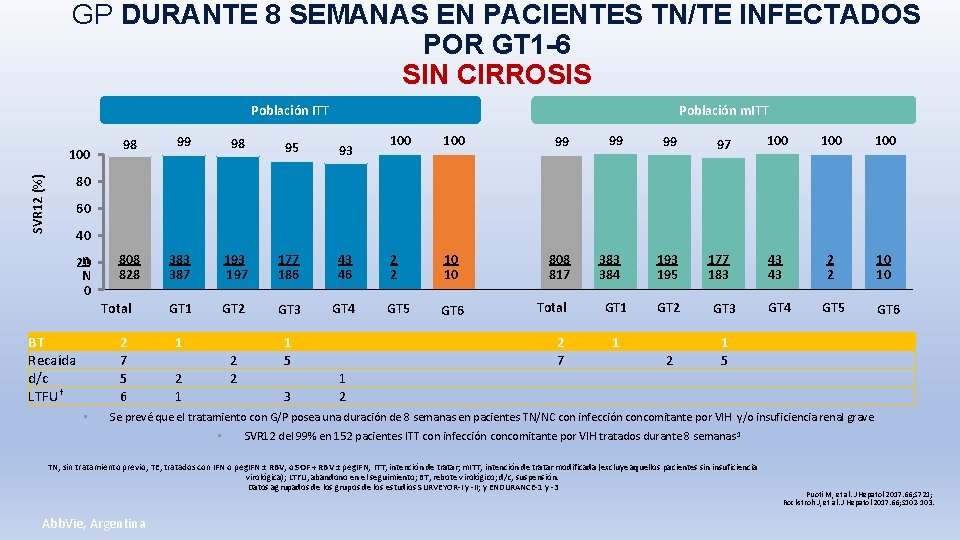
GP DURANTE 8 SEMANAS EN PACIENTES TN/TE INFECTADOS POR GT 1 -6 SIN CIRROSIS Población m. ITT Población ITT 100 98 99 98 95 93 808 828 383 387 193 197 177 186 43 46 GT 1 GT 2 GT 3 GT 4 100 99 99 99 97 2 2 10 10 808 817 383 384 193 195 177 183 GT 5 GT 6 100 100 43 43 2 2 10 10 GT 4 GT 5 SVR 12 (%) 80 60 40 n 20 N 0 Total BT Recaída d/c LTFU† 2 7 5 6 • 1 2 2 2 1 1 5 3 1 2 Total 2 7 GT 1 1 GT 2 GT 3 2 1 5 GT 6 Se prevé que el tratamiento con G/P posea una duración de 8 semanas en pacientes TN/NC con infección concomitante por VIH y/o insuficiencia renal grave • SVR 12 del 99% en 152 pacientes ITT con infección concomitante por VIH tratados durante 8 semanas 1 TN, sin tratamiento previo; TE, tratados con IFN o peg. IFN ± RBV, o SOF + RBV ± peg. IFN; ITT, intención de tratar; m. ITT, intención de tratar modificada (excluye aquellos pacientes sin insuficiencia virológica); LTFU, abandono en el seguimiento; BT, rebote virológico; d/c, suspensión. Datos agrupados de los grupos de los estudios SURVEYOR-I y -II; y ENDURANCE-1 y -3 Abb. Vie, Argentina Puoti M, et al. J Hepatol 2017. 66; S 721; Rockstroh J, et al. J Hepatol 2017. 66; S 102 -103.
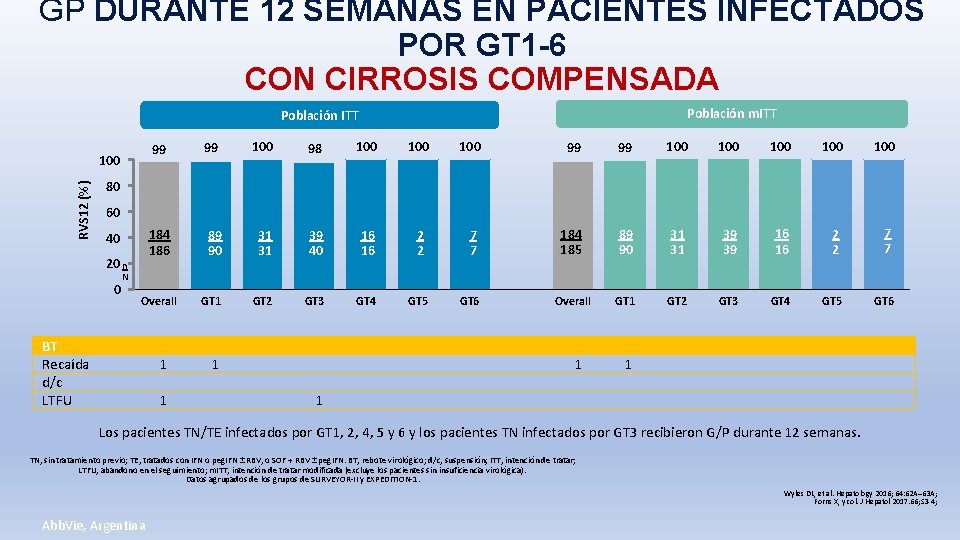
GP DURANTE 12 SEMANAS EN PACIENTES INFECTADOS POR GT 1 -6 CON CIRROSIS COMPENSADA Población m. ITT Población ITT RVS 12 (%) 100 99 99 100 98 100 100 99 99 100 100 100 184 186 89 90 31 31 39 40 16 16 2 2 7 7 184 185 89 90 31 31 39 39 16 16 2 2 7 7 GT 1 GT 2 GT 3 GT 4 GT 5 GT 6 Overall GT 1 GT 2 GT 3 GT 4 GT 5 GT 6 80 60 40 20 n 0 N Overall BT Recaída d/c LTFU 1 1 1 Los pacientes TN/TE infectados por GT 1, 2, 4, 5 y 6 y los pacientes TN infectados por GT 3 recibieron G/P durante 12 semanas. TN, sin tratamiento previo; TE, tratados con IFN o peg. IFN ± RBV, o SOF + RBV ± peg. IFN. BT, rebote virológico; d/c, suspensión; ITT, intención de tratar; LTFU, abandono en el seguimiento; m. ITT, intención de tratar modificada (excluye los pacientes sin insuficiencia virológica). Datos agrupados de los grupos de SURVEYOR-II y EXPEDITION-1. Wyles DL, et al. Hepatology 2016; 64: 62 A– 63 A; Forns X, y col. J Hepatol 2017. 66; S 3 -4; Abb. Vie, Argentina
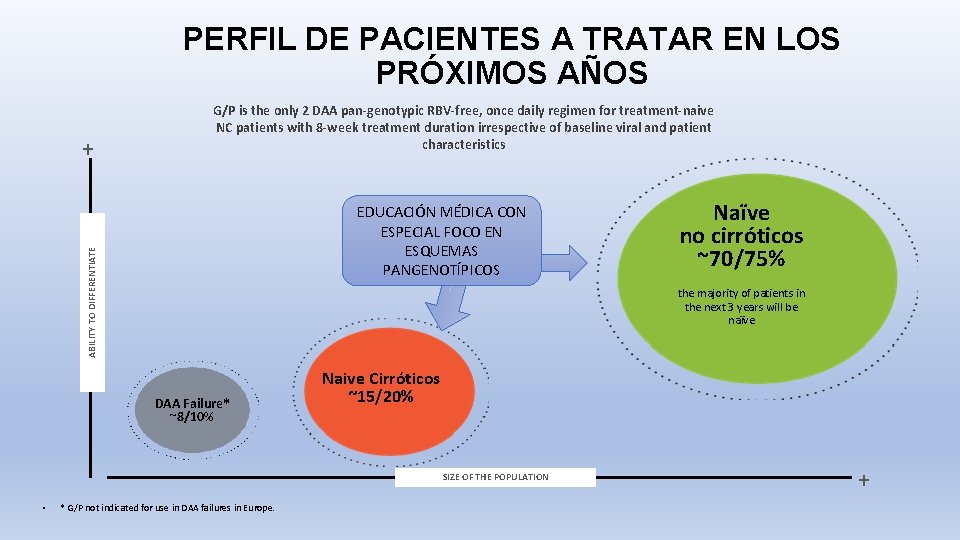
PERFIL DE PACIENTES A TRATAR EN LOS PRÓXIMOS AÑOS EDUCACIÓN MÉDICA CON ESPECIAL FOCO EN ESQUEMAS PANGENOTÍPICOS ABILITY TO DIFFERENTIATE + G/P is the only 2 DAA pan-genotypic RBV-free, once daily regimen for treatment-naive NC patients with 8 -week treatment duration irrespective of baseline viral and patient characteristics the majority of patients in the next 3 years will be naïve DAA Failure* ~8/10% Naive Cirróticos ~15/20% SIZE OF THE POPULATION • Naïve no cirróticos ~70/75% * G/P not indicated for use in DAA failures in Europe. +
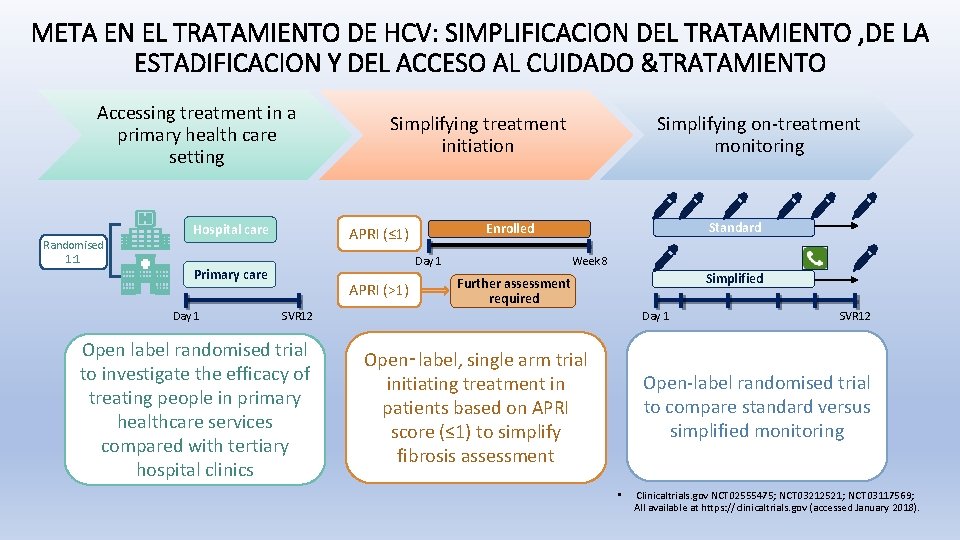
META EN EL TRATAMIENTO DE HCV: SIMPLIFICACION DEL TRATAMIENTO , DE LA ESTADIFICACION Y DEL ACCESO AL CUIDADO &TRATAMIENTO Accessing treatment in a primary health care setting Randomised 1: 1 Hospital care Day 1 APRI (>1) Simplifying on-treatment monitoring Standard Enrolled APRI (≤ 1) Primary care Day 1 Simplifying treatment initiation Week 8 Simplified Further assessment required SVR 12 Open label randomised trial to investigate the efficacy of treating people in primary healthcare services compared with tertiary hospital clinics Day 1 Open‑label, single arm trial initiating treatment in patients based on APRI score (≤ 1) to simplify fibrosis assessment SVR 12 Open-label randomised trial to compare standard versus simplified monitoring • Clinicaltrials. gov NCT 02555475; NCT 03212521; NCT 03117569; All available at https: //clinicaltrials. gov (accessed January 2018).

DATOS DE LA VIDA REAL UNIDAD DE HIGADO HOSPITAL PRIVADO UNIVERSITARIO DE CORDOBA Datos preliminares en análisis actual……. .
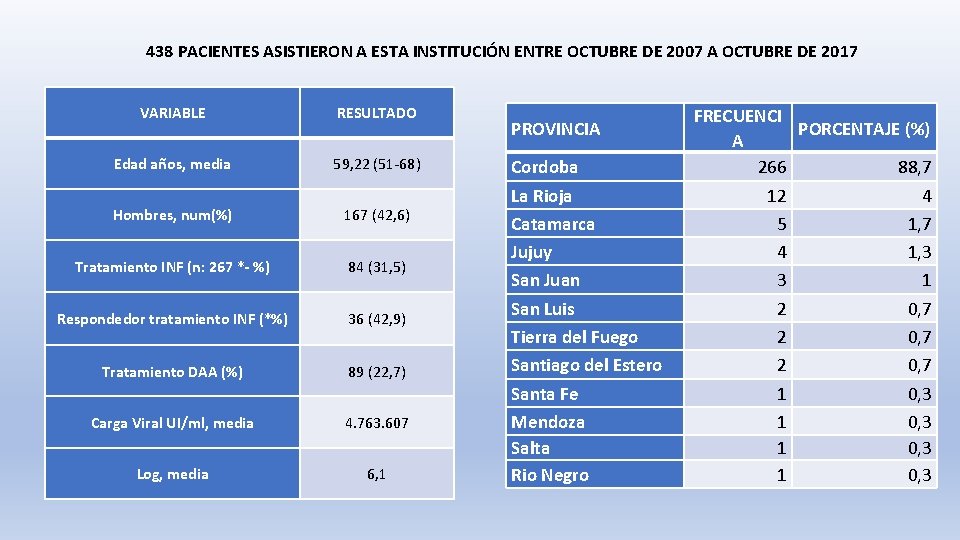
438 PACIENTES ASISTIERON A ESTA INSTITUCIÓN ENTRE OCTUBRE DE 2007 A OCTUBRE DE 2017 VARIABLE RESULTADO Edad años, media 59, 22 (51 -68) Hombres, num(%) 167 (42, 6) Tratamiento INF (n: 267 *- %) 84 (31, 5) Respondedor tratamiento INF (*%) 36 (42, 9) Tratamiento DAA (%) 89 (22, 7) Carga Viral UI/ml, media 4. 763. 607 Log, media 6, 1 PROVINCIA Cordoba La Rioja Catamarca Jujuy San Juan San Luis Tierra del Fuego Santiago del Estero Santa Fe Mendoza Salta Rio Negro FRECUENCI PORCENTAJE (%) A 266 88, 7 12 4 5 1, 7 4 1, 3 3 1 2 0, 7 1 0, 3
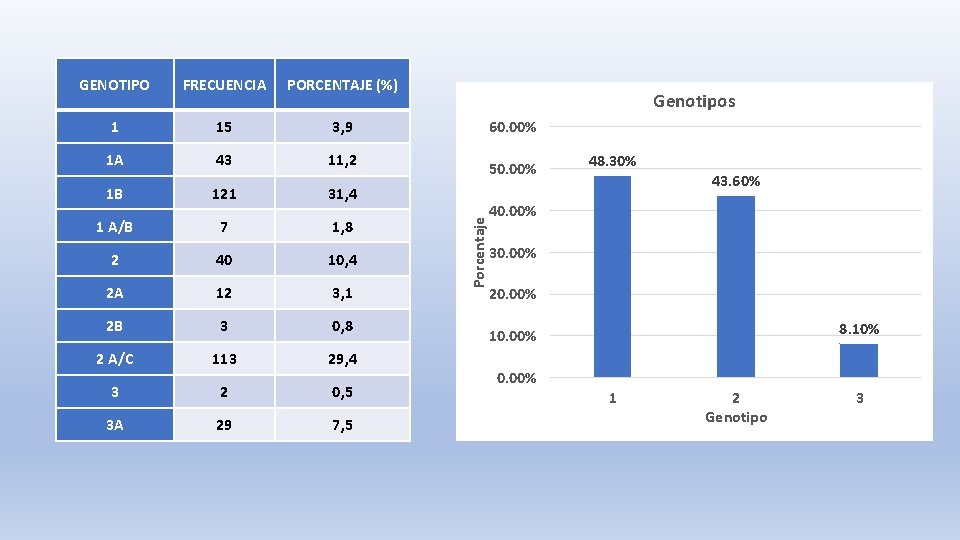
FRECUENCIA PORCENTAJE (%) 1 15 3, 9 1 A 43 11, 2 1 B 121 31, 4 1 A/B 7 1, 8 2 40 10, 4 2 A 12 3, 1 2 B 3 0, 8 2 A/C 113 29, 4 3 2 0, 5 3 A 29 7, 5 Genotipos 60. 00% 50. 00% Porcentaje GENOTIPO 48. 30% 43. 60% 40. 00% 30. 00% 20. 00% 8. 10% 10. 00% 1 2 Genotipo 3
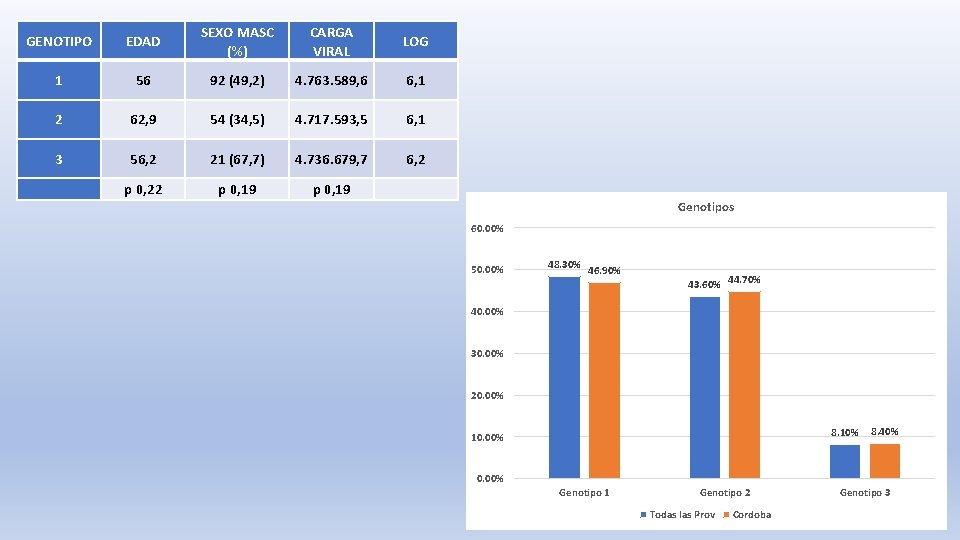
GENOTIPO EDAD SEXO MASC (%) CARGA VIRAL LOG 1 56 92 (49, 2) 4. 763. 589, 6 6, 1 2 62, 9 54 (34, 5) 4. 717. 593, 5 6, 1 3 56, 2 21 (67, 7) 4. 736. 679, 7 6, 2 p 0, 22 p 0, 19 Genotipos 60. 00% 50. 00% 48. 30% 46. 90% 43. 60% 44. 70% 40. 00% 30. 00% 20. 00% 8. 10% 10. 00% 8. 40% 0. 00% Genotipo 1 Genotipo 2 Todas las Prov Cordoba Genotipo 3
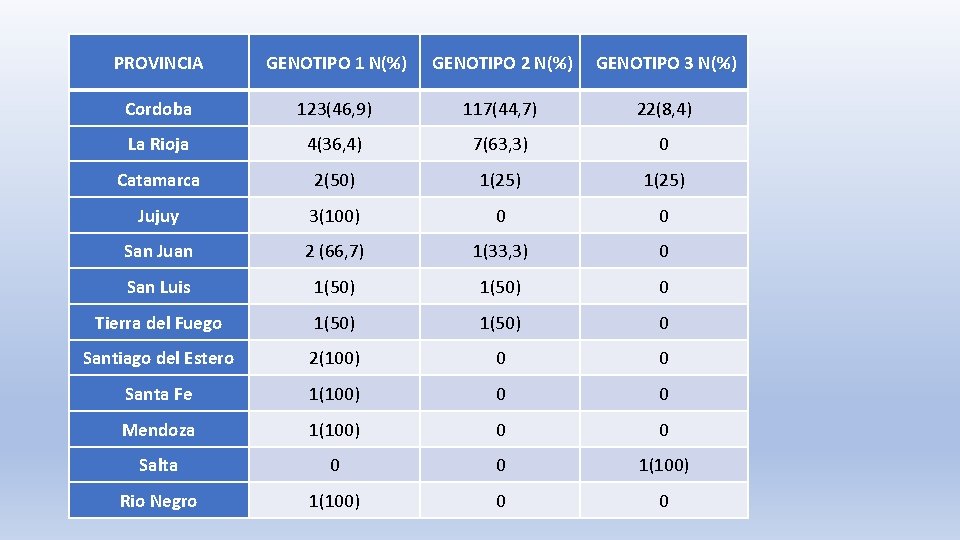
PROVINCIA GENOTIPO 1 N(%) GENOTIPO 2 N(%) GENOTIPO 3 N(%) Cordoba 123(46, 9) 117(44, 7) 22(8, 4) La Rioja 4(36, 4) 7(63, 3) 0 Catamarca 2(50) 1(25) Jujuy 3(100) 0 0 San Juan 2 (66, 7) 1(33, 3) 0 San Luis 1(50) 0 Tierra del Fuego 1(50) 0 Santiago del Estero 2(100) 0 0 Santa Fe 1(100) 0 0 Mendoza 1(100) 0 0 Salta 0 0 1(100) Rio Negro 1(100) 0 0
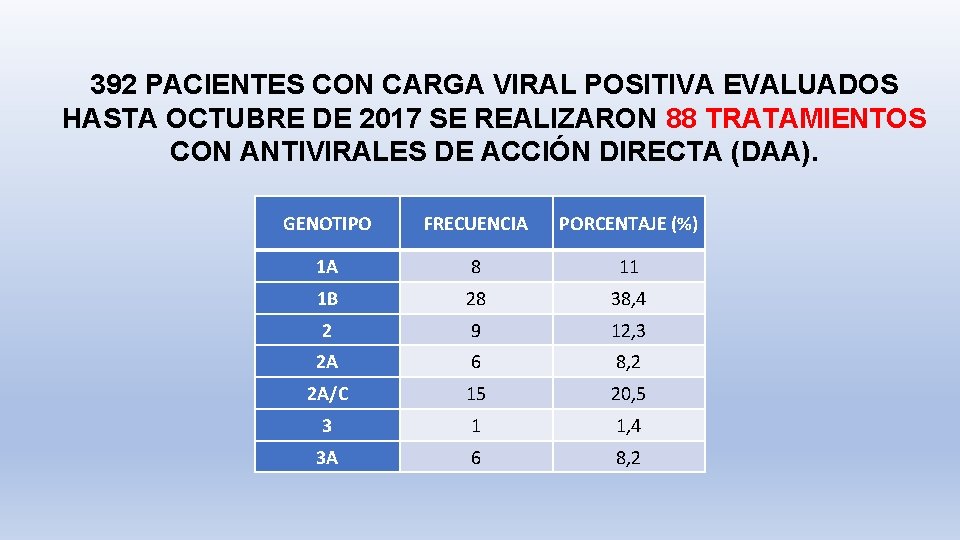
392 PACIENTES CON CARGA VIRAL POSITIVA EVALUADOS HASTA OCTUBRE DE 2017 SE REALIZARON 88 TRATAMIENTOS CON ANTIVIRALES DE ACCIÓN DIRECTA (DAA). GENOTIPO FRECUENCIA PORCENTAJE (%) 1 A 8 11 1 B 28 38, 4 2 9 12, 3 2 A 6 8, 2 2 A/C 15 20, 5 3 1 1, 4 3 A 6 8, 2
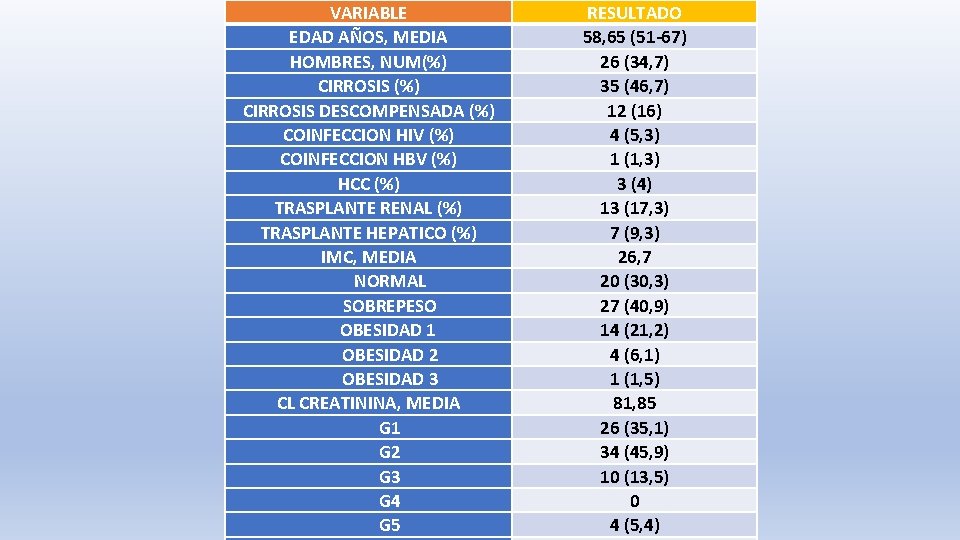
VARIABLE EDAD AÑOS, MEDIA HOMBRES, NUM(%) CIRROSIS DESCOMPENSADA (%) COINFECCION HIV (%) COINFECCION HBV (%) HCC (%) TRASPLANTE RENAL (%) TRASPLANTE HEPATICO (%) IMC, MEDIA NORMAL SOBREPESO OBESIDAD 1 OBESIDAD 2 OBESIDAD 3 CL CREATININA, MEDIA G 1 G 2 G 3 G 4 G 5 RESULTADO 58, 65 (51 -67) 26 (34, 7) 35 (46, 7) 12 (16) 4 (5, 3) 1 (1, 3) 3 (4) 13 (17, 3) 7 (9, 3) 26, 7 20 (30, 3) 27 (40, 9) 14 (21, 2) 4 (6, 1) 1 (1, 5) 81, 85 26 (35, 1) 34 (45, 9) 10 (13, 5) 0 4 (5, 4)
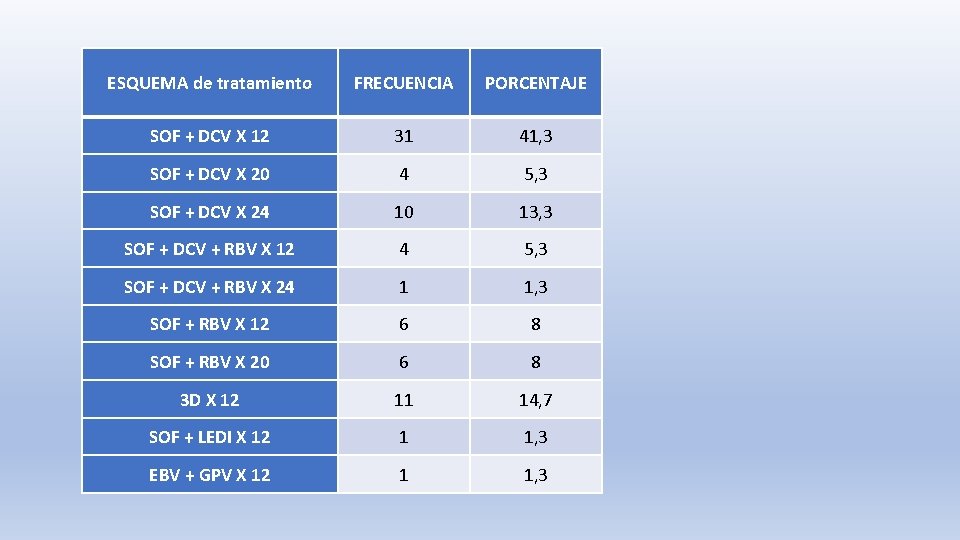
ESQUEMA de tratamiento FRECUENCIA PORCENTAJE SOF + DCV X 12 31 41, 3 SOF + DCV X 20 4 5, 3 SOF + DCV X 24 10 13, 3 SOF + DCV + RBV X 12 4 5, 3 SOF + DCV + RBV X 24 1 1, 3 SOF + RBV X 12 6 8 SOF + RBV X 20 6 8 3 D X 12 11 14, 7 SOF + LEDI X 12 1 1, 3 EBV + GPV X 12 1 1, 3
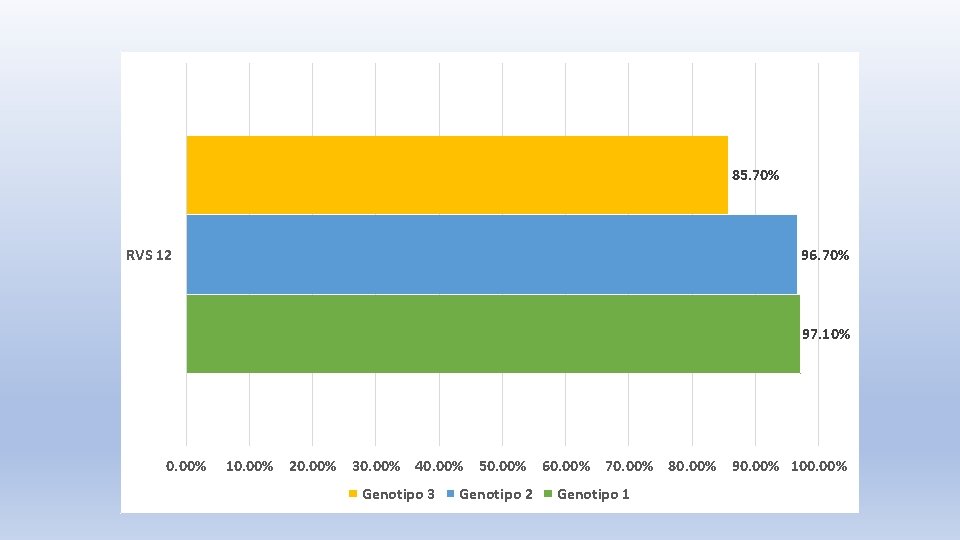
85. 70% RVS 12 96. 70% 97. 10% 0. 00% 10. 00% 20. 00% 30. 00% 40. 00% 50. 00% 60. 00% 70. 00% 80. 00% 90. 00% 100. 00% Genotipo 3 Genotipo 2 Genotipo 1
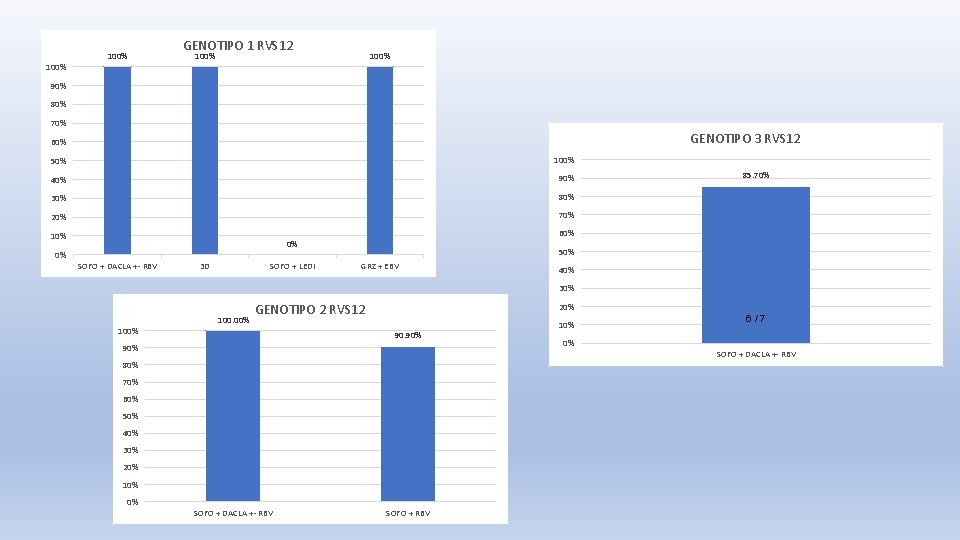
100% GENOTIPO 1 RVS 12 100% 90% 80% 70% GENOTIPO 3 RVS 12 60% 50% 100% 40% 90% 30% 80% 20% 70% 10% 0% 60% 0% SOFO + DACLA +- RBV 3 D SOFO + LEDI 85. 70% 50% GRZ + EBV 40% 30% 100. 00% GENOTIPO 2 RVS 12 20% 90. 90% 80% 70% 60% 50% 40% 30% 20% 10% 0% SOFO + DACLA +- RBV SOFO + RBV 10% 0% 6 / 7 SOFO + DACLA +- RBV
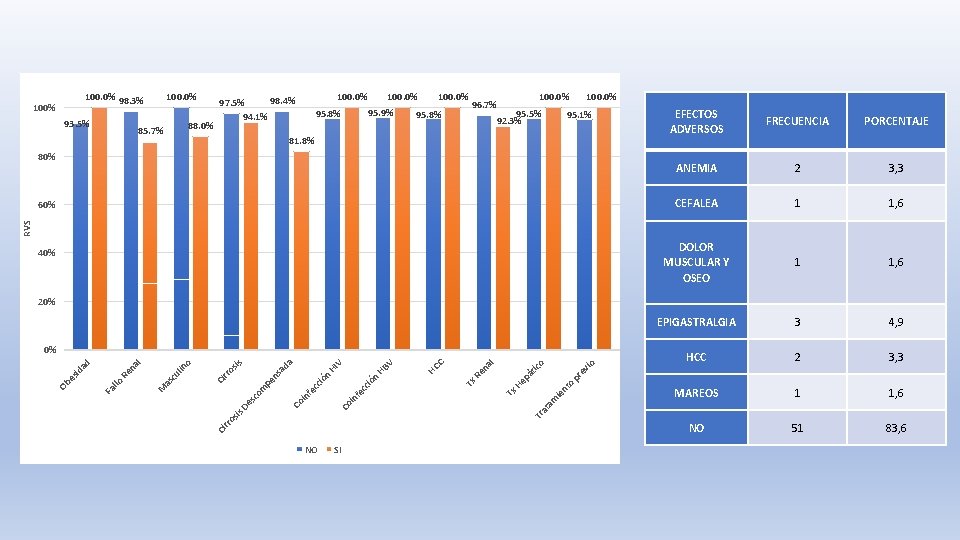
100. 0% 98. 3% 100% 93. 5% 100. 0% 88. 0% 85. 7% 100. 0% 98. 4% 97. 5% 94. 1% 100. 0% 95. 9% 95. 8% 100. 0% 96. 7% 95. 5% 92. 3% 100. 0% 95. 1% 81. 8% 80% FRECUENCIA PORCENTAJE ANEMIA 2 3, 3 CEFALEA 1 1, 6 DOLOR MUSCULAR Y OSEO 1 1, 6 EPIGASTRALGIA 3 4, 9 HCC 2 3, 3 MAREOS 1 1, 6 NO 51 83, 6 RVS 60% EFECTOS ADVERSOS 40% 20% ev i o ico p r át Ci rr o nt o ie am Tr at C en al R ep Tx H fe cc in Co Tx n H ió ió fe cc in HC BV IV n H da om es c sis D Co pe ns a sis rr o Ci o M as cu lin en al R llo Fa Ob es id ad 0% NO SI

GRACIAS…
- Slides: 53