Abbiamo visto equilibrio dinamico in 1 Un liquido

Abbiamo visto equilibrio dinamico in: 1. Un liquido evapora in un contenitore chiuso e dopo un certo tempo, il numero di molecole che condensano allo stato liquido è uguale a quelle che evaporano alo stato gassoso. La tensione di vapore resta quindi costante nel tempo ed è quindi una proprietà legata ad una condizione di equilibrio dinamico. 2. Un soluto si scioglie in un solvente e a un certa quantità di soluto aggiunto ottengo una soluzione satura, alla quale la quantità del soluto che si solubilizza è uguale alla quantità di soluto che cristallizza, e la concentrazione del soluto resta costante nel tempo. La solubilità è quindi una proprietà legata ad una condizione di equilibrio dinamico. Sono equilibri fisici ma posso estendere questo concetto ad una reazione chimica e parlare di….

Equilibrio chimico: un equilibrio dinamico

Equilibrio chimico Data la reazione: 2 Cu 2+ + Sn 2+ 2 Cu+ + Sn 4+ all’inizio avviene la reazione diretta soltanto, ma appena si formano i prodotti inizia la reazione inversa. Col tempo la reazione diretta rallenta e la reazione inversa accellera. Alla fine, le reazioni diretta e inversa procedanno a velocità uguali e la miscela è all’equilibrio dinamico. Si scrive quindi : 2 Cu 2+ + Sn 2+ 2 Cu+ + Sn 4+ All’equilibrio la quantità dei prodotti e reagenti rimane costante nel tempo. Ma le quantità all’equilibrio dipendono dalle quantità di reagenti e prodotti presenti inizialmente…
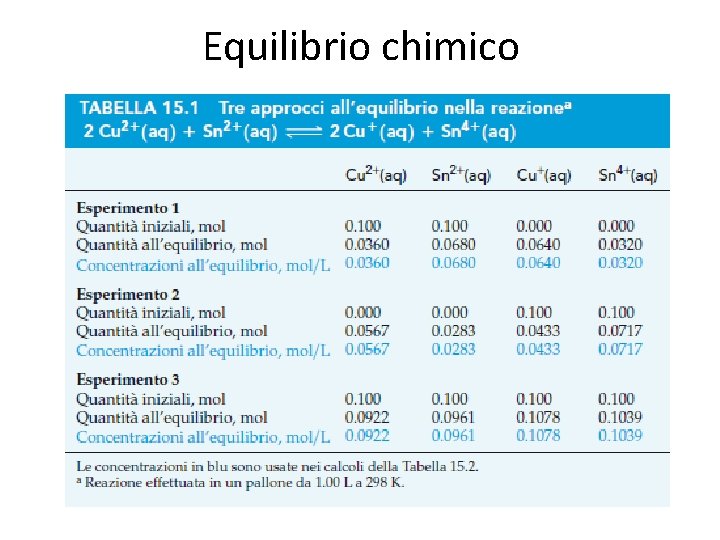
Equilibrio chimico
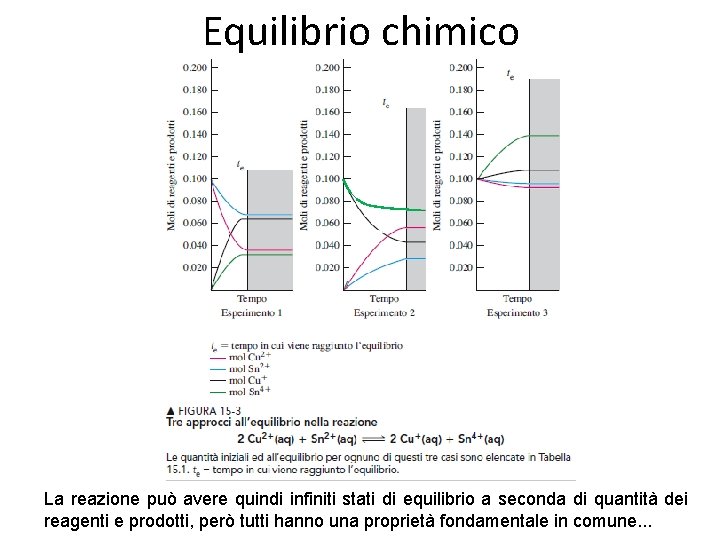
Equilibrio chimico La reazione può avere quindi infiniti stati di equilibrio a seconda di quantità dei reagenti e prodotti, però tutti hanno una proprietà fondamentale in comune. . .

La Costante di Equilibrio Si definisce quindi una costante di equilibrio, costante a T costante : Kc = [Cu +]eq 2 [Sn 4+]eq/[Cu 2+]eq 2 [Sn 2+]eq questo rapporto non varia per tutti i possibili infiniti stati di equilibrio, a T costante
L’ Equilibrio chimico N 2 O 4 incolore

L’ equilibrio chimico in reazioni gassose N 2 O 4 incolore Pressione iniziale di N 2 O 4 = 1 atm La pressione totale aumenta rapidamente all’inizio poi sempre più lentamente, per poi stabilizzarsi a un valore costante inferiore a 2 atm 2 NO 2

L’ Equilibrio chimico NO 2

L’ Equilibrio chimico 2 NO 2 N 2 O 4 Gas incolore Pressione iniziale di NO 2 = 1 atm La pressione totale diminuisce rapidamente all’inizio poi sempre più lentamente, per poi stabilizzarsi a un valore costante superiore a 0. 5 atm
L’ Equilibrio chimico N 2 O 4 2 NO 2 N 2 O 4 Quando le quantità di NO 2 e N 2 O 4 che si trasformano nell’unità di tempo sono uguali a quelle che si riformano siamo all’equilibrio chimico che è un equilibrio dinamico Gas incolore + gas rosso scuro
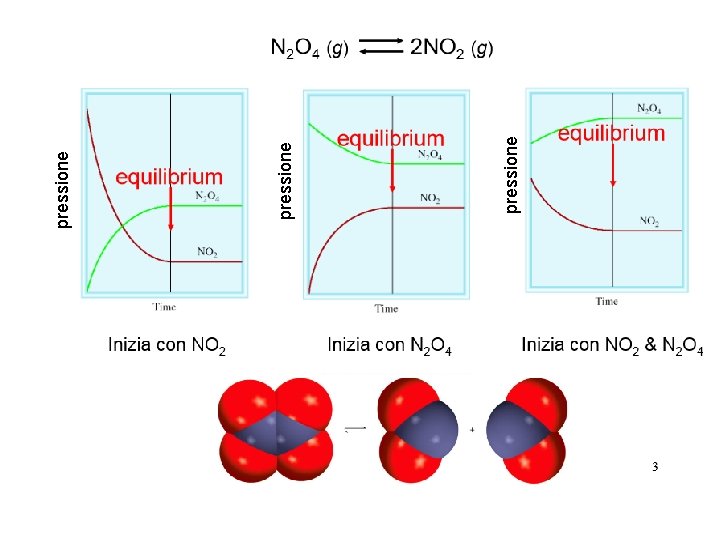
pressione
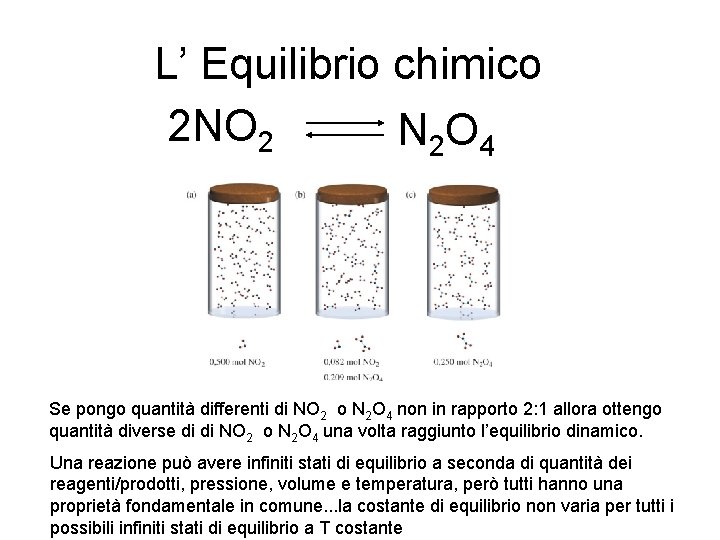
L’ Equilibrio chimico 2 NO 2 N 2 O 4 Equilibrio dinamico Se pongo quantità differenti di NO 2 o N 2 O 4 non in rapporto 2: 1 allora ottengo quantità diverse di di NO 2 o N 2 O 4 una volta raggiunto l’equilibrio dinamico. Una reazione può avere infiniti stati di equilibrio a seconda di quantità dei reagenti/prodotti, pressione, volume e temperatura, però tutti hanno una proprietà fondamentale in comune. . . la costante di equilibrio non varia per tutti i possibili infiniti stati di equilibrio a T costante

L’ Equilibrio chimico Per un sistema chimico all’equilibrio, il rapporto fra il prodotto delle concentrazioni molari dei prodotti di reazione e il prodotto delle concentrazioni molari dei reagenti, ciascuna concentrazione essendo elevata a una potenza pari al coefficiente stechiometrico con la specie compare nella reazione, è COSTANTE A TEMPERATURA COSTANTE a. A +b. B c c. C + d. D

L’ Equilibrio chimico ATTENZIONE Le concentrazioni SONO QUELLE DELLE SPECIE ALL’EQUILIBRIO! a. A +b. B c c. C + d. D
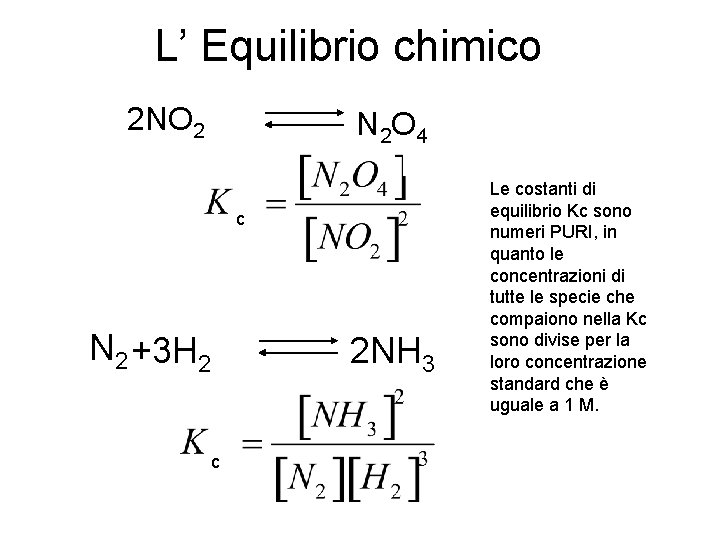
L’ Equilibrio chimico 2 NO 2 N 2 O 4 c N 2 +3 H 2 c 2 NH 3 Le costanti di equilibrio Kc sono numeri PURI, in quanto le concentrazioni di tutte le specie che compaiono nella Kc sono divise per la loro concentrazione standard che è uguale a 1 M.

Costante di Equilibrio Ha un senso solo se associata ad un equilibrio chimico, scritto con una precisa stechiometria cioè dipende da come è scritta la reazione Ma una volta scritta la reazione la Keq dipende solo da T e non dalle conc. dei reagenti e prodotti, volume e pressione
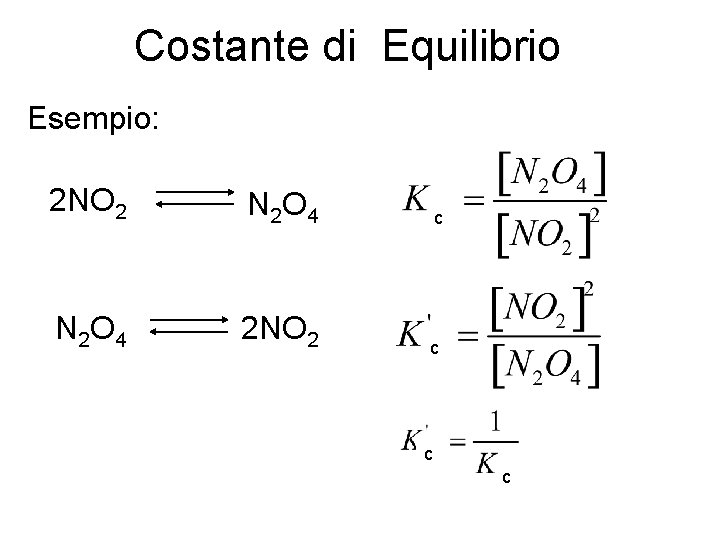
Costante di Equilibrio Esempio: 2 NO 2 N 2 O 4 c N 2 O 4 2 NO 2 c c c

Costante di Equilibrio Esempio: N 2 +3 H 2 2 NH 3 ½ N 2 + 3/ 2 H 2 c NH 3 c c

Costante di Equilibrio Esempio: N 2 O +1/2 O 2 2 NO K = ? N 2 + 1/2 O 2 N 2 O K 1 = 5. 4 x 10 -19 N 2 + O 2 2 NO K 2 = 4. 6 x 10 -31 K = (K 1)-1 X K 2 = 8. 5 x 10 -13

Costante di Equilibrio Può essere espressa anche in funzione delle pressioni parziali (in particolare nel caso di equilibri gassosi) Anche le Kp sono numeri PURI, in quanto le pressioni parziali di tutte le specie che compaiono nella Kp sono divise per la loro pressione standard che è uguale a 1 bar. N 2 +3 H 2 2 NH 3 p p. N 2 p 3 H 2 Considerando PV = n. RT si ottiene Kp = (RT)Dn Kc Dn è la differenza tra le moli dei prodotti e quelle dei reagenti Espresso come 0. 08314472 bar dm 3 K-1 mol-1

Equilibrio in fase eterogenea Gli esempi fino a qui discussi riguardavano sistemi in fase gassosa o ioni in solvente acquoso, dove tutte le specie chimiche definivano l’equilibrio chimico si trovano nella stessa fase.

Equilibrio in fase eterogenea Ca. CO 3 solido Ca. O+ CO 2 solido gas , c Keqc = Keqc ’ [Ca. CO 3]/[Ca. O] Le concentrazioni delle specie condensate (solido e liquido) pure nelle proprie fasi sono costanti (fintanto che la fase è presente), mentre le concentrazioni delle specie in fase gassosa sono variabili. A temperatura costante la concentrazione del solido o del liquido puro ha un valore costante, indipendente dalla quantità totale del solido o liquido (se aumenta la massa aumenta anche il volume e il numero di moli contenute nell'unità di volume rimane costante).
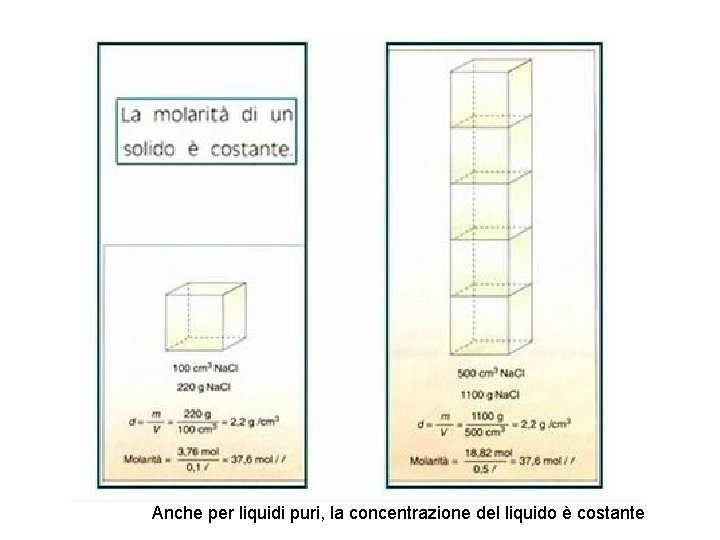
Anche per liquidi puri, la concentrazione del liquido è costante
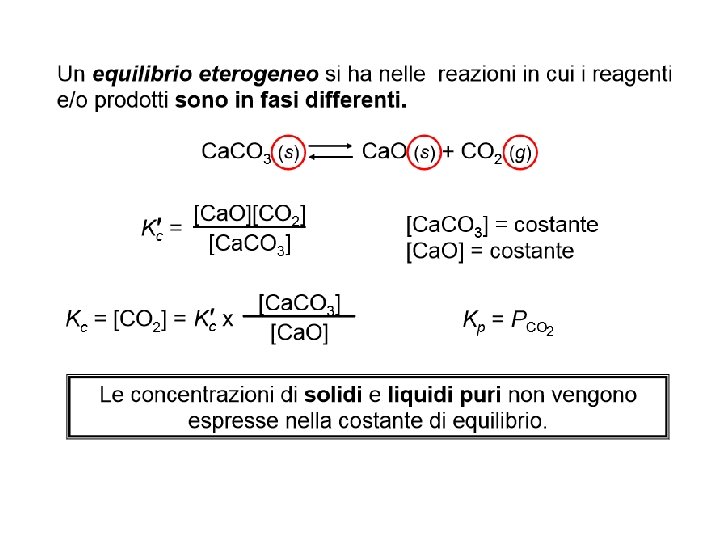

Equilibrio in fase eterogenea La P all’equilibrio di CO 2 è indipendente dalle quantità di Ca. CO 3 e Ca. O che posso introdurre nel recipiente(purche’ siano sempre presenti), ma dipende solo dalla T
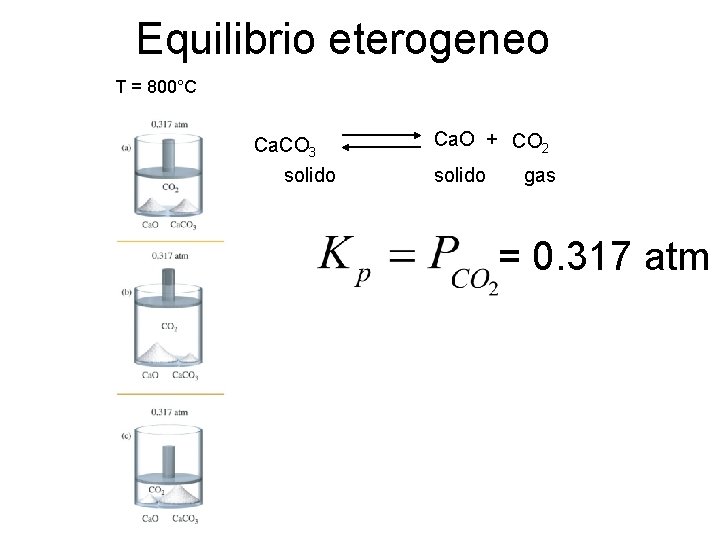
Equilibrio eterogeneo T = 800°C Ca. CO 3 solido Ca. O + CO 2 solido gas = 0. 317 atm

Equilibrio eterogeneo Solo le specie in fase gassosa determinano l’equilibrio C(s)+H 2 O(g) H 2(g)+ CO(g) c H 2 O(l) c c H 2 O(g) Kc = [H 2 O(g)] e Kp = PH 2 O(g) La tensione di vapore per liquidi puri corrisponde alla Kp

Valore della costante di equilibrio Una reazione si considera a completamento se K > 1010, mentre una reazione si considera non avvenire in senso diretto se K < 1010

Il Quoziente di reazione Nell’esempio dell’esperimento 3: Q c = (0. 1)2 (0. 1)/(0. 1)2 (0. 1) = 1 Dato che Qc<Keq che era 1. 48, la reazione avviene in senso diretto verso destra

Una reazione può avere infiniti stati di equilibrio a seconda di quantità dei reagenti/prodotti, pressione, volume e temperatura, però tutti hanno una proprietà fondamentale in comune. . . la costante di equilibrio non varia per tutti i possibili infiniti stati di equilibrio a T costante

Il significato della costante di equilibrio Permette di calcolare le concentrazioni delle specie all’equilibrio, ossia a fine reazione. Esempio: CO 2 CO + ½ O 2 Kc = 10 -36 a 100°C Se 1 mole di CO 2 in 1 dm 3 a 100°C ho: CO 2 CO O 2 Stato iniziale 1 mol 0 mol Stato finale di equilibrio 1 -x mol ½ x mol Kc = [O 2]1/2 [CO]/[CO 2]= (½ x)1/2 · x /(1 -x) = 10 -36 e risolvendo x = 10 -24

Il significato della costante di equilibrio Calcolare la composizione all’equilibrio della miscela che si ottiene quando HI è posto in un recipiente in concentrazione 2. 1 m. M e scaldato a 490°C. A questa T, la Kc della reazione 2 HI H 2 + I 2 è 0. 022. Kc = [H 2][I 2]/ [HI]2 Iniziale Finale [HI] 2. 1 x 10 -3 – 2 x [H 2] 0 x [I 2] 0 x Kc = x 2/ (2. 1 x 10 -3 – 2 x)2 x = 0. 24 x 10 -3

Il significato della costante di equilibrio Calcolare la composizione all’equilibrio della miscela che si ottiene quando HI è posto in un recipiente in concentrazione 2. 1 m. M e scaldato a 490°C. A questa T, la Kc della reazione 2 HI H 2 + I 2 è 0. 022. Kc = [H 2][I 2]/ [HI]2 Iniziale Finale [HI] 2. 1 x 10 -3 – x [H 2] 0 x/2 [I 2] 0 x/2 Kc = (x/2)2/ (2. 1 x 10 -3 –x)2 x = 0. 28 x 10 -3

Equazioni di secondo grado nei calcoli di equilibrio chimico ax 2 + bx + c = 0 x = [-b (b 2 -4 ac)1/2]/2 a Solo una delle due soluzioni possibili avrà significato fisico. Per esempio, una concentrazione non può mai essere negativa. Quindi una x che dà luogo ad una concentrazione negativa deve essere scartata. Notare però che x di per sé rappresenta una variazione di concentrazione e quindi può avere entrambi i segni.

Il significato della costante di equilibrio Data la seguente reazione a: PCl 5(g) PCl 3(g) + Cl 2(g) con Kc = 0. 800 a 340 °C Calcolare le concentrazioni all’equilibrio sapendo che le concentrazioni iniziali delle tre sostanze sono 0. 120 M. Kc = [PCl 3][Cl 2]/[PCl 5]= 0. 800 Mi calcolo Qc = [PCl 3][Cl 2]/[PCl 5]= 0. 120*0. 120/0. 120 = 0. 120 Qc<Kc reazione va a destra, quindi: PCl 3 0. 120+x Cl 2 0. 120+x PCl 5 0. 120 -x Kc = (0. 120 + x)2/(0. 120 -x) =0. 800 x 2 + 1. 040 x – 0. 0816 = 0 x 1 = 0. 0733 x 2 = -1. 113 x 2 darebbe conc. < 0 per i prodotti, quindi va scartata.

Esercizio • Azoto e idrogeno sono posti in un recipiente alle concentrazioni di 0. 500 M and 0. 800 M, rispettivamente. All’equilibrio, la concentrazione di NH 3 è 0. 150 M. Quale è il valore della costante di equilibrio per questa reazione? N 2 + 3 H 2 2 NH 3 Keq = [NH 3]2/[N 2][H 2]3 [N 2] [H 2] [NH 3] Iniziale 0. 500 0. 800 0 Equilibrio 0. 500 -0. 075 = 0. 425 0. 800 -0. 225 = 0. 575 0. 150 Keq = (0. 150)2/(0. 425)(0. 575)3 = 0. 278

Esercizio • Azoto e idrogeno sono posti in un recipiente alle concentrazioni di 0. 500 M and 0. 800 M, rispettivamente. All’equilibrio, la concentrazione di NH 3 è 0. 150 M. Quale è il valore della costante di equilibrio per questa reazione? N 2 + 3 H 2 2 NH 3 Keq = [NH 3]2/[N 2][H 2]3 [N 2] [H 2] [NH 3] Iniziale 0. 500 0. 800 0 Equilibrio 0. 500 -0. 075 = 0. 425 0. 800 -0. 225 = 0. 575 0. 150 Keq = (0. 150)2/(0. 425)(0. 575)3 = 0. 278

Equilibrio in fase gassosa Esercizi 1) Una miscela di iodio e idrogeno è scaldata a 490°C. Le concentrazioni all’equilibrio sono [I 2] = 3. 1 m. M e [HI] = 2. 7 m. M. Calcolare la concentrazione all’equilibrio di H 2, sapendo che a questa T, Kc per la reazione H 2 + I 2 2 HI Kc= 46
![Equilibrio in fase gassosa Esercizi Kc = [HI]2/[H 2][I 2]=46 [H 2] = [HI]2/ Equilibrio in fase gassosa Esercizi Kc = [HI]2/[H 2][I 2]=46 [H 2] = [HI]2/](http://slidetodoc.com/presentation_image_h/8ea91d3013603d0cafaa7d1e371e7c9c/image-40.jpg)
Equilibrio in fase gassosa Esercizi Kc = [HI]2/[H 2][I 2]=46 [H 2] = [HI]2/ [I 2] Kc = (2. 7 x 10 -3)2/[(3. 1 x 10 -3) • 46] [H 2] =0. 051 x 10 -3

Equilibrio in fase gassosa Esercizi Poiché le costanti di equilibrio di tutte le reazioni piu’ importanti sono note e tabulate a varie temperature, l’equazione dell’equilibrio chimico puo’ SEMPRE essere utilizzata per ricavare il valore di una concentrazione incognita, SE LE ALTRE SONO NOTE
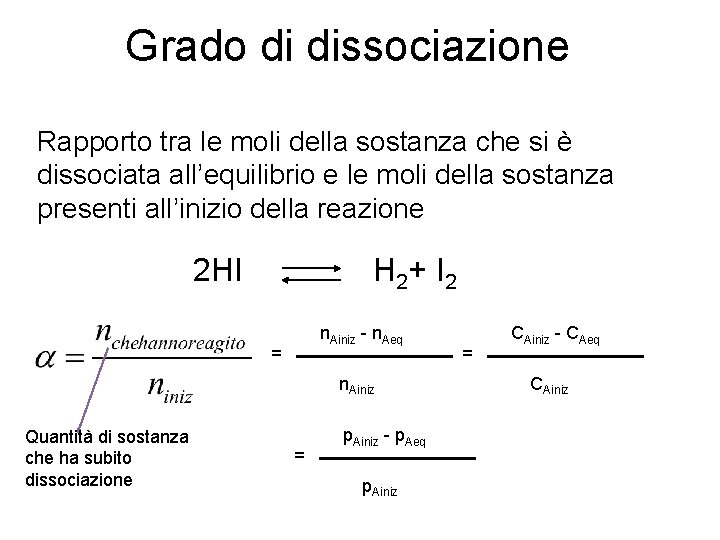
Grado di dissociazione Rapporto tra le moli della sostanza che si è dissociata all’equilibrio e le moli della sostanza presenti all’inizio della reazione 2 HI H 2+ I 2 n. Ainiz - n. Aeq = n. Ainiz Quantità di sostanza che ha subito dissociazione = p. Ainiz - p. Aeq p. Ainiz = CAiniz - CAeq CAiniz

Esempio 2 HI H 2+ I 2 All’inizio ho 10 moli di HI Quando si instaura l’equilibrio, % di a= 40% Quante moli di HI, H 2, I 2 all’equilibrio?

Esempio Se a= 40% , significa che il 40% delle moli di HI si sono dissociate. niniz*a =moli che hanno reagito, quindi 10*40/100 =4 moli di HI dissociate Avro’ dunque 6 moli di HI all’equilibrio: n. HIiniz – n. HIeq= nchehannoreagito 10 -x= 4 => x= 6 Dato che la stechiometria della reazione è la seguente: 2 HI H 2+ I 2 dalla dissociazione di 4 moli di HI si otterranno 2 moli di H 2 e 2 moli di I 2 RISULTATO: 6 moli di HI, 2 moli di H 2 e 2 moli di I 2

Costante di equilibrio e grado di dissociazione 2 HI Moli all’eq. : n 0 ½H H 22++ I½ 2 I 2 n 0½ a [H 2]½ [I 2]½ n 0½ a Per ogni mole iniziale di HI, all’equilibrio ne rimangono (1 -a)n 0 (n 0 sono le moli inizia. Ii) dato che una frazione di esse pari ad an 0 si dissociano. Per ogni an 0 moli che si dissociano si formano a/2 n 0 moli di I 2 e H 2. ½ ½ a 2
- Slides: 45