A talajban l aerob nitrognfixl baktriumok izollsa s

A talajban élő aerob nitrogénfixáló baktériumok izolálása és azonosítása Készítette: Kozma Réka 1

Bevezetés, alapfogalmak Nitrogénfixáló, diazotróf baktériumok: A nitrogén az egyik legfontosabb elem az élő szervezetek számára. Bár a levegő 78%-a nitrogén, a fejlettebb élőlények közvetlen módon azt nem tudják hasznosítani. A talajban, főleg a rizoszféra szintjén élő nitrogénfixáló, ún. diazotróf baktériumok képesek a nitrogén megkötésére; ehhez aerob közeg, tehát levegő, illetve oxigén jelenléte szükséges. A diazotróf baktériumok a molekuláris N 2 -t, a légkör elemi nitrogénjét képesek megkötni és nitrogenáz enzim segítségével a növények számára hozzáférhető ammóniává redukálni. 1 mol N 2 redukálásához 16 mol ATP és 8 elektron szükséges az alábbi reakcióegyenlet szerint N 2 + 10 H+ + 8 e- 2 NH 4+ + H 2 2

Visszatekintés 1970 -es évekig : Kizárólag olyan aerob diazotróf baktériumok voltak ismertek, melyek rendelkeznek ún. „oxigén-védelmi” mechanizmussal, ami megvédi a nitrogenáz enzimet az oxigéntől Ezek a baktériumok az Azotobacter, Azomonas, Derxia és Beijerinckia nemzetségek tagjai, melyekre kevéssé jellemző a növényekkel való társulás 1970 -es évektől: Új, oxigén-védelmi mechanizmussal nem rendelkező fajokat fedeztek fel, melyek azonban hatékonyabbnak bizonyultak a nitrogénfixációhoz szükséges szénhasználat tekintetében Ezek a leggyakoribb növényhez kötődő diazotrófok az Azospirillum, Herbaspirillum, Azoarcus és Acetobacter nemzetségekhez tartoznak. 3

Izolálási és azonosítási módszerek - Döbereiner A módszer lényege: Az Azotobacter, Azomonas, Derxia és Beijerinckia nemzetségekhez tartozó fajok levegővel inkubált agarlemezeken ellenálló telepeket képeznek, megvédve a nitrogenáz enzimet az oxigéntől. Ez az oxigén-védelmi képesség egyszerűbbé teszi az izolációt, mivel semmilyen más baktérium nem tud növekedni ilyen tápagaron. Szükséges készülékek és eszközök: 25 és 35 o. C között szabályozható inkubátor Petri csészék Szilikagél lemezek Autokláv Tiszta munkafelület Steril üvegeszközök Mikroszkóp 4

Izolálási és azonosítási módszerek - Döbereiner Vegyszerek és oldatok I. : Azotobacter és Azomonas izoláláshoz szükséges tápagar (LG tápagar): 20 g szacharózt, 0, 05 g K 2 HPO 4 -ot, 0, 15 g KH 2 PO 4 -ot, 0, 01 g Ca. Cl 2 -ot, 0, 2 g Mg. SO 4. 7 H 2 O-t, 2 mg Na 2 Mo. O 4. 2 H 2 O-t, 0, 01 g Fe. Cl 2 -t, 2, 00 ml 0, 5 %-os etanolban oldott brómtimolkéket, 1 g Ca. CO 3 -at és 15 g agart feloldunk 800 ml desztillált vízben, majd desztillált vízzel 1000 ml-re töltjük fel Derxia izoláláshoz szükséges tápagar: ugyanaz, mint az Azotobacter esetben, azzal az eltéréssel, hogy a szacharóz helyett glükózt vagy keményítőt, valamint a Ca. CO 3 helyett 0, 01 g Na. HCO 3 -ot használunk Beijerinckia izoláláshoz és szilikagél lemezek előkészítéséhez szükséges közeg: A oldat: 1, 1 -es sűrűségűre hígított HCL oldat B oldat: 1, 06 -os sűrűségű Na 2 O 5. Si. O 2 (vízüveg) oldat Winogradsky só –oldat (C oldat): 5 g KH 2 PO 4 -ot, 2, 5 g Mg. SO 4. 7 H 2 O- t, 2, 5 g Na. Cl-ot, 5 mg Na 2 Mo. O 4. 2 H 2 O-t, 0, 05 g Mn. SO 4. 4 H 2 O és 0, 05 g Fe 2(SO 4)3 -ot feloldunk 800 ml desztillált vízben, beállítjuk a p. H-t 6, 5 re, majd desztillált vízzel 1000 ml-re töltjük fel 5

Izolálási és azonosítási módszerek - Döbereiner Vegyszerek és oldatok II. : Folyamatos kevergetés mellett 503 ml A oldatba 500 ml B oldatot öntünk, majd az elkészült oldatot azonnal 30 ml-es Petri csészékbe osztjuk szét Ezeket 24 -48 órán keresztül hagyjuk szilárdulni, majd folyó víz alá helyezzük körülbelül 3 napra, mindaddig, amíg az Ag. NO 3 -teszt negatív nem lesz kloridra Az ilyen módon elkészített lemezek hónapokig eltarthatóak zárt edényben Használat előtt a maradék klorid eltávolítása végett a lemezeket forró desztillált vízbe merítéssel kell sterilizálni Ezután glükózt adagolunk a Winogradsky oldathoz a 10%-os koncentráció eléréséig Ebből 2 ml-es mennyiségeket kis kémcsövekben forrásig melegítünk, majd a felforralt mintákat lemezekre öntjük, amelyek így száríthatóvá válnak tiszta szárító sütőben 6
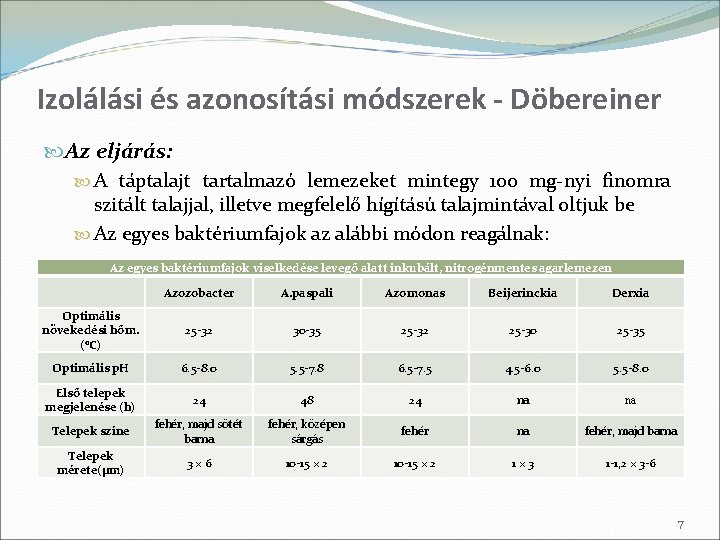
Izolálási és azonosítási módszerek - Döbereiner Az eljárás: A táptalajt tartalmazó lemezeket mintegy 100 mg-nyi finomra szitált talajjal, illetve megfelelő hígítású talajmintával oltjuk be Az egyes baktériumfajok az alábbi módon reagálnak: Az egyes baktériumfajok viselkedése levegő alatt inkubált, nitrogénmentes agarlemezen Azozobacter A. paspali Azomonas Beijerinckia Derxia Optimális növekedési hőm. (o. C) 25 -32 30 -35 25 -32 25 -30 25 -35 Optimális p. H 6. 5 -8. 0 5. 5 -7. 8 6. 5 -7. 5 4. 5 -6. 0 5. 5 -8. 0 Első telepek megjelenése (h) 24 48 24 na na Telepek színe fehér, majd sötét barna fehér, középen sárgás fehér na fehér, majd barna Telepek mérete(μm) 3× 6 10 -15 × 2 1× 3 1 -1, 2 × 3 -6 7

Izolálási és azonosítási módszerek - Döbereiner Derxia fajok izolálása és azonosítása: A D. gummosa azonosítása egyszerűbb 35 o. C-on, 7 napi inkubálást követően A képződött széles és kemény telepeket eltávolítjuk, majd homokkal és steril vízzel való összekeverés után 2 órára állni hagyjuk. A kész szuszpenzió LG közegen 2 különböző típusú telepet alkot: kicsi, bézs színű, N 2 fixálásra nem képes telepeket, és nagy, barna N 2 -fixáló telepeket. A telepek számának meghatározása nem egyszerű, a legjobb becslést a Derxia-t tartalmazó talajszemcsék illetve gyökérdarabok aránya adja 8

Izolálási és azonosítási módszerek - Döbereiner Beijerinckia fajok izolálása és azonosítása: A Beijerinckia fajok a legjobban szilikagél lemezen izolálhatóak: Levegőztetett, finomra szitált (1 mm) talaj 20 -100 mg-ját egyenletesen eloszlatjuk a lemezen 4 -10 napos , 30 o. C-on történő inkubálás után : A Beijernickia indica kisméretű, fehér telepeket képez, amik rövid időn belül széles, és ellenálló telepekké alakulnak A B. fluminense telepei kicsik, világos bézs színűek és szárazak A telepek számának meghatározása a talajban előforduló mikrotelepek alapján történhet, melyek 103 -104 telepet alkotnak szilikagél lemezen 9

Azospirillum izolálása és azonosítása – Reinhold, Khammas és Döbereiner A módszer lényege: Az ide tartozó 5 faj felfedezése egy olyan nitrogénmentes félig szilárd közeg bevezetésének köszönhető, amelyen a mikroorganizmusok a közeg azon régiójába gyűlnek, ahol a légzési sebességük egyensúlyban van az oxigén diffúziós sebességével Nagyon jellegzetes fátyolszerű filmet képeznek 5 mm-re a felszíntől, majd a N 2 -függő növekedésük miatt egyre közelebb húzódnak a felszínhez, ahol egyre több sejt halmozódik fel, ezt használjuk ki az izolálási eljárás során. Szükséges készülékek és eszközök: 35 és 41 o. C között szabályozható inkubátor Petri csészék Autokláv Tiszta munkafelület Steril üvegeszközök Mikroszkóp 10

Azospirillum izolálása és azonosítása – Reinhold, Khammas és Döbereiner Vegyszerek és oldatok I. : Azospirillum izoláláshoz szükséges (NFb) alapközeg: 5 g D, L- almasavat, 0, 5 g K 2 HPO 4 -ot, 0, 2 g Mg. SO 4. 7 H 2 O-t, 0, 1 g Na. Cl-t, 0, 02 g Ca. Cl 2. 2 H 2 O-t, 2, 00 ml „minor element” oldatot, 2, 00 ml 0, 5 %-os, 0, 2 M-os KOH-ban oldott 0, 5 %-os brómtimolkéket, 1, 64%-os Fe EDTA oldatot, 1, 00 ml vitamin oldatot és 1, 75 g agar-agart feloldunk 800 ml desztillált vízben, KOH segítségével a p. H-t 6, 8 -ra állítjuk, majd az oldatot desztillált vízzel 1000 ml-re töltjük fel. Fontos, hogy az egyes komponenseket a megjelölt sorrendben adagoljuk, hogy elkerüljük a vas illetve más sok csapadékképzését. „Minor element” oldat: 0, 40 g Cu. SO 4. 5 H 2 O-t, 0, 12 g Zn. SO 4. 7 H 2 O-t, 1, 4 g H 2 BO 4 -ot, 1, 00 g Na 2 Mo. O 4. 2 H 2 O-t és 1, 5 g Mn. SO 4. H 2 O-t feloldunk 800 ml desztillált vízben, majd desztillált vízzel 1000 ml-re töltjük fel. Vitamin oldat: 10 mg biotin, 20 mg pyridoxol- HCl és 100 ml desztillált víz keveréke 11

Azospirillum izolálása és azonosítása – Reinhold, Khammas és Döbereiner Vegyszerek és oldatok II. : Burgonya közeg: 200 g friss, hámozott burgonyát 30 percig 1000 ml desztillált vízben főzünk, majd pamutlapokon keresztül szűrünk. 2, 5 g D, L-almasav, 2, 5 g szacharóz és 15 g agar hozzáadása után a p. H-t 6, 8 -ra állítjuk. Félig szilárd közeg az A. amazonese izolálásához (LGI) : 0, 20 g K 2 HPO 4 -ot, 0, 60 g KH 2 PO 4 -ot, 0, 002 g Ca. Cl 2. 2 H 2 O-t, 0, 20 g Mg. SO 4. 7 H 2 O-t, 0, 002 g Na 2 Mo. O 4. 2 H 2 O-t, 0, 01 g Fe. Cl 3 -ot, 5 ml 0, 2 Mos KOH-ban oldott 0, 5 %-os brómtimolkéket, 5 g szacharózt és 1, 8 g agar-agart feloldunk 800 ml desztillált vízben, majd desztillált vízzel 1000 ml-re töltjük fel. 12

Azospirillum izolálása és azonosítása – Reinhold, Khammas és Döbereiner Az eljárás menete az A. brasilense, A. lipoferum és A. irakense izolálásához: a fentiekben ismertetett NFb (nitrogénmentes bázis) közeget 0, 1 ml talaj vagy gyökér szuszpenzióval oltjuk be, majd 35, illetve az A. irakense esetében 30 o. C-on inkubáljuk → 3 -5 nap elteltével papírszerű fehér film képződik a közeg felületén A kinőtt baktériumkultúrát 15 g/l-es 0, 02 g élesztőkivonatot tartalmazó NFb tápagarra átoltjuk → 1 hét elteltével kicsi, fehér és hullámos telepek figyelhetőek meg A különálló telepeket ezután új NFb közegbe helyezzük, majd tisztítjuk burgonyás közegbe való átoltással → 1 hét elteltével kicsi, rózsaszínes telepeket ismét áthelyezünk egy új NFb közegre oltjuk át, ahonnan a baktériumok már mikroszkóppal azonosíthatóak Az eljárás menete az A. halopraeferans esetében: Az eljárás itt is NFb közegben történik, de a p. H-t 8, 5 -re kell beállítani, 1, 2%-os Na. Cl hozzáadása hőmérséklet 41 o. C szükséges, valamint az inkubálási 13

Azospirillum izolálása és azonosítása – Reinhold, Khammas és Döbereiner Az eljárás menete az A. amazonense izolálásánál: Ebben az esetben LGI közeget használunk, amin beoltás és 35 o. C-on történő inkubálás után 3 -5 nap elteltével fehér film figyelhető meg A kinőtt baktériumkultúrát 20 g/l-es 0, 02 g élesztőkivonatot tartalmazó LGI agarlemezekre átoltjuk → 5 nap elteltével kicsi, fehér és hullámos telepek figyelhetőek meg A különálló telepeket ezután új LGI közegre oltjuk át a savképződés nélküli nitrogénfüggő növekedés érdekében A tisztító szélesztést szacharózt és malátát tartalmazó burgonyás közegen végezzük → a képződő telepek fehérek, 5 mm szélesek és nagyban különböznek a előzőekben vizsgált fajok telepeitől 14

Endofita diazotrófok izolálása és azonosítása (Döbereiner, Cavalcante, Gillis, Reinhold-Hurek) A módszer lényege: A Herbaspirillum, Azoarcus nemzetségekhez tartozó fajok és az A. diazotrophicus obligát növényi endofiták, a növény belsejében élő baktériumok, ezért csak a gazdanövényből lehet őket izolálni Ehhez a tulajdonsághoz sokkal hatékonyabb biológiai nitrogénkötési képesség társul, ami pedig előny a növény növekedésében Szükséges készülékek és eszközök: 30 és 35 o. C között szabályozható inkubátor Petri csészék Autokláv Tiszta munkafelület Steril üvegeszközök Mikroszkóp 15

Endofita diazotrófok izolálása és azonosítása (Döbereiner, Cavalcante, Gillis, Reinhold-Hurek) Vegyszerek és oldatok : Herbaspirillum spp. , H. seropedicae és H. rubrisubalbicans izoláláshoz szükséges félig szilárd (JNFb) tápagar: 5 g D, L-almasavat, 1, 5 g K 2 HPO 4 -ot, 0, 2 g Mg. SO 4. 7 H 2 O-t, 0, 02 g Na. Cl 2. 2 H 2 O-t, 2, 00 ml „minor element” oldatot (lásd az Azospirillum részben), 1, 00 ml vitamin oldatot (lásd az Azospirillum részben), 4 ml 1, 64%-os Fe EDTA oldatot, 2 ml 0, 2 M-os KOH-ban oldott 0, 5 %-os brómtimolkéket és 2, 0 g agar-agart feloldunk 800 ml desztillált vízben, a p. H-t 6, 0 -ra állítjuk, majd az oldatot desztillált vízzel 1000 ml-re töltjük fel. Fontos, hogy az egyes adalékokat a megjelölt sorrendben adagoljuk. Burgonya közeg: 200 g friss, hámozott burgonyát 30 percig 1000 ml desztillált vízben főzzük, majd pamutlapokon keresztül szűrjük. 2, 5 g D, L-almasav, 2, 5 g szacharóz és 15 g agar hozzáadása után a p. H-t 6, 8 -ra állítjuk. 16

Endofita diazotrófok izolálása és azonosítása (Döbereiner, Cavalcante, Gillis, Reinhold-Hurek) Izolálási eljárás a Herbaspirillum fajok esetében: Mindhárom említett faj leginkább félig szilárd JNFb közeg gyökér-, vagy levélminta 10 -2 -10 -6 hígítású szuszpenziójából identifikálható: A H. seropedicae fajok esetében bármilyen típusú Gramineae levél, a H. rubrisubalbicans fajoknál pedig cukornád beoltását követően vékony, az Azopirillum spp. -nél tapasztalt filmréteg figyelhető meg, ami ebben az esetben kisebb sejtekből (0, 6 -0, 7 × 3 -5 μm) áll Az izolálás 0, 02 g élesztőkivonat és 4 ml brómtimolkék tartalmú NFb agarlemezen történik A képződő kicsi, nedves, fehér színű telepek közepe egy hét elteltével sötétkék színűvé válik A szacharóz és maláta tartalmú burgonyaagaron történő tisztító szélesztés apró, nedves, emelt telepeket eredményez, melyek közepe barnás 17

Endofita diazotrófok izolálása és azonosítása (Döbereiner, Cavalcante, Gillis, Reinhold-Hurek) Izolálási eljárás a Azoarcus fajok esetében: A félig szilárd NFb közegben történő izolálási eljárás megegyezik a Herbaspirillum fajok esetében ismertetett módszerrel A telepek szétoszthatatlan, sárgás pigmenteket képeznek a közeg felszínén, melyek etanol (mint szénforrás) alkalmazásánál még intenzívebbek Izolálási eljárás az Acetobacter diazotrophicus esetében: Az izolálás félig szilárd LGIP közegen történik : az A. amazonense fajok esetében ismertetett LGI közeg 100 g/l-re növelt szacharóz vagy cukornád koncentrációval, illetve 2, 0 g agar koncentrációval A p. H-t ecetsav segítségével 5, 5 -re állítjuk Ezt a közeget 0, 1 ml cukornád szár- vagy levélmintával beoltva 4 -6 nap elteltével megfigyelhető, hogy az eredetileg a felszín alatt található filmréteg a felszín felé mozog és sötét narancssárgás színt ölt Hasonló közegben 20 g/l-es agarlemezeken apró, nedves, sötét narancs színű telepek képződnek 1 hét elteltével A tisztítás ebben az esetben is burgonya közegen történik (maltóz helyett 10% cukornád tartalommal), amin 7 nap múltán sötétbarna, nedves telepek képződése figyelhető meg 18

Források J. Döbereiner: Enrichement, isolation and counting of soil microorganisms -Isolation and identification of aerobic nitrogenfixing bacteria from soil and plants –In: Alef K. and Nannipieri P. (Editors): Methods in Applied Soil Microbiology and Biochemistry, Academic Press Limited, London, 1995 Nitrogénkötő baktériumok izolálása dús füves területekről: http: //www. fermentia. hu/pdf/nitrogenkoto. pdf Nitrogénfixáló baktériumok szerepe a tápanyagellátásban: http: //www. greenpack. hu/agrobio_system. php? page=Bio-Nitro. Phos%20 bakt%E 9 riumtr%E 1 gya Nitrogenáz és nitrogénfixálás: http: //www. chem. science. unideb. hu/Oktatas/K 3125 Eload 8. pdf A nitrogén körforgása: A biológiai nitrogénkötés - Putnoky: http: //www. ttk. pte. hu/biologia/genetika/libr_gen/N 2 fix_1. pdf 19

Képek http: //www. jircas. affrc. go. jp/english/publication/hig hlights/2003 -17. html http: //www. maximumyield. com/article_sh_db. php? a rticle. ID=406 20
- Slides: 20