A tabela peridica dos elementos Estrutura da tabela

A tabela periódica dos elementos Estrutura da tabela periódica

1. Períodos Famílias na Tabela

A Tabela Periódica surgiu da necessidade de se organizar os elementos químicos. O químico russo Dimitri Ivanovitch Mendeleev foi o primeiro a dar forma à estrutura da Tabela. Graças a este cientista, suas anotações e descobertas posteriores, a Tabela adquiriu a forma que encontramos hoje. Para saber como a Tabela evoluiu, basta ficar atento ao fato de que no primeiro formato ela possuía apenas 63 elementos e atualmente já possui mais de 100, e ainda está aberta a novas descobertas, ou seja, está sempre evoluindo. Um grande quesito usado por Mendeleev na organização foi agrupar os elementos de acordo com características comuns. Foi assim que surgiram as famílias (grupos). As principais são:

Família I A: metais alcalinos Família II A: metais alcalinoterrosos Família III A: família do Boro Família IV A: família do Carbono Família V A: família do Nitrogênio Família VI A: Calcogênios Família VII A: Halogênios Família 0: Gases Nobres

Os elementos situados na mesma família apresentam propriedades semelhantes e se posicionam nas linhas verticais da tabela. Existem 18 famílias na classificação atual. Outro critério usado para organizar os elementos corresponde aos períodos que se encontram nas linhas horizontais da tabela. Neste caso, recebem a numeração de 1 a 7 correspondente às sete camadas eletrônicas (K, L, M, N, O, P, Q), sendo que no período 1 a distribuição de elétrons vai até a camada K, e no período 2 os elétrons ocupam a camada L, e assim sucessivamente.

Como exemplo, acompanhe a distribuição dos elétrons do elemento Lítio: K 1 s 2 L 2 s 1 M 3 s 2 p 3 p 3 d Observe que foram ocupados apenas dois subníveis: K e L. Dizemos, então, que o Lítio pertence ao período 2 porque a distribuição eletrônica foi até a camada 2.
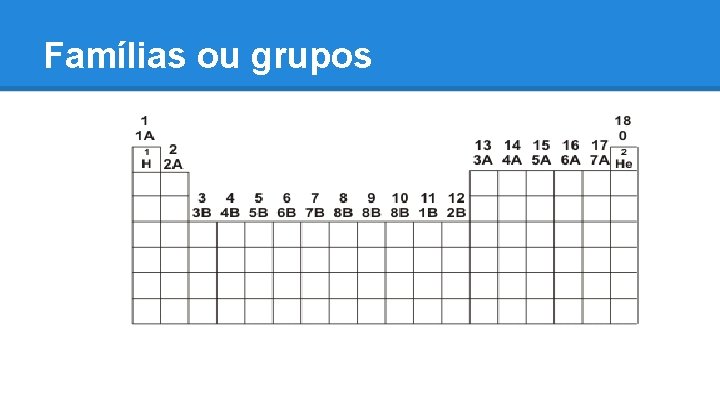
Famílias ou grupos

Ao contrário dos períodos, as Famílias da Tabela Periódica são distribuídas de forma vertical, em 18 colunas. Os elementos químicos que estão localizados na mesma coluna da Tabela Periódica são considerados da mesma família pois possuem propriedades físicas e químicas semelhantes. Esse elementos fazem parte de um mesmo grupo porque apresentam a mesma configuração de elétrons na última camada (camada de valência). A numeração das Famílias da Tabela Periódica se inicia no 1 A (representado em nossa tabela periódica com o número 1) e continua até o zero ou 8 A (representado em nossa tabela periódica pelo número 18). Existe também a Família B.

A Tabela Periódica é divida em Metais, Não. Peri. Metais e Semi-Metais e suas famílias são: A Tabela Periódica é divida em Metais, Não-Metais e Semi-Metais e suas famílias são: Família 1 A (Grupo 1): Metais Alcalinos Família 2 A (Grupo 2): Metais Alcalino-Terrosos Família B (Grupo 3 à 12): Metais de Transição Família 3 A (Grupo 13): Família do Boro Família 4 A (Grupo 14): Família do Carbono Família 5 A (Grupo 15): Família do Nitrogênio Família 6 A (Grupo 16): Calcogênios Família 7 A (Grupo 17): Halogênios Família 0 ou 8 A (Grupo 18): Gases Nobres • • •

O primeiro grupo é conhecido como Metais alcalinos (com exceção do Hidrogénio (H)) e a segunda família é a dos Metais Alcalino-Terrosos. O conjunto formado entre o grupo 3 e o grupo 12 ou Família B denomina-se Metais de Transição. Depois desse conjunto vem o grupo 13 que é conhecido por Família do Boro, seguido da Família do Carbono (Grupo 14) e da Família do Nitrogênio (Grupo 15). O grupo 16 é conhecido como Calcogênios, o grupo 17 como Halogênios e, por fim, o grupo 18 que compreende os Gases Nobres. As duas últimas linhas da Tabela Periódica representam as Famílias dos Lantanídeos e dos Actinídeos, como pode ser visto na nossa Tabela Periódica Completa.
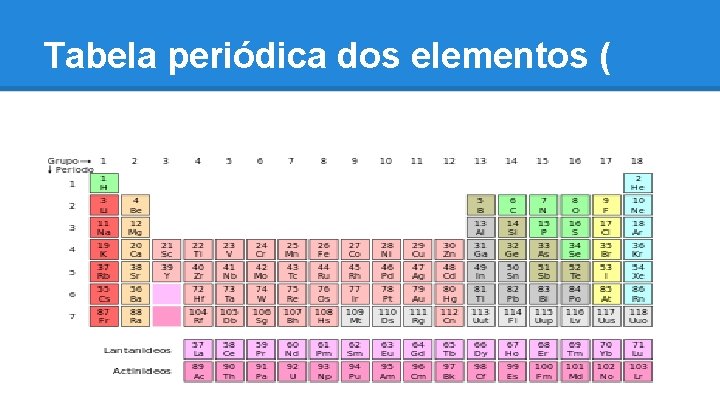
Tabela periódica dos elementos (

Leia as seguintes afirmações: I. O elemento químico de número atômico 53 possui 1 elétron de valência. II. A configuração eletrônica do elemento químico com número atômico 45 possui 7 elétrons no subnível d. III. 3 s 23 p 6 corresponde à configuração eletrônica dos elétrons de valência do elemento químico de númeroatômico 34. IV. A configuração eletrônica do elemento químico de número atômico 39 possui 5 níveis energéticos

Estão corretas as afirmações em: a) I e II apenas. b) I e III apenas. c) II e III apenas. d) II e IV apenas. e) III e IV apenas

Os elementos de transição formam compostos coloridos. Devido a essa característica, sãoutilizados para várias finalidades, como, por exemplo, em tatuagens. Os pigmentos coloridos maiscomumente utilizados incluem sais de cádmio (amarelo ou vermelho), de cromo (verde), de cobalto (azul)e de ferro (castanho, rosa e amarelo). Todos os metais citados no texto: a) estão situados no quarto período da Tabela Periódica. b) são denominados elementos de transição interna. c) pertencem ao bloco f da Tabela Periódica. d) são denominados elementos representativos. e) apresentam o elétron de maior energia situado no subnível d.

A classificação atual dos elementos químicos é feita em períodos, ou seja, em sequências desuas propriedades. Essas sequências ou períodos são dispostos na ordem crescente dos númerosatômicos dos elementos químicos. Assinale V para verdadeiro e F para falso a respeito da tabelaperiódica: a) ( ) Os elementos pertencentes ao grupo 17 são os que apresentam menor eletronegatividade. b) ( ) Os metais alcalinos apresentam os menores potenciais de ionização. c) ( ) Num mesmo período, o raio atômico do halogênio é sempre maior do que o do metal alcalino. d) ( ) Os símbolos dos elementos químicos: criptônio, cádmio, arsênio são, respectivamente, Cr, Cd, Ar.

Com relação ao elemento químico, cujo número atômico é igual a 26, é correto afirmar que: a) É um metal e está localizado no bloco s, família 2, 3º período da tabela periódica. b) É um metal e está localizado no 4ºperíodo da tabela periódica, família 8. c) É um metal e está localizado no bloco d, família 6, 4º período da tabela periódica. d) É um ametal e está localizado no bloco d, 3º período da tabela periódica. e) É um ametal e está localizado no bloco d, 4º período da tabela periódica
- Slides: 16