a Reazioni che non comportano variazione del numero

















- Slides: 20




a) Reazioni che non comportano variazione del numero di ossidazione degli atomi di sostanze che partecipano alla reazione (nessun trasferimento di e-): reazioni acido-base e reazioni di scambio. b) Reazioni che comportano variazione del numero di ossidazione di alcuni atomi di sostanze che partecipano alla reazione (trasferimento di e-): reazioni di ossido-riduzione o reazioni redox.

Reazioni acido-base (reazioni di salificazione) Reazioni fra una sostanza a carattere acido (ossoacidi, idracidi, ossidi acidi) e una sostanza a carattere basico (idrossidi, ossidi basici, basi protoniche) con formazione di sali. • HNO 3 + Na. OH = Na. NO 3 + H 2 O • 2 HCl + Ca. O = Ca. Cl 2 + H 2 O • SO 3 + Ba. O = Ba. SO 4 • CO 2 + Ca(OH)2 = Ca. CO 3 + H 2 O • H 2 SO 4 + 2 NH 3 = (NH 4)2 SO 4 Base protonica

La maggior parte di reazioni in soluzione acquosa avvengono tra elettroliti cioè sostanze che si dissociano in ioni. Si dissociano: • Acidi • Basi • Sali

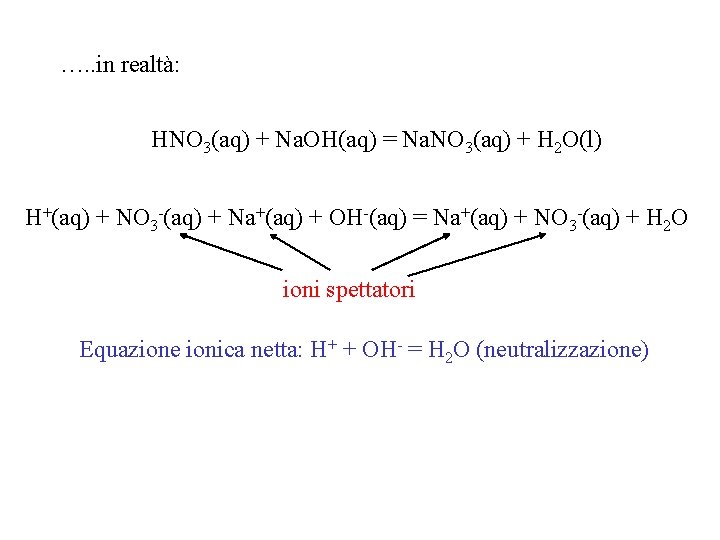
…. . in realtà: HNO 3(aq) + Na. OH(aq) = Na. NO 3(aq) + H 2 O(l) H+(aq) + NO 3 -(aq) + Na+(aq) + OH-(aq) = Na+(aq) + NO 3 -(aq) + H 2 O ioni spettatori Equazione ionica netta: H+ + OH- = H 2 O (neutralizzazione)

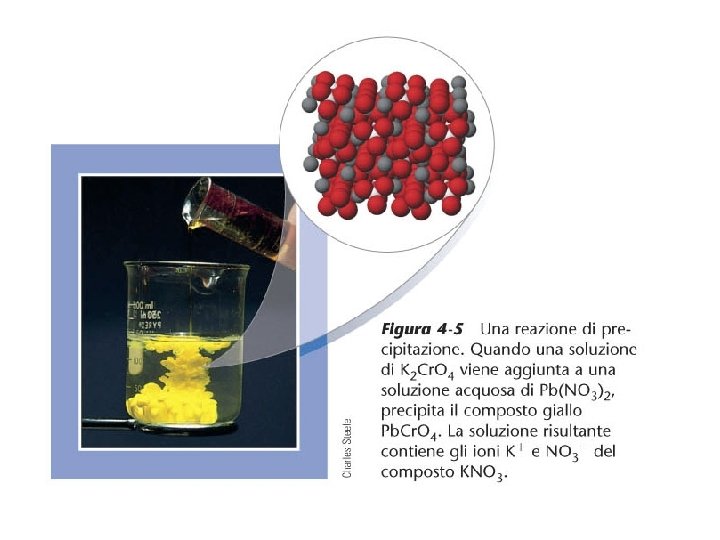
Reazioni di scambio Tali reazioni comportano lo scambio di porzioni (cationi o anioni) delle sostanze reagenti Fe. S(s) + 2 HCl(aq) = Fe. Cl 2 + H 2 S(g) Na 2 CO 3(aq) + Ca(OH)2(aq) = Ca. CO 3(s) + 2 Na. OH(aq) (precipitazione) 2 KI(aq) + Pb(NO 3)2(aq) = 2 KNO 3(aq) + Pb. I 2(s) Ca. CO 3(s) + 2 CH 3 COOH(aq) = Ca(CH 3 COO)2(aq) + H 2 CO 3(aq) = H 2 O(l) + CO 2(g)


Reazione di precipitazione.

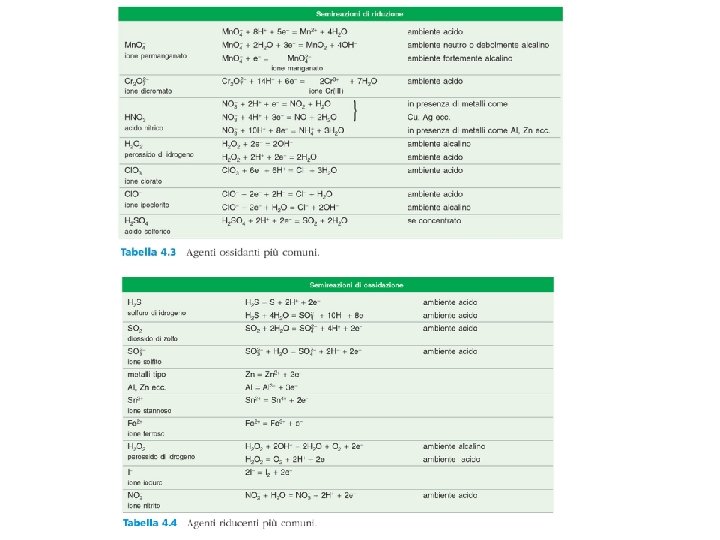
Reazioni in cui alcuni atomi variano il loro numero di ossidazione: si ha trasferimento di e- tra le specie coinvolte. Se vi è una sostanza contenente un elemento che aumenta il proprio n. o. , deve necessariamente essere presente un’altra sostanza che contiene un elemento che diminuisce il proprio n. o. Ossidazione: una specie chimica perde elettroni n. o. aumenta Riduzione: una specie chimica acquista elettroni n. o. diminuisce Riducente: specie che aumenta il proprio n. o. (si ossida perde e-) Ossidante: specie che riduce il proprio n. o. (si riduce acquista e-) CH 4(g) + 2 O 2(g) = CO 2(g) + 2 H 2 O(g) (reazione di combustione) 3 H 2(g) + N 2(g) = 2 NH 3(g) (sintesi dell’ammoniaca) Cu(s) + 2 Ag. NO 3(aq) = 2 Ag(s) + Cu(NO 3)2 (aq) (reazione di spostamento)




K 2 Cr 2 O 7(aq) + 6 Fe. SO 4(aq) + 7 H 2 SO 4(aq) = Cr 2(SO 4)3(aq) + 3 Fe 2(SO 4)3 (aq) + K 2 SO 4 (aq) + 7 H 2 O(l)

Bi 2 O 3 (s) + 2 Na. Cl. O(aq) + 2 Na. OH(aq) = 2 Na. Bi. O 3(aq) + 2 Na. Cl(aq) + H 2 O(l)


Reazioni di disproporzionamento o dismutazione Una sola specie chimica agisce sia da ossidante che da riducente Cl 2 + 2 Na. OH = Na. Cl + Na. Cl. O + H 2 O 3 NO 2 + H 2 O = 2 HNO 3 + NO

