A nanotechnolgia kolloidkmiai alapjai BMEVEFAA 409 ltalnos ismertet

A nanotechnológia kolloidkémiai alapjai (BMEVEFAA 409) Általános ismertető: Dr. Hórvölgyi Zoltán egy. tanár, BME Fizikai Kémia és Anyagtudományi Tanszék, Fizikai Kémia Laboratórium F ép. I. lépcsőház, magasföldszint (balra); Telefon: 463 2911; e-mail: horvolgyi. zoltan@vbk. bme. hu A Kolloidkémia Csoport Instagram oldala : instagram. com/nanokollofficial Helyszín: Teams (on-line) Időpontok: Minden hétfőn és pénteken: 8: 15 -10: 00

Felkészülés: Az előadások vázlatos anyaga (amelyeket az előadáson kivetítek) hozzáférhető a tárgy Teams-csoportjában. Segédanyag: Elektronikus jegyzet Hórvölgyi Zoltán: A nanotechnológia kolloidkémiai alapjai, Budapest: Typotex Kiadó, 2011 http: //www. interkonyv. hu/konyvek/A%20 nanotechnol%C 3%B 3 gia%20 kolloidk%C 3%A 9 miai%20 alapjai Érdemjegy: Az előadáson kerül meghirdetésre.

A tantárgy célkitűzése: 1. A kolloidkémiai szemlélet kialakítása. 2. A klasszikus kolloidkémiai iparokat és eljárásokat ismertető tárgyak megalapozása, valamint a kolloidika modern anyagtudományi (nanotechnológiai) szerepének bemutatása. Az előadás keretében ismertetjük a különböző kolloid rendszerek legfontosabb tulajdonságait. Foglalkozunk a kolloidstabilitás általános és speciális kérdéseivel. Tárgyaljuk a kolloid rendszerek előállításának fontosabb szempontjait. Válogatást adunk a kolloid rendszerek vizsgálati módszereiről. Néhány konkrét példán keresztül rávilágítunk a tanultak gyakorlati jelentőségére.

A nanovilág felé a tudományban: 1856: Michael Faraday: aranyszol, John Tyndall-jelenség 1860: Thomas Graham: a kolloidok elnevezése az enyv (κολλα) görög neve Az anyagok csoportosítása: - krisztalloidok (jól kristályosíthatók, diffúziójuk gyors) - kolloidok (nem kristályosíthatók, diffúziójuk lassú) A századforduló fő kérdései a kolloidokkal kapcsolatban: 1. Homogén vagy heterogén rendszerek? - oldatokról van szó (homogén: oldatelmélet)! - szuszpenziók (heterogén: szuszpenzió elmélet)! 2. Speciális anyagfajta (enyvszerű anyagok)?
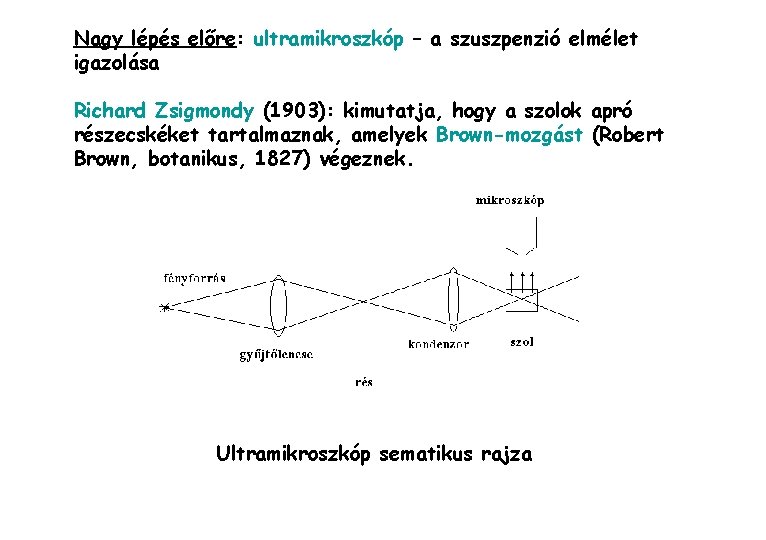
Nagy lépés előre: ultramikroszkóp – a szuszpenzió elmélet igazolása Richard Zsigmondy (1903): kimutatja, hogy a szolok apró részecskéket tartalmaznak, amelyek Brown-mozgást (Robert Brown, botanikus, 1827) végeznek. Ultramikroszkóp sematikus rajza

Korabeli ultramikroszkóp https: //www. flickr. com/photos/zeissmicro/6892932822 Nanoméretű (kolloid) Ag-szemcsék diszperziója https: //pubs. acs. org/doi/10. 1021/nl 034372 s Dark-field optical image of Ag nanoparticles. The field of view is approximately 130 × 170 μm 2. Ultramikroszkóp összeállítása és a Brown-mozgás megfigyelése https: //www. youtube. com/watch? v=wiat. SDf. Ki 44

Diszperz rendszerek (Wolfgang Ostwald: diszperzrendszer elmélete) Diszperz rendszer: egyik komponens a másikban diszpergált (eloszlatott) formában van jelen A kolloidokat a homogén (molekuláris, atomi szintű keveredés) és heterogén rendszerek közé helyezi el: Amikroszkópos valódi oldat (pl. cukor-oldat) Szubmikroszkópos kolloid rendszerek 1 -1000 nm-es részecskék HOMOGÉN 1 vízmolekula kb. 0, 3 nm KOLLOID 1 nm = 10 -9 m Durva mikroheterogén rendszerek (vízben ülepedő homok) HETEROGÉN

Peter Petrovich von Weimarn vizsgálatai szerint minden anyag (még a kristályosak is!) kolloid állapotba hozhatók (l. később a Weimarn-szabályt, ill. görbét). A válaszok rövid megfogalmazása: 1. A kolloid rendszerek a homogén és a heterogén rendszerek közé helyezhetők el. 2. A kolloid nem anyagfajta, hanem állapot.
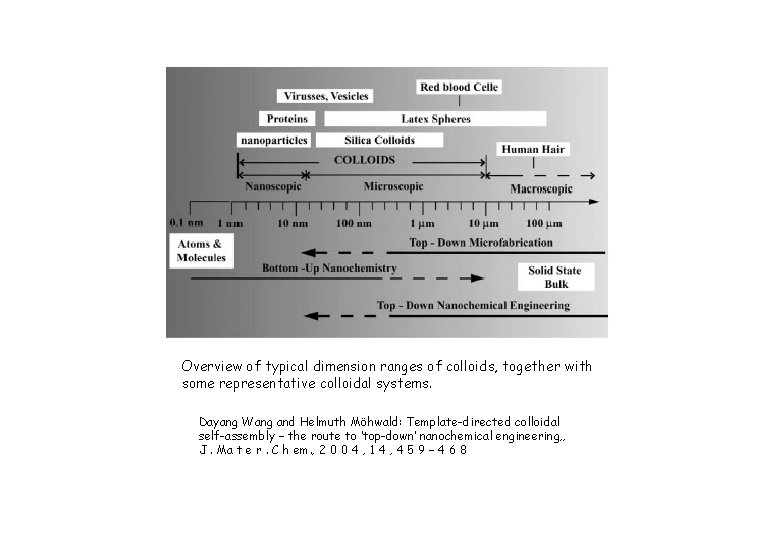
Overview of typical dimension ranges of colloids, together with some representative colloidal systems. Dayang Wang and Helmuth Möhwald: Template-directed colloidal self-assembly – the route to ‘top-down’ nanochemical engineering, , J. Ma t e r. C h em. , 2 0 0 4 , 1 4 , 4 5 9 – 4 6 8

A nanotechnológia kezdetei: „ösztönös” nanotechnológusok Markus Niederberger, 2006 Markus. Niederberger@mpikg. m pg. de

A nanotechnológia kezdetei: a program 1959 – Richard P. Feynman MINIATÜRIZÁLÁS There's Plenty of Room at the Bottom 1. „Enciklopédia egy tű hegyén”: >>> nanolitográfia 2. Molekuláris gépek előállítása A FOGYASZTÁSI JAVAK MINÉL KISEBB MÉRETEKBEN, MINÉL HATÉKONYABBAN TÖRTÉNŐ ELŐÁLLÍTÁSA (a természet utánzása): ELEKTRONIKA, SZÁMÍTÓGÉPIPAR, OPTIKA, stb. Fotó: Főző A. internetes anyagából

A nanotechnológia kezdetei: elnevezés A nanotechnológia szót Norio Taniguchi használta először 1974 -ben azon folyamatok elnevezésére, amelyek során az anyagot nanométeres skálán manipuláljuk. Ma a fogalom (a nano-biotechnológiával együtt) magába foglalja mindazokat az eljárásokat, amelyek során előállítjuk, jellemezzük és működtetjük a nanoléptékben strukturált halmazokat és nanoléptékű objektumokat.

A nanovilág felé a technológiákban Miniatürizálás Önszerveződés Természetutánzás (Transzhumanizmus)
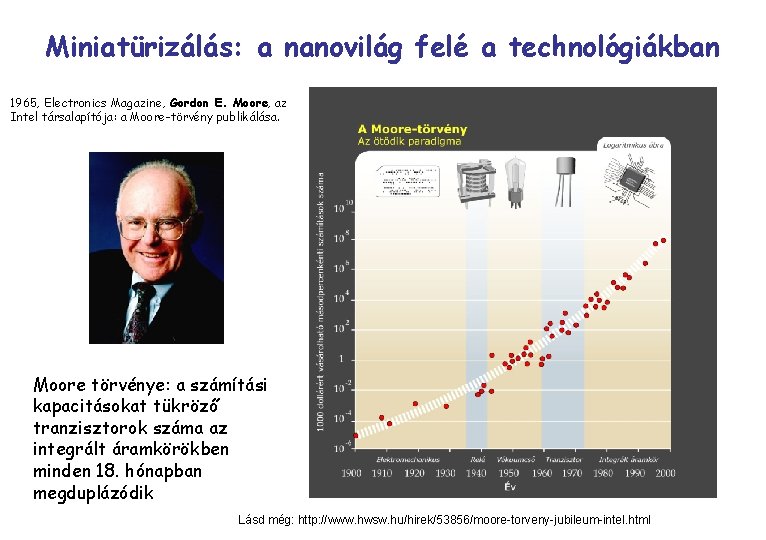
Miniatürizálás: a nanovilág felé a technológiákban 1965, Electronics Magazine, Gordon E. Moore, az Intel társalapítója: a Moore-törvény publikálása. Moore törvénye: a számítási kapacitásokat tükröző tranzisztorok száma az integrált áramkörökben minden 18. hónapban megduplázódik Lásd még: http: //www. hwsw. hu/hirek/53856/moore-torveny-jubileum-intel. html
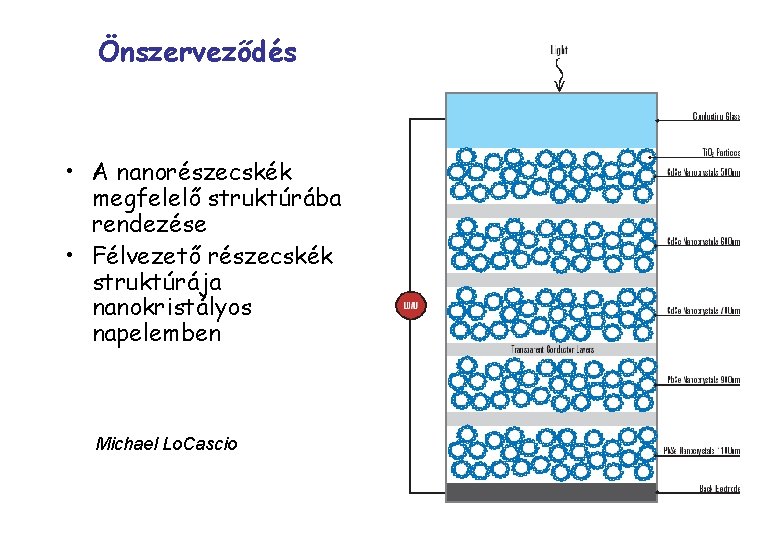
Önszerveződés • A nanorészecskék megfelelő struktúrába rendezése • Félvezető részecskék struktúrája nanokristályos napelemben Michael Lo. Cascio
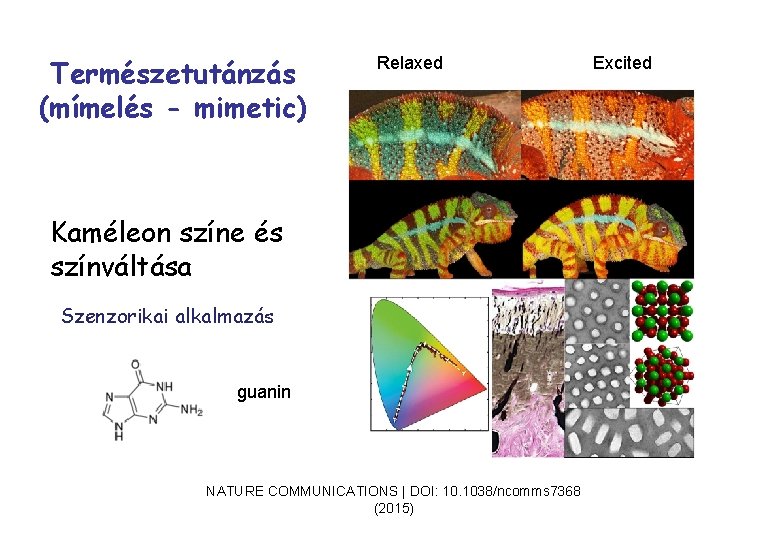
Természetutánzás (mímelés - mimetic) Relaxed Kaméleon színe és színváltása Szenzorikai alkalmazás guanin NATURE COMMUNICATIONS | DOI: 10. 1038/ncomms 7368 (2015) Excited

A nanotechnológia definíciója Megfelelő atomok, molekulák, nano-részecskék megfelelő struktúrákba* való rendeződése (rendezése), majd ezen struktúrák valamilyen előnyös funkciójában való működtetése. Nanoanyagok (nem folytonos, 1 -100 nm léptékben szabdalt) Szerkezeti – Funkcionális – Reszponzív (intelligens) anyagok *Nanoléptékű strukturáltság, ill. objektum (pl. fehérjemolekula)

A nanotechnológiai területek csoportosítása 1. nanotechnológiai megoldások (szenzorok, bevonatok, kompozitok, membránok stb. ), amelyek létező iparágakhoz kapcsolódnak, ezen iparágak termékeinek hozzáadott értékét növelik (öntisztító bevonatok) 2. ún. „romboló” technológiai megoldásokat (disrupters), amelyek létező termékeket és/vagy technológiai megoldásokat szorítanak ki a piacról (világítástechnika) 3. A harmadik csoportba kerülnek azok a nanotechnológiai megoldások, amelyekre építve új, korábban nem létező iparágak jelennek meg, és alakítják át a feldolgozóipar (és a szolgáltatások) szerkezeti összetételét. (diagnosztika és gyógyászat) (A NANOTECHNOLÓGIA ÉS A JELENLEGI JÖVŐ IPARÁGAK, 2005, Szalavetz Andrea)

Szerkezeti nanoanyagok Nanorészecskékkel töltött polimerek: nanokompozitok Előnyösebb mechanikai (szerkezeti) tulajdonság Egyfalú szénnanocsövek szakítószilárdsága (GPa) összevetve már alkalmazást nyert, nagy szilárdságú anyagokéval (K. -T. Lau és D. Hui, Composites B, 33, 2002, 263)
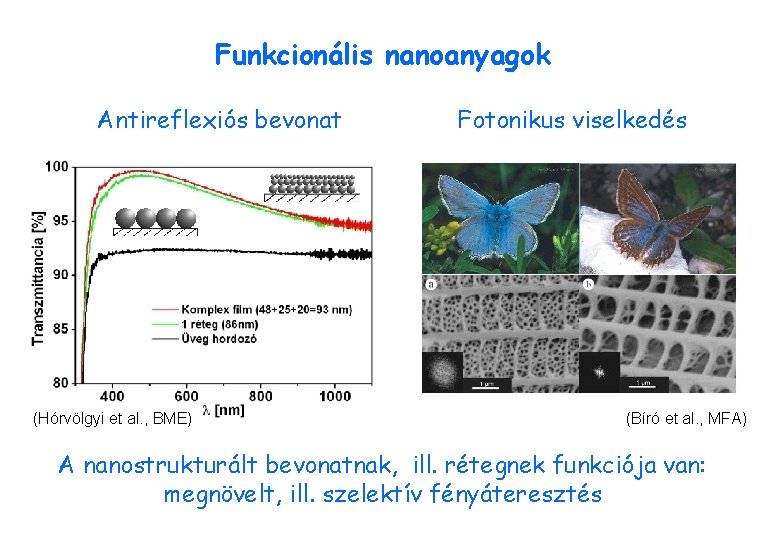
Funkcionális nanoanyagok Antireflexiós bevonat (Hórvölgyi et al. , BME) Fotonikus viselkedés (Bíró et al. , MFA) A nanostrukturált bevonatnak, ill. rétegnek funkciója van: megnövelt, ill. szelektív fényáteresztés

Reszponzív (válaszadó) nanoanyagok Fény által kiváltott ismételhető nedvesíthetőség változás Ti. O 2 Zn. O (Hórvölgyi et al. , BME)
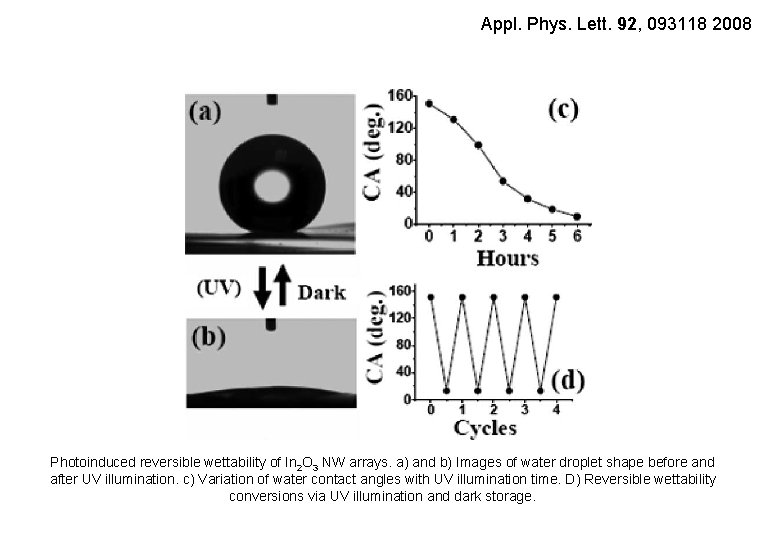
Appl. Phys. Lett. 92, 093118 2008 Photoinduced reversible wettability of In 2 O 3 NW arrays. a) and b) Images of water droplet shape before and after UV illumination. c) Variation of water contact angles with UV illumination time. D) Reversible wettability conversions via UV illumination and dark storage.

Nanotechnológia vs. nanotudomány Nanotudomány? Fizika – Kémia – Biológia Kolloidkémia-Kolloidika (Colloid Science) A kolloid rendszerek a homogén és a heterogén rendszerek közé helyezhetők el. A kolloid nem anyagfajta, hanem állapot. Korszerű megfogalmazásban: a kolloid rendszerekre a szubmikroszkópos diszkontinuitások (1 -500 nm) jellemzők. Mind a kolloid részecskék mérete (legalább az egyik térbeli irányban) mind a rendszereikben ható erők hatótávolsága ebbe a távolság tartományba esik. A kolloidika a kolloid rendszerek kémiájával és fizikájával foglalkozik. A kolloid jelenségek fontosak mind az élettelen, mind az élő világban. A kolloidika interdiszciplináris tudomány.

Kolloid rendszerek: csoportosítás 1. Csoportosítás a kolloid részecskék minősége és szerkezete szerint: A kolloid rendszerek, amelyek szupermolekuláris halmazokat tartalmazó rendszerek, a kolloid részecskék minősége és szerkezete szerint a következőképpen csoportosíthatók: - fáziskolloidok (diszperziók), amelyben a kolloid részecskék mikrofázisok - makromolekulás kolloid oldatok (kolloid részecskék: makromolekulák) - micella v. asszociációs oldatok (kolloid részecskék: micellák) A mikrofázisokat tartalmazó rendszereket diszperzióknak, míg a makromolekulákat vagy micellákat tartalmazókat kolloid oldatoknak is szokás nevezni.

Mikrofázisok: -felülettel rendelkező halmazok: megkülönböztethetők benne külső és belső molekulák (atomok) (ezek minimális száma: 1+6+3+3 = 13) -mivel a mikrofázisok mérete kicsi, az összes (vagy tömegre, ill. térfogatra normált = fajlagos) felület nagy 1 μm élhosszúságú kockák esetén a fajlagos felület: 6 m 2/cm 3 1 nm élhosszúságú kockák esetén a fajlagos felület: 6000(!) m 2/cm 3 Nagy felület >>> nagy (határ)felületi szabadenergia többlet >>> a fáziskolloidok termodinamikailag nem stabilak! CSAK KINETIKAI STABILITÁSRÓL BESZÉLHETÜNK! Következmény: számos határfelületi jelenség (pl. adszorpció) A HATÁRFELÜLETEK JELENTŐSÉGE! -a mikrofázisok halmazállapota lehet: S (szilárd; kristályos v. amorf), L (folyadék), G (gáz) -durva diszperziók: eloszlási állandóság nincs
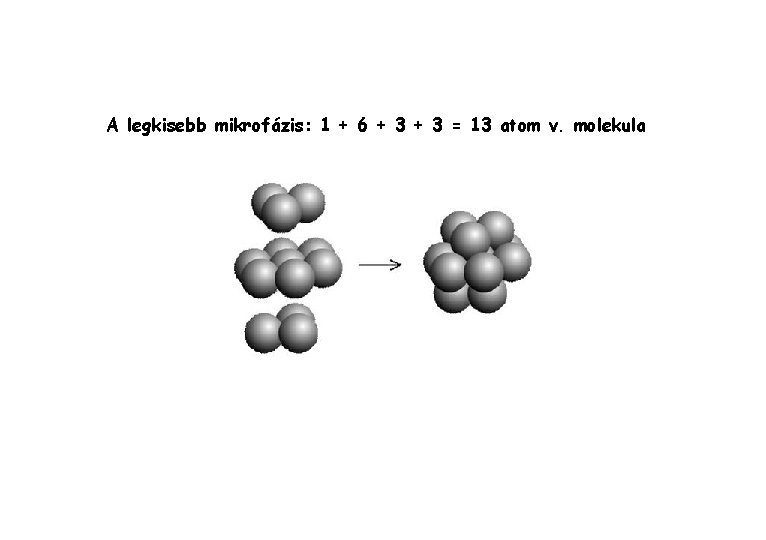
A legkisebb mikrofázis: 1 + 6 + 3 = 13 atom v. molekula
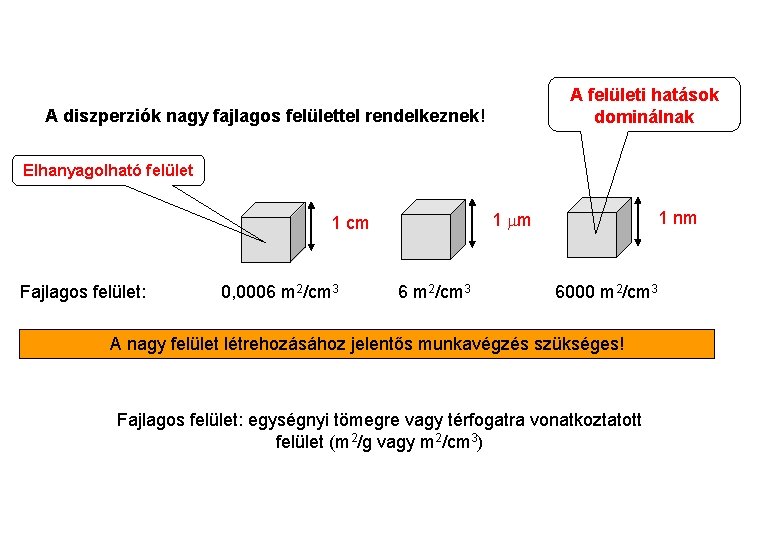
A felületi hatások dominálnak A diszperziók nagy fajlagos felülettel rendelkeznek! Elhanyagolható felület Fajlagos felület: 0, 0006 m 2/cm 3 1 nm 1 cm 6 m 2/cm 3 6000 m 2/cm 3 A nagy felület létrehozásához jelentős munkavégzés szükséges! Fajlagos felület: egységnyi tömegre vagy térfogatra vonatkoztatott felület (m 2/g vagy m 2/cm 3)

Makromolekulák oldatok): (általában makromolekulákat tartalmazó -a makromolekulák keletkezése: polimerizációval, kondenzációval -méret: M = 104 - 107 Dalton -szegmens: a molekula (viszonylag) önálló mozgásra képes része (a kolloid állapotra jellemző, új tulajdonságok megjelenése: pl. kaucsukrugalmasság, amely entrópia rugalmasság). A szegmensek mozgását nevezzük mikro Brown-mozgásnak. A makromolekulát az oldószer többé-kevésbé képes “átjárni”: >>> rossz oldószer, jó oldószer és theta-oldószer A molekula mérete nő: jó oldószer-szegmens kölcsönhatás esetén és az. ún. kizárt térfogati hatás miatt.
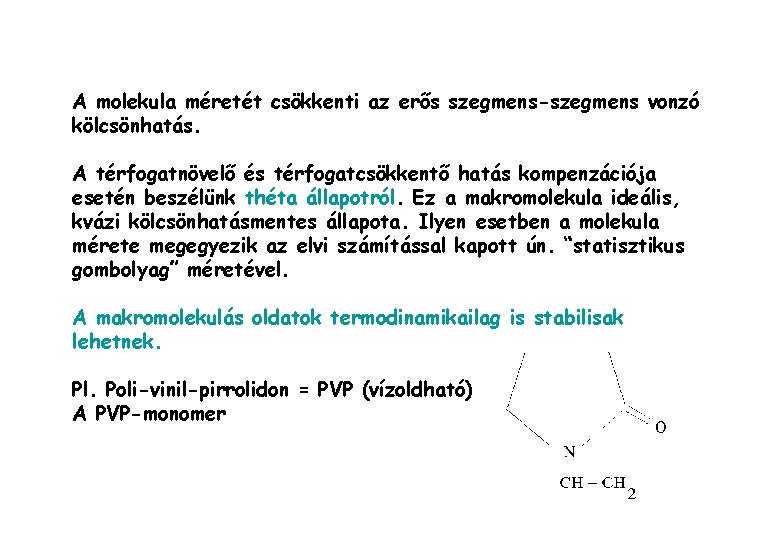
A molekula méretét csökkenti az erős szegmens-szegmens vonzó kölcsönhatás. A térfogatnövelő és térfogatcsökkentő hatás kompenzációja esetén beszélünk théta állapotról. Ez a makromolekula ideális, kvázi kölcsönhatásmentes állapota. Ilyen esetben a molekula mérete megegyezik az elvi számítással kapott ún. “statisztikus gombolyag” méretével. A makromolekulás oldatok termodinamikailag is stabilisak lehetnek. Pl. Poli-vinil-pirrolidon = PVP (vízoldható) A PVP-monomer

Micellák: A micellát alkotó molekulák felépítése: apoláris ( ___ ) + poláris (O) molekularész térben elkülönülve (amfipatikus v. amfifil molekula) Termodinamikailag stabil kolloid rendszer; dinamikus egyensúly. Kis- és nagymicellák; fordított micella (apoláris közegben).

A kolloid rendszerek közé soroljuk ezeken kívül mindazokat, amelyekben legalább az egyik térbeli irányban kolloid méretű diszkontinuitás van (lamellák, fibrillák: difform rendszerek). A határfelületek vizsgálata is a kolloidika témakörébe tartozik, mivel azok megjelenése kolloidális méretű diszkontinuitásokat okoz.

2. A fáziskolloidok csoportosítása a diszperz rész és a diszperziós közeg halmazállapota szerint: Diszperz rész/Diszperziós közeg L: folyadék, G: gáz, S: szilárd fázisok Aeroszolok L/G (köd) S/G (füst) Lioszolok G/L (hab, ill. gázdiszperzió) L 1/L 2 (emulzió, ill. mikroemulzió) S/L (szuszpenzió vagy köznapi néven szol) Xeroszolok G/S (porózus test) L/S (folyadékkal töltött pórusok) S 1 /S 2 (bizonyos ötvözetek és kompozit anyagok)

3. Csoportosítás a diszperz részek vázalkotása szempontjából: Döntő: a diszperz részek vonzó (kolloid) kölcsönhatási energiájának /Wkoll/ és a Brown-mozgás energiájának /WBrown/ a viszonya: Ha (1) Wkoll > WBrown és a töménység eléri a (2) gélpontot, akkor a szolból gél képződik. A gélek alaktartó, nem túl nagy mechanikai behatásra rugalmasan viselkedő, akár elfolyósodó kolloid rendszerek. Video származási helye: http: //www. microscopy-uk. org. uk/index. html? http: //www. microscopyuk. org. uk/amateurs/avi. html

Az ún. liogélekre (lioszolból keletkeznek a folyadéktartalom megőrzésével) jellemző a magas folyadéktartalom. 99%-nál nagyobb mennyiségű folyadékot tartalmazó gél: szemlencse. A xerogélek a liogélek kiszáradásával keletkeznek. Az aerogélek szilárd mikrofázisok levegőn történő összekapcsolódásával (pl. Aerosil) Példák liogélekre: makromolekula gél (kocsonya) micellagél (szappan) mikrofázis gél (króm-hidroxid gél) Reverzibilis gél: a hőmérséklet változtatására és/vagy mechanikai behatásra a gél újra szollá alakul. Irreverzibilis gélek: pl. főtt tojásfehérje Tixotrópia: izoterm, reverzibilis szol-gél átmenet

A kolloid rendszerek jelentősége Hagyományos területek: Kolloid iparok: festék-, papír-, műanyag-, bőr-, fotó-, mosószer-, kozmetikai-, kerámia- és építőipar Technológiák: adszorpció, ülepítés és szűrés, flotálás, őrlés és emulgeálás, gyógyszer- és növényvédőszer formálás, olajbányászat, víz- és levegő tisztítás, útépítés, stb. Társtudományokkal való kapcsolat: Kolloidok nélkül nincs életjelenség: gélek és membránok (határfelületek)
- Slides: 35