A multicentre openlabel randomised twoarm phase III trial

A multi-centre, open-label, randomised, two-arm phase III trial to evaluate optimal treatment duration of first-line bevacizumab in combination with carboplatin and paclitaxel in patients with primary epithelial ovarian, fallopian tube or peritoneal cancer AGO-OVAR 17 Prof. Dr. med. Jacobus Pfisterer

Rationale I u Sicherheit und Toxizität in beiden Studien in Ordnung u Verlängerung des Progressionsfreien Überlebens um 3, 8 Monate (mit 11 Monate längerer Therapie) in GOG 218 u Verlängerung des Progressionsfreien Überlebens um 1, 7 Monate (mit 8 Monate längerer Therapie) in AGO-OVAR 11/ICON 7 u Erhaltungstherapie wichtig

Rationale II Offene Fragen nach GOG 218 und AGO-OVAR 11/ICON 7 u Optimale u (7. 5 mg vs 15 mg) ? u Optimale u (12 u Bevacizumab Dosierung Dauer der Bevacizumab Therapie Mo vs 15 Mo vs bis PD) ? in GOG 218 sind viele Patientinnen de facto bis PD mit Bev behandelt worden u In AGO-OVAR 11/ICON 7 ist die Mehrheit der Patientinnen nicht bis PD mit Bev behandelt worden
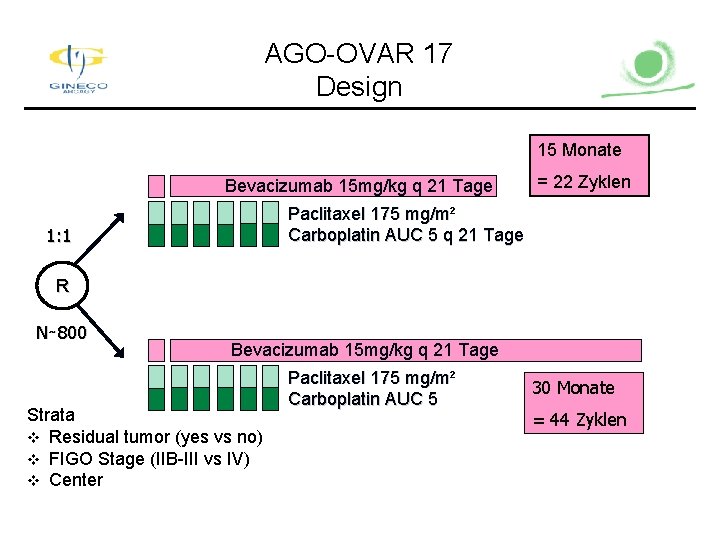
AGO-OVAR 17 Design 15 Monate Bevacizumab 15 mg/kg q 21 Tage = 22 Zyklen Paclitaxel 175 mg/m² Carboplatin AUC 5 q 21 Tage 1: 1 R N∼ 800 Bevacizumab 15 mg/kg q 21 Tage Strata v Residual tumor (yes vs no) v FIGO Stage (IIB-III vs IV) v Center Paclitaxel 175 mg/m² Carboplatin AUC 5 30 Monate = 44 Zyklen

Studienziele u Primäres Zielkriterium Vergleich der progressionsfreien Überlebenszeit (PFS) nach RECIST 1. 1 Sekundäre Zielkriterien Ansprechrate (ORR) Gesamtüberleben (OS) Lebensqualität (QOL) Sicherheit und Verträglichkeit u u Patientinnen n ∼ 800

Neuigkeiten - Besonderheiten u Keine Zulassungsstudie u ENGOT Studie (European Network of Gynaecological Oncology Trials Group) der AGO Studiengruppe (Leading Gruppe) und der GINCECO u Rekrutierung kompetitiv (“first come, first recruit”) u Bevacizumab wird gestellt, solange keine Zulassung bzw. Kostenerstattung durch die Kassen bzw. sofern Kostenerstattung durch die Kassen für Patientinnen, die außerhalb der möglichen Zulassung / Kostenerstattung behandelt werden (Bev > 15 Monate) u Therapie muss komplett zwingend im Prüfzentrum durchgeführt werden

AGO Studiengruppe LKP: Prof. Dr. Jacobus Pfisterer Zentrales Studienmanagement AGO Studiengruppe Kaiser-Friedrich-Ring 71 65185 Wiesbaden Tel. : 0611 8804 67 -0 Fax: 0611 8804 67 -67 office-wiesbaden@ago-ovar. de www. ago-ovar. de


Zeitlicher Ablauf Behandlungsbeginn - nicht später als 6 Wochen nach Operation - nicht früher als 4 Wochen nach Operation - falls Chemotherapie früher nötig, dann erster Chemotherapiezyklus ohne Bevacizumab

Tumor Evaluierung Gemäß RECIST 1. 1 - gynäkologische Untersuchung inkl. Ultraschall - CT Abdomen, Becken und Thorax bei klinischer Indikation - Baseline und danach alle 12 Wochen für mindestens 30 Monate oder bis zur Progression - Patienten ohne Tumorrest benötigen kein CT; nur bei Verdacht auf Progression

Follow-up Untersuchungen - Safety Follow-up Untersuchung 28 Tage (± 7 Tage) nach Ende der Behandlung - danach alle 6 Monate (± 14 Tage) während der ersten 5. Jahre - anschließend jährlich
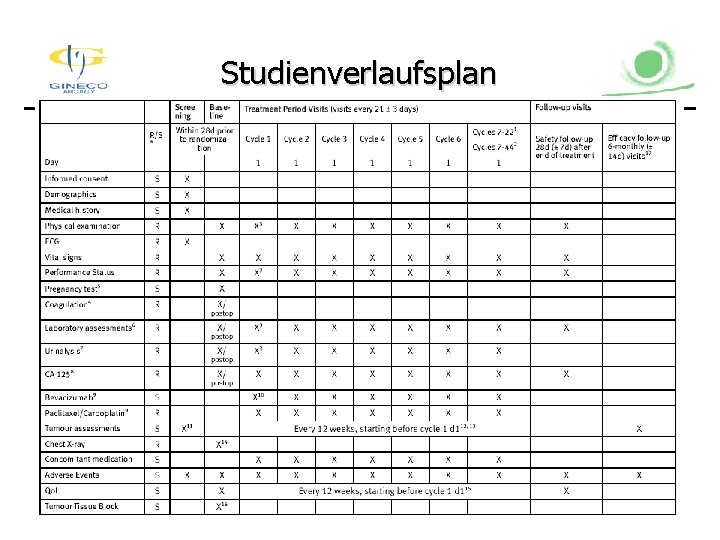
Studienverlaufsplan

Einschlusskriterien - Patientinnen mit histologisch gesichtertem epithelialem Ovarial-, Peritonealoder Tubenkarzinom FIGO IIb – IV (unabhängig von Grad und Histologie) - 18 Jahre, schriftliche Einwilligungserklärung nach erfolgter Aufklärung - Therapiebeginn innerhalb von 6 Wochen nach zytoreduktiver Operation (OP gemäß den Richtlinien des GCIG Conference Consensus Statement) - ECOG 2 - Adäquate Knochenmarks-, Nieren- und Leberfunktionen - Adäquate Gerinnungsparameter - GFR 40 ml/min (Cockroft-Gault-Formel) - Urinuntersuchung zur Erfassung von Proteinurie < 2+, wenn Teststreifen ≥ 2+, muss durch 24 -Stunden-Urin ≤ 1 g Protein innerhalb von 24 Stunden nachgewiesen werden - Lebenserwartung > 3 Monate

Ausschlusskriterien I - Ovarialtumoren mit niedrigem malignen Potential (Borderline Tumore) und FIGO Ia - IIa - Nicht-epitheliale Ovarialtumoren einschließlich Müller’scher Mischtumor - Vorherige systemische Therapie des Ovarialkarzinoms (z. B. Chemotherapie, Monoklonale Antikörper, Tyrosinkinasehemmer, Hormontherapie) - OP innerhalb von 4 Wochen vor der ersten geplanten Dosis Bevacizumab - Geplante OP’s während der Behandlungsphase + 4 Wochen danach - Traumatische Verletzung innerhalb von 4 Wochen, oder Radiotherapie - Gehirnmetastasen oder Rückenmarkskompression - Anfallsleiden oder Erkrankungen des zentralen Nervensystems - Störungen der Wundheilung, Ulzerationen oder Knochenfrakturen - < 5 Jahre zurückliegende maligne Diagnose - Behandlung mit anderen Prüfpräparaten oder Teilnahme an anderen Studien innerhalb von 4 Wochen vor Therapiestart oder begleitend zu dieser Studie

Ausschlusskriterien II - thrombotische oder hämorrhagische Störungen - Apoplexie, transiente ischämische Attacke (TIA) oder Subarachnoidalblutung (SAH) innerhalb von 6 Wochen vor Randomisierung - Vorbestehende sensorische und motorische Neuropathie ≥ Grad 2 - Unkontrollierte Hypertonie - Einnahme von Aspirin > 325 mg/Tag innerhalb von 10 Tagen vor 1. Zyklus - Orale oder parenterale Antikoagulation oder thrombolytische Substanzen (Ausnahme: zur Erhaltung der Durchgängigkeit von venösen Zugängen) - Bekannte Überempfindlichkeit auf Bevacizumab und dessen chemische Bestandteilem, Produkte aus Ovarialzellen Chinesischer Hamster oder andere rekombinante humane oder humanisierte Antikörper - Schwangere oder stillende Frauen, Gebärfähige Frauen, die nicht zu adäquater Verhütung bereit sind

Ausschlusskriterien III - Patientinnen mit simultanem primärem Endometriumkarzinom werden ausgeschlossen, es sei denn, ALLE der folgenden Kriterien treffen für das Endometriumkarzinom zu: - Stadium ≤ 1 a keine lympho-vaskuläre Invasion nicht niedrig differenziert (< Grad 3; serös-papillär oder klarzellig) - klinisch signifikante kardiovaskuläre Erkrankung, einschließlich: - Myokardinfarkt oder instabile Angina pectoris innerhalb von 6 Monaten vor Randomisierung Kongestive Herzinsuffizienz (NYHA ≥ 2) Schlecht eingestellte Arrhythmie trotz Medikation (Patientinnen mit frequenzkontrolliertem Vorhofflimmern können teilnehmen) - periphere Gefäßerkrankung Grad ≥ 3 (d. h. symptomatisch und die Aktivitäten des täglichen Lebensbeeinträchtigend, Intervention oder Revision notwendig) - Hinweis auf andere Erkrankungen, metabolische Dysfunktion, Befunde körperlicher Untersuchungen oder Laborbefunde, die den Verdacht einer Krankheit oder eines Zustandes nahelegen, die eine Kontraindikation zur Prüfmedikation darstellen oder die Patientin behandlungsbedingten Risiken aussetzt
- Slides: 16