A cukorbetegsg kezelse Ger Lszl dr A diabetes

A cukorbetegség kezelése Gerő László dr.

A diabetes mellitus kezelése • 1 -es típus: életmód terápia+inzulin • 2 -es típus: életmód terápia +orális antidiabetikum (OAD) • vagy +OAD+inzulin • vagy +inzulin

Az 1 -es típusú diabetes kezelése • Kezdettől inzulin terápia szükséges • Cél: az egészséges (nem-diabeteses) egyén napi inzulin profiljának utánzása • 1. Intenzív konzervatív inzulin terápia • (napi többszöri inzulin injekció: a főétkezések előtt gyorshatású, éjszaka (és esetleg reggel is) elhúzódó hatású inzulin adása) • 2. Folyamatos inzulinadás pumpa segítségével • (3. szimultán ves+pancreas transzpantáció)
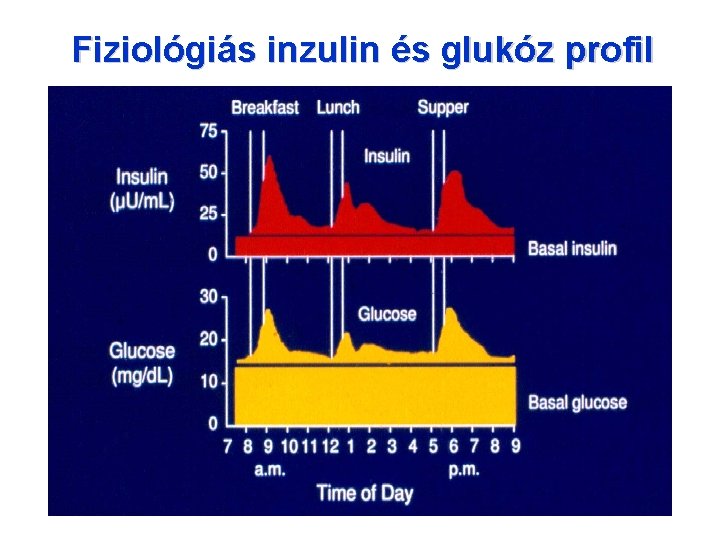
Fiziológiás inzulin és glukóz profil

Az inzulinadás és az étkezések összehangolása az intenzív kezelés során • Inz étk étk inz étk • 7. 00 7. 30 10. 00 12. 15 14. 45 17. 30 17. 45 • Insulin mennyiség: • 12 IE 8 IE • Szénhidrát: • 35 g 20 g étk 20. 30 10 IE 50 g 20 g inz 22. 00 12 -14 IE 40 g 20 g • (IR napi ritmusa ! Kivárás a sc. inz. lassú felszívódása miatt. CH-felszívódás. Inzulin analóg kezelés mellett a „kivárás” elhagyható, a három „közti étkezés” elhagyható)

Gyorshatású és intermedier humán inzulinok farmakokinetikája • gyári név • Actrapid HM • Humulin R • Insulatard • Humulin N • Insuman B hatásmaximum 90 -150 perc 4 -6 óra hatástartam 4 -6 óra 12 -16 óra

Intenzív inzulin terápia - intenzív diabetes gondozás • Napi többszöri (>3 -szori) inzulinadás • • Rendszeres otthoni vércukormérés (az inzulin beadása előtt, ill. postprandiálisan 1, 5 -2 órával és 00. 03 -kor) • • Rendszeres konzílium a diabetes gondozó centrumban (eredmények naplóban vezetése, kiértékelése, szükséges változtatások megbeszélése) • Szövődmények vizsgálata, követése • • • BETEGOKTATÁS Diéta (CH, kalória, glikémiás index), PEN és vércukormérő használata, [diabetológus orvos(ok), szakápoló, diétetikus, szemész, nephrologus, podiáter, psychológus]. A betegség természete, szövődményei, az optimális beállítás előnyei. •

A DCCT tanulmány – szövődmények • • A micro- és macroangiopath szövődmények kockázatának csökkenése (ICIT vs. conv th, Hb. A 1 c 7, 1 vs 9, 4%, p<0, 01) -------------------------------- • • RPD kialakulása RPD progressziója (Macula oedema Lézerkezelés Microalbuminuria Macroalbuminuria Neuropathia Macroangiopathia RRR 76 % 54 % 23% 56%) 39 % 54 % 60 % 41 % 95% CI 62 -85 % 39 -66 % 21 -52 % 19 -74 % 35 -74 % • ICIT: a hypoglykaemia kockázata 3, 28 x ↑ • a testsúly ~ 4 kg-mal ↑ P< 0, 001 0, 001 =0, 06 (NS)

Az intenzív vs. konvencionális inzulin terápia hatása a szövődményekre • DCCT: Diabetes Control and Complication Trial • intenzív vs. konvencionális kezelés • n= 730 711 (6, 5 év) • Hb. A 1 c 7, 1% 8, 9% • Kockázatcsökkenés (RRR) • • RPD lézerkezelés nephropathia neuropathia 54 -76% 56% 34 -43% 57 -69% P<0, 001 • (de: hypoglykaemia 3, 3 x ↑, testsúly átl. 4, 6 kg ↑ )
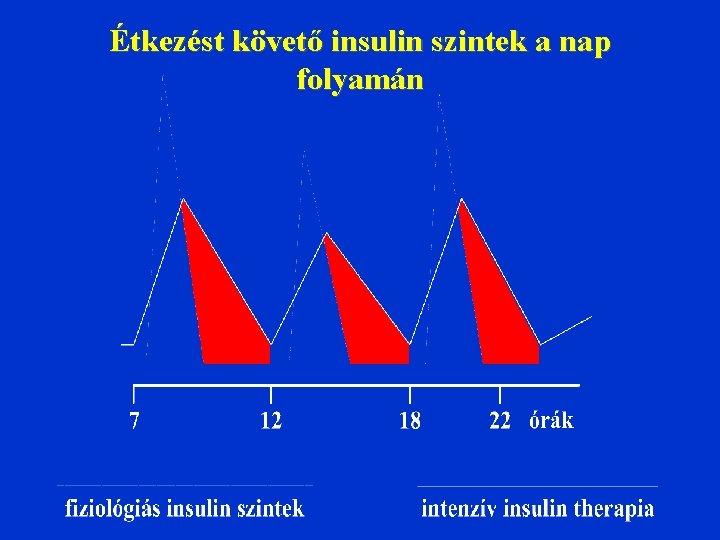
Étkezést követő insulin szintek a nap folyamán
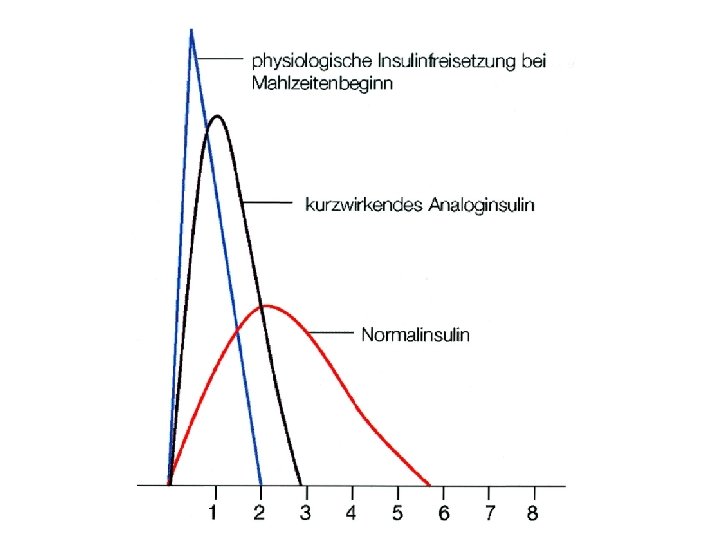
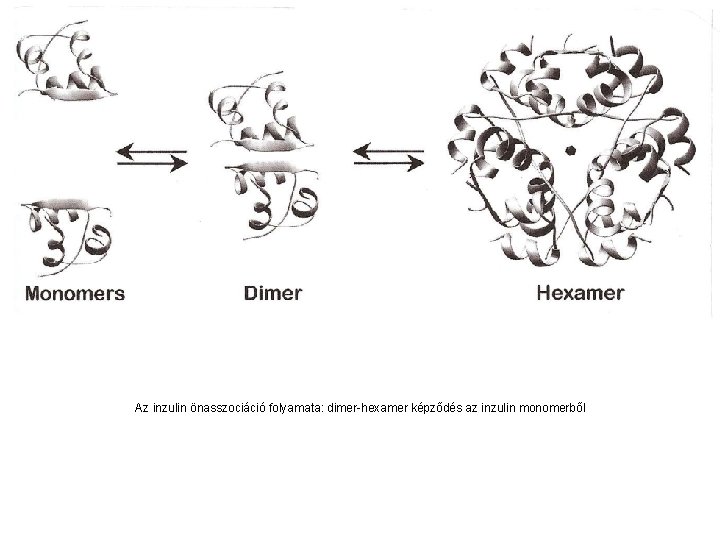
Az inzulin önasszociáció folyamata: dimer-hexamer képződés az inzulin monomerből
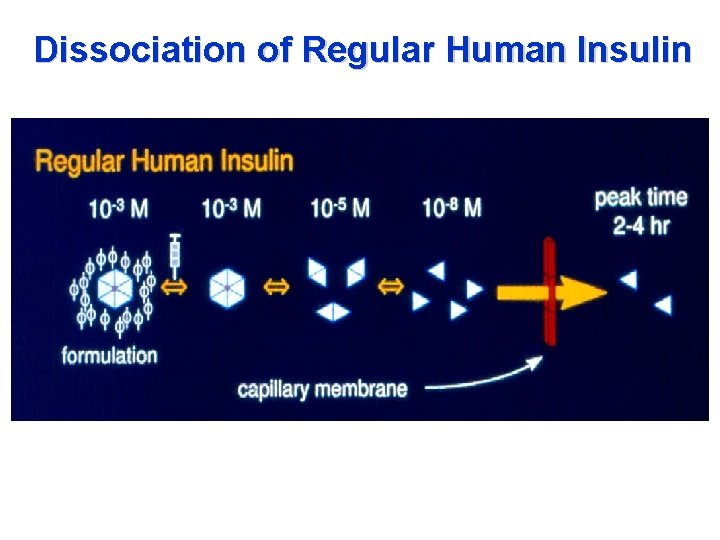
Dissociation of Regular Human Insulin
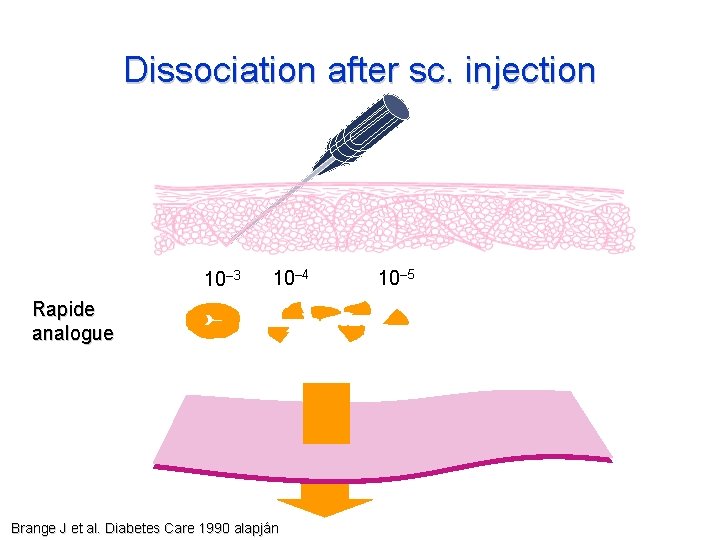
Dissociation after sc. injection 10– 3 10– 4 Rapide analogue Brange J et al. Diabetes Care 1990 alapján 10– 5 10– 8 mol/l


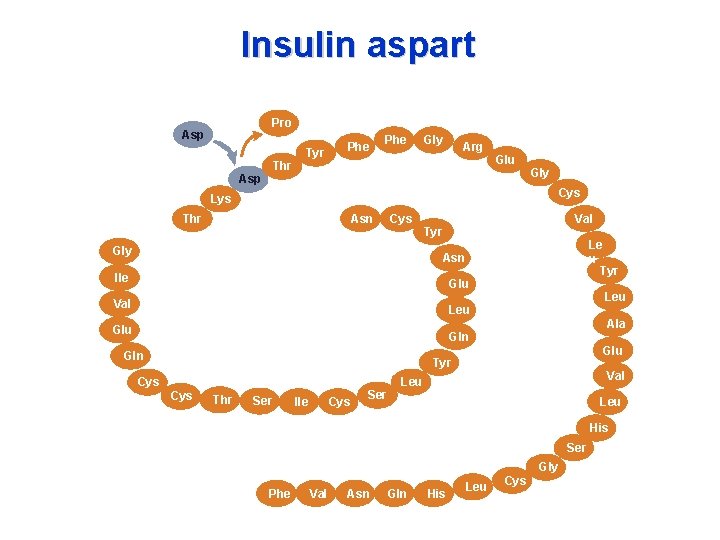
Insulin aspart Pro Asp Thr Asp B 30 A 1 Lys Phe Tyr Phe Gly Arg Glu Gly Cys B 28 Thr A 21 Asn Cys Gly Val Tyr Le u Tyr Asn Ile Glu Val Leu Glu Ala Gln Glu Tyr Cys Thr Ser Ile Cys Ser Val Leu His Ser B 1 Phe Val Asn Gln His Leu Cys Gly
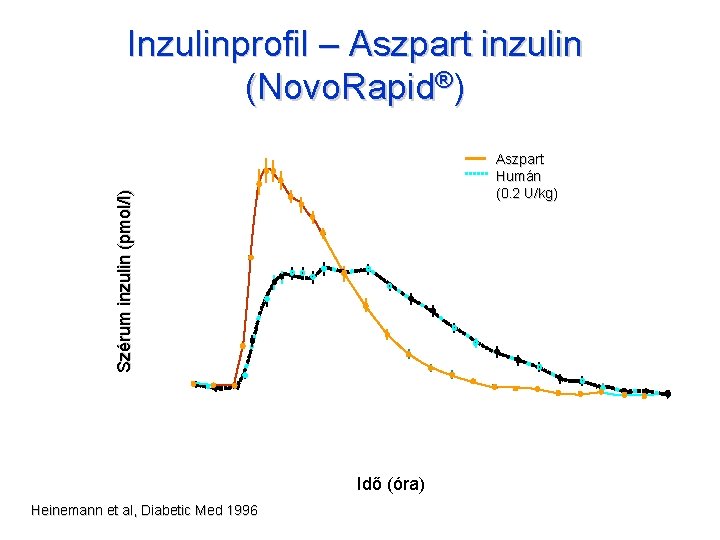
Inzulinprofil – Aszpart inzulin (Novo. Rapid®) Szérum inzulin (pmol/l) Aszpart Humán (0. 2 U/kg) -1 0 1 2 3 4 Idő (óra) Heinemann et al, Diabetic Med 1996 5 6 7 8 9 10
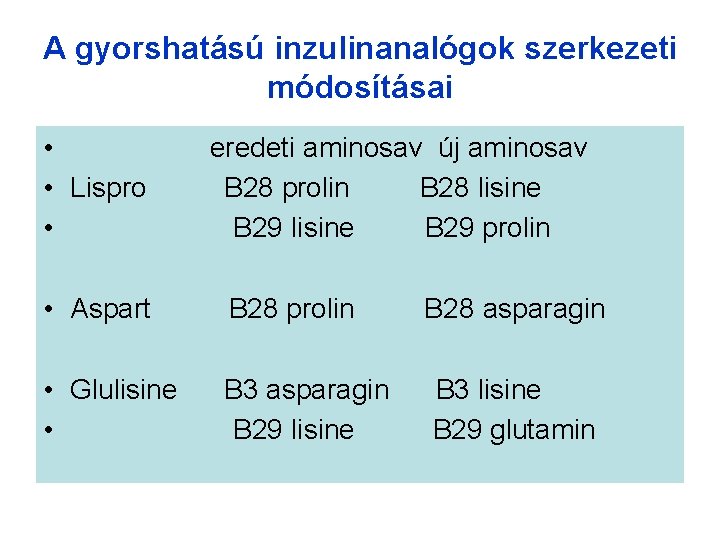
A gyorshatású inzulinanalógok szerkezeti módosításai • • Lispro • eredeti aminosav új aminosav B 28 prolin B 28 lisine B 29 prolin • Aspart B 28 prolin B 28 asparagin • Glulisine • B 3 asparagin B 29 lisine B 3 lisine B 29 glutamin

Az inzulinadás és az étkezések összehangolása az intenzív kezelés során • Inz étk étk inz étk • 7. 00 7. 30 10. 00 12. 15 14. 45 17. 30 17. 45 • Insulin mennyiség: • 12 IE 8 IE • Szénhidrát: • 35 g 20 g étk 20. 30 10 IE 50 g 20 g inz 22. 00 12 -14 IE 40 g 20 g • (IR napi ritmusa ! Kivárás a sc. inz. lassú felszívódása miatt. CH-felszívódás. Inzulin analóg kezelés mellett a „kivárás” elhagyható, a három „közti étkezés” elhagyható)

A gyorshatású insulinanalógok alkalmazásának előnyei Az injekciózás után nincs szükség „kivárásra”“ A prandiális vércukorszint-emelkedés mérséklődik Kevesebb lesz a hypoglykaemia (étkezések között és éjszaka) Nincs szükség „közti” étkezésre (testsúly !) Soronkívüli étkezés (társasági vacsora, fogadás, stb. ) lehetséges Az életvitel könnyebb, flexibilisebb lesz

A gyorshatású insulinanalógok alkalmazásának indikációi “diéta-rezisztens” túlzott posztprandiális vércukorszint-emelkedés soronkívüli étkezés (társasági vacsora, fogadás, stb. ) nincs idő “kivárásra” (pl. étkezés az iskolai szünetben) gyakori “késői” (preprandiális) hypoglykaemia gyakori éjszakai hypoglykaemia gyakori “post-exercise” (késői) hypoglykaemia vércukorszint „gyors korrekciója” insulin allergia ? (De: tökéletes bázisinzulin kell !)
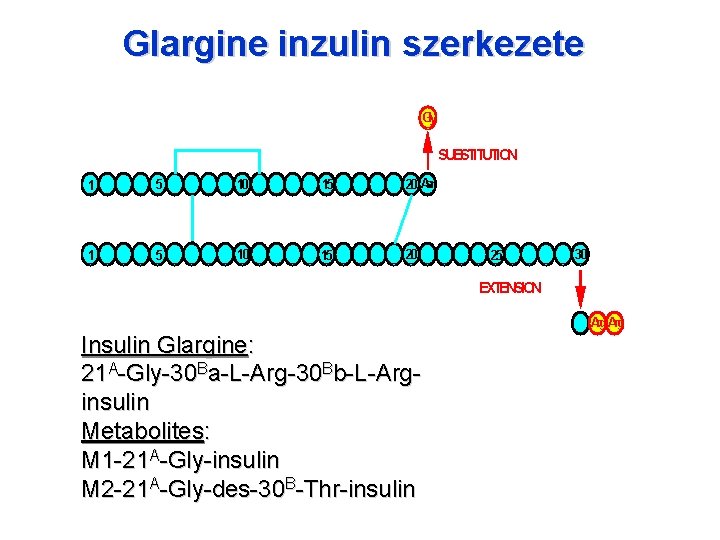
Glargine inzulin szerkezete Gly A-CHAIN SUBSTITUTION 1 5 10 15 20 Asn 1 5 10 15 20 25 30 EXTENSION B-CHAIN Arg Insulin Glargine: 21 A-Gly-30 Ba-L-Arg-30 Bb-L-Arginsulin Metabolites: M 1 -21 A-Gly-insulin M 2 -21 A-Gly-des-30 B-Thr-insulin
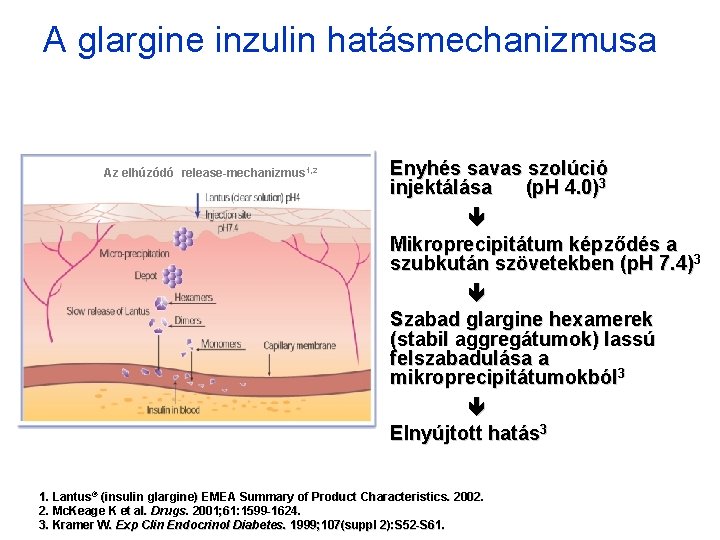
A glargine inzulin hatásmechanizmusa Az elhúzódó release-mechanizmus 1, 2 Enyhés savas szolúció injektálása (p. H 4. 0)3 Mikroprecipitátum képződés a szubkután szövetekben (p. H 7. 4)3 Szabad glargine hexamerek (stabil aggregátumok) lassú felszabadulása a mikroprecipitátumokból 3 Elnyújtott hatás 3 1. Lantus® (insulin glargine) EMEA Summary of Product Characteristics. 2002. 2. Mc. Keage K et al. Drugs. 2001; 61: 1599 -1624. 3. Kramer W. Exp Clin Endocrinol Diabetes. 1999; 107(suppl 2): S 52 -S 61.
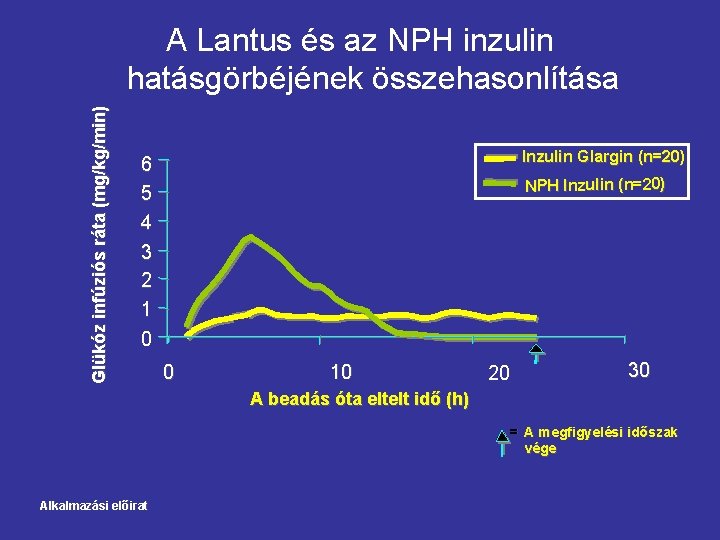
Glükóz infúziós ráta (mg/kg/min) A Lantus és az NPH inzulin hatásgörbéjének összehasonlítása Inzulin Glargin (n=20) 6 5 4 3 2 1 0 Inzulin (n=20) NPH Inz 0 10 20 30 A beadás óta eltelt idő (h) = A megfigyelési időszak vége Alkalmazási előirat
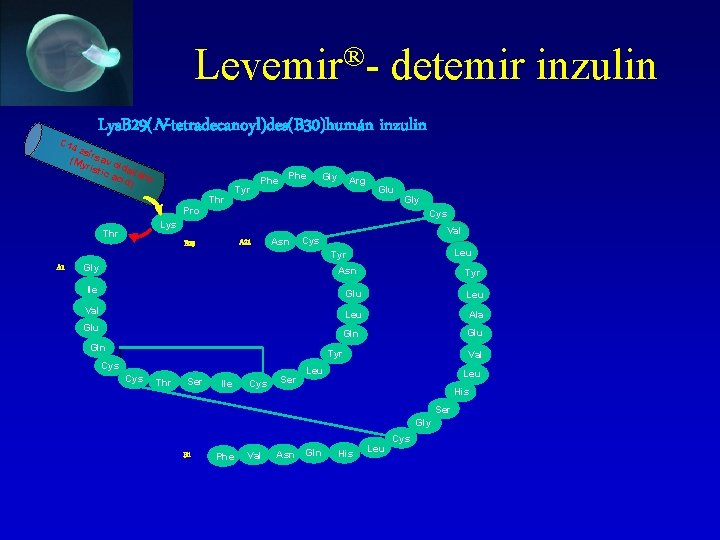
Levemir®- detemir inzulin Lys. B 29(N-tetradecanoyl)des(B 30)humán inzulin C 14 zsí (My rsav o rist l ic a dallán c cid ) Thr Tyr Phe Gly Arg Glu Pro Cys Lys Thr Lys A 1 Gly A 21 B 29 Asn Val Cys Leu Tyr Gly Asn Tyr Ile Glu Leu Val Leu Ala Gln Glu Gln Tyr Cys Thr Ser Ile Cys Ser Val Leu His Ser Gly B 1 Phe Val Asn Gln His Leu Cys
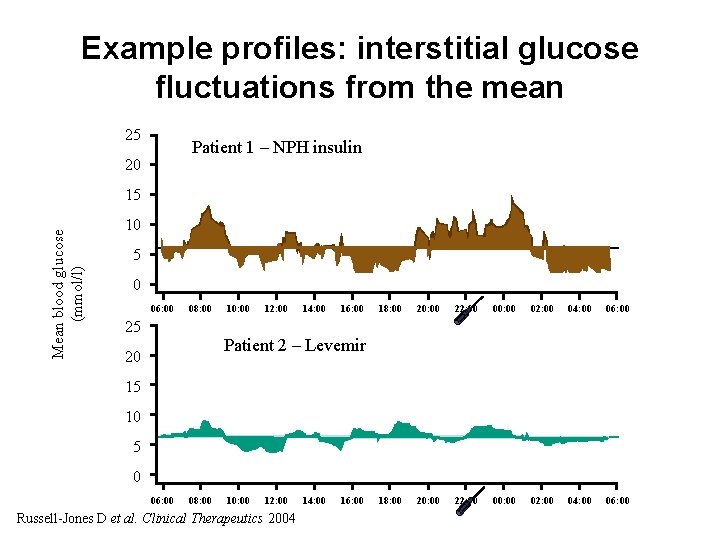
Example profiles: interstitial glucose fluctuations from the mean 25 Patient 1 – NPH insulin 20 Mean blood glucose (mmol/l) 15 10 5 0 06: 00 08: 00 10: 00 12: 00 14: 00 16: 00 18: 00 20: 00 22: 00 00: 00 02: 00 04: 00 06: 00 25 Patient 2 – Levemir 20 15 10 5 0 06: 00 08: 00 10: 00 12: 00 Russell-Jones D et al. Clinical Therapeutics 2004 14: 00 16: 00 Time
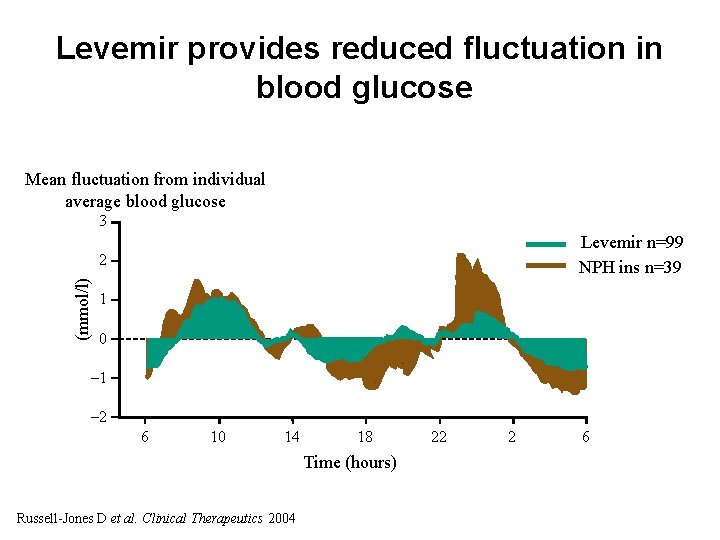
Levemir provides reduced fluctuation in blood glucose Mean fluctuation from individual average blood glucose 3 Levemir n=99 NPH ins n=39 (mmol/l) 2 1 0 – 1 – 2 6 10 14 18 Time (hours) Russell-Jones D et al. Clinical Therapeutics 2004 22 2 6

Pancreas és Langerhans-sziget transzplantáció • Kérdés: a DM vagy az immunszuppresszív kezelés veszélyei a nagyobbak ? • 1 -es típusú cukorbetegeken, végstádiumú veseelégtelenség alakult ki és veseátültetés jön szóba, akkor • vese+pancreas transzplantációt kell végezni • Előnyök: a beteg mind az uraemiából • mind a diabetesből kigyógyul • nem kell tartani diabeteszes veseszövődménytől a • graft vesében • Ha korábban már történt veseátültetés és a CH-acs. labilis • akkor Langerhans-sziget transzplantáció jön szóba • (nem kell második műtét, CH-acs. stabil lesz, inzulin ? )

A 2 -es típusú diabetes kezelése
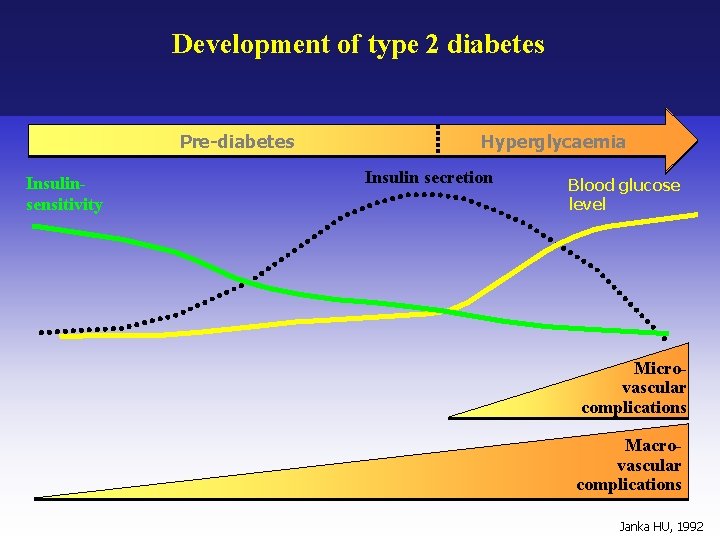
Development of type 2 diabetes Pre-diabetes Insulinsensitivity Hyperglycaemia Insulin secretion Blood glucose level Microvascular complications Macrovascular complications Janka HU, 1992
![Two subtypes of type 2 diabetes kb. 90% Overweight [BMI >25] Insulinresistent Insulinsensitizer should Two subtypes of type 2 diabetes kb. 90% Overweight [BMI >25] Insulinresistent Insulinsensitizer should](http://slidetodoc.com/presentation_image_h2/132a9f4fca2974560e23219f34dc9481/image-32.jpg)
Two subtypes of type 2 diabetes kb. 90% Overweight [BMI >25] Insulinresistent Insulinsensitizer should be preferred kb. 10% ‘Normal’ body weight [BMI ≤ 25] Insulin sensitive Insulin secretagog is preferred ?

Orális antidiabeticumok A. Non-secretagog készítmények I. II. Biguanidok (Phenphormin-Buformin-Metformin) Thiazolidinedionok (“Glitazonok”) (Troglitazone, Rosiglitazone, Pioglitazone) III. Alpha-glucosidase-hydroxylase gátlók (Acarbose, Miglitol) B. Insulin secretagog készítmények I. Sulfanylureák II. Meglitinid származékok (pl. : repaglinid - Novo. Norm) III. D-Phenylalanin származékok (pl. nateglinid - Starlix) IV. DPP-4 (dipeptidyl-peptidase-4) gátlók (un. gliptinek)

Biguanidok (Phenformine : gyakori laktát acidosis miatt kivonták); Buformin (Adebit): nem elég hatékony; Metformin (hatékonyabb és biztonságosabb) Hatásmechanizmus: 1. / hepatikus glukóztermelés gátlása (gluconeogenesist és a glykogenolysist egyaránt csökkenti vércukorszint ) 2. / izomszövet glukózfelvételének fokozása (IRS-2 aktiválása, jelátvitel gyorsítása, GLUT-4 expressio fokozása) 3. / CH-felszívódás gátlása (B 12 -vitamin hiány) Egyéb hatások: össz- és LDL-cholesterin szint , a lipid oxidáció ↑ Csökkenti a PAI-1 szintet (antithrombotikus hatás)

A metformin klinikofarmakológiája • Absorptio gyors, a csúcs-koncentráció a vérben 1, 5 -2 órával a bevétel után alakul ki; • Biohasznosulás: 50 -60% (500 mg bevétele után – nagyobb dózis esetén a felszívódás és a hasznosulás progresszíven csökken); • Max. dózis: 3 x 850 -3 x 1000 mg (? ); • Max. hatás: napi 1700 -2000 mg mellett figyelhető meg; • Kiválasztás: a gyógyszer 90%-a a vesén át ürül ki 12 órán belül; •

A metformin klinikai alkalmazása I. Indikáció: első gyógyszerként ajánlott a 2 -es típusú cukorbetegségben, (az életmód terápiával egyidőben indítva, ADA/EASD 2006) Kezelési stratégia: kis dózisokkal kell kezdeni (250 -500 mg, fokozatos dózis növelés a GI mellékhatások miatt) Hatékonyság: placebo-kontrollos vizsgálatokban a Hb. A 1 c szintje 0, 6 -1, 6%-kal, az éhomi vércukorszint 2 -3 mmol/l-rel csökkent. PP vércukorszint ~

A metformin klinikai alkalmazása II. Kombinált kezelés: jól kombinálható: glitazonokkal (Avandamet) sulfanylurea készítményekkel (UKPDS ? ) újabb secretagog vegyületekkel (DPP-4 gátlókkal) insulinnal (bed time, 2 -4 x) (az insulin igény csökken, a testsúly is [enyhén] csökken) PCOS (polycystás ovarium syndroma) kezelése anovulatio, hirsutismus, 17 -OH-Prog. , inzulin rezisztencia (insulin receptor béta-alegységén excessív szerin-foszforiláció) Metformin kezelés hatására csökken: 17 -OH-prog androgének inzulin reziszt. visszatér az ovuláció és a normális cyclus;

A metformin monoterápia hatása a CV szövődményekre (342 vs 411 beteg), UKPDS 34* • Szövődmény RR (95% CI) p= • DM-al összefüggő • összes végpont 0, 68 (0, 53 -0, 87) 0, 0023 • DM-al összefüggő • halálozás 0, 58 (0, 37 -0, 91) 0, 017 • Össz-halálozás 0, 64 (0, 41 -0, 89) 0, 011 • Szívinfarktus 0, 61 (0, 41 -0, 89) 0, 010 • UKPDS 34, Lancet 1998

A metformin kezelés hatása az új T 2 DM kialakulására • Diabetes Prevention Program (DPP) • n=3234 IGT-s beteg, 3 kezelési csoport: • Új T 2 DM kialakulás kockázatának csökkenése: • Metformin 2 x 850 mg 31% • Életmód változtatás 58% • (placeboval szemben)

A metformin kezelés kontraindikációi • --Vesebetegség (clearence < 60 ml/min, GFR <50 ml/min, se creatinin > 130 umol/l) • --Előrement májbetegség • --Hypoxiás állapotok (cardioresp. insuff. , perif. keringési elégt. , láz, sepsis, ) • --Idős kor (>75 ? > 80 év) • --Erélyes fogyókúra (napi CH bevitel<100 g, kcal<1000) • --Anamnézisben laktát-acidosis (ritka komplikáció, de 50 % a lethalitas) • --Iv. jódos kontrasztanyagos rtg vizsgálat (tubularis károsodás !) • -- Mitochondriális diabetes • (ha a fentieket betartják, a laktát acidózis< 50/1 millió eset)

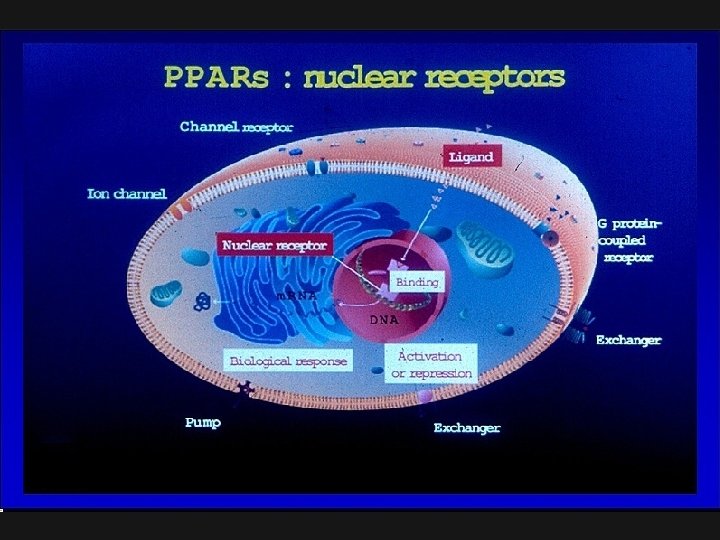
THIAZOLIDINEDIONOK (Glitazonok, “insulin sensitizer”-ek) (Troglitazone), Rosiglitazone, Pioglitazone Valódi “insulin sensitizer” vegyületek, vércukor-szintet csökkentik az insulin-szint emelkedése nélkül (inkább enyhe csökkenése mellett); kifejezetten béta-sejt kímélők: állatkísérletekben (diabeteses állatokon) a de-granulált béta-sejtek regranulációját idézték elő; Hatásmechanizmusuk: PPARgamma magreceptor aktiválás→ → géntranszkripció → zsírsejtek érési folyamatának módosítása;
www. e-collegium. org

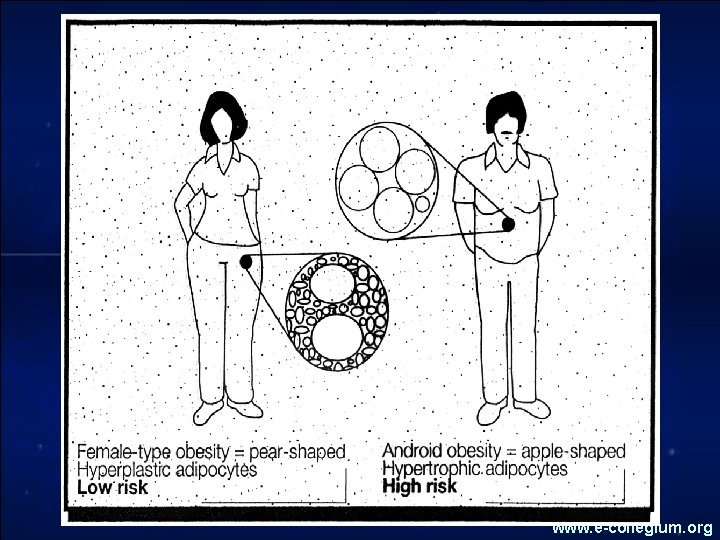
GLITAZONOK HATÁSA AZ INZULIN REZISZTENCIÁRA Pre-adipocyta érés befolyásolása Kis méretű (inzulin érzékeny) zsírsejtek keletkezése Lipolysis csökkenése (FFA deponálódik a zsírsejtekben) Izomsejt felé a szubsztrát kínálat (FFA, TG) csökken Izomsejt glukózégetése fokozódik

A glitazonok hatása a glukózfelvételre a lipidanyagcserére és a vérnyomásra • A glitazonok fokozzák a perifériás glukózfelvételt, mert növelik az izomzat GLUT-4 expressiót • A glitazonok (elsősorban a pioglitazon) előnyösen befolyásolják a lipidprofilt: csökkentik az LDL-Ch és a TG szintjét; • A glitazonok (mind a rosi-, mind a pioglitazon) csökkentik a vérnyomást; • A glitazonok a zsírszövet redisztribúcióját okozzák; • (a testsúly nő, a derék: csípő hányados csökken)
www. e-collegium. org

Pioglitazone kezelés CV hatásai (a Proactive tanulmány eredményei) • n=5238 beteg (T 2 DM, pioglitazone vs placebo • kezelés, 34 hónapon át) • Az „össz-halálozás+nem-halálos AMI+stroke” kombinált végpontja szignifikánsan csökkent : RR: 0, 84 (95% CI 0, 72 – 0, 98, p=0, 027)

Klinikai vizsgálatok glitazonokkal • Acut coronaria sy-ban stent behelyezés után az • in-stent stenosis kialakulását szignifikánsan csökkentette • mind rosiglitazon (Diab Care 2004) • mind a pioglitazon (Diab Care 2006) • A carotis-fal intima-media vastagodást a rosiglitazon szignifikánsan csökkentette a placebo kezeléssel szemben • (Arterioscler Thromb Vasc Res 2004)

Glitazonkezelés hatása az új T 2 DM kialakulására II. • • A DREAM tanulmány; n=5269 beteg (IGT és/vagy IFG) napi 8 mg rosiglit vs PLAC 3 éven át T 2 DM diagnózisa WHO szerint • Rosiglitazon • Új T 2 DM 280 (10, 6%) • Halálozás 1, 1% PLAC HR 95% CI P< 658 (25%) 0, 38% 0, 33 -0, 44) 0, 0001 1, 3% P=0, 7
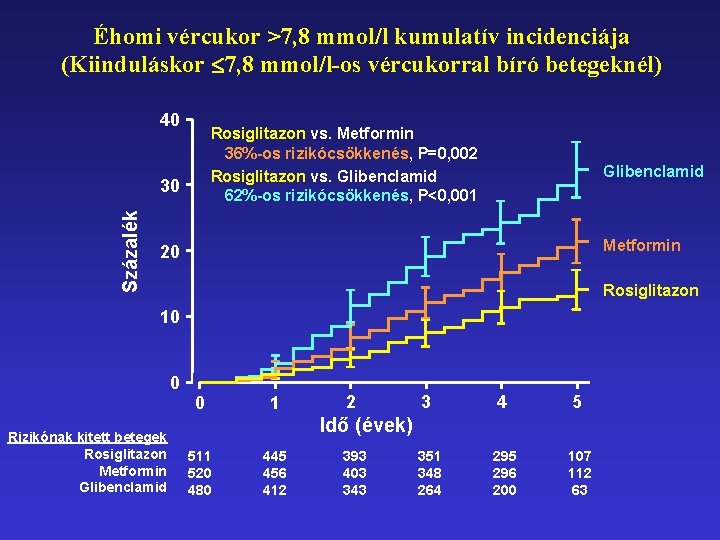
Éhomi vércukor >7, 8 mmol/l kumulatív incidenciája (Kiinduláskor 7, 8 mmol/l-os vércukorral bíró betegeknél) 40 Rosiglitazon vs. Metformin 36%-os rizikócsökkenés, P=0, 002 Rosiglitazon vs. Glibenclamid 62%-os rizikócsökkenés, P<0, 001 Százalék 30 Glibenclamid Metformin 20 Rosiglitazon 10 0 0 Rizikónak kitett betegek Rosiglitazon Metformin Glibenclamid 1 2 3 4 5 351 348 264 295 296 200 107 112 63 Idő (évek) 511 520 480 445 456 412 393 403 343
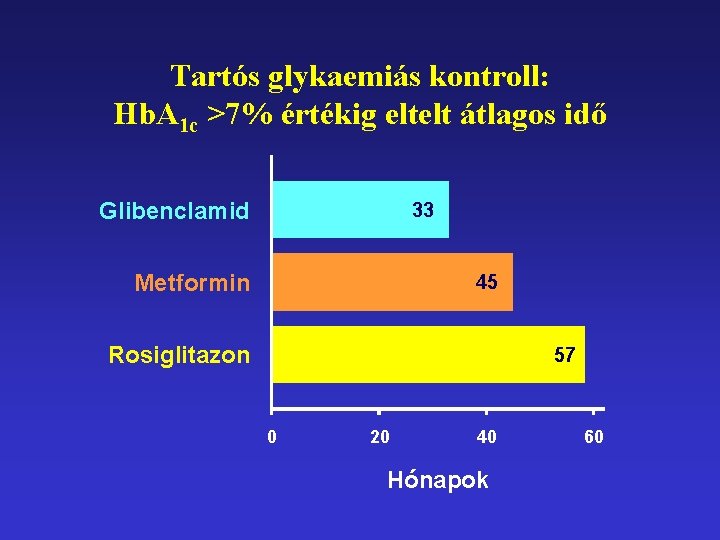
Tartós glykaemiás kontroll: Hb. A 1 c >7% értékig eltelt átlagos idő Glibenclamid 33 Metformin 45 Rosiglitazon 57 0 20 40 Hónapok 60
![Glitazonok klinikai alkalmazása • Mellékhatások: hepatotoxicitás (Troglitazone !) (Rosiglitazon és pioglitazon nem [alig] hepatotoxikus Glitazonok klinikai alkalmazása • Mellékhatások: hepatotoxicitás (Troglitazone !) (Rosiglitazon és pioglitazon nem [alig] hepatotoxikus](http://slidetodoc.com/presentation_image_h2/132a9f4fca2974560e23219f34dc9481/image-52.jpg)
Glitazonok klinikai alkalmazása • Mellékhatások: hepatotoxicitás (Troglitazone !) (Rosiglitazon és pioglitazon nem [alig] hepatotoxikus ) • testsúly növekedés, folyadék retenció! • (card. decomp. -ban kontraindikált); • együttadás insulinnal ? • Rosiglitazon mellett EKG (sz. e. ergometria), carotis UH, AV-i keringés ellenőrzése szükséges.

Alpha-glucosidase-hydroxylase gátlók Képviselőik: acarbose (Glucobay, miglitol (Diastabol, 25, voglibose 50 és 100 mg tabletta) Hatásmechanizmus: a vékonybélben, a kefeszegély sejtjeiben lévő maltase, isomaltase, saccharase és alpha-amylase enzimekhez kötődve kompetitítv módon gátolják a komplex szénhidrátok enzimatikus hasítását cukor-felszívódás lelassul PP vércukor alacsonyabb lesz (un. smoothing effect) kórosan emelkedett késői inzulin válasz mérséklődik (“béta-sejt kímélő” hatás); komplex CH-ok a distalis ileumban fokozzák a glucagon-like peptide (GLP-1) elválasztását

Alpha-glucosidase gátlók klinikai alkalmazása Kiegészítő szerként használjuk, ha a pp vércukorszint magas (obesitas!) Hosszútávú hatékonyság főleg kombinációban jó Kombinálhatók: sulfanylurea készítményekkel és az újabb secretagog gyógyszerekkel is kombinálhatók elvben metforminnal is, de: GI mellékhatások hasonlóak ! kombinálás insulin sensitizerrel ? kombinálható insulinnal (mind 2 -es, mind 1 -es típusú cukorbetegen is – hypoglykaemia ! Mellékhatások: komplex CH-ok fermentálódnak puffadás, flatulencia, hasi görcsök, diarrhoe - ez kezdetben acarbose kezelés mellett 10 -30%, három-négy hónap után < 10% (kezdet: kis dózis !)

SULFANYLUREA KÉSZÍTMÉNYEK I. Elnyújtott hatástartamú szerek Glibenclamide vegyületek: Gilemal 5 mg Gilemal micro 3, 5 mg Glucobene (3, 5 és 1, 75 mg) Glibenclamid (Pharmavit) 3, 5 mg (Diaprel MR) • Kevésbé ill. nem-elnyújtott hatású szerek Glimepiride: Amaryl (1 – 2 – 4 mg) Gliclazide: Diaprel (80 mg), (Gluctam) Gliquidone: Glurenorm (30 mg) Glipizide: Minidiab (5 mg)
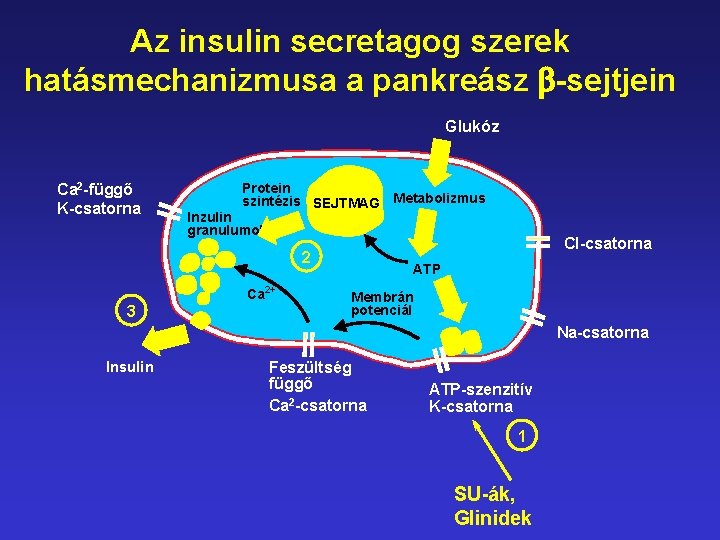
Az insulin secretagog szerek hatásmechanizmusa a pankreász b-sejtjein Glukóz Ca 2 -függő K-csatorna Protein szintézis SEJTMAG Metabolizmus Inzulin granulumok Cl-csatorna 2 Ca 2+ 3 ATP Membrán potenciál Na-csatorna Insulin Feszültség függő Ca 2 -csatorna ATP-szenzitív K-csatorna 1 SU-ák, Glinidek

SULFANYLUREA KÉSZÍTMÉNYEK EGYEDI SAJÁTOSSÁGAI – I. Glibenclamide kifejezetten elnyújtott hatás (hypoglyk. !) metabolitok is hypoglykaemizáló hatásúak intracellulárisan is hat a béta-sejtben gátolja az insulin bioszintézisét negatív cardiális hatás (olcsó) Gilemal 3, 5 mg micro

SULFANYLUREA KÉSZÍTMÉNYEK EGYEDI SAJÁTOSSÁGAI – II. Glimepiride mérsékelten elnyújtott hatás hypoglyk < glibenclamide kifejezett extrapancreaticus hatások (glukózfelvétel fokozása az izom- és zsírszövetben, GLUT-4 aktivitás fokozása)

SULFANYLUREA KÉSZÍTMÉNYEK EGYEDI SAJÁTOSSÁGAI – III. Gliklazide kevésbé elnyújtott hatás (korai hatás is igazolt) kedvező haemorheológiai hatás antioxidáns hatás Gliquidone kevésbé elnyújtott hatás veseelégtelenségben is adható Glipizide viszonylag gyors, rövid hatás (de: prandiális insulin szekréciót nem váltanak ki)

Sulfanylureák előnytelen hatásai: Elhúzódóan emelik a vér insulin szintjét (a „késői fázist” fokozzák) Gyakran okoznak hypoglykaemiát (pre-prandiálisan és éjszaka) Növelik az étvágyat és a testsúlyt (mellékhatások hosszabb hatástartamú SU-nál kifejezettebbek) egyes sulfanylureák cardiális mellékhatásai a szívizom sejtjein és az érfalban lévő ATP-dependens K+csatornákhoz is kötődnek növelik a coronaria-rezisztenciát csökkentik a szívizom hypoxia-tűrését felfüggesztik az un. iszkémiás prekondicionálást

SU-ák és iszkémiás prekondicionálás -- Szívizom védekezik a hypoxia ellen („hypoxia-tűrés”); • -- K-csatorna „nyitvatartók” (cromakalin, nicorandil) szerepe: • a Ca++-beáramlás csökken, az akciós potenciál lerövidül, a contractilitas és a coronaria-rezisztencia csökken, a • myocardium számára az energia tartalékolódik; • -- Glibenclamid: felfüggeszti a fenti előnyös hatásokat; • -- Gliklazid nem, glimepirid és a glinidek gyakorlatilag nem befolyásolják az iszkémiás prekondicionálást;
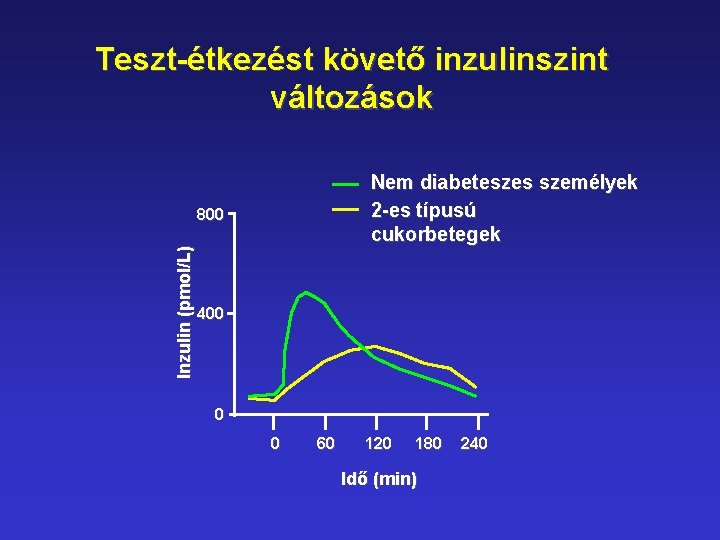
Teszt-étkezést követő inzulinszint változások Nem diabeteszes személyek 2 -es típusú cukorbetegek Inzulin (pmol/L) 800 400 0 0 60 120 180 Idő (min) 240

Inzulin szekréció diabeteses patkányokban

Prompt hatású secretagóg készítmények előnyei • Aktuális, de rövid időtartamú hatás („analóg” tabletta) • PP vércukor erőteljesen csökken • Kevesebb a hypoglykaemia • Bevétel: közvetlenül a főétkezések előtt • (one meal-one dose, no meal-no dose) • Flexibilisebb életmódot • Az étvágy és a testsúly kisebb mértékben nő
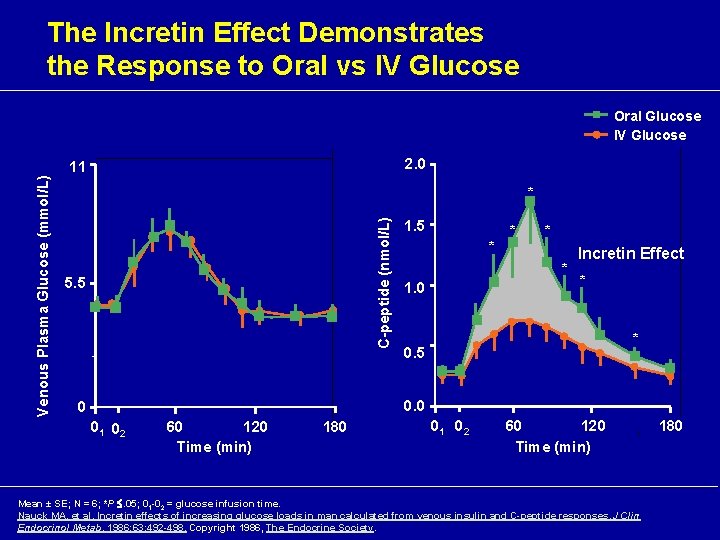
The Incretin Effect Demonstrates the Response to Oral vs IV Glucose 2. 0 11 * C-peptide (nmol/L) Venous Plasma Glucose (mmol/L) Oral Glucose IV Glucose 5. 5 1. 5 * * 1. 0 Incretin Effect * * 0. 5 0. 0 0 01 02 60 120 Time (min) 180 01 02 60 120 Time (min) Mean ± SE; N = 6; *P . 05; 01 -02 = glucose infusion time. Nauck MA, et al. Incretin effects of increasing glucose loads in man calculated from venous insulin and C-peptide responses. J Clin Endocrinol Metab. 1986; 63: 492 -498. Copyright 1986, The Endocrine Society. 180

Az incretin hatás magyarázata • A gastrointestinális tractusban olyan anyag/ok (incretinek) képződnek, amelyek táplálkozás (glukóz bevitel) után termelődnek, és (tovább) fokozzák az inzulin szekréciót; • mai tudásunk szerint a 2 fő incretin hormon a • GIP (gastric inhibitory peptide glucose-dependent insulinotropic peptide) és a • GLP-1 (glucagon-like peptide-1) • termelődés: • GIP a duodenum és a jejunum K-sejtjeiben GLP-1 az ileum és a prox colon L-sejtjeiben www. e-collegium. org
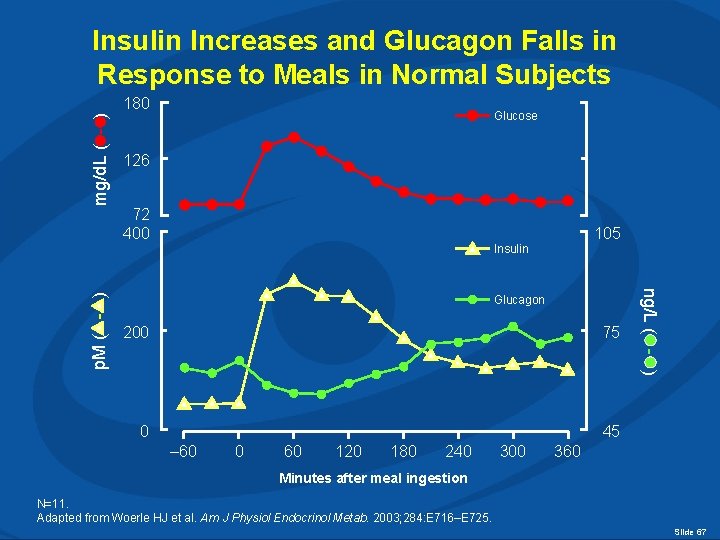
180 Glucose 126 72 400 105 Insulin Glucagon 200 75 0 45 – 60 0 60 120 180 240 300 ng/L ( - ) p. M ( - ) mg/d. L ( - ) Insulin Increases and Glucagon Falls in Response to Meals in Normal Subjects 360 Minutes after meal ingestion N=11. Adapted from Woerle HJ et al. Am J Physiol Endocrinol Metab. 2003; 284: E 716–E 725. Slide 67
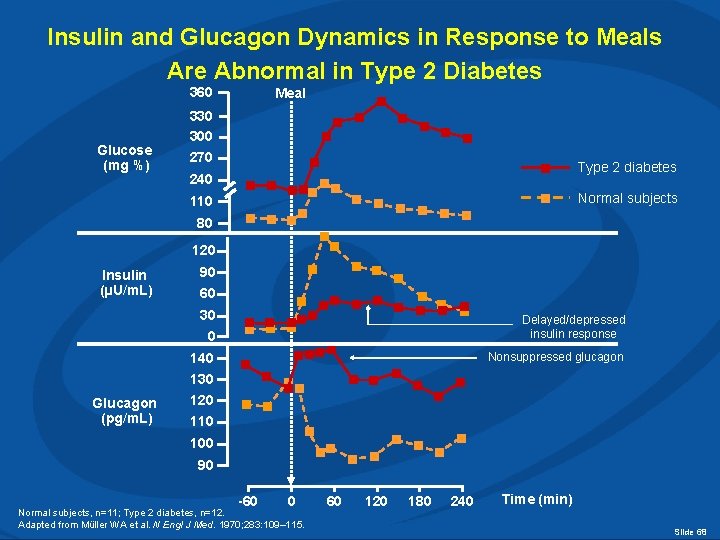
Insulin and Glucagon Dynamics in Response to Meals Are Abnormal in Type 2 Diabetes 360 Glucose (mg %) Meal 330 300 270 Type 2 diabetes 240 Normal subjects 110 80 120 Insulin (µU/m. L) 90 60 30 Delayed/depressed insulin response 0 Nonsuppressed glucagon 140 130 Glucagon (pg/m. L) 120 110 100 90 -60 0 Normal subjects, n=11; Type 2 diabetes, n=12. Adapted from Müller WA et al. N Engl J Med. 1970; 283: 109– 115. 60 120 180 240 Time (min) Slide 68
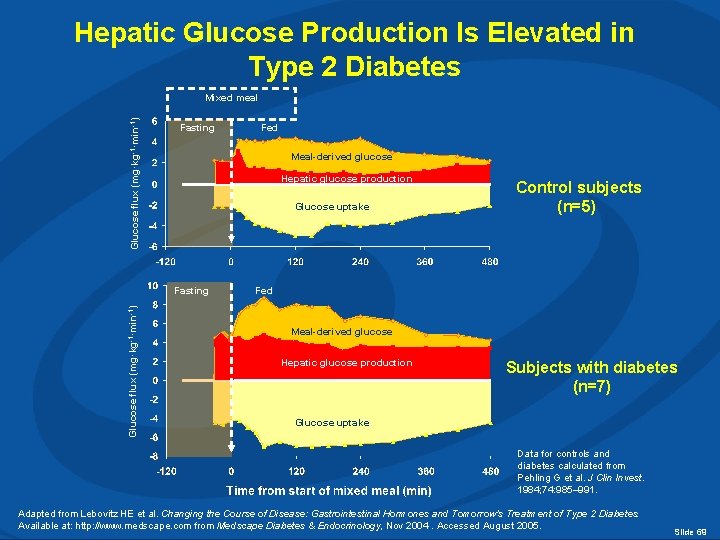
Hepatic Glucose Production Is Elevated in Type 2 Diabetes Glucose flux (mg·kg-1·min-1) Mixed meal Fasting Meal-derived glucose Hepatic glucose production Glucose uptake Fasting Glucose flux (mg·kg-1·min-1) Fed Control subjects (n=5) Fed Meal-derived glucose Hepatic glucose production Subjects with diabetes (n=7) Glucose uptake Data for controls and diabetes calculated from Pehling G et al. J Clin Invest. 1984; 74: 985– 991. Adapted from Lebovitz HE et al. Changing the Course of Disease: Gastrointestinal Hormones and Tomorrow's Treatment of Type 2 Diabetes. Available at: http: //www. medscape. com from Medscape Diabetes & Endocrinology, Nov 2004. Accessed August 2005. Slide 69
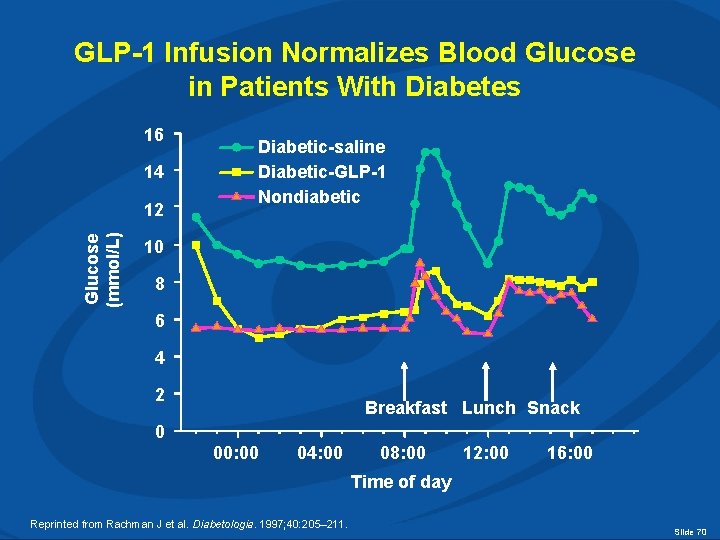
GLP-1 Infusion Normalizes Blood Glucose in Patients With Diabetes 16 14 Glucose (mmol/L) 12 Diabetic-saline Diabetic-GLP-1 Nondiabetic 10 8 6 4 2 Breakfast Lunch Snack 0 00: 00 04: 00 08: 00 12: 00 16: 00 Time of day Reprinted from Rachman J et al. Diabetologia. 1997; 40: 205– 211. Slide 70

GLP-1 hatásai • • • --erős insulinotróp hatás (korai szekréció fokozása) --fokozta az insulin bioszintézis minden lépését --gátolta a pancreas-glucagon elválasztását --gátolta a gastrointestinalis motilitást --csökkentette az étvágyat és a testsúlyt • állatkísérletekben gátolta a B-sejtek apoptózisát • segítette fenntartani a Langerhans-szigetek integritását • növelte a B-sejt replikációt és a B-sejt neogenezist Slide 71
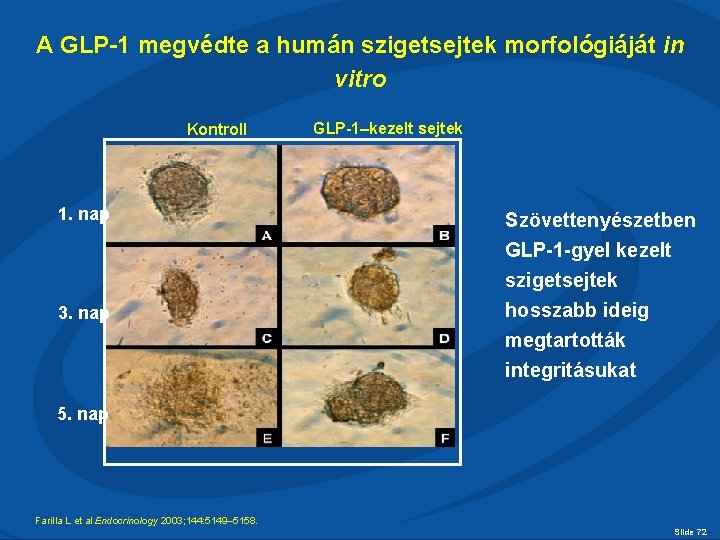
A GLP-1 megvédte a humán szigetsejtek morfológiáját in vitro Kontroll 1. nap 3. nap GLP-1–kezelt sejtek Szövettenyészetben GLP-1 -gyel kezelt szigetsejtek hosszabb ideig megtartották integritásukat 5. nap Farilla L et al Endocrinology 2003; 144: 5149– 5158. Slide 72
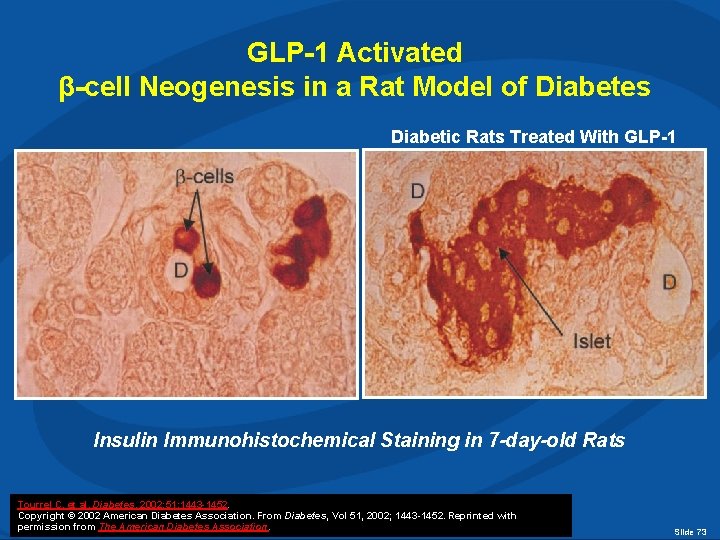
GLP-1 Activated β-cell Neogenesis in a Rat Model of Diabetes Diabetic Rats Treated With GLP-1 Untreated Diabetic Rats Insulin Immunohistochemical Staining in 7 -day-old Rats Tourrel C, et al. Diabetes. 2002; 51: 1443 -1452. Copyright © 2002 American Diabetes Association. From Diabetes, Vol 51, 2002; 1443 -1452. Reprinted with permission from The American Diabetes Association. Slide 73

Native GLP-1 Is Rapidly Degraded by DPP-4 7 9 37 T½=1– 2 minutes (IV) MCR=5– 10 L/min MCR=metabolic clearance rate. Vilsbøll T et al. J Clin Endocrinol Metab. 2003; 88: 220– 224. Slide 74

Incretin hatású gógyszerek • A GLP-1 -et perceken belül elbontja a DPP-4 enzim • MEGOLDÁS: • GLP-1 analógok (pl. exendin-4) • DPP-4 gátlók (sitagliptin, vildagliptin) Slide 75

Incretinek terápiás alkalmazása I. • GLP-1: plazma félidő 1 -2 perc; clearance 5 -10 L/perc • (azonnal elbontja a dipeptidyl-peptidase-4 enzim) • Csak folyamatos infúzióban hatásosak • Pumpa-kezelés (6 héten át): FPG 5 mmol/l • átlagos napi vércukorszint: 5 mmol/l • Hb. A 1 c : 1, 2% testsúly : 2 kg-mal • visszaállt a korai insulin-válasz • De: ez a kezelés csak szelektált, kis beteganyagon végezhető, • tömeges kezelésre nem alkalmas; Slide 76

Development of Exenatide: An Incretin Mimetic Exenatide (Exendin-4) • Synthetic version of salivary protein found in the Gila monster • Approximately 50% identity with human GLP-1 - Binds to known human GLP-1 receptors on cells in vitro - Resistant to DPP-IV inactivation Exenatide H G E G T F T S D L S K Q M E E E A V R L F I E W L K N G G P S S G A P P P S – NH 2 GLP-1 Human H A E G T F T S D V S S Y L E G Q A A K E F I A W L V K G R – NH 2 Site of DPP-IV Inactivation Adapted from Nielsen LL, et al. Regulatory Peptides. 2004; 117: 77 -88. ; Fineman MS, et al. Diabetes Care. 2003; 26: 2370 -2377. Reprinted from Regulatory Peptides, 117, Nielsen LL, et al, Pharmacology of exenatide (synthetic exendin-4): a potential therapeutic for improved glycemic control of type 2 diabetes, 77 -88, 2004, with permission from Elsevier.
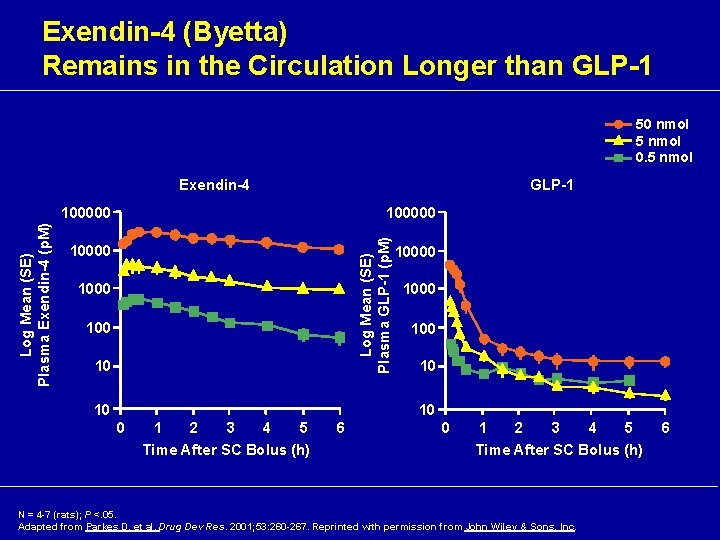
Exendin-4 (Byetta) Remains in the Circulation Longer than GLP-1 50 nmol 5 nmol 0. 5 nmol GLP-1 Exendin-4 100000 Log Mean (SE) Plasma GLP-1 (p. M) Log Mean (SE) Plasma Exendin-4 (p. M) 100000 1000 10 10 1000 100 10 10 0 1 2 3 4 5 Time After SC Bolus (h) 6 0 1 2 3 4 5 Time After SC Bolus (h) N = 4 -7 (rats); P <. 05. Adapted from Parkes D, et al. Drug Dev Res. 2001; 53: 260 -267. Reprinted with permission from John Wiley & Sons, Inc. 6

KLINIKAI VIZSGÁLATOK EXENATIDDAL I. ♦ 2 vizsgálatban a T 2 DM betegek addigi kezelését vagy exenatiddal vagy inzulinnal (1) glargin (2) Novo. Mix (30/70 premix) egészítették ki. Hb. A 1 c azonos mértékben csökkent Éhomi vércukorszint azonos mértékben csökkent PP vércukorszint jobban csökkent az exenatide mellett Ts: exenatide mellett csökkent, inzulin mellett nőtt (p<, 001) Hypoglykaemia gyak. azonos volt (de más időpontban) Hányinger: EXE 57% (vs 9%); hányás EXE 17% (vs 4%) Beteg kivonási ráta: EXE 21, 3% vs 10, 1%

KLINIKAI VIZSGÁLATOK EXENATIDDAL II. ♦ Exenatide-LAR (long acting release) ♦ mikroszférikus partikulumokból lassan szabadul fel a gyógyszer ♦ heti 1 x sc injectio elegendő ♦ egyenletes hatás ♦ heti 2 mg mellett 15 hetes kezelés során -- a Hb. A 1 c 1, 7%-kal, -- ts 3, 8 kg-mal csökkent -- betegek 86%-án a Hb. A 1 c< 7, 0% 15 hét után a betegek 57%-án mutattak ki exenatide antitesteket
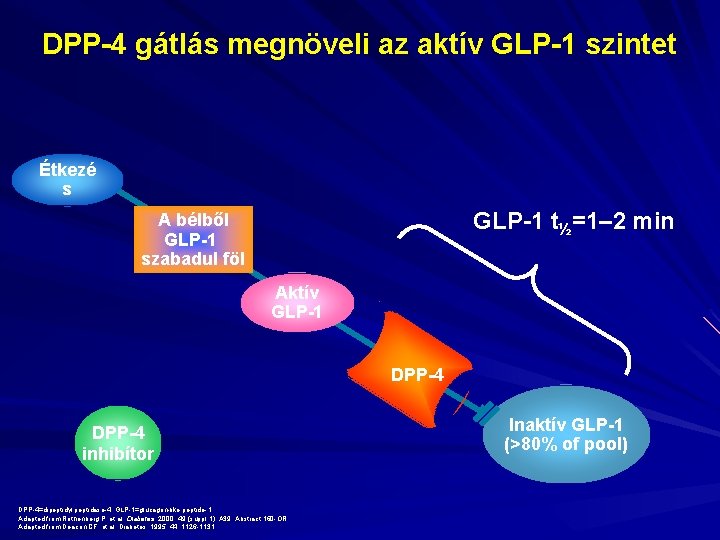
DPP-4 gátlás megnöveli az aktív GLP-1 szintet Étkezé s GLP-1 t½=1– 2 min A bélből GLP-1 szabadul föl Aktív GLP-1 DPP-4 inhibítor DPP-4=dipeptidyl peptidase-4; GLP-1=glucagon-like peptide-1 Adapted from Rothenberg P, et al. Diabetes. 2000; 49 (suppl 1): A 39. Abstract 160 -OR. Adapted from Deacon CF, et al. Diabetes. 1995; 44: 1126 -1131. Inaktív GLP-1 (>80% of pool)

KLINIKAI VIZSGÁLATOK SITAGLIPTINNEL I. • Add-on vizsgálatok (50 -100 mg per os naponta 1 -2 -szer) • Sitagliptine Pioglitazone monoterápia: 24 hetes kezelés • során szign javulás a CH anyagcsere paramétereiben • Sitagliptin Metformin monoterápia: jelentős javulás (vércukor profil, Hb. A 1 c, PP vércukorszint) Sitagliptin vs Glipizide (hasonló anyagcsere hatások, de kevesebb hypoglykaemia és nem volt hízás) (Vildagliptin: hasonló eredmények)

KLINIKAI VIZSGÁLATOK SITAGLIPTINNEL • Sitagliptin monoterápia • Add-on vizsgálatok (50 -100 mg per os naponta 1 -2 -szer) • Sitagliptin Metformin monoterápia: jelentős javulás (vércukor profil, Hb. A 1 c, PP vércukorszint) • Sitagliptine Pioglitazone monoterápia: 24 hetes kezelés során szign javulás a CH anyagcsere paramétereiben Sitagliptin vs Glipizide (hasonló anyagcsere hatások, de kevesebb hypoglykaemia és nem volt hízás) Sitagliptin + Metformin: Hb. A 1 c szint csökkenés > 2%
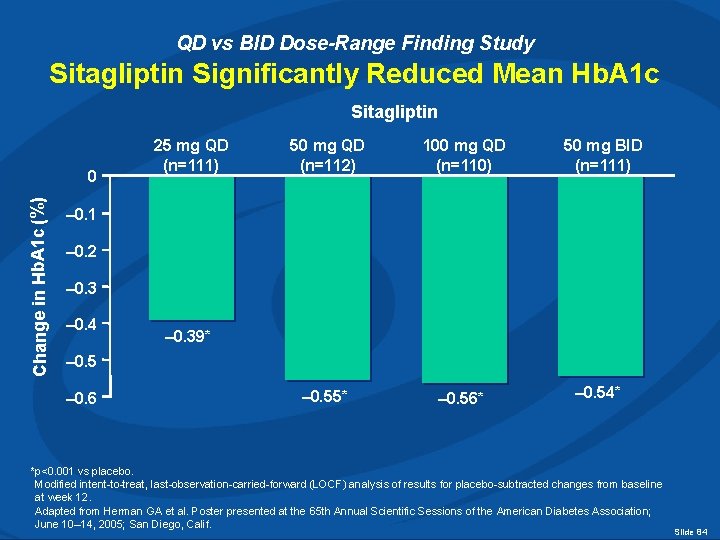
QD vs BID Dose-Range Finding Study Sitagliptin Significantly Reduced Mean Hb. A 1 c Sitagliptin Change in Hb. A 1 c (%) 0 25 mg QD (n=111) 50 mg QD (n=112) 100 mg QD (n=110) – 0. 55* – 0. 56* 50 mg BID (n=111) – 0. 1 – 0. 2 – 0. 3 – 0. 4 – 0. 39* – 0. 5 – 0. 6 – 0. 54* *p<0. 001 vs placebo. Modified intent-to-treat, last-observation-carried-forward (LOCF) analysis of results for placebo-subtracted changes from baseline at week 12. Adapted from Herman GA et al. Poster presented at the 65 th Annual Scientific Sessions of the American Diabetes Association; June 10– 14, 2005; San Diego, Calif. Slide 84
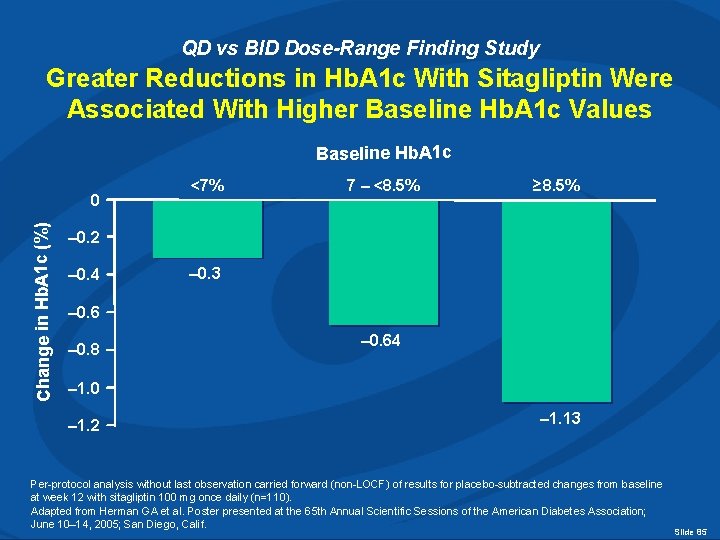
QD vs BID Dose-Range Finding Study Greater Reductions in Hb. A 1 c With Sitagliptin Were Associated With Higher Baseline Hb. A 1 c Values Baseline Hb. A 1 c Change in Hb. A 1 c (%) 0 <7% 7 – <8. 5% ≥ 8. 5% – 0. 2 – 0. 4 – 0. 3 – 0. 6 – 0. 8 – 0. 64 – 1. 0 – 1. 2 – 1. 13 Per-protocol analysis without last observation carried forward (non-LOCF) of results for placebo-subtracted changes from baseline at week 12 with sitagliptin 100 mg once daily (n=110). Adapted from Herman GA et al. Poster presented at the 65 th Annual Scientific Sessions of the American Diabetes Association; June 10– 14, 2005; San Diego, Calif. Slide 85
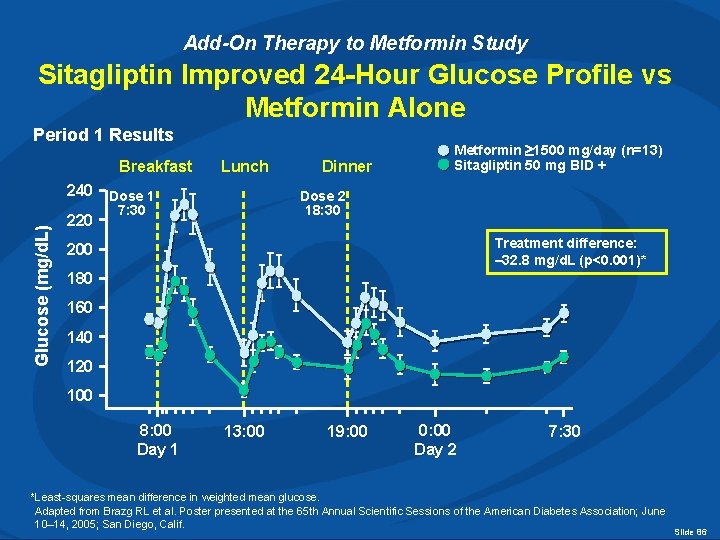
Add-On Therapy to Metformin Study Sitagliptin Improved 24 -Hour Glucose Profile vs Metformin Alone Period 1 Results Breakfast Lunch Glucose (mg/d. L) 240 Dose 1 220 Dinner Metformin 1500 mg/day (n=13) Sitagliptin 50 mg BID + Dose 2 18: 30 7: 30 Treatment difference: – 32. 8 mg/d. L (p<0. 001)* 200 180 160 140 120 100 8: 00 Day 1 13: 00 19: 00 0: 00 Day 2 7: 30 *Least-squares mean difference in weighted mean glucose. Adapted from Brazg RL et al. Poster presented at the 65 th Annual Scientific Sessions of the American Diabetes Association; June 10– 14, 2005; San Diego, Calif. Slide 86
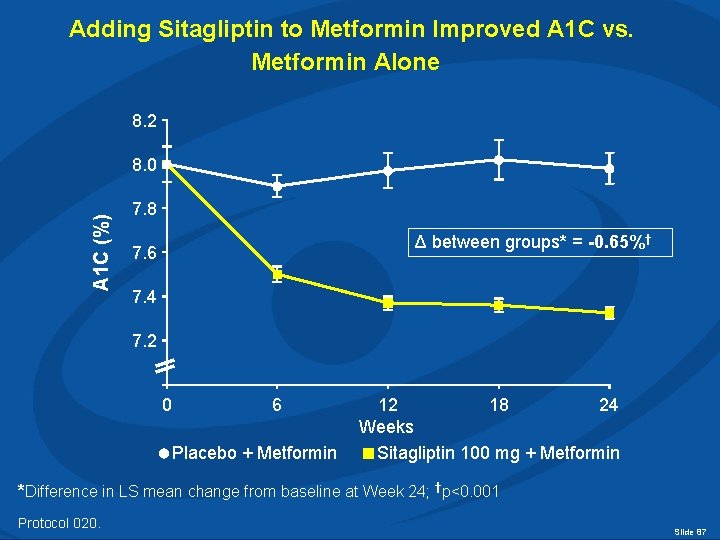
Adding Sitagliptin to Metformin Improved A 1 C vs. Metformin Alone 8. 2 A 1 C (%) 8. 0 7. 8 Δ between groups* = -0. 65%† 7. 6 7. 4 7. 2 0 6 Placebo + Metformin 12 18 24 Weeks Sitagliptin 100 mg + Metformin *Difference in LS mean change from baseline at Week 24; †p<0. 001 Protocol 020. Slide 87
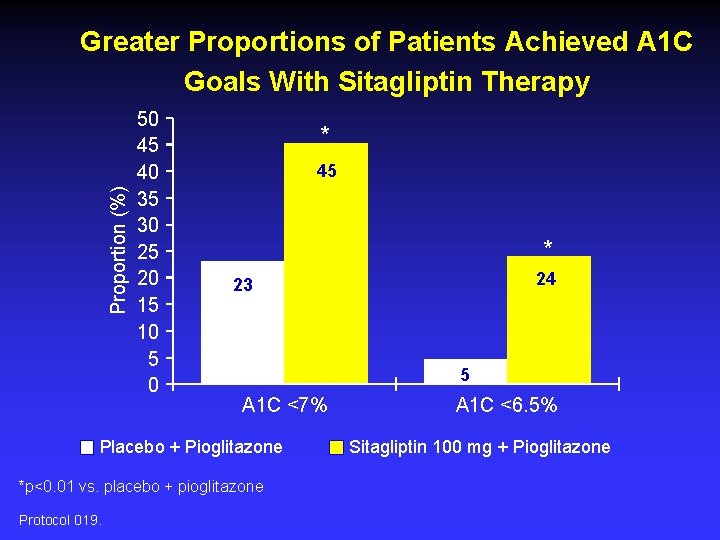
Proportion (%) Greater Proportions of Patients Achieved A 1 C Goals With Sitagliptin Therapy 50 45 40 35 30 25 20 15 10 5 0 * 45 * 5 A 1 C <7% Placebo + Pioglitazone *p<0. 01 vs. placebo + pioglitazone Protocol 019. 24 23 A 1 C <6. 5% Sitagliptin 100 mg + Pioglitazone
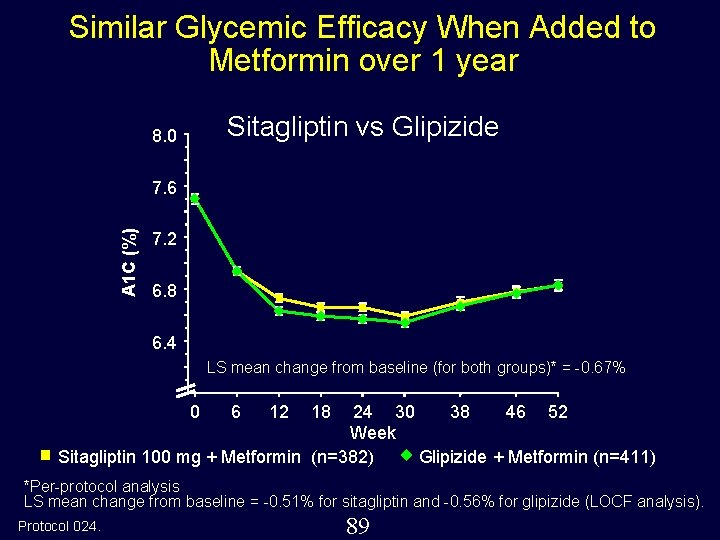
Similar Glycemic Efficacy When Added to Metformin over 1 year Sitagliptin vs Glipizide 8. 0 A 1 C (%) 7. 6 7. 2 6. 8 6. 4 LS mean change from baseline (for both groups)* = -0. 67% 0 6 12 18 24 30 38 46 52 Week Sitagliptin 100 mg + Metformin (n=382) Glipizide + Metformin (n=411) *Per-protocol analysis LS mean change from baseline = -0. 51% for sitagliptin and -0. 56% for glipizide (LOCF analysis). Protocol 024. 89
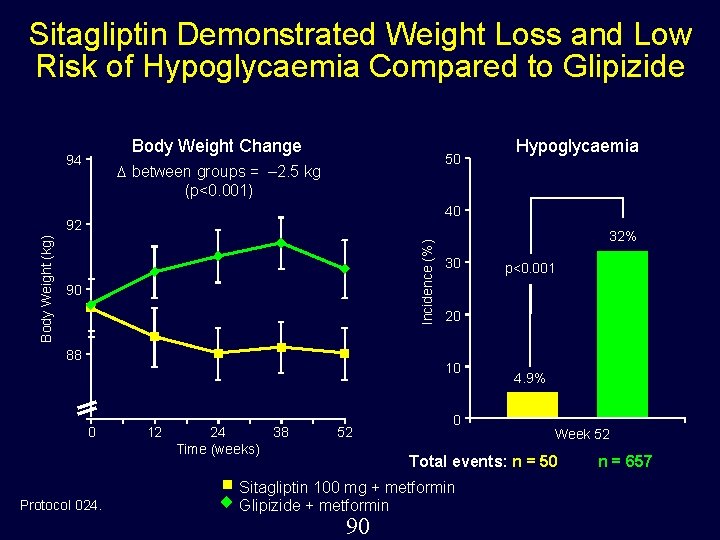
Sitagliptin Demonstrated Weight Loss and Low Risk of Hypoglycaemia Compared to Glipizide Body Weight Change 94 50 between groups = – 2. 5 kg (p<0. 001) 40 Incidence (%) 92 Body Weight (kg) Hypoglycaemia 90 88 32% 30 20 10 0 Protocol 024. 12 24 38 Time (weeks) 52 p<0. 001 0 4. 9% Week 52 Total events: n = 50 Sitagliptin 100 mg + metformin Glipizide + metformin 90 n = 657
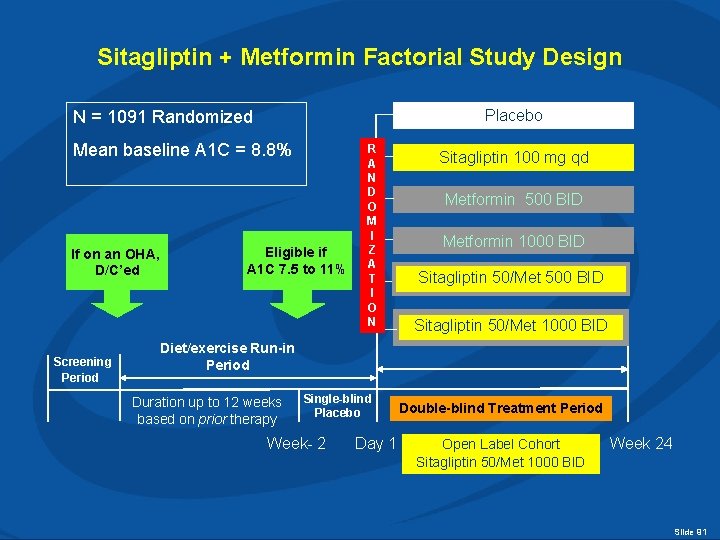
Sitagliptin + Metformin Factorial Study Design Placebo N = 1091 Randomized Mean baseline A 1 C = 8. 8% If on an OHA, D/C’ed Screening Period Eligible if A 1 C 7. 5 to 11% R A N D O M I Z A T I O N Sitagliptin 100 mg qd Metformin 500 BID Metformin 1000 BID Sitagliptin 50/Met 500 BID Sitagliptin 50/Met 1000 BID Diet/exercise Run-in Period Duration up to 12 weeks based on prior therapy Single-blind Placebo Week- 2 Day 1 Double-blind Treatment Period Open Label Cohort Sitagliptin 50/Met 1000 BID Week 24 Slide 91

Initial Combination of Sitagliptin and Metformin Produced a Marked Improvement in A 1 C Mean baseline A 1 C = 8. 8% Sita 100 mg q. d. MF 500 mg b. i. d. MF 1000 mg b. i. d. -0. 8 Sita 50 mg + MF 500 mg b. i. d. -1. 0 -1. 3 Sita 50 mg + MF 1000 mg b. i. d. -1. 6 -2. 1 Open Label Sita 50 mg + MF 1000 mg b. i. d. Placebo change from Baseline = 0. 17 % *Placebo-subtracted LS mean change from baseline at Week 24 Slide 92
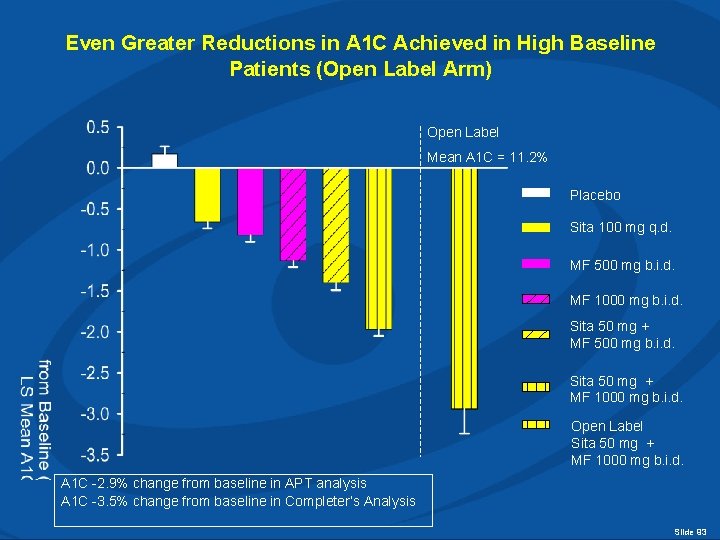
Even Greater Reductions in A 1 C Achieved in High Baseline Patients (Open Label Arm) Open Label Mean A 1 C = 11. 2% Placebo Sita 100 mg q. d. MF 500 mg b. i. d. MF 1000 mg b. i. d. Sita 50 mg + MF 500 mg b. i. d. Sita 50 mg + MF 1000 mg b. i. d. Open Label Sita 50 mg + MF 1000 mg b. i. d. A 1 C -2. 9% change from baseline in APT analysis A 1 C -3. 5% change from baseline in Completer’s Analysis Slide 93
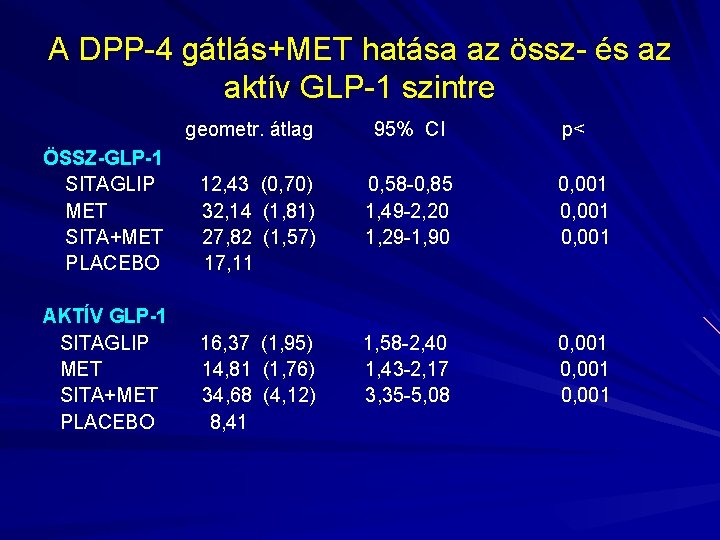
A DPP-4 gátlás+MET hatása az össz- és az aktív GLP-1 szintre geometr. átlag 95% CI p< ÖSSZ-GLP-1 SITAGLIP MET SITA+MET PLACEBO 12, 43 (0, 70) 32, 14 (1, 81) 27, 82 (1, 57) 17, 11 0, 58 -0, 85 1, 49 -2, 20 1, 29 -1, 90 0, 001 AKTÍV GLP-1 SITAGLIP MET SITA+MET PLACEBO 16, 37 (1, 95) 14, 81 (1, 76) 34, 68 (4, 12) 8, 41 1, 58 -2, 40 1, 43 -2, 17 3, 35 -5, 08 0, 001
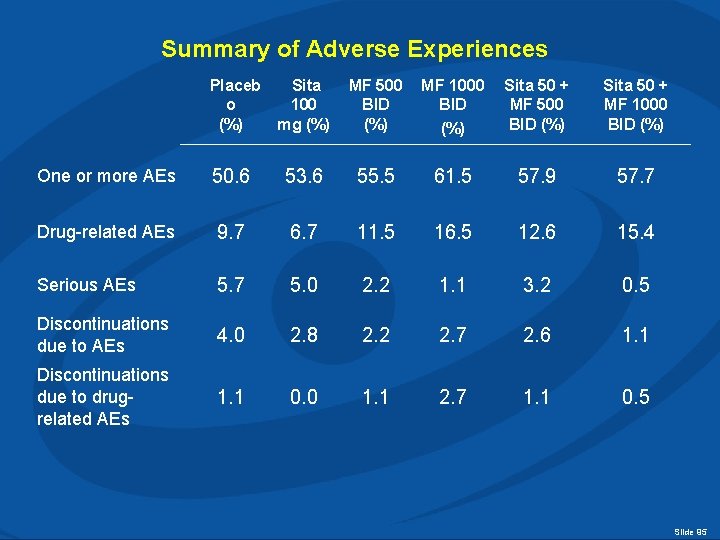
Summary of Adverse Experiences Placeb o (%) Sita 100 mg (%) MF 500 BID (%) MF 1000 BID (%) Sita 50 + MF 500 BID (%) Sita 50 + MF 1000 BID (%) One or more AEs 50. 6 53. 6 55. 5 61. 5 57. 9 57. 7 Drug-related AEs 9. 7 6. 7 11. 5 16. 5 12. 6 15. 4 Serious AEs 5. 7 5. 0 2. 2 1. 1 3. 2 0. 5 Discontinuations due to AEs 4. 0 2. 8 2. 2 2. 7 2. 6 1. 1 Discontinuations due to drugrelated AEs 1. 1 0. 0 1. 1 2. 7 1. 1 0. 5 Slide 95
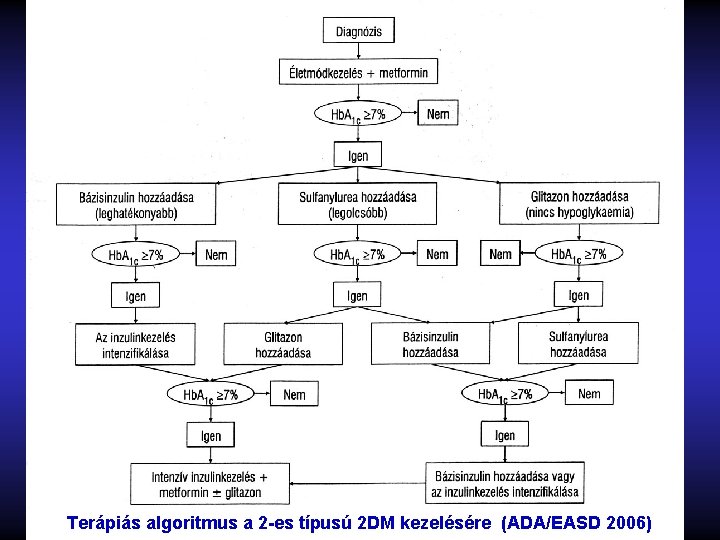
Terápiás algoritmus a 2 -es típusú 2 DM kezelésére (ADA/EASD 2006)

Mellékhatások OAD kezelés mellett • • METF • SU Hypoglyk. ↓ ↑↑ • GLIT • DPP-4 gátlók Ts ↑↑ Szívelégt. ↓↓ ? ↑ ↑↑ ↓ CV szöv. ↑↑ ? ↑↓ ? ?

A metformin+DPP-4 gátlás előnyei Kombinált alkalmazás esetén a két szer synergista módon növeli az aktív GLP-1 mennyiségét; Fix kombináció alkalmazása is lehetséges; Mellékhatás kevés ( placebo mellékhatásaival) (Mo-on: Januvia [sitagliptin] 100 mg Janumet [sita+met] 50+1000 Galvus [vildagliptin] 50 mg Eucreas [vilda+met] 50+1000 Xelevia 100 mg Velmetia 50+100 2008 aug-tól, 2009 febr-tól) 2008 nov-től 2009
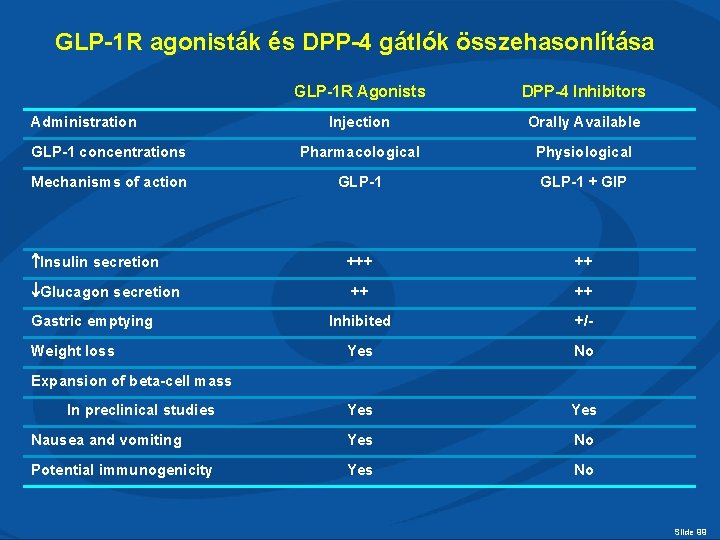
GLP-1 R agonisták és DPP-4 gátlók összehasonlítása GLP-1 R Agonists DPP-4 Inhibitors Injection Orally Available GLP-1 concentrations Pharmacological Physiological Mechanisms of action GLP-1 + GIP Insulin secretion +++ ++ Glucagon secretion ++ ++ Inhibited +/- Yes No Yes Nausea and vomiting Yes No Potential immunogenicity Yes No Administration Gastric emptying Weight loss Expansion of beta-cell mass In preclinical studies Slide 99

Inzulinkezelés T 2 DM-ben I. • Idős emberen: bed time inzulin (és nappal tabletta) Ha a fenti kezelés nem biztosít anyagcsereegyensúlyt, váltás napi 2 x-i premix inzulinra (15/85, 25/75, 30/70, 50/50 arányban gyors/elhúzódó inzulinkeverék)

Inzulinkezelés T 2 DM-ben II. • Klasszikus ICIT T 2 DM-ben: • • Indikációk: viszonylag fiatal életkor nagy inzulin igény vascularis katasztrófa (? )

Inzulinkezelés T 2 DM-ben III. • Előkevert (premix) inzulinok (bifázisos humán inzulinok) használatának előnyei • Humulin M 3: 30% Hum-R+70% Hum-N • Insuman Comb 15/85, 25/75, 50/50 • (hátrányok: kivárás, , magas PP vércukor, ts növekedés)

Inzulinkezelés T 2 DM-ben IV. • Analóg premix indikációi (OEP): • PP vércukorszint>10, 0 m. M/L • gyakori hypoglykaemia • jelentős testsúlynövekedés a humán premix inzulin kezelésen

Inzulinkezelés T 2 DM-ben V. • Analóg premix készítmények: • Novo. Mix 30 (30% Aspart+70% prot-Aspart) • Humalog Mix 25, 50 és 75 (25, 50 ill. 75% Humalog és 75, 50 ill. 25% NPL).
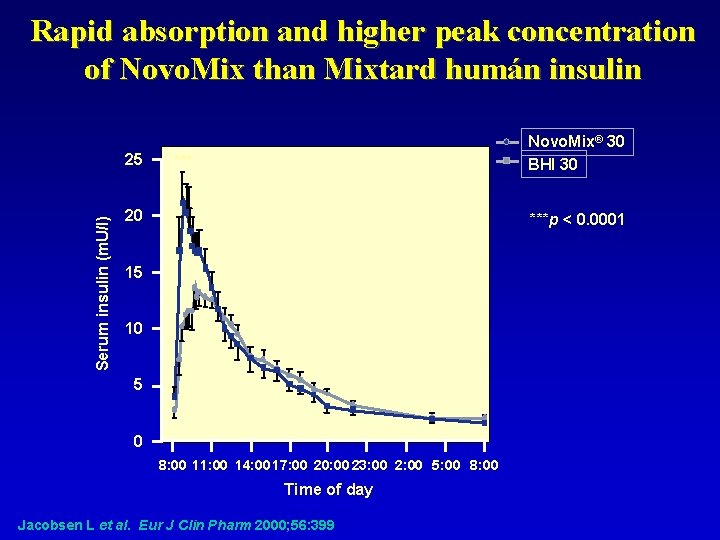
Rapid absorption and higher peak concentration of Novo. Mix than Mixtard humán insulin Serum insulin (m. U/l) 25 Novo. Mix® 30 BHI 30 *** 20 ***p < 0. 0001 15 10 5 0 8: 00 11: 00 14: 00 17: 00 20: 00 23: 00 2: 00 5: 00 8: 00 Time of day Jacobsen L et al. Eur J Clin Pharm 2000; 56: 399
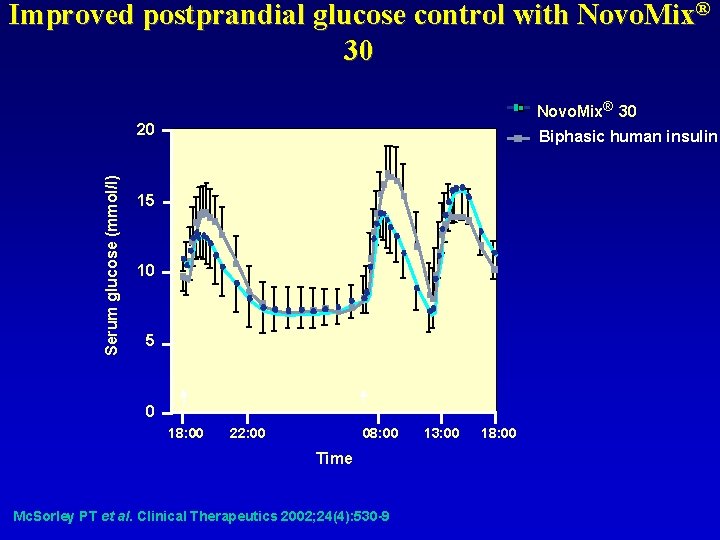
Improved postprandial glucose control with Novo. Mix® 30 Serum glucose (mmol/l) 20 Biphasic human insulin 15 10 5 0 18: 00 22: 00 08: 00 Time Mc. Sorley PT et al. Clinical Therapeutics 2002; 24(4): 530 -9 13: 00 18: 00

Inzulinkezelés T 2 DM-ben VI. • Napi 2 -szeri pemix inzulin (ebéd után már nincs prandiális hatás) • Napi 3 -szori premix analóg kezelés: igen jó beállítást lehet elérni • (PPT: prandiális premix terápia)
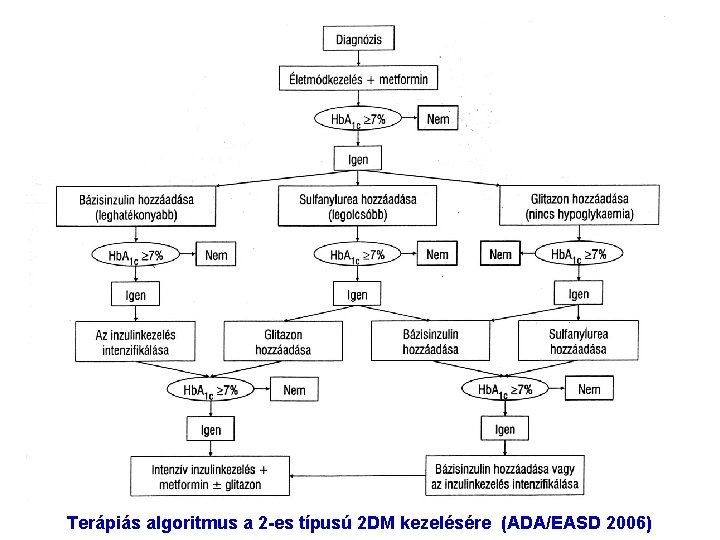
Terápiás algoritmus a 2 -es típusú 2 DM kezelésére (ADA/EASD 2006)
- Slides: 108