7 Alkena Struktur dan Reaktivitas Based on Mc

7. Alkena: Struktur dan Reaktivitas Based on Mc. Murry’s Organic Chemistry, 8 th edition © 2012 Ronald Kluger Department of Chemistry University of Toronto
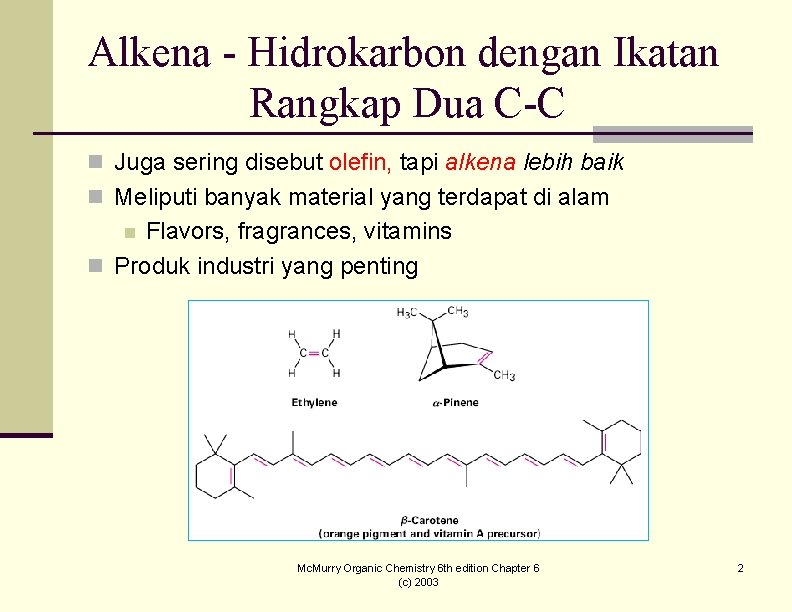
Alkena - Hidrokarbon dengan Ikatan Rangkap Dua C-C n Juga sering disebut olefin, tapi alkena lebih baik n Meliputi banyak material yang terdapat di alam Flavors, fragrances, vitamins n Produk industri yang penting n Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 2

7. 2 Tingkat ketidakjenuhan n Berhubungan dengan rumus molekul untuk struktur yang n n mungkin Tingkat ketidakjenuhan: jumlah ikatan rangkap atau cincin Rumus untuk senyawa asiklik yang jenuh adalah: Cn. H 2 n+2 Masing-masing cincin atau ikatan rangkap menggantikan 2 H Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 3
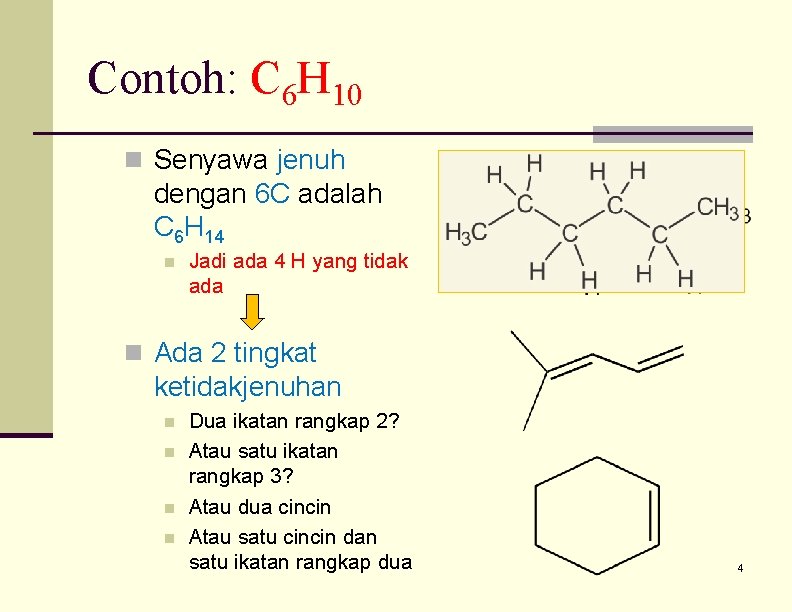
Contoh: C 6 H 10 n Senyawa jenuh dengan 6 C adalah C 6 H 14 n Jadi ada 4 H yang tidak ada n Ada 2 tingkat ketidakjenuhan n n Dua ikatan rangkap 2? Atau satu ikatan rangkap 3? Atau dua cincin Atau satu cincin dan satu ikatan rangkap dua 4
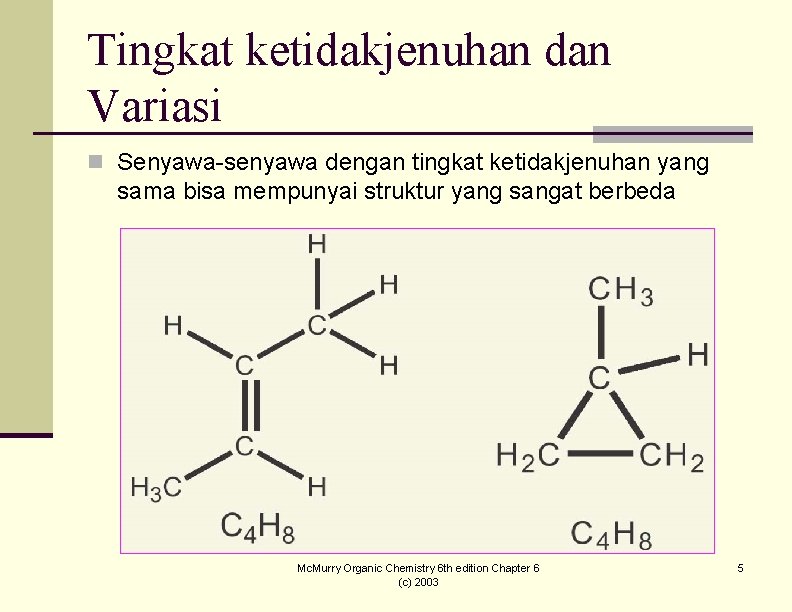
Tingkat ketidakjenuhan dan Variasi n Senyawa-senyawa dengan tingkat ketidakjenuhan yang sama bisa mempunyai struktur yang sangat berbeda Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 5
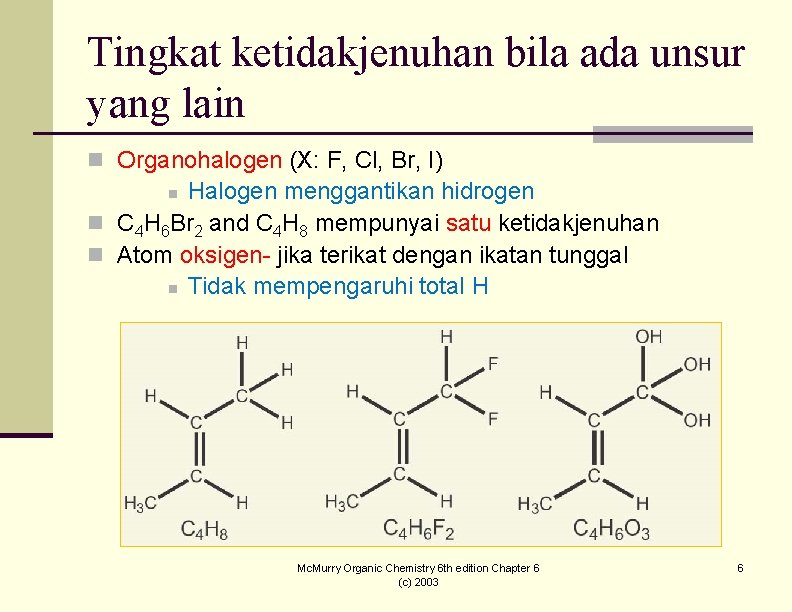
Tingkat ketidakjenuhan bila ada unsur yang lain n Organohalogen (X: F, Cl, Br, I) Halogen menggantikan hidrogen n C 4 H 6 Br 2 and C 4 H 8 mempunyai satu ketidakjenuhan n Atom oksigen- jika terikat dengan ikatan tunggal n Tidak mempengaruhi total H n Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 6
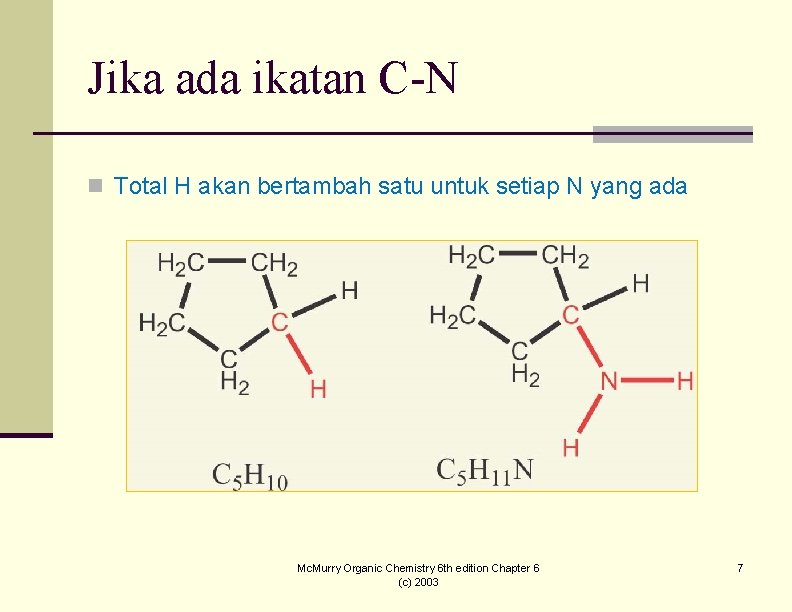
Jika ada ikatan C-N n Total H akan bertambah satu untuk setiap N yang ada Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 7
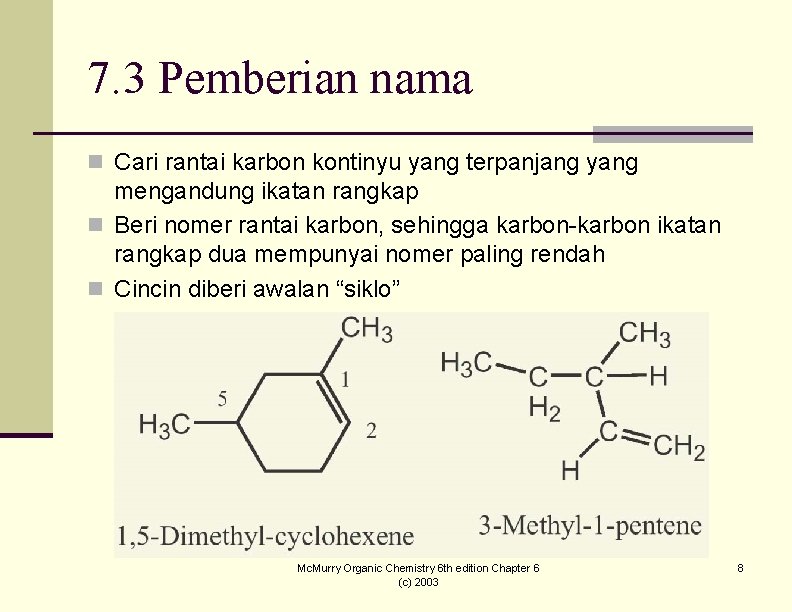
7. 3 Pemberian nama n Cari rantai karbon kontinyu yang terpanjang yang mengandung ikatan rangkap n Beri nomer rantai karbon, sehingga karbon-karbon ikatan rangkap dua mempunyai nomer paling rendah n Cincin diberi awalan “siklo” Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 8
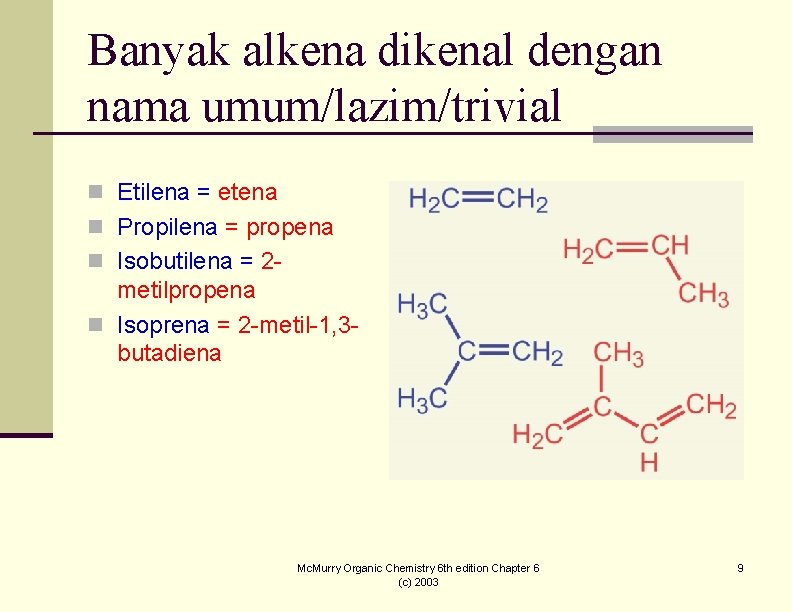
Banyak alkena dikenal dengan nama umum/lazim/trivial n Etilena = etena n Propilena = propena n Isobutilena = 2 - metilpropena n Isoprena = 2 -metil-1, 3 butadiena Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 9

7. 4 Struktur elektronik alkena n Atom karbon ikatan rangkap terhibridisasi sp 2 n Punya tiga orbital sp 2 yang ekivalen terpisah 120º pada bidang datar n Punya satu orbital p n Kombinasi elektron dalam dua orbital sp 2 dari dua atom karbon membentuk ikatan diantaranya n Tumpang tindih orbital p secara lateral membentuk ikatan n Adanya orbital terisi menghalangi rotasi sekitar ikatan n Rotasi dicegah dengan adanya penghalang energi tinggi ikatan , sekitart 268 k. J/mole dalam etilena 10
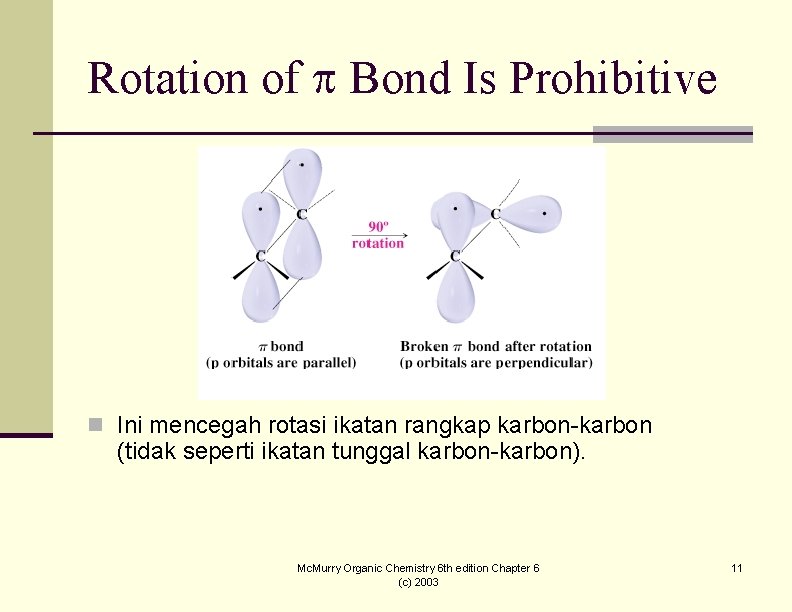
Rotation of Bond Is Prohibitive n Ini mencegah rotasi ikatan rangkap karbon-karbon (tidak seperti ikatan tunggal karbon-karbon). Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 11

6. 5 Cis-Trans Isomerism in Alkenes n Adanya ikatan rangkap karbon-karbon dapat menghasilkan dua struktur yang mungkin n isomer cis- dua gugus yang sama terdapat pada sisi yang sama pada ikatan rangkap dua n isomer trans-gugus yang sama terletak berseberangan n Masing-masing karbon harus mengikat dua gugus yang berbeda Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 12
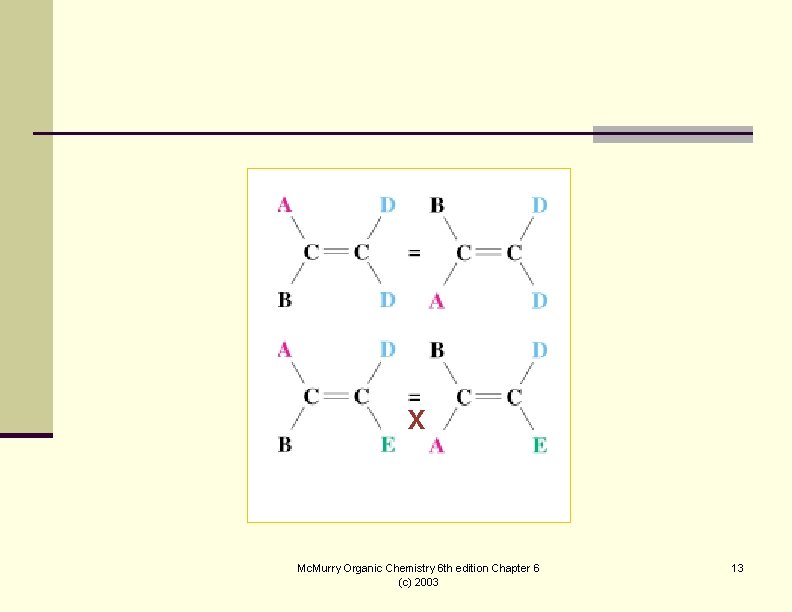
X Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 13
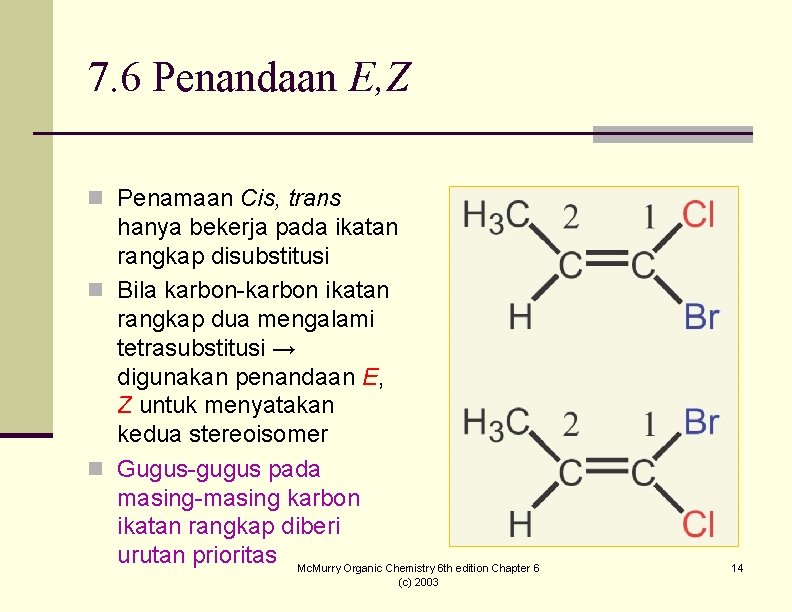
7. 6 Penandaan E, Z n Penamaan Cis, trans hanya bekerja pada ikatan rangkap disubstitusi n Bila karbon-karbon ikatan rangkap dua mengalami tetrasubstitusi → digunakan penandaan E, Z untuk menyatakan kedua stereoisomer n Gugus-gugus pada masing-masing karbon ikatan rangkap diberi urutan prioritas Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 14
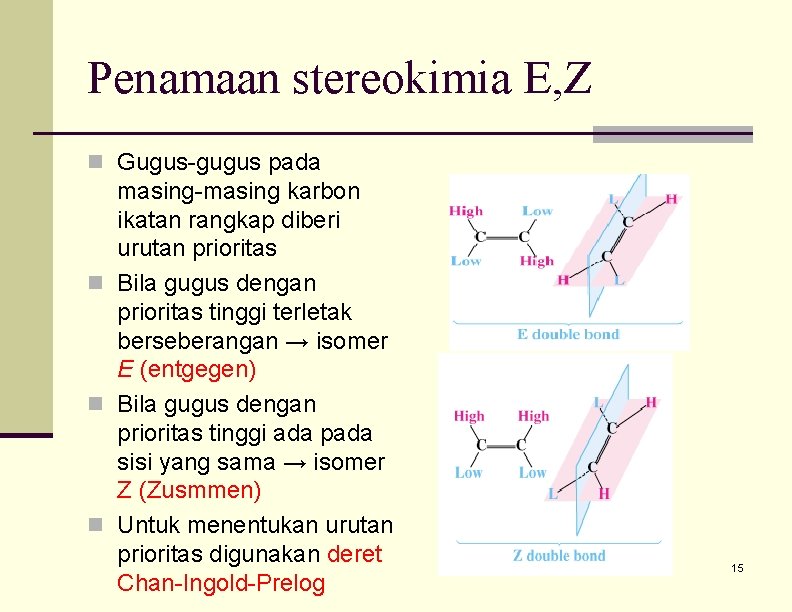
Penamaan stereokimia E, Z n Gugus-gugus pada masing-masing karbon ikatan rangkap diberi urutan prioritas n Bila gugus dengan prioritas tinggi terletak berseberangan → isomer E (entgegen) n Bila gugus dengan prioritas tinggi ada pada sisi yang sama → isomer Z (Zusmmen) n Untuk menentukan urutan prioritas digunakan deret Chan-Ingold-Prelog 15

7. 7 Stabilitas Alkena n Cis alkena kurang stabil dibanding trans alkena n Dibandingkan dengan panas hidrogensinya: Ho n Isomer yang kurang stabil adalah yang berenergi tinggi n Membebaskan panas yang lebih tinggi Alkena yang lebih tersubstitusi lebih stabil dari pada yang kurang tersubstitusi n Tetrasubstitusi > trisubstitusi > disubstitusi > monosusbtitusi n hyperconjugation menstabilkan alkena Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 16
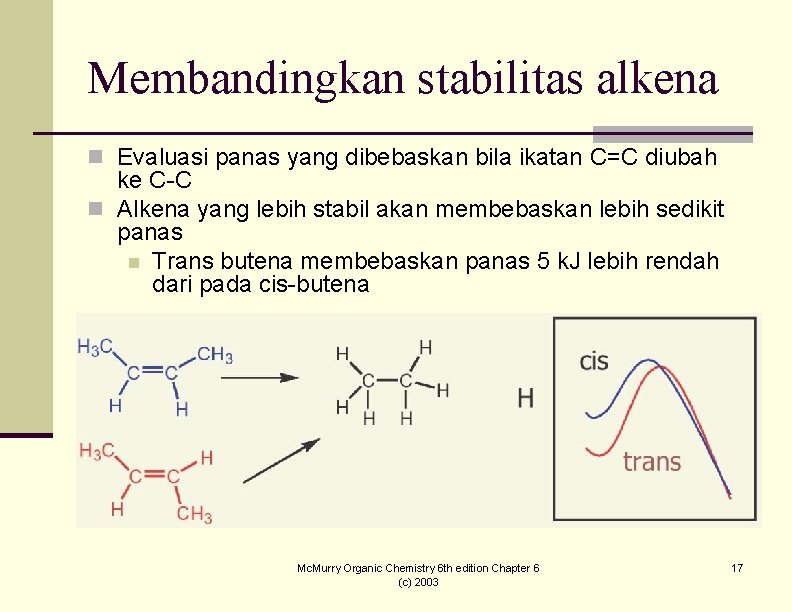
Membandingkan stabilitas alkena n Evaluasi panas yang dibebaskan bila ikatan C=C diubah ke C-C n Alkena yang lebih stabil akan membebaskan lebih sedikit panas n Trans butena membebaskan panas 5 k. J lebih rendah dari pada cis-butena Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 17
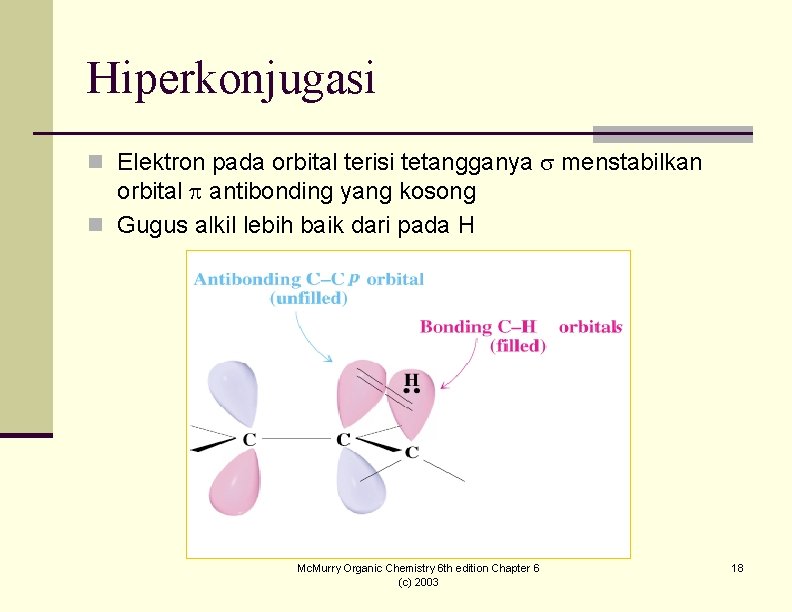
Hiperkonjugasi n Elektron pada orbital terisi tetangganya menstabilkan orbital antibonding yang kosong n Gugus alkil lebih baik dari pada H Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 18

7. 8 Adisi Elektrofilik pada Alkena n Reaksi yang khas untuk alkena adalah reaksi adisi elektrofilik Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 19

7. 8 Adisi Elektrofilik HX ke Alkena n Mekanisme reaksi umum: adisi elektrofilik n Penyerangan elektrofil (seperti HBr) pada ikatan alkena n Menghasilkan karbokation dan ion bromida n Karbokation adalah suatu elektrofil, kemudian bereaksi dengan ion bromida (suatu nukleofil) Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 20
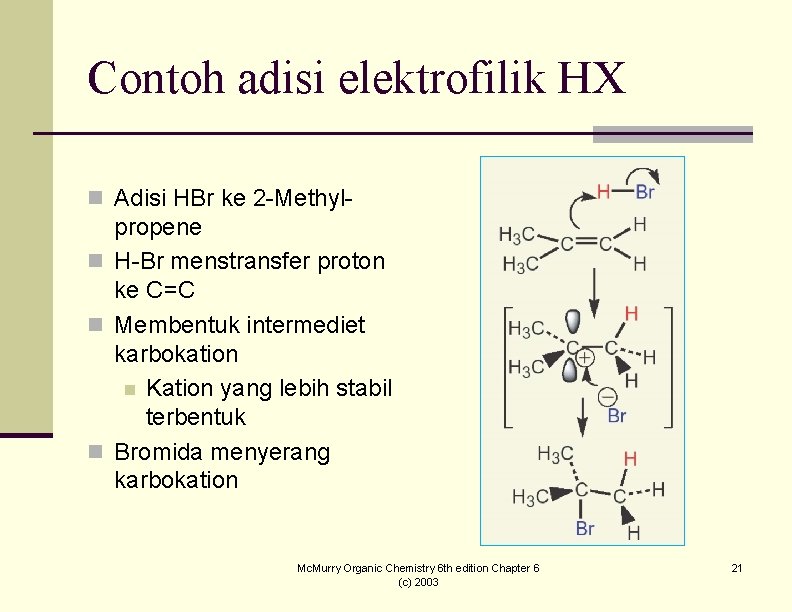
Contoh adisi elektrofilik HX n Adisi HBr ke 2 -Methyl- propene n H-Br menstransfer proton ke C=C n Membentuk intermediet karbokation n Kation yang lebih stabil terbentuk n Bromida menyerang karbokation Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 21
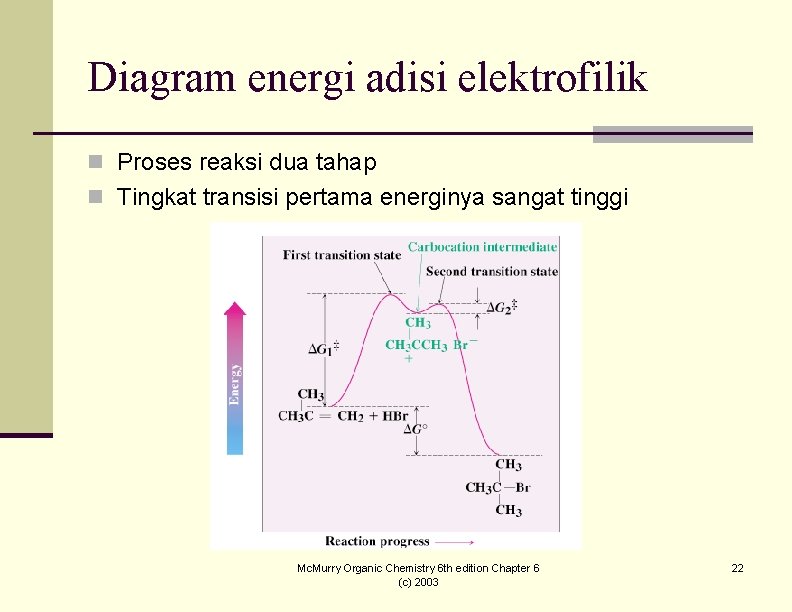
Diagram energi adisi elektrofilik n Proses reaksi dua tahap n Tingkat transisi pertama energinya sangat tinggi Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 22

7. 9 Orientasi adisi elektrofilik: Hukum Markovnikov n Dalam alkena yang tidak simetris, HX dapat bereaksi dengan dua cara, tapi satu cara lebih disukai dari pada yang lain (regiospesifik) n Hukum Markovnikov: Adisi HX pada alkena yang tidak simetris, H akan terikat pada karbon yang kurang tersubstitusi (mempunyai H lebih banyak) dan X terikat pada karbon yang tersubstitusi alkil lebih banyak (mempunyai H lebih sedikit) Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 23
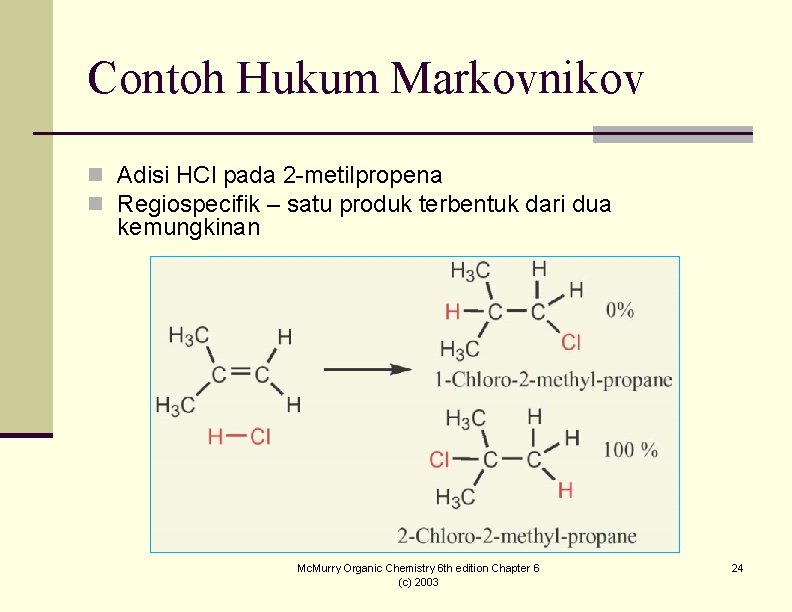
Contoh Hukum Markovnikov n Adisi HCl pada 2 -metilpropena n Regiospecifik – satu produk terbentuk dari dua kemungkinan Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 24
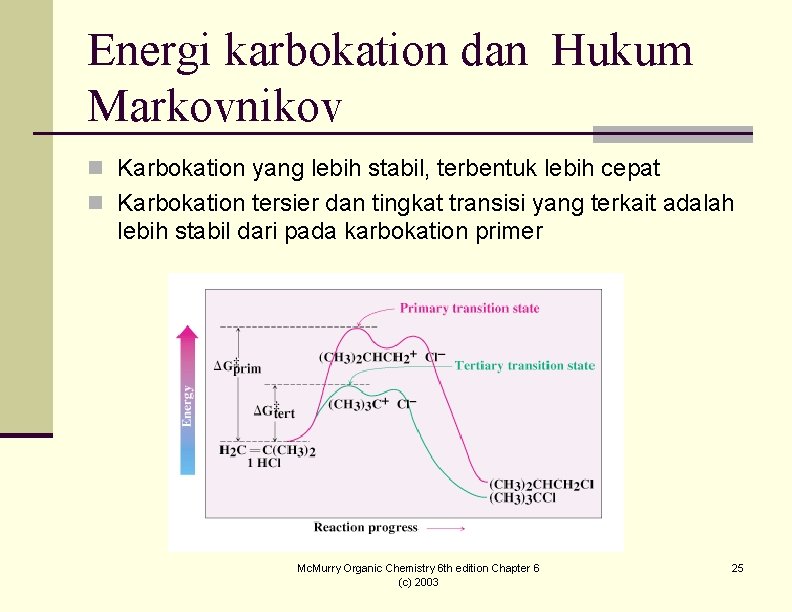
Energi karbokation dan Hukum Markovnikov n Karbokation yang lebih stabil, terbentuk lebih cepat n Karbokation tersier dan tingkat transisi yang terkait adalah lebih stabil dari pada karbokation primer Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 25
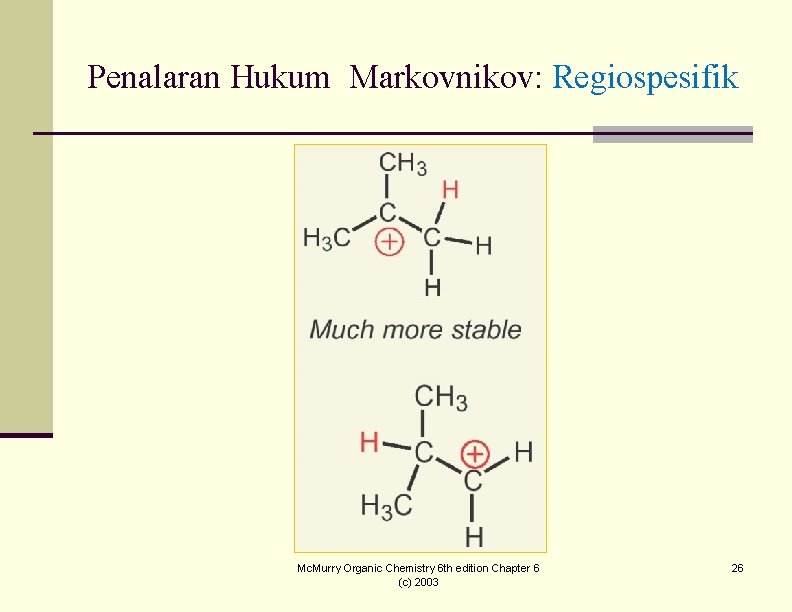
Penalaran Hukum Markovnikov: Regiospesifik Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 26

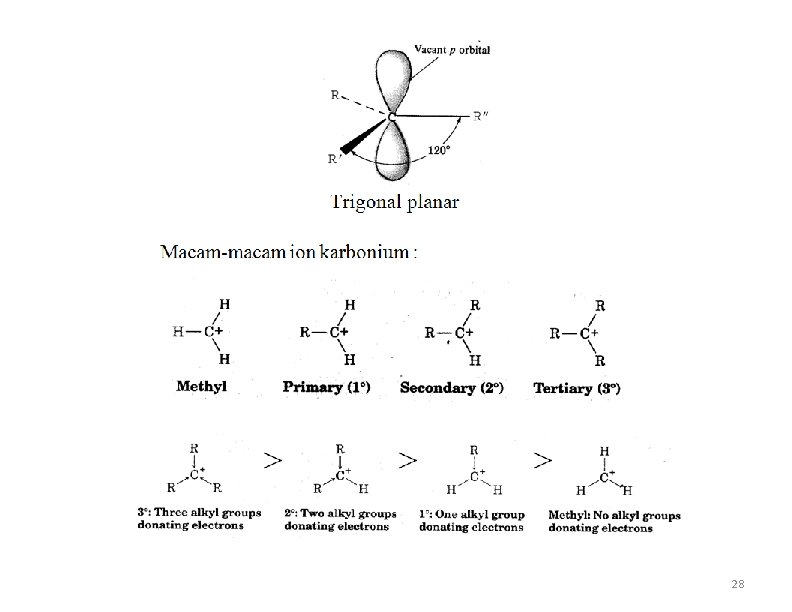
7. 10 Struktur Karbokation dan Stability n Karbokation adalah planar dan karbon trikoordinat dikelilingi oleh 6 elektron dalam orbital sp 2 n Orbital yang keempat dari karbon adalah orbital p yang kosong n Stabilitas dari karbokation tersebut urutannya (dari yang paling stabil) adalah: Karbokation: 3º > 2º > 1º > +CH 3 Mc. Murry Organic Chemistry 6 th edition Chapter 6 (c) 2003 27
28
- Slides: 28