6 ORBITALES MOLCULAIRES DES MOLCULES POLYATOMIQUES HYBRIDATION DES

6 ) ORBITALES MOLÉCULAIRES DES MOLÉCULES POLYATOMIQUES. HYBRIDATION DES ORBITALES ATOMIQUES. 6. 1 ) Introduction Soit Be. H 2 Représentation de Lewis Be [He] 2 s 2 H 1 s 1 H Be H Géométrie ; AX 2 E 0 d ’où molécule linéaire Question : peut-on expliquer l ’orientation des liaisons Be-H dans le cadre de la théorie des O. M. ?
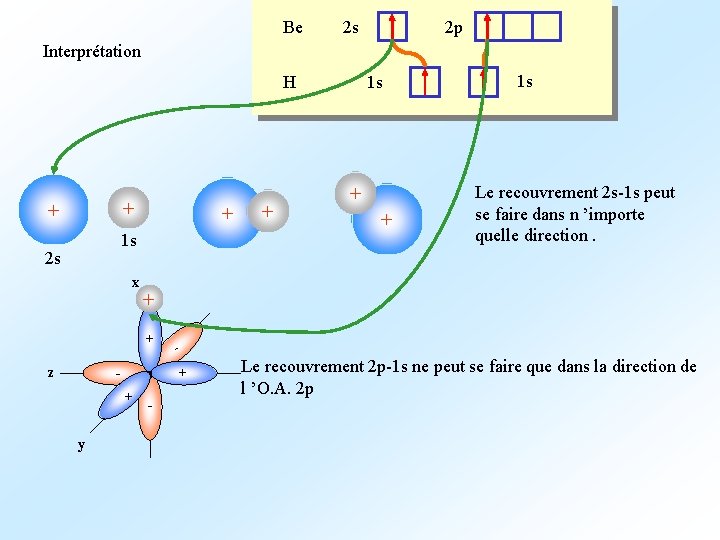
Be 2 s 2 p Interprétation H + + + 1 s 2 s x y + Le recouvrement 2 s-1 s peut se faire dans n ’importe quelle direction. - + + + 1 s + + z + 1 s - Le recouvrement 2 p-1 s ne peut se faire que dans la direction de l ’O. A. 2 p
![Exemple de BH 3 B [He] 2 s 2 2 p 1 2 s Exemple de BH 3 B [He] 2 s 2 2 p 1 2 s](http://slidetodoc.com/presentation_image_h/844dcfd26a27e112ac017c457569799d/image-3.jpg)
Exemple de BH 3 B [He] 2 s 2 2 p 1 2 s H 1 s 2 p 1 s H B 1 s H H Géométrie ; A X 3 E 0 d ’où molécule plane avec des angles H-B-H de 120° + + 1 s 2 s x + + z - + + y Le recouvrement 2 s-1 s peut se faire dans n ’importe quelle direction. - + Le recouvrement 1 s-2 p ne peut se faire que dans la direction de l ’orbitale 2 p.
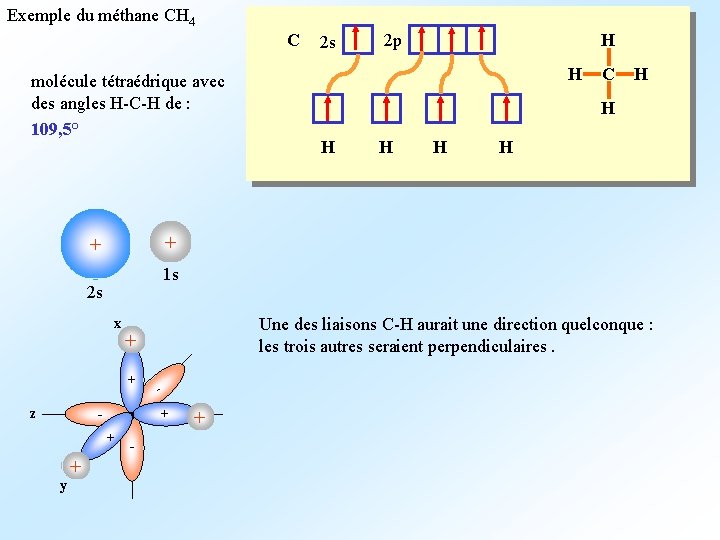
Exemple du méthane CH 4 C molécule tétraédrique avec des angles H-C-H de : 109, 5° x C H H H Une des liaisons C-H aurait une direction quelconque : les trois autres seraient perpendiculaires. + + - + + y H 1 s 2 s + H 2 p + + z 2 s - +
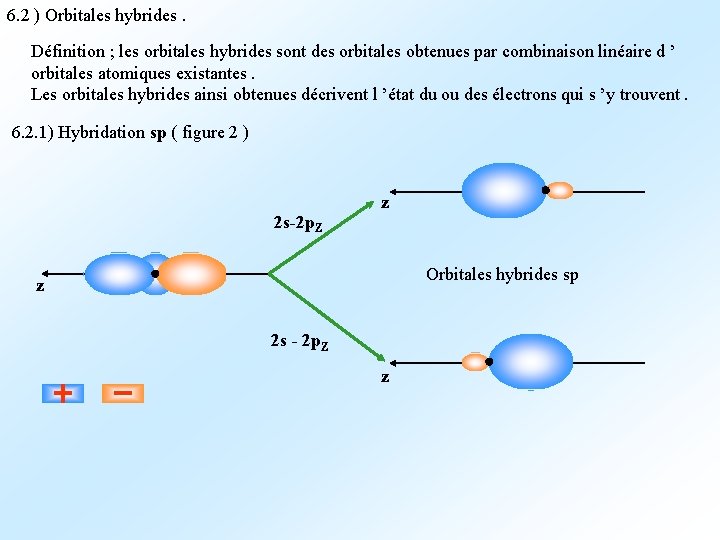
6. 2 ) Orbitales hybrides. Définition ; les orbitales hybrides sont des orbitales obtenues par combinaison linéaire d ’ orbitales atomiques existantes. Les orbitales hybrides ainsi obtenues décrivent l ’état du ou des électrons qui s ’y trouvent. 6. 2. 1) Hybridation sp ( figure 2 ) 2 s-2 p. Z z Orbitales hybrides sp z 2 s - 2 p. Z z
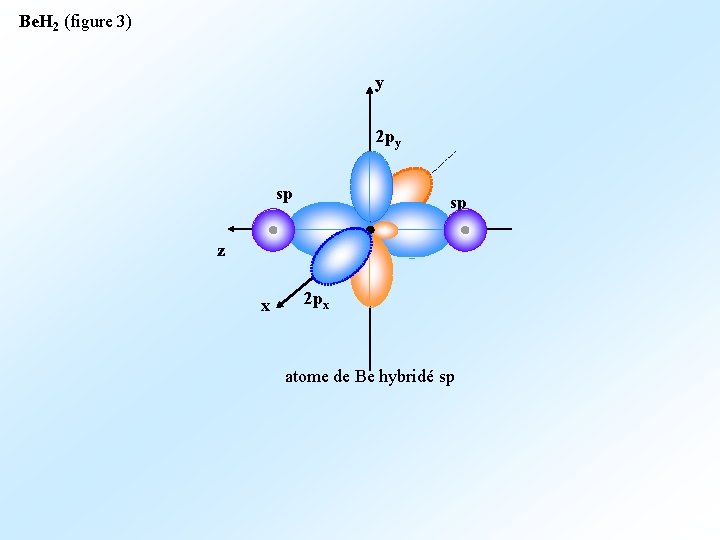
Be. H 2 (figure 3) y 2 py sp sp z x 2 px atome de Be hybridé sp
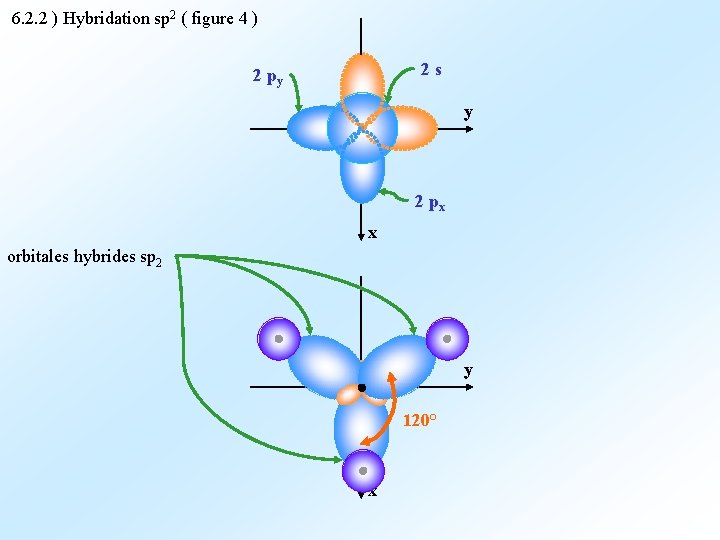
6. 2. 2 ) Hybridation sp 2 ( figure 4 ) 2 s 2 py y 2 px x orbitales hybrides sp 2 y 120° x
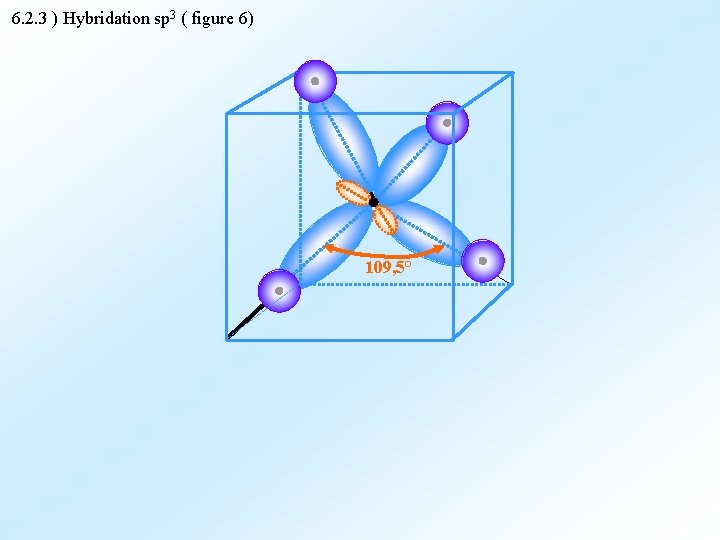
6. 2. 3 ) Hybridation sp 3 ( figure 6) 109, 5°
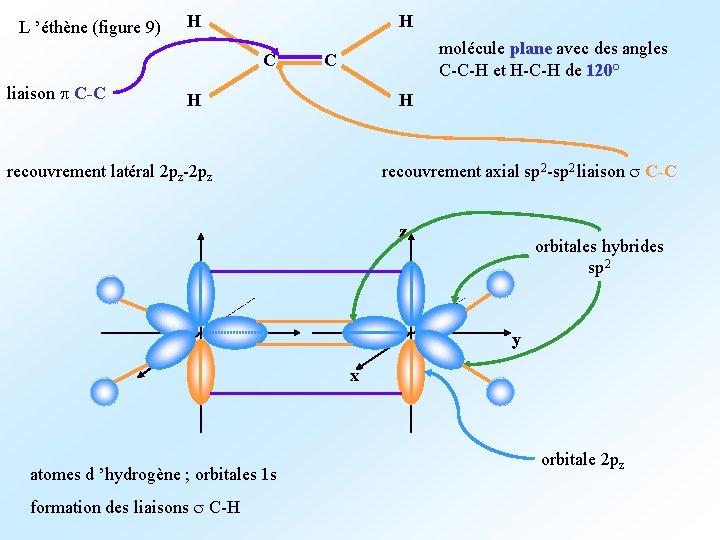
L ’éthène (figure 9) H H C liaison p C-C molécule plane avec des angles C-C-H et H-C-H de 120° C H H recouvrement latéral 2 pz-2 pz recouvrement axial sp 2 -sp 2 liaison s C-C z orbitales hybrides sp 2 y x atomes d ’hydrogène ; orbitales 1 s formation des liaisons s C-H orbitale 2 pz
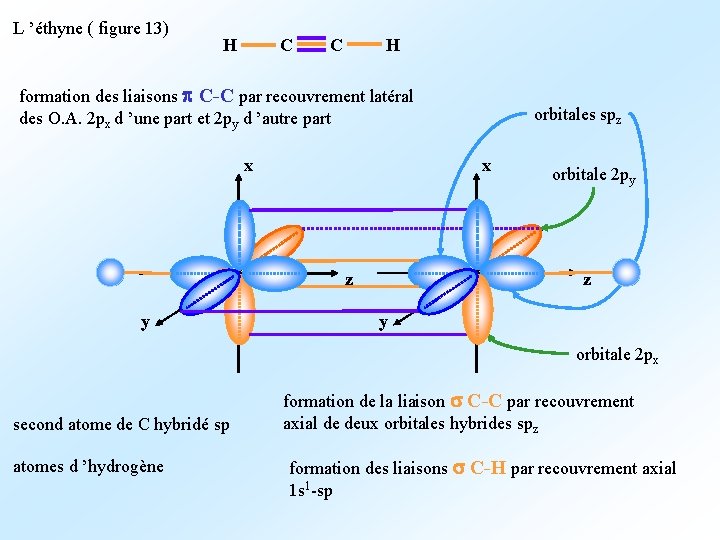
L ’éthyne ( figure 13) C H formation des liaisons p C-C par recouvrement latéral des O. A. 2 px d ’une part et 2 py d ’autre part x x orbitale 2 py z z y orbitales spz y orbitale 2 px second atome de C hybridé sp atomes d ’hydrogène formation de la liaison s C-C par recouvrement axial de deux orbitales hybrides spz formation des liaisons s C-H par recouvrement axial 1 s 1 -sp
- Slides: 10