6 Korrzi Elektrokmia kinetika rta Rauscher dm Bemutat

6 Korrózió Elektrokémia kinetika Írta: Rauscher Ádám Bemutató: Kutsán György
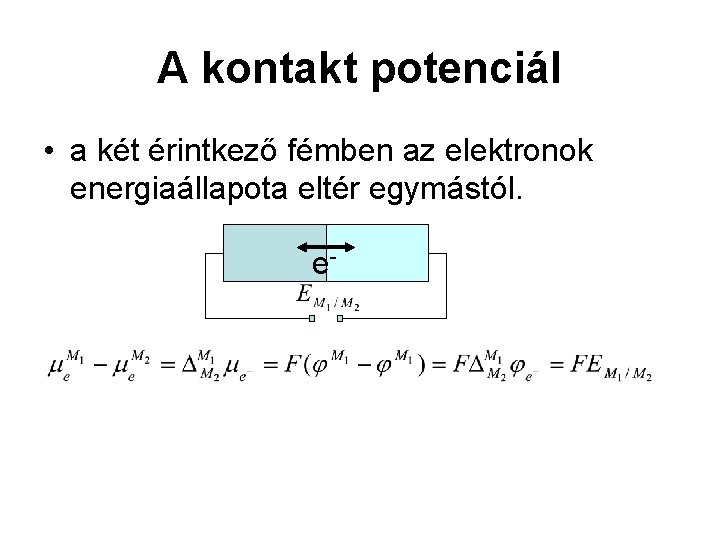
A kontakt potenciál • a két érintkező fémben az elektronok energiaállapota eltér egymástól. e-
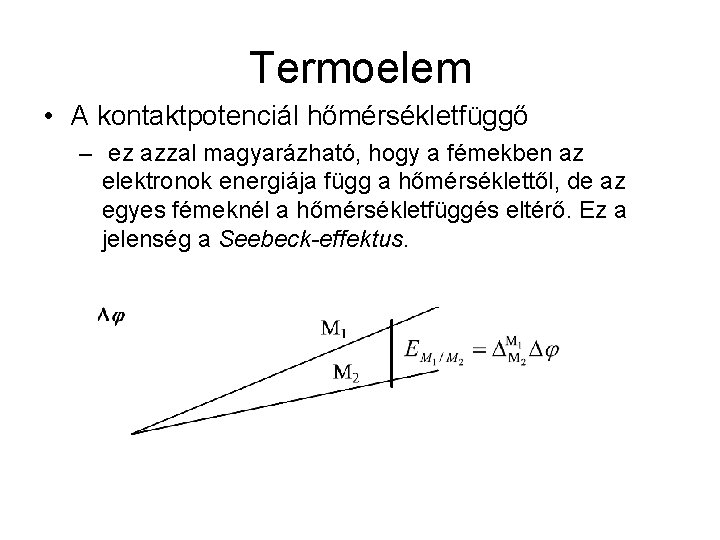
Termoelem • A kontaktpotenciál hőmérsékletfüggő – ez azzal magyarázható, hogy a fémekben az elektronok energiája függ a hőmérséklettől, de az egyes fémeknél a hőmérsékletfüggés eltérő. Ez a jelenség a Seebeck-effektus.
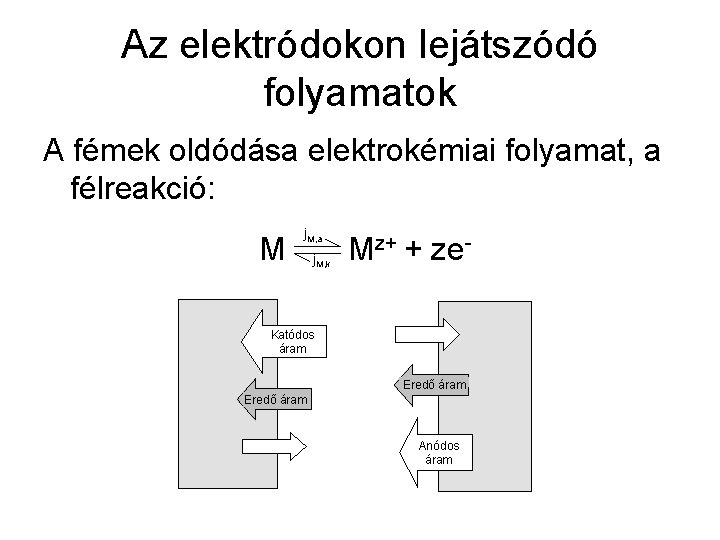
Az elektródokon lejátszódó folyamatok A fémek oldódása elektrokémiai folyamat, a félreakció: M j. M, a j. M, k Mz+ + ze- Katódos áram Eredő áram Anódos áram
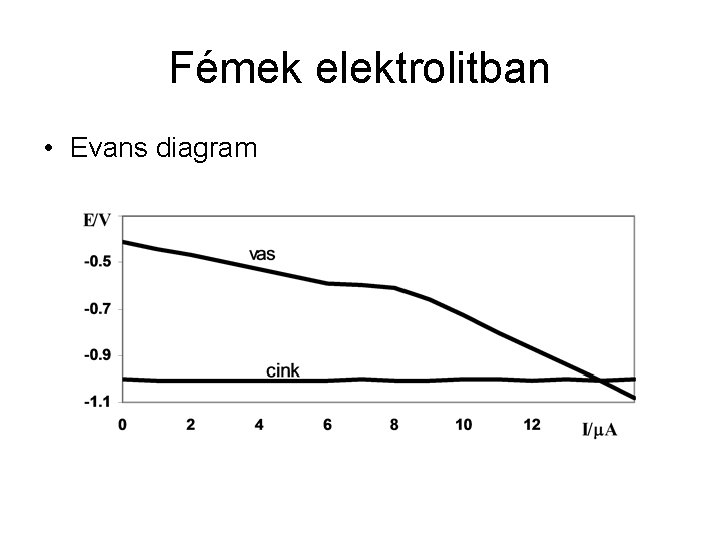
Fémek elektrolitban • Evans diagram

Cella • A cella két elektródja között potenciálkülönbség mérhető: ez a fázisok között fennálló potenciálkülönbségek eredője. • A fázisok belsejében a potenciál gyakorlatilag állandó • A változás a határrétegben történik. Itt nagy az elektromos térerősség, ami erősen befolyásolja a töltéssel rendelkező reakciópartnerek (ionok vagy elektronok) kémiai reakcióit. • A cellapotenciál mérése és szabályozása ezért az elektród kinetika gyakorlatának egyik legfontosabb eleme.

Munkaelektród • Az elektrokémiai cella két félcellából áll: ezekben egymástól független kémiai reakciók zajlanak. • Mindkét reakciót befolyásolják a megfelelő elektródon fennálló potenciálviszonyok, ezeket azonban külön-külön nem tudjuk szabályozni. • A reakciók egyikét vizsgáljuk: ez lesz a munka - vagy indikátorelektródon. • A másik elektródot "szabványosítjuk" : ez a referenciaelektród.

Elektrolízis • A Faraday-áram és az elektrolízis sebessége közötti egyenes arányosság van: • Az elektródpotenciál (vagy a cellapotenciál) eltérését az egyensúlyi (nernsti, vagy stacionárius) értéktől polarizációnak nevezzük • A polarizáció mértékét túlfeszültségnek nevezzük, és h-val jelöljük: h=E-Eeq

Tafel egyenlet: • Ahol: – h: túlfeszültség, – a, b: konstansok – i: áram

Túlfeszültség • Polarizáció • Reverzibilis potenciál - leválási potenciál • A túlfeszültség kialakulásának oka: – polarizációs, – diffúziós

Elektródfolyamat • Heterogén reakció, lépései: 1. 2. 3. 4. 5. 6. 7. Hidratált ionok elektródfelülethez jutása Adszorpciója a felületen Dehidratáció Elektronátlépés, elektrokémiai reakció Termék adszorpció, vagy kristályrácsba épülés Szekunder termékek kialakulása Deszorpció
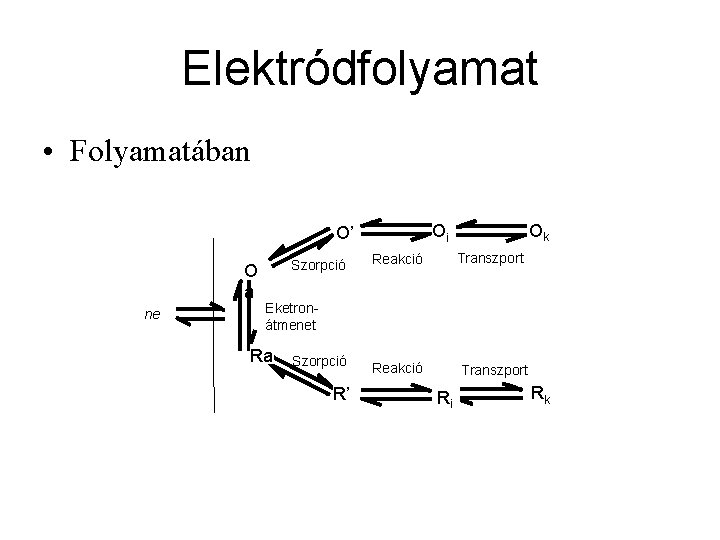
Elektródfolyamat • Folyamatában O a ne Szorpció Ok Oi O’ Transzport Reakció Eketronátmenet Ra Szorpció R’ Reakció Transzport Ri Rk

Elektródfolyamat sebessége • Az egységnyi elektródfelületen időegység alatt képződött, vagy semlegesített anyag: • v=j/z. F – v: mol/(s cm 2) – j: A/cm 2 [C/sec/cm 2] – F: C/mol – z: átlépő elektronok száma

Reakciókinetika • A Faraday áram: (a fizikából ismert) • A felület elektródreakció sebessége

Csereáram • Reverzibilis elektródon, egyensúlyban: │ik│=│ia│= i 0 • Ahol: b : átlépési faktor: 0<b<1 z: töltés j: túlfeszültség
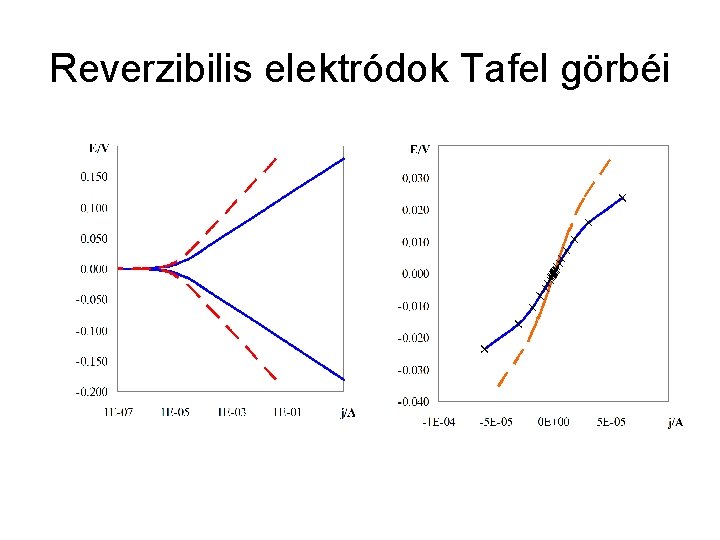
Reverzibilis elektródok Tafel görbéi
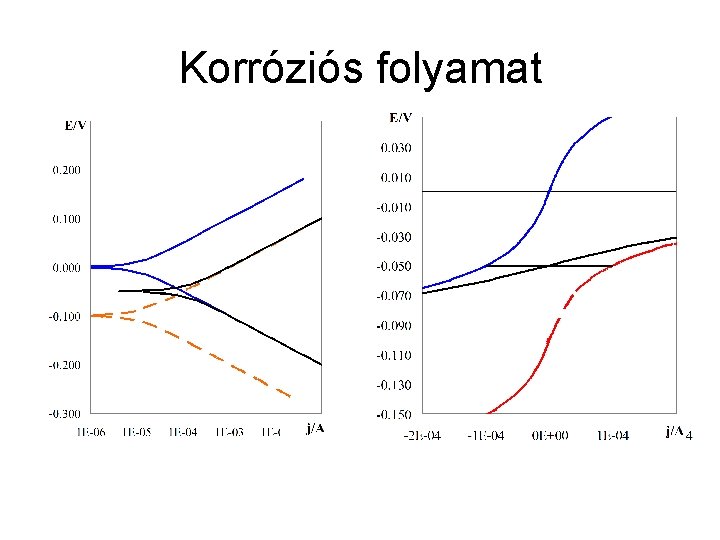
Korróziós folyamat
- Slides: 17