6 Equilibrios cidobase I Qumica 1 S Grado

6. Equilibrios ácido-base I Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I

Contenidos Equilibrios ácido-base I • • Ácidos y bases Producto iónico del agua. Disoluciones neutras, ácidas y básicas. Concepto de p. H. Ácidos y bases fuertes y débiles: Ka y Kb. Grado de ionización. Ácidos polipróticos. Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 2

Bibliografía recomendada • Petrucci: Química General, 8ª edición. R. H. Petrucci, W. S. Harwood, F. G. Herring, (Prentice Hall, Madrid, 2003). – Secciones 17. 1, 17. 2, 17. 3, 17. 4, 17. 5, 17. 6, 17. 9 Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 3

Ácidos y bases Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I

Ácidos y bases • Teoría de Arrhenius: (punto de partida, superada) – Ácido: sustancia que produce protones (H+) en agua – Base o álcali: sustancia que produce iones hidroxilo (OH-) en agua – ¿Por qué es alcalino el amoniaco, NH 3? • “Porque en disolución acuosa forma NH 4 OH, que cede OH-. ” • ¡Pero nunca se ha detectado la especie química NH 4 OH en agua! • Necesitamos otra teoría [Lectura: Petrucci 17. 1] Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 5
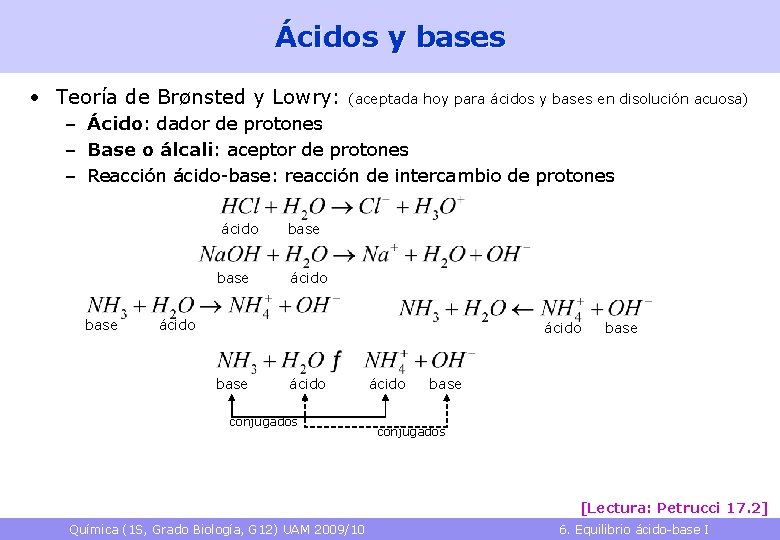
Ácidos y bases • Teoría de Brønsted y Lowry: (aceptada hoy para ácidos y bases en disolución acuosa) – Ácido: dador de protones – Base o álcali: aceptor de protones – Reacción ácido-base: reacción de intercambio de protones ácido base ácido base ácido conjugados ácido base conjugados [Lectura: Petrucci 17. 2] Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 6
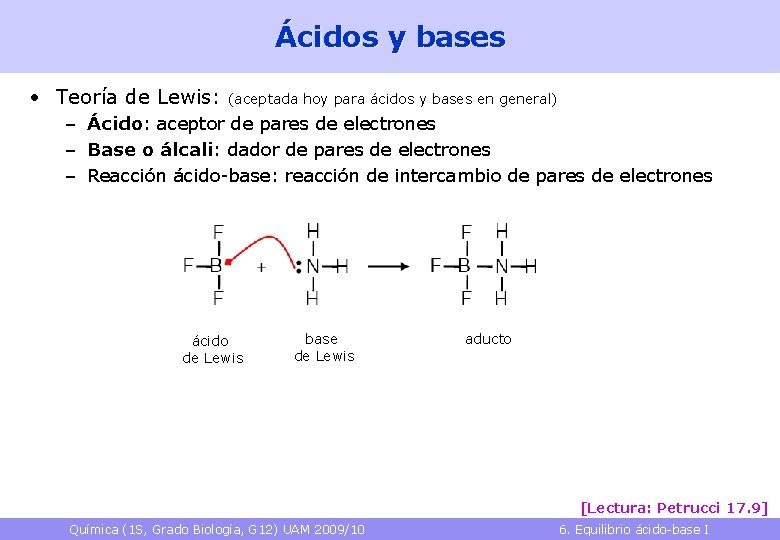
Ácidos y bases • Teoría de Lewis: (aceptada hoy para ácidos y bases en general) – Ácido: aceptor de pares de electrones – Base o álcali: dador de pares de electrones – Reacción ácido-base: reacción de intercambio de pares de electrones ácido de Lewis base de Lewis aducto [Lectura: Petrucci 17. 9] Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 7

Ácidos y bases en disolución Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I

Equilibrio de autoionización. Producto iónico del agua base débil ácido fuerte base fuerte Anfótero: sustancia que puede actuar como ácido y como base (Aunque no escribimos el subíndice eq, nos referirnos a concentraciones de equilibrio de aquí en adelante) Agua pura: a 25ºC: a 60ºC: Dsln. ácida Dsln. neutra Dsln. básica o alcalina [Lectura: Petrucci 17. 3] Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 9

p. H, p. OH y p. K Las concentraciones molares de H 3 O+ y de OH- en disolución suelen ser mucho menores que 1 M; p. ej: Def. : [Lectura: Petrucci 17. 3] Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 10
![Basicidad Acidez p. H, p. OH y p. K [Lectura: Petrucci 17. 3] Química Basicidad Acidez p. H, p. OH y p. K [Lectura: Petrucci 17. 3] Química](http://slidetodoc.com/presentation_image_h/1413abfc7d97d4e247930e91611e0bf3/image-11.jpg)
Basicidad Acidez p. H, p. OH y p. K [Lectura: Petrucci 17. 3] Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 11

p. H y p. OH Una muestra de agua de lluvia tiene p. H=4, 35. ¿Cuánto vale [H 3 O+]? Una muestra de un amoniaco de uso doméstico tiene p. H=11, 28. ¿Cuánto vale [OH-]? Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 12

Ácidos y bases fuertes Tienen el equilibrio de ionización muy desplazado a la derecha - puede considerarse totalmente desplazado, salvo en disoluciones muy concentradas - el aporte de la autoionización del agua a la concentración de H 3 O+ en las disoluciones de ácidos fuertes y de OH- en las de bases fuertes es despreciable Ácidos fuertes más frecuentes Bases fuertes más frecuentes (sólo la 1ª ionización) [Lectura: Petrucci 17. 4] Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 13

Ácidos y bases fuertes Ejemplo: Disolución HCl(ac) 0, 015 M. ¿Cuánto valen las concentraciones molares de las especies presentes en la disolución y el p. H? 1 • los Cl- proceden de la ionización del ácido 2 ~ todo el H 3 O+ procede de la ionización del ácido 3 3 • [H 3 O+] y [OH-] deben ser consistentes con Kw • los OH- proceden de la ionización del agua 4 [Lectura: Petrucci 17. 4] Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 14

Ácidos y bases fuertes Ejemplo: Disolución saturada de Ca(OH)2(ac). ¿Cuánto valen las concentraciones molares de las especies presentes en la disolución y el p. H? [Ca(OH)2: solubilidad a 25ºC 0, 16 g/100 ml. ] 1 • los Ca 2+ proceden de la ionización de la base disuelta 3 2 1 • la concentración de base disuelta e ionizada es su solubilidad molar • los H 3 O+ proceden de la ionización del agua ~ todo el OH-procede de la ionización del la base disuelta 3 • [H 3 O+] y [OH-] deben ser consistentes con Kw 4 [Lectura: Petrucci 17. 4] Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 15

Ácidos y bases débiles Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I

Ácidos y bases débiles Es necesario considerar su equilibrio de ionización Constante de ionización o de acidez del ácido HA - ácidos más fuertes cuanto mayor Ka (cuanto menor p. Ka) Constante de ionización o de basicidad de la base B - bases más fuertes cuanto mayor Kb (cuanto menor p. Kb) [Lectura: Petrucci 17. 5] Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 17

Ácidos débiles Fuerza del ácido Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 18

Fuerza de la base Bases débiles Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 19

Ácidos débiles Disolución HA(ac) c 0 M. ¿Concentraciones molares de las especies presentes en la disolución? 1 • el HA se ioniza parcialmente; ¿es Ka suficientemente pequeña para que c 0 -x=c 0? 2 • los A- proceden de la ionización del ácido ~ todo el H 3 O+ procede de la ionización del ácido (Kw<<Ka) • los OH- proceden de la ionización del agua 1 NO SI 2 [Lectura: Petrucci 17. 5] Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 20

Si que equivale a aproximar La aproximación se hace para calcular Para calcular la concentración de equilibrio de HA se puede usar Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 21

Bases débiles Disolución B(ac) c 0 M. ¿Concentraciones molares de las especies presentes en la disolución? 1 • la B se ioniza parcialmente; ¿es Kb suficientemente pequeña para que c 0 -x=c 0? • los HB+ proceden de la ionización de la base 2 ~ todo el OH- procede de la ionización de la base (Kw<<Kb) • los H 3 O+ proceden de la ionización del agua 1 NO SI 2 [Lectura: Petrucci 17. 5] Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 22

Ácidos débiles Ejemplo: Disolución HF(ac) 0, 15 M. ¿Cuánto valen las concentraciones molares de las especies presentes en la disolución y el p. H? [HF: Ka=6, 6 x 10 -4] SI [Lectura: Petrucci 17. 5] Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 23

Ácidos débiles Ejemplo: Disolución HF(ac) 0, 00150 M. ¿Cuánto valen las concentraciones molares de las especies presentes en la disolución y el p. H? [HF: Ka=6, 6 x 10 -4] NO [Lectura: Petrucci 17. 5] Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 24

Ácidos débiles Ejemplo: El p. H de una disolución HF(ac) 0, 0015 M es 3, 14. ¿Cuánto vale la constante de ionización del HF? Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 25

Bases débiles Ejemplo: Disolución piridina(ac) 0, 0015 M. ¿Concentraciones molares de las especies presentes en la disolución y p. H? [Piridina: Kb=1, 5 x 10 -9] SI Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 26

Bases débiles Ejemplo: El p. H de una disolución de piridina(ac) 0, 0015 M es 8, 18 ¿Cuánto vale la constante de ionización de la piridina? no es necesario considerar si se desprecia frente a c 0 o no Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 27
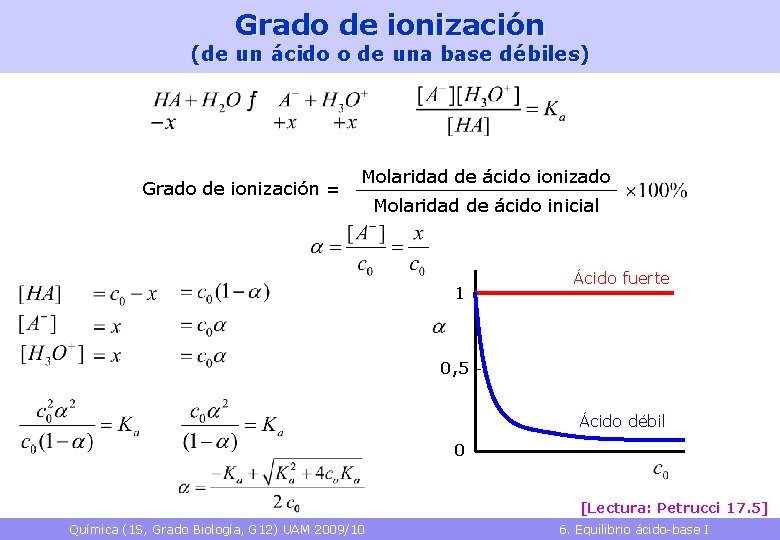
Grado de ionización (de un ácido o de una base débiles) Grado de ionización = Molaridad de ácido ionizado Molaridad de ácido inicial 1 Ácido fuerte 0, 5 Ácido débil 0 [Lectura: Petrucci 17. 5] Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 28
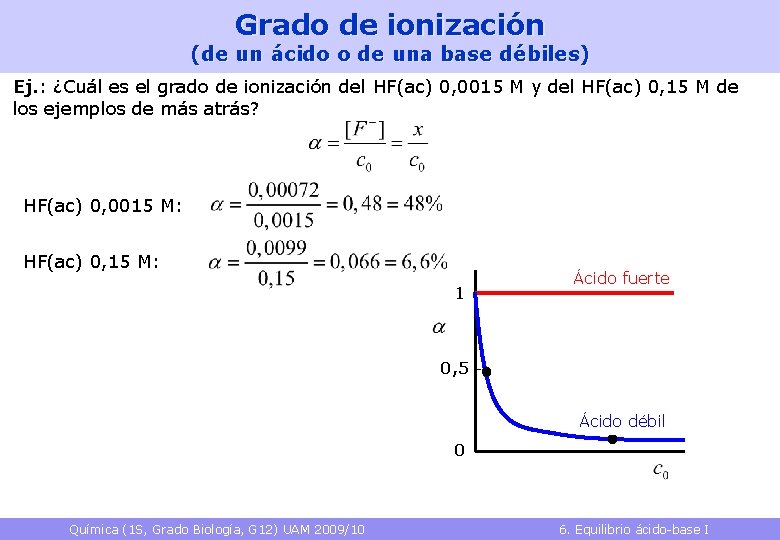
Grado de ionización (de un ácido o de una base débiles) Ej. : ¿Cuál es el grado de ionización del HF(ac) 0, 0015 M y del HF(ac) 0, 15 M de los ejemplos de más atrás? HF(ac) 0, 0015 M: HF(ac) 0, 15 M: 1 Ácido fuerte 0, 5 Ácido débil 0 Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 29

Ácidos polipróticos Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I

Ácidos polipróticos Ejemplo: H 3 PO 4, con Ka 1 >> Ka 2 >> Ka 3 1 2 3 4 [Lectura: Petrucci 17. 6] Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 31

Ácidos polipróticos Ejemplo: Disolución H 3 PO 4(ac) 3. 00 M. ¿Cuánto valen las concentraciones molares de las especies presentes en la disolución y el p. H? 1 SI 2 3 4 1 2 3 4 [Lectura: Petrucci 17. 6] Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 32

Ácidos polipróticos: El ácido sulfúrico H 2 SO 4 1ª ionización: ácido fuerte; 2ª ionización: ácido débil Ejemplo: Disolución H 2 SO 4(ac) 0, 50 M. ¿Concentraciones molares de las especies presentes en la disolución y p. H? [Ka 2=1, 1 x 10 -2] [Lectura: Petrucci 17. 6] Química (1 S, Grado Biología, G 12) UAM 2009/10 6. Equilibrio ácido-base I 33
- Slides: 33