6 DOSAGES ACIDOBASIQUES 6 1 Dosage d un

6 ) DOSAGES ACIDO-BASIQUES 6. 1) Dosage d ’un acide ou d ’une base 6. 1. 1) Définition Doser une solution d ’un acide ( ou d ’une base) consiste à déterminer la concentration apportée d ’acide ou de base dans cette solution. 6. 1. 2) Équivalence acido-basique Soit le dosage d ’un monoacide AH par une solution d ’hydroxyde de sodium , l ’équation de la réaction de dosage s ’écrit : AH + OH- = A- + H 2 O K 0 = A l ’équivalence, la quantité d ’ions hydroxyde introduite est égale à al quantité totale de protons libérés ou libérables par l ’acide : néq(OH-) = n 0(AH)

6. 2) Dosage acide fort base forte. 6. 2. 1) Présentation. bécher : acide chlorhydrique : CA = 0, 100 mol. L-1 ; VA = 10, 0 m. L. burette : hydroxyde de sodium : CB = 0, 100 mol. L-1 ; VB = 15, 0 m. L. Question 1 : écrire l ’équation de la réaction de dosage ; exprimer puis calculer sa constante d ’équilibre. H 3 O+ + OH- = 2 H 2 O K 0 = Question 2 : calculer le volume équivalent Veq. à l ’équivalence : néq(OH-) = n 0(H 3 O+) CB Véq = CA VA d ’où Véq = 10, 0 m. L 1, 0 1014
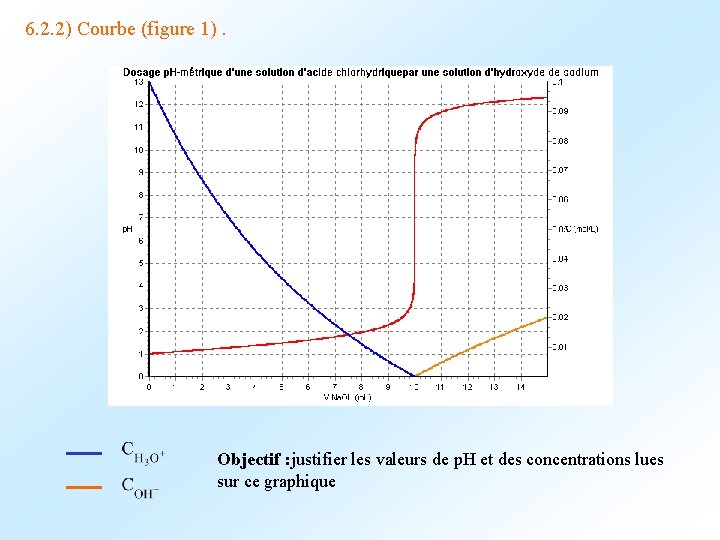
6. 2. 2) Courbe (figure 1). Objectif : justifier les valeurs de p. H et des concentrations lues sur ce graphique

Exemple : pour VNa. OH = 5, 0 m. L, on relève p. H= 1, 5 = 3, 02 10 -13 mol. L-1 = 3, 30 10 -2 mol. L-1 calcul Méthode : celà revient à calculer le p. H ( et la composition ) de la solution résultant d ’un mélange ( ici 10, 0 m. L d ’acide chlorhydrique et 5, 0 m. L d ’hydroxyde de sodium). Calculer les concentrations apportées en tenant compte de la dilution du mélange. On a une réaction prépondérante qui est comme la réaction de dosage : elle peut-être considérée quantitative On écrit son bilan de matière On détermine le p. H et la composition du nouveau système obtenu.

Calcul des concentrations apportées : acide chlorhydrique: CA ’ = 6, 67 10 -2 mol. L-1 hydroxyde de sodium: CB ’ = 3, 33 10 -2 mol. L-1 Réaction prépondérante : H 3 O+ E. I. E. F. (mol. L-1) + OH- = 2 H 2 O CA ’ K 0 = 1, 0 1014 CB ’ Remarque CA ’- CB ’ = e 3, 34 10 -2 mol. L-1 Calcul : énoncé Le système obtenu à l ’issue de la R. P. est stable. p. H = -log([H 3 O+]) = 1, 5 [OH-] = 2, 99 10 -13 mol. L-1

Application : pour VNa. OH = 12, 0 m. L, on relève p. H= 12, 0 = 9, 08 10 -3 mol. L-1 Justifier ces valeurs = 1, 10 10 -12 mol. L-1

6. 3) Dosage acide faiblet base faible. 6. 3. 1) Présentation. bécher : acide éthanoïque : CA = 0, 100 mol. L-1 ; VA = 10, 0 m. L. burette : hydroxyde de sodium : CB = 0, 100 mol. L-1 ; VB = 15, 0 m. L. Question 1 : écrire l ’équation de la réaction de dosage ; exprimer puis calculer sa constante d ’équilibre. p. KA = 4, 8 AH + OH- = A- + H 2 O K 0 = Question 2 : calculer le volume équivalent Veq. à l ’équivalence : néq(OH-) = n 0(AH) CB Véq = CA VA d ’où Véq = 10, 0 m. L 1, 6 109
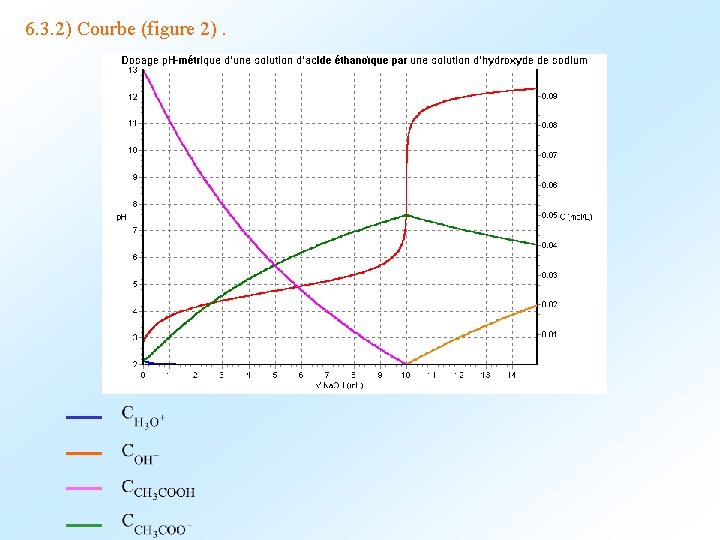
6. 3. 2) Courbe (figure 2).

Question : pour VNa. OH = 4, 0 m. L, on relève : p. H = 4, 6 CAH = 4, 30 10 -2 mol. L-1 et CA- = 2, 85 10 -2 mol. L-1. Justifier ces valeurs. Ecrire le bilan de matière de la réaction de dosage en exprimant les quantités de matière. Bilan de matière de la réaction prépondérante AH E. I. E. F. (mol) + OH- = A- + H 2 O CA VA- CB VB type de la solution obtenue ? [AH] = [A-] = CB VB e Vt K 0 = 1, 6 109 CB VB C ’est un mélange de l ’acide faible AH et de sa base conjuguée A- , avec : 4, 29 10 -2 mol. L-1 2, 86 10 -2 mol. L-1 et

Réaction prépondérante ? Hypothèse ? AH + A- = A- + AH avec K 0 = rappel Les réactions secondaires et en particulier , la réaction de l ’acide avec l ’eau AH + H 2 O = A- + H 3 O+ sont négligeables. Hypothèse valide car p. H ? 1 p. H = or CA VA = CB Véq d ’où p. H = formule d ’Henderson A. N. : p. H = 4, 6
![Application : VB(m. L) p. H [AH] (mol. L-1) [A-] (mol. L-1) 5, 0 Application : VB(m. L) p. H [AH] (mol. L-1) [A-] (mol. L-1) 5, 0](http://slidetodoc.com/presentation_image_h/9cce4cc3ae7188debdd2b82be89ac867/image-11.jpg)
Application : VB(m. L) p. H [AH] (mol. L-1) [A-] (mol. L-1) 5, 0 4, 8 3, 33 10 -2 10, 0 8, 75 e 5, 00 10 -2 12, 0 e 4, 54 10 -2 Justifier ces valeurs

Recherche R. P. : On a une solution de l ’acide faible CH 3 COOH et de sa base faible conjuguée CH 3 COO- , solution tampon p. Ka OH- CH 3 COOForce des bases H 2 O 14, 0 H 2 O R. P. ? CH 3 COOH + CH 3 COO- = CH 3 COO- + CH 3 COOH Force des de constante K 10 = 1 acides réactions secondaires ? CH 3 COOH 2 acide avec l ’eau : CH 3 COOH + H 2 O = CH 3 COO- + H 3 O+ 4, 8 0 3 base avec l ’eau : CH 3 COO- + H 2 O = CH 3 COOH + OH- H 3 O+ 4 autoprotolyse de l ’eau : parmi ces trois réactions , laquelle doit éventuellement être prise en compte ? 2 car Calcul du p. H : conséquence ? formule ? 1, 58 10 -5 hypothèse ? 6, 31 10 -10 les réactions secondaires et surtout R 2 sont négligeables la composition du système n ’est pas modifiée ou les concentrations de l ’acide et de la base restent inchangées. retour calcul

Bilan de matière écrit en concentration H 3 O+ E. I. E. F. (mol. L-1) Retour calcul + OH- = 2 H 2 O CA ’ CB ’ CA ’- CB ’ = e K 0 = 1, 0 1014 3, 34 10 -2 mol. L-1 Le bilan peut aussi être écrit en exprimant les quantités de matières ( moles ) H 3 O+ E. I. E. F. (mol) + OH- = 2 H 2 O CA VA- CB VB = CB VB e Vt 0, 500 mol d ’où [H 3 O+] = 3, 33 10 -2 mol. L-1 K 0 = 1, 0 1014

6. 3) Dosage acide faiblet base faible. 6. 3. 1) Présentation. bécher : acide éthanoïque : CA = 0, 100 mol. L-1 ; VA = 10, 0 m. L. burette : hydroxyde de sodium : CB = 0, 100 mol. L-1 ; VA = 10, 0 m. L. Question 1 : écrire l ’équation de la réaction de dosage ; exprimer puis calculer sa constante d ’équilibre. p. KA = 4, 8 AH + OH- = A- + H 2 O K 0 = Question 2 : calculer le volume équivalent Veq. à l ’équivalence : néq(OH-) = n 0(AH) CB Véq = CA VA d ’où Véq = 10, 0 m. L 1, 6 109
- Slides: 14