6 Curso Evaluacin y Seleccin de Medicamentos Palma





























- Slides: 43

6 Curso Evaluación y Selección de Medicamentos Palma de Mallorca, 6 -8 Mayo 2008 Evaluación de la Equivalencia Terapéutica Dra. Olga Delgado Hospital Universitario Son Dureta odelgado@hsd. es

• Estudios de Equivalencia y Noinferioridad • Niveles de Evidencia de Equivalencia • Programas de Intercambio Terapéutico

• Estudios de Equivalencia y Noinferioridad • Niveles de Evidencia de Equivalencia • Programas de Intercambio Terapéutico

Equivalencia terapéutica La diferencia entre los tratamientos está dentro de un margen preestablecido que se considera clínicamente irrelevante.

de la superioridad a la equivalencia terapéutica Disponible Nada Tratamiento Buen tratamiento Objetivo Eficacia Mejor eficacia/segurida d Igual eficacia y mejor en otros aspectos Comparad or Placebo Otros tratamientos Tratamiento estándar Superiorida d Superioridad Equivalencia/ No-inferioridad Ensayos ¿Cuándo se realizan estudios de equivalencia? • Mayor seguridad • Eficacia difícil superar • Tratamientos alternativos o segundas líneas • Éticamente no es aceptable utilizar placebo

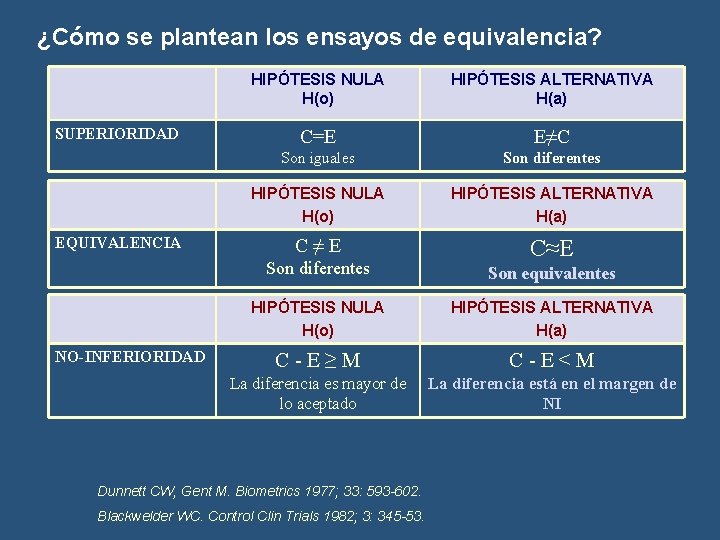
¿Cómo se plantean los ensayos de equivalencia? SUPERIORIDAD EQUIVALENCIA NO-INFERIORIDAD HIPÓTESIS NULA H(o) HIPÓTESIS ALTERNATIVA H(a) C=E E≠C Son iguales Son diferentes HIPÓTESIS NULA H(o) HIPÓTESIS ALTERNATIVA H(a) C ≠ E C≈E Son diferentes Son equivalentes HIPÓTESIS NULA H(o) HIPÓTESIS ALTERNATIVA H(a) C - E ≥ M C - E < M La diferencia es mayor de lo aceptado La diferencia está en el margen de NI Dunnett CW, Gent M. Biometrics 1977; 33: 593 -602. Blackwelder WC. Control Clin Trials 1982; 3: 345 -53.

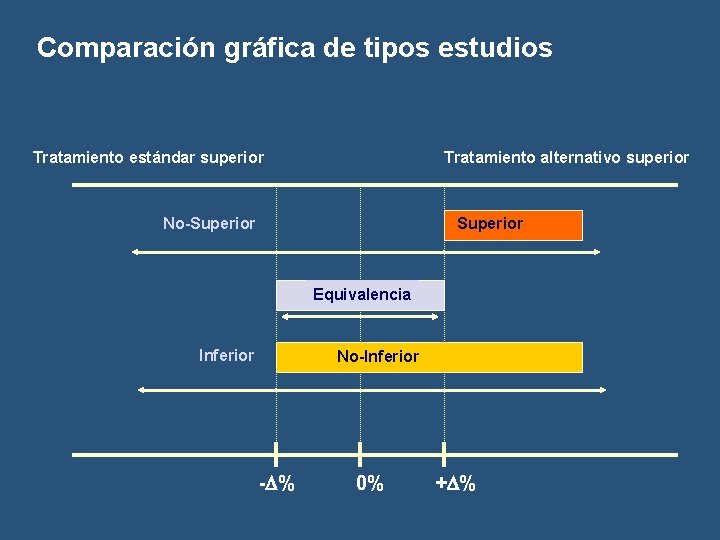
Comparación gráfica de tipos estudios Tratamiento estándar superior Tratamiento alternativo superior No-Superior Equivalencia Inferior No-Inferior - % 0% + %

US Department of Health and Human Services, Food and Drug Administration and Center for Drug Evaluation and Research. Guidance for industry: antiretroviral drugs using plasma HIV RNA measurements -- clinical considerations for accelerated and traditional approval. http: //www. fda. gov/CDER/GUIDANCE/3647 fnl. pdf (accessed May 1, 2008).

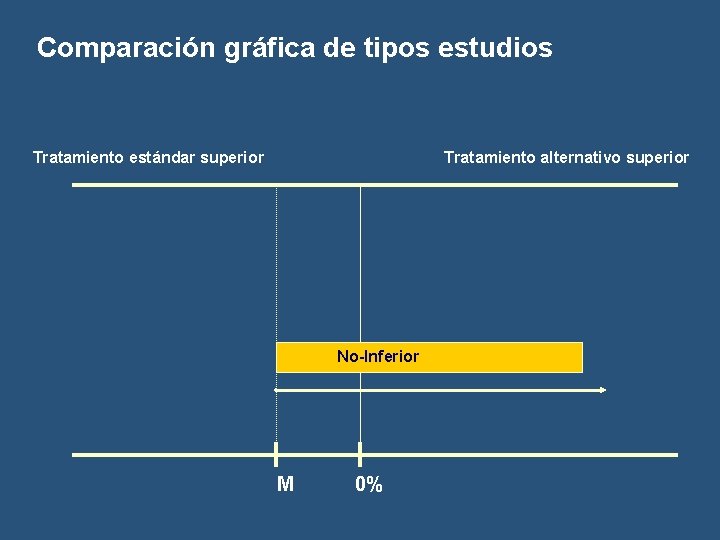
Comparación gráfica de tipos estudios Tratamiento estándar superior Tratamiento alternativo superior No-Inferior M 0%

Estudios para establecer la equivalencia JAMA, July 14, 2004 (292)No. 2

Metodología para el diseño e interpretación de ensayos de equivalencia y no-inferioridad Objetivo Delta IC 95% P Tamaño muestral Análisis Eficacia Aspectos éticos

Objetivo Delta IC 95% P Tamaño muestral Análisis Eficacia Aspectos éticos Heine RJ. Exenatide versus Insulin Glargine in Patient with Suboptimally Controlled Type 2 Diabetes. Ann Intern Med 2005; 143: 559 -569.

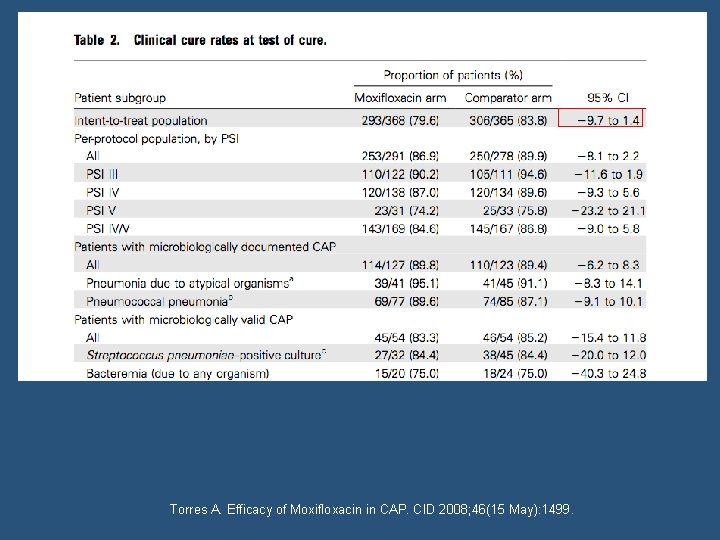
Statistical analysis. This study was powered to support the primary efficacy objective that sequential intravenous and oral moxifloxacin (400 mg once per day) was noninferior to intra- venous ceftriaxone plus sequential intravenous and oral levo- floxacin for treatment of CAP with a PSI of III–V on the basis of clinical success at the test-of-cure assessment for the clinically valid population. Sample size was determined to be 304 clin- ically valid patients in each treatment group on the basis of a predicted failure rate of 15% in the comparator treatment group, an equivalence (clinically relevant) D of 10%, a p (1 -sided), and power of 90% (the power calculation in-0. 025 cluded an adjustment of 10% to account for the multicenter design of the study). Noninferiority of treatment with moxi- floxacin was to be concluded if the lower limit of the 95% CI for cure rate at the test-of-cure visit was greater than 10% and if the upper 95% CI value was 10. The 95% CI was cal- culated using Mantel-Haenszel weights reflecting regions and PSI categorization (class III versus IV/ Torres A. Efficacy of Moxifloxacin in CAP. CID 2008; 46(15 May): 1499.

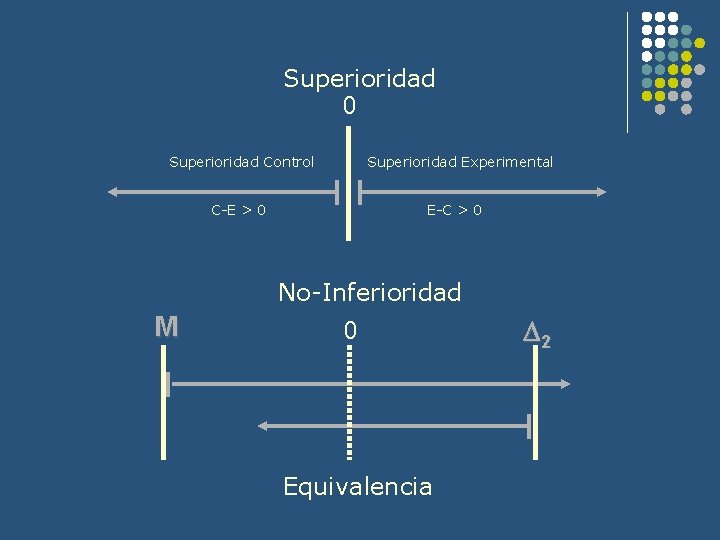
Superioridad 0 Superioridad Control Superioridad Experimental C-E > 0 E-C > 0 No-Inferioridad M 0 Equivalencia 2

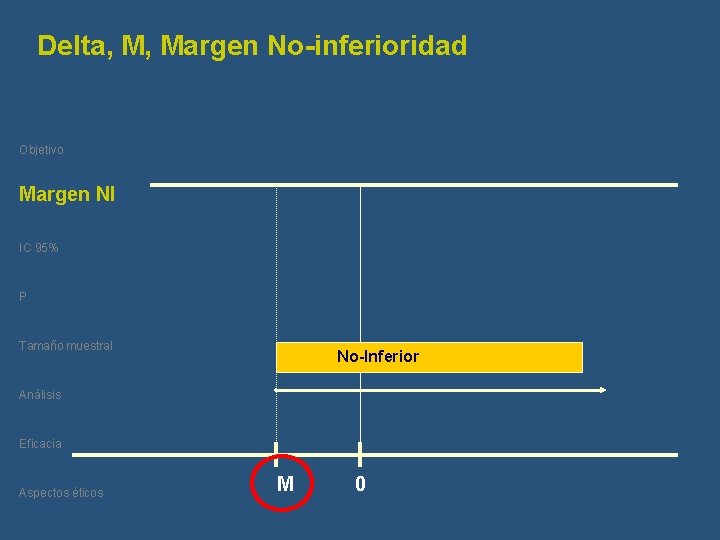
Delta, M, Margen No-inferioridad Objetivo Margen NI Delta IC 95% P Tamaño muestral No-Inferior Análisis Eficacia Aspectos éticos M 0

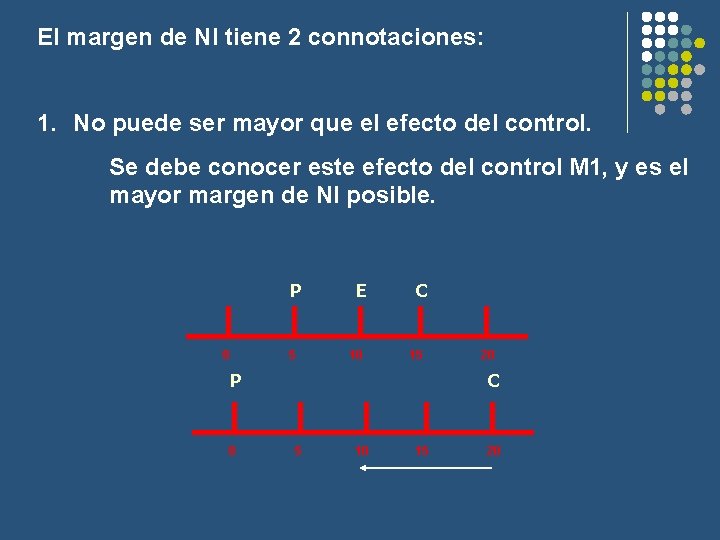
El margen de NI tiene 2 connotaciones: 1. No puede ser mayor que el efecto del control. Se debe conocer este efecto del control M 1, y es el mayor margen de NI posible. P 0 5 E 10 C 15 P 0 20 C 5 10 15 20

Ensayos No Inferioridad (NI) El margen de NI tiene 2 connotaciones: 2. La inferioridad debe ser clínicamente aceptable. 1. 2. Es un tema clínico, no estadístico. La mayor diferencia clínicamente aceptable se denomina M 2, y no puede ser mayor a M 1. Cáncer: Equivalencia 20% supervivencia Control no lo había demostrado frente a no tratamiento Temple, 2008.


Valores utilizados FDA 1992 Comité Asesor Cardio Renal: recomendó la mitad del efecto del tratamiento estándar como margen de no inferioridad para nuevos trombolíticos FDA Oct 2002: Guidance for Industry Antirretrovirales: 10 -12% (RAR) del % pacientes con carga viral indetectable FDA: Antiinfecciosos, delta modulable según la tasa de respuesta

US Department of Health and Human Services, Food and Drug Administration and Center for Drug Evaluation and Research. Guidance for industry: antiretroviral drugs using plasma HIV RNA measurements -- clinical considerations for accelerated and traditional approval. http: //www. fda. gov/CDER/GUIDANCE/3647 fnl. pdf (accessed May 1, 2008).

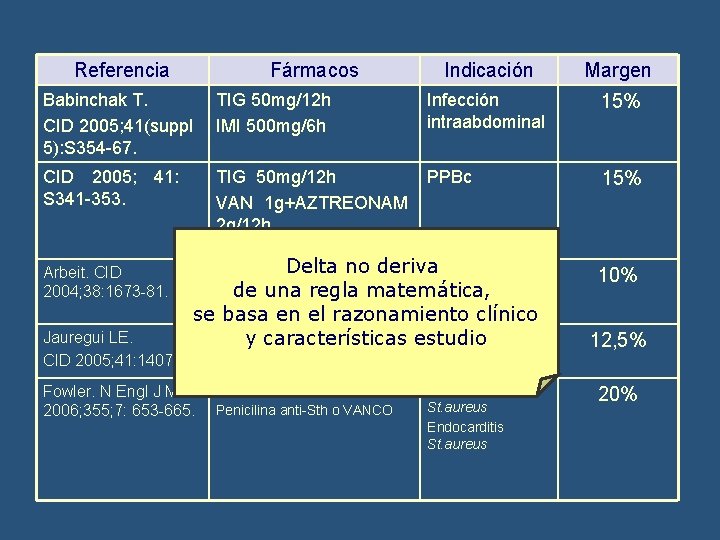
Referencia Fármacos Indicación Margen Babinchak T. CID 2005; 41(suppl 5): S 354 -67. TIG 50 mg/12 h IMI 500 mg/6 h Infección intraabdominal 15% CID 2005; 41: S 341 -353. TIG 50 mg/12 h VAN 1 g+AZTREONAM 2 g/12 h PPBc 15% Arbeit. CID 2004; 38: 1673 -81. Delta no deriva Daptomicina 4 mg/Kg/d PPBc VAN, OXA; CLOX; NAFCI; FLUC de una regla matemática, LOX (+AZT; +METRO) se basa en el razonamiento clínico Dalbavancin vs Linezolid PPBc y características estudio Jauregui LE. CID 2005; 41: 1407 -15 Fowler. N Engl J Med 2006; 355; 7: 653 -665. Daptomicina 6 mg/Kg/d Penicilina anti-Sth o VANCO Bacteriemia St. aureus Endocarditis St. aureus 10% 12, 5% 20%

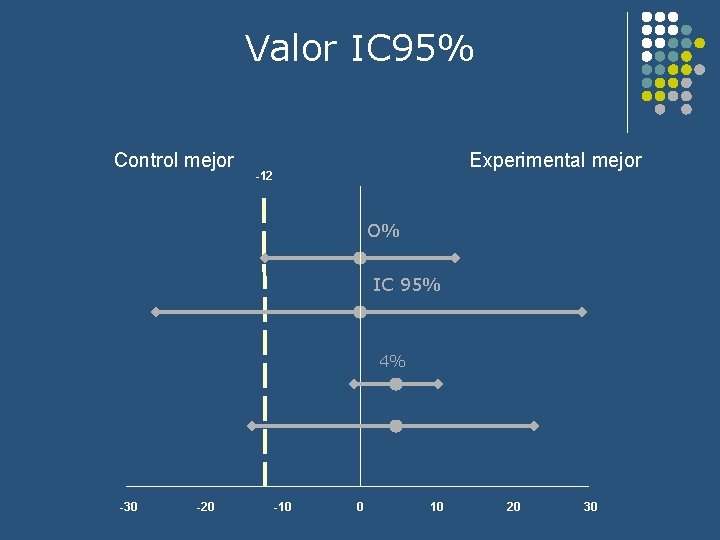
Intervalo de Confianza El IC es la llave que nos permite salir del ensayo clínico Objetivo Delta IC IC 95% El valor medio de una medida no es el real P Tamaño muestral Análisis Eficacia Aspectos éticos Todos los valores que engloba el IC 95% de la diferencia deben estar POR ENTERO, dentro de los límites de No-inferioridad

Valor IC 95% Control mejor Experimental mejor -12 O% IC 95% 4% -30 -20 -10 0 10 20 30

Valor de p Objetivo Delta IC 95% p P Tamaño muestral Análisis Eficacia Aspectos éticos Ensayos diferencia: rechaza Ho probabilidad error 5% p<0, 05 es definitivo Ensayos No-inferioridad: La interpretación se hace por el IC 95% Puede haber valores estadísticamente significativos y no-inferiores p de no-inferioridad

Torres A. Efficacy of Moxifloxacin in CAP. CID 2008; 46(15 May): 1499.

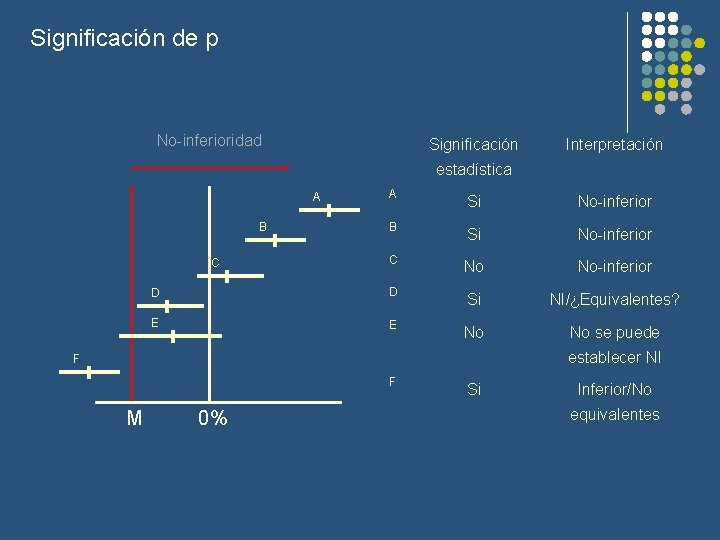
Significación de p No-inferioridad Significación Interpretación estadística A Si No-inferior B Si No-inferior C No No-inferior D D Si NI/¿Equivalentes? E E No No se puede A B C establecer NI F F M 0% Si Inferior/No equivalentes

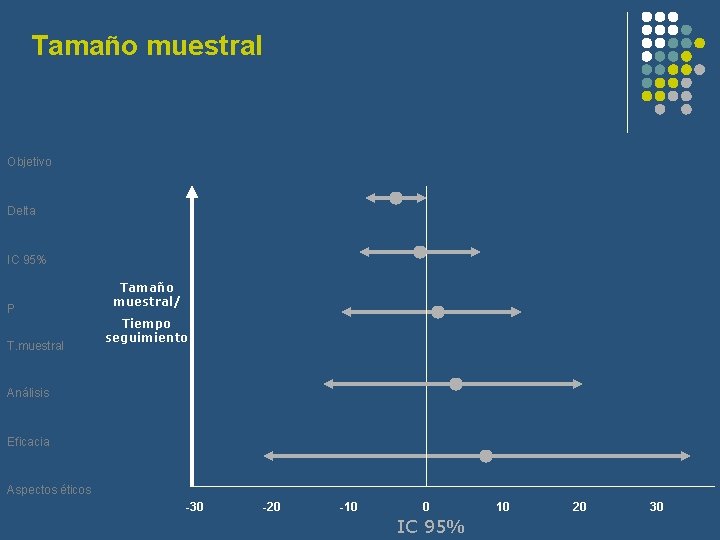
Tamaño muestral Objetivo Delta IC 95% P T. muestral Tamaño muestral/ Tiempo seguimiento Análisis Eficacia Aspectos éticos -30 -20 -10 0 IC 95% 10 20 30

Análisis de los resultados Objetivo Delta Ensayos de diferencias: Análisis intención tratar o según aleatorización: Las pérdidas no se deben al azar Garantizar la comparación de los grupos IC 95% Dificulta las diferencias P Tamaño muestral Análisis Ensayos de No-inferioridad: Análisis por protocolo o de casos válidos: Aumentan las diferencias Dificulta la conclusión de que son iguales Eficacia Aspectos éticos Ambos y detectar causas de las diferencias si las hay

Sensibilidad de los ensayos No-inferioridad ¡Ni No-inferioridad ni equivalencia es Eficacia! Objetivo Delta Medidas términos relativos Puede ocurrir que sean iguales. . . pero ¡ineficaces! IC 95% P Tamaño muestral Análisis Volume 124(8) August 1998 pp 879 -885 Homeopathic vs Conventional Treatment of Vertigo: A Randomized Double-blind Controlled Clinical Study Weiser, Michael MBCh. B; Strosser, Wolfgang MD, MBCh. B; Klein, Peter MSc Betahistina retiró FDA mercado 1968 falta eficacia Inconsistente Eficacia Aspectos éticos Conocer el efecto del control y valorar datos absolutos

Ensayos No Inferioridad (NI) El control ha tenido que tener un efecto en este estudio (M 1). No se mide el efecto del control, y se asume la sensibilidad del ensayo. Se tiene que asumir el efecto del control según experiencias pasadas o datos históricos. Si estamos equivocados, podemos asumir que un tratamiento inefectivo funciona.

Riesgos de asumir la eficacia histórica Población, criterios inclusión, tratamientos previos • Mortalidad post-IAM por betabloqueantes está modificada por nuevos tratamientos (hipolipemiante, antiplaquetarios) o procedimientos (angioplastia) • Efectos IECAs en ICC está modificado por uso rutinario de betabloqueantes o antagonistas aldosterona. • Trombolítico por el momento en el que se hace Temple RJ. FDA Experience and Perspective on Non-Inferiority Trials. FDA Workshop on CAP. January 18, 2008.

Lasagna, L. Eur J Clin Pharm 1979; 15: 373 -374. En situaciones graves, pero menos críticas, se puede justificar una comparación entre el nuevo fármaco y el estándar, …pero este ensayo tiene sentido si es un estudio de superioridad respecto al tratamiento estándar. Si es inferior, o indistinguible del estándar, los resultados no se pueden interpretar. En ausencia de placebo, no se sabe si el nuevo fármaco tiene eficacia en absoluto.

Sensibilidad del ensayo Resultados de eficacia clara: Heparina TVP UTI Leucemia aguda, Ca testicular Betaagonistas broncoespasmo Profilaxis asma con corticoides Trombolíticos IAM Para la mayoría de los tratamientos sintomáticos, no se ha visto efecto en EECCs: Ansiedad Depresión Insomnio Rinitis alérgica Profilaxis asma Síntomas ICC Angina GERD reflujo gastroesofágico Síndrome intestino irritable Dolor Temple RJ. FDA Experience and Perspective on Non-Inferiority Trials. FDA Workshop on CAP. January 18, 2008.

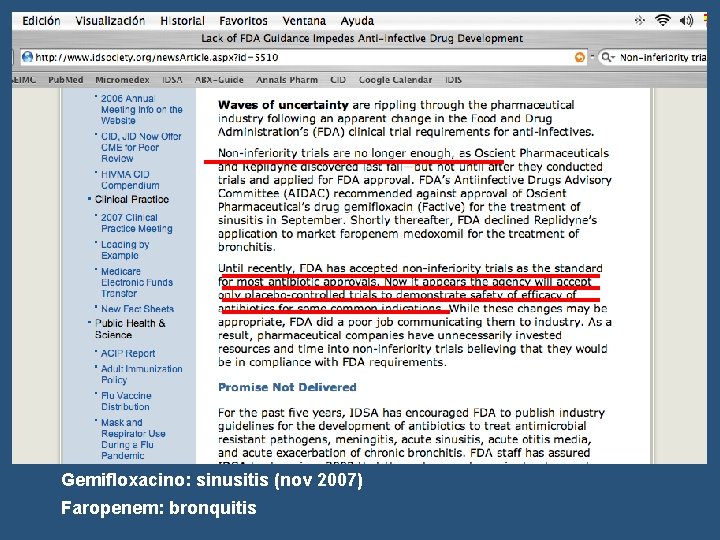
Gemifloxacino: sinusitis (nov 2007) Faropenem: bronquitis

FDA. Public workshop cosponsored with IDSA: Clinical Trial Design for Community-Acquired Pneumonia. January 17, 2008. Crowne Plaza Hotel. Silver Spring.

Aspectos éticos de los ensayos equivalencia Objetivo Delta Principio de incertidumbre IC 95% Beneficio para los participantes P T. muestral Consentimiento informado Tamaño muestral Análisis Eficacia Ética Margen de No-inferioridad

Calidad

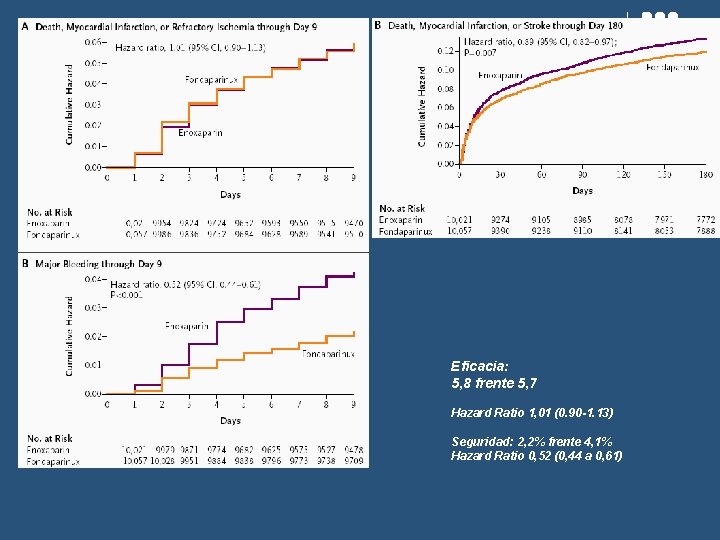
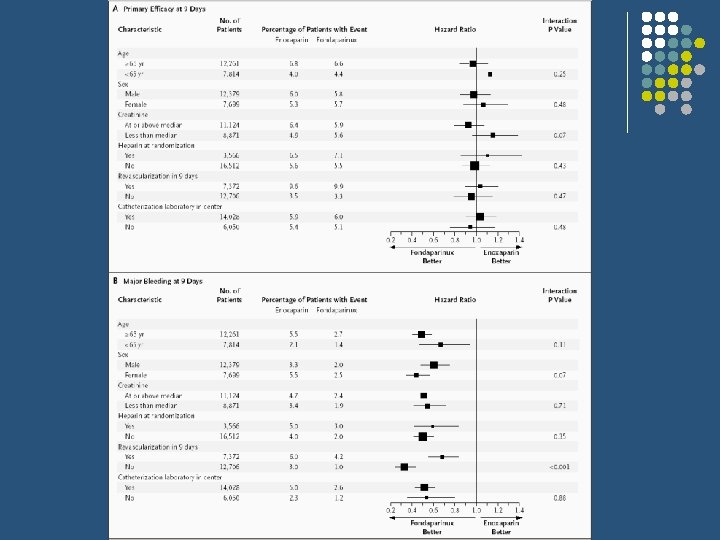
Ensayos, objetivos, variables mixtas N Engl J Med 2006; 354. 24 March. Oasis 5: Fondaparinux vs Enoxaparina en Síndromes Coronarios Adudos. Variable principal eficacia: muerte, infarto miocardio, isquemia refractaria Variable principal seguridad: hemorragia mayor Objetivo: demostrar la no-inferioridad de FON al 9º día con superioridad en seguridad Margen No-inferioridad: 1. 185 RR

Eficacia: 5, 8 frente 5, 7 Hazard Ratio 1, 01 (0. 90 -1. 13) Seguridad: 2, 2% frente 4, 1% Hazard Ratio 0, 52 (0, 44 a 0, 61)



Cornely OA. Posaconazole vs. Fluconazole or Itraconazole Prophylaxis in Patients with Neutropenia. N Engl J Med 2007; 356: 348 -59.

• Estudios de Equivalencia y Noinferioridad • Niveles de Evidencia de Equivalencia • Programas de Intercambio Terapéutico