6 Absorption en UVVisible Transitions les plus frquentes

6 Absorption en UV-Visible Transitions les plus fréquentes

6 Absorption en UV-Visible Transitions les plus fréquentes
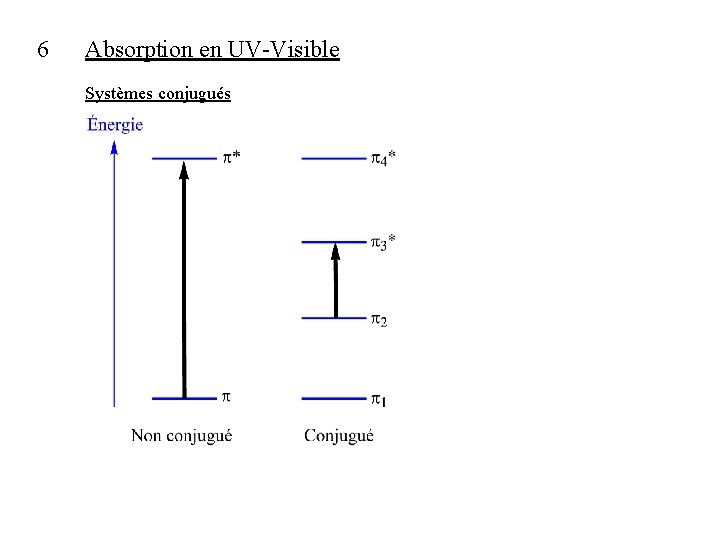
6 Absorption en UV-Visible Systèmes conjugués
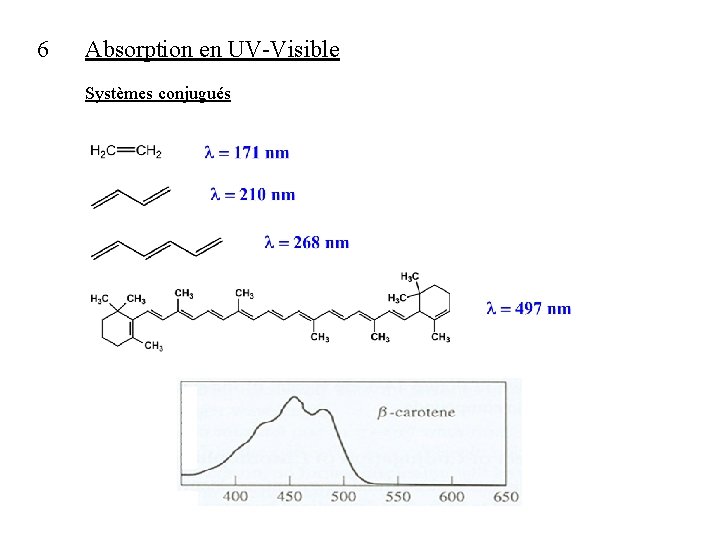
6 Absorption en UV-Visible Systèmes conjugués

6 Absorption en UV-Visible Les chromophores
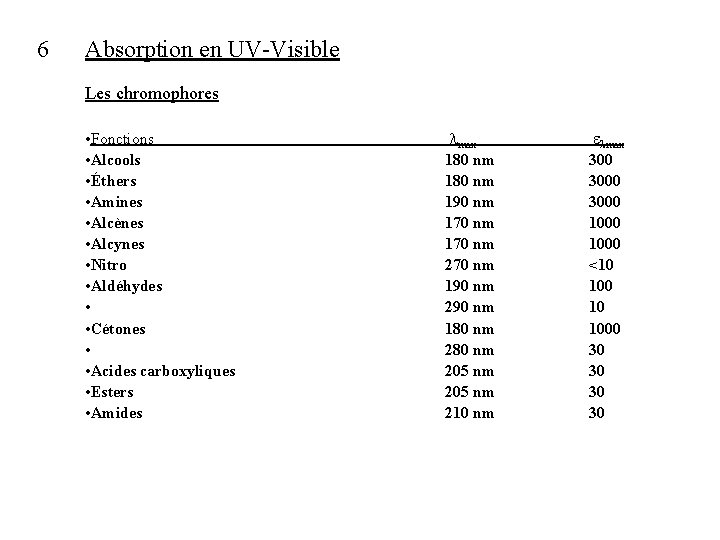
6 Absorption en UV-Visible Les chromophores • Fonctions • Alcools • Éthers • Amines • Alcènes • Alcynes • Nitro • Aldéhydes • • Cétones • • Acides carboxyliques • Esters • Amides lmax 180 nm 190 nm 170 nm 270 nm 190 nm 290 nm 180 nm 205 nm 210 nm elmax 3000 1000 <10 10 1000 30 30

6 Absorption en UV-Visible Métaux de transition (chimie inorganique) Les métaux de transition ont la particularité suivante : Leurs orbitales d ne sont pas toujours complètement remplies d’électrons; Que ce soit en phase solide cristalline ou lorsque des ions métalliques de transitions sont solvatés (entourés de molécules d’eau), les orbitales d ne sont plus dégénérées : Alors des transitions sont possibles entre les niveaux d’énergie des orbitales d. Ex : composé où des molécules ou ions sont disposés en octaèdre autour d’un ion métallique de transition. (Ex : Solution de Cu 2+ . 6 H 2 O où Cu 2+ : [Ar] 4 s 03 d 9, couleur bleue). La différence d’énergie entre les nouveaux niveaux des orbitales d correspond à l’énergie de la lumière visible. Les absorptivités sont faibles, mais cela explique la couleur éclatante de nombreux cristaux.
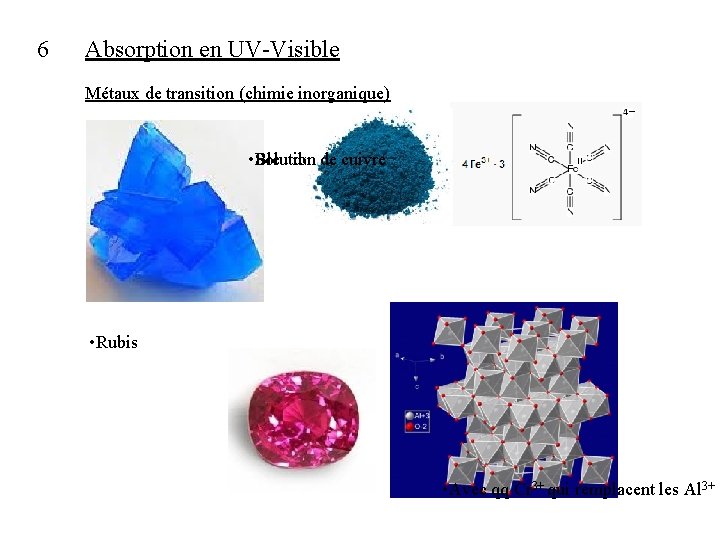
6 Absorption en UV-Visible Métaux de transition (chimie inorganique) • Solution de cuivre Bleu de prusse • Rubis • Avec qq Cr 3+ qui remplacent les Al 3+

6 Absorption en UV-Visible Analyse quantitative : relation entre T et A 9

6 Absorption en UV-Visible Analyse quantitative : relation entre T et A 10 0, 900 0, 0458 0, 100 1, 00 0, 0100 2, 00 0, 00100 3, 00

6 Absorption en UV-Visible Analyse quantitative : Loi de Beer-Lambert 11
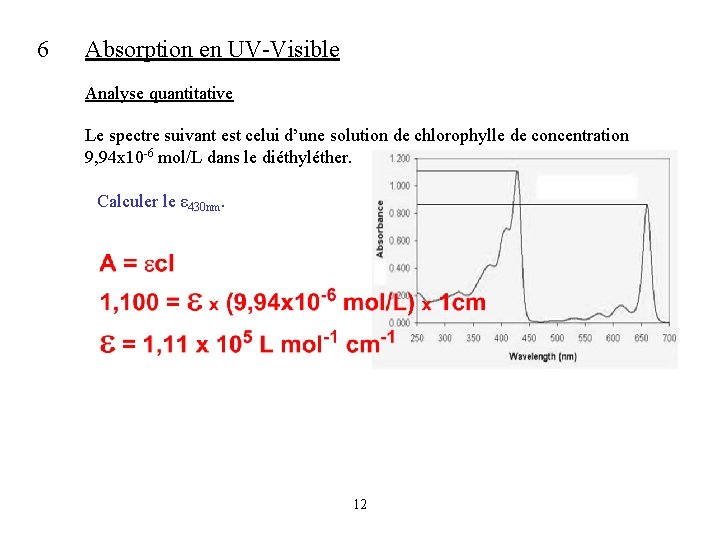
6 Absorption en UV-Visible Analyse quantitative Le spectre suivant est celui d’une solution de chlorophylle de concentration 9, 94 x 10 -6 mol/L dans le diéthyléther. Calculer le ε 430 nm. 12

6 Absorption en UV-Visible Analyse quantitative Pour exprimer l’absorptivité d’une substance, on utilise aussi le Cette valeur exprime l’absorbance qu’aurait une solution de concentration 1% (m/V), soit 1 g / 100 m. L lorsque le trajet optique est de 1 cm. Selon le Merck Index, le du lycopène (C 40 H 56) serait de 2250 à 446 nm. Calculer le ε. 13

6 Absorption en UV-Visible Analyse quantitative Calculer le de l’acétaminophène sachant qu’une solution de concentration 5, 07 x 10 -5 mol/L donne une absorbance de 0, 700 dans l’éthanol (M. M. = 151, 16 g/mol). 14
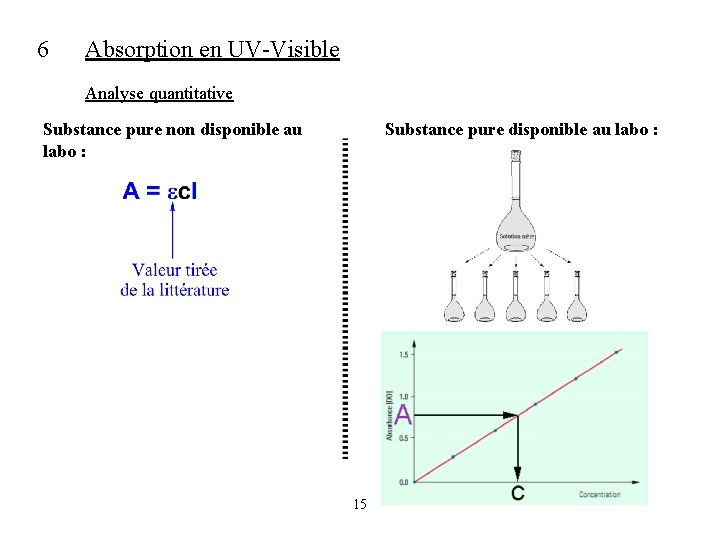
6 Absorption en UV-Visible Analyse quantitative Substance pure non disponible au labo : Substance pure disponible au labo : 15
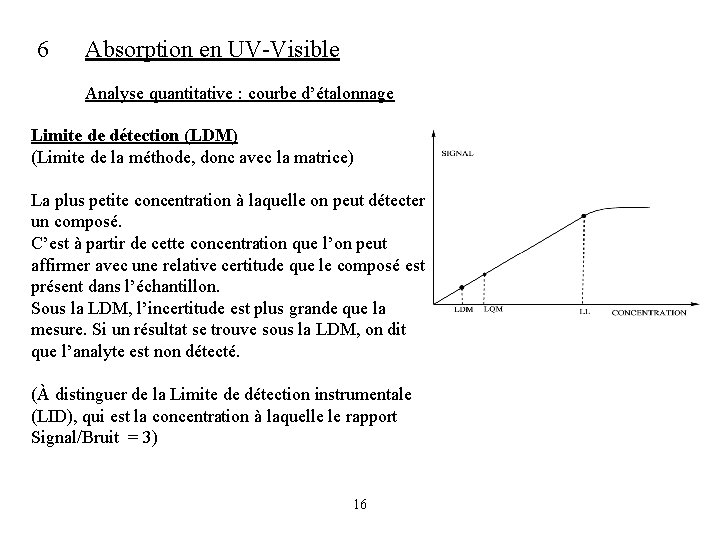
6 Absorption en UV-Visible Analyse quantitative : courbe d’étalonnage Limite de détection (LDM) (Limite de la méthode, donc avec la matrice) La plus petite concentration à laquelle on peut détecter un composé. C’est à partir de cette concentration que l’on peut affirmer avec une relative certitude que le composé est présent dans l’échantillon. Sous la LDM, l’incertitude est plus grande que la mesure. Si un résultat se trouve sous la LDM, on dit que l’analyte est non détecté. (À distinguer de la Limite de détection instrumentale (LID), qui est la concentration à laquelle le rapport Signal/Bruit = 3) 16
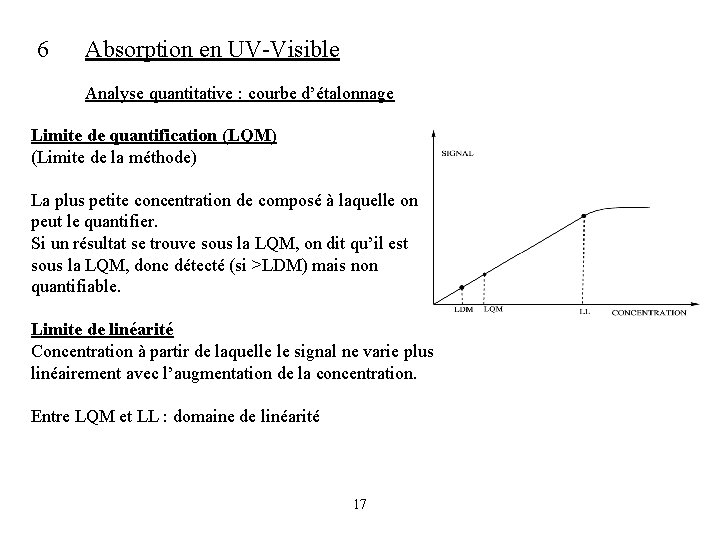
6 Absorption en UV-Visible Analyse quantitative : courbe d’étalonnage Limite de quantification (LQM) (Limite de la méthode) La plus petite concentration de composé à laquelle on peut le quantifier. Si un résultat se trouve sous la LQM, on dit qu’il est sous la LQM, donc détecté (si >LDM) mais non quantifiable. Limite de linéarité Concentration à partir de laquelle le signal ne varie plus linéairement avec l’augmentation de la concentration. Entre LQM et LL : domaine de linéarité 17

6 Absorption en UV-Visible Analyse quantitative : courbe d’étalonnage Coefficient de détermination (R 2) Aussi appelé à tort coefficient de corrélation, qui est plutôt (R); Mesure la force de la relation linéaire entre deux variables (par exemple x et y); Il est compris entre 0 et 1, où 1 indique une corrélation parfaite, et 0, aucune corrélation. Plus le coefficient est proche de 1, plus les points de la droite sont bien alignés : Exemple : R 2 = 1 R 2= 0, 64 18
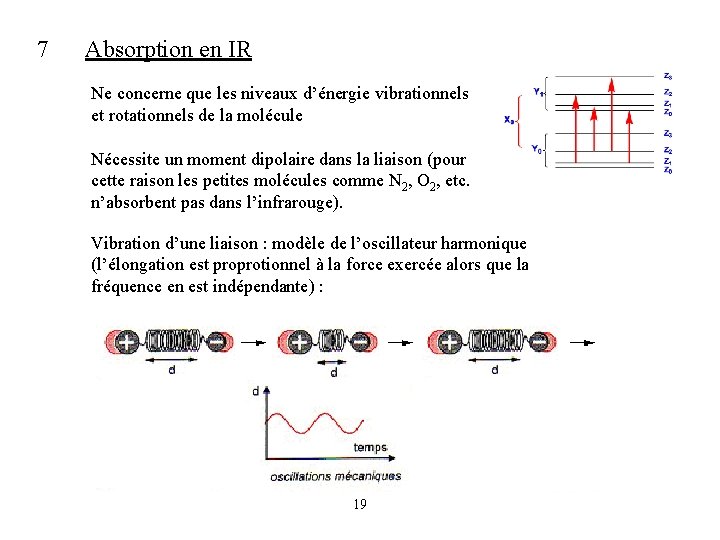
7 Absorption en IR Ne concerne que les niveaux d’énergie vibrationnels et rotationnels de la molécule Nécessite un moment dipolaire dans la liaison (pour cette raison les petites molécules comme N 2, O 2, etc. n’absorbent pas dans l’infrarouge). Vibration d’une liaison : modèle de l’oscillateur harmonique (l’élongation est proprotionnel à la force exercée alors que la fréquence en est indépendante) : 19

7 Absorption en IR Interaction entre une liaison et une onde lumineuse ayant la même fréquence que la vibration de la liaison : Plus la liaison est forte, plus le mode vibrationnel d’élongation est difficile à exciter, donc plus d’énergie requise (plus vers la gauche du spectre) Lien simple C-O: vers 1050 -1150 cm-1 Lien double C=O: vers 1700 cm-1 20
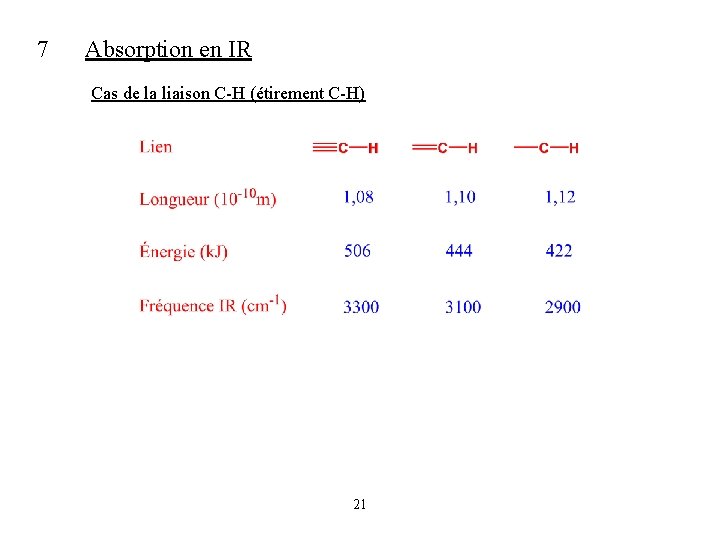
7 Absorption en IR Cas de la liaison C-H (étirement C-H) 21
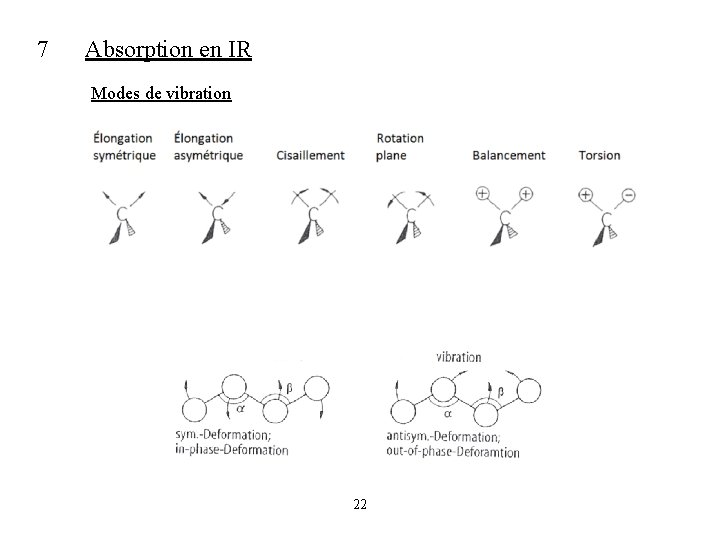
7 Absorption en IR Modes de vibration 22

7 Absorption en IR Modes de vibration 23
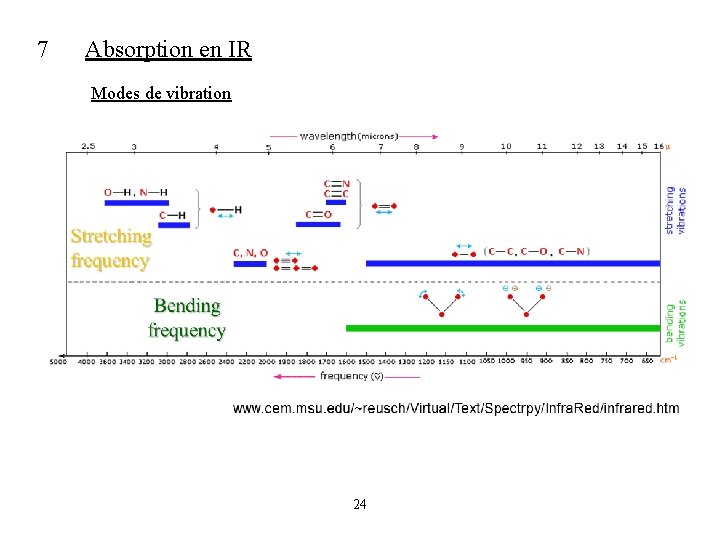
7 Absorption en IR Modes de vibration 24
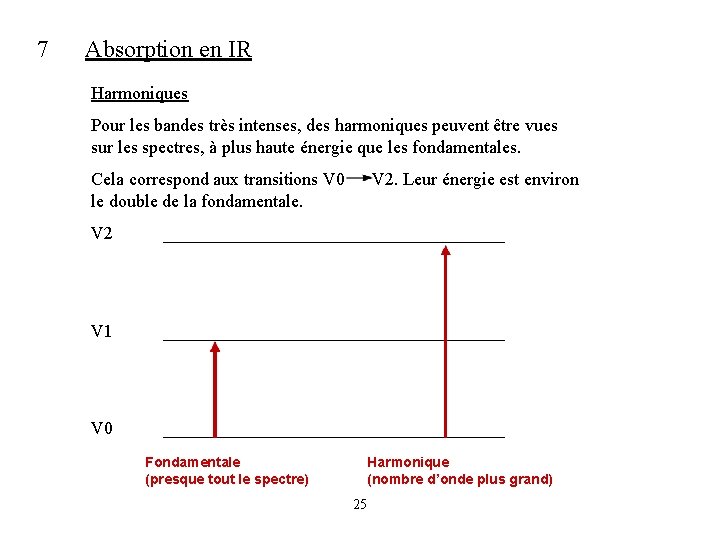
7 Absorption en IR Harmoniques Pour les bandes très intenses, des harmoniques peuvent être vues sur les spectres, à plus haute énergie que les fondamentales. Cela correspond aux transitions V 0 V 2. Leur énergie est environ le double de la fondamentale. V 2 ___________________ V 1 ___________________ V 0 ___________________ Fondamentale (presque tout le spectre) Harmonique (nombre d’onde plus grand) 25
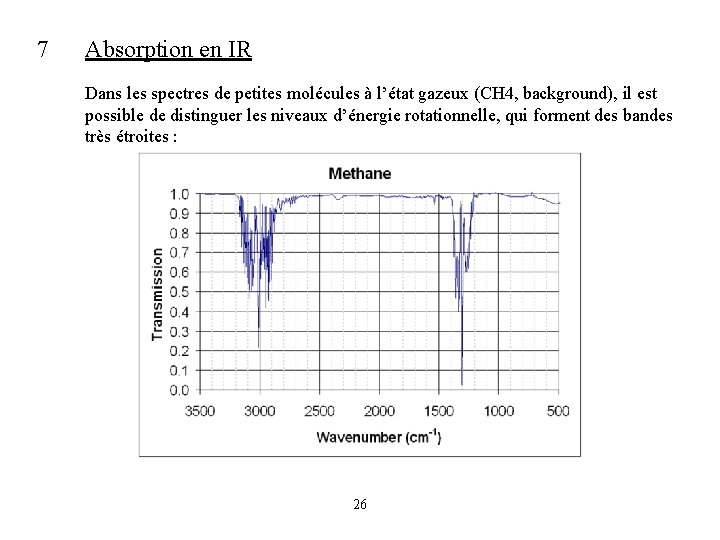
7 Absorption en IR Dans les spectres de petites molécules à l’état gazeux (CH 4, background), il est possible de distinguer les niveaux d’énergie rotationnelle, qui forment des bandes très étroites : 26
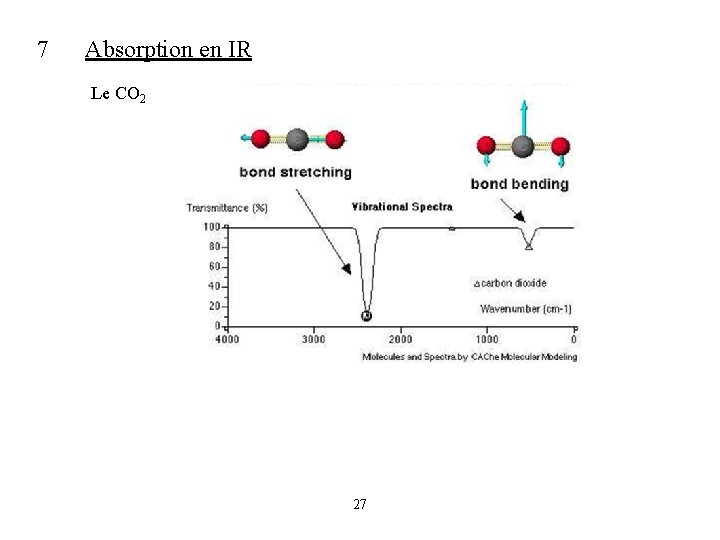
7 Absorption en IR Le CO 2 27
- Slides: 27