5 VWO Hst 8 zuren en basen Inleiding

5 VWO Hst 8 – zuren en basen

Inleiding • Opd 1, 20 min in tweetallen • Nakijken evt vragen stellen
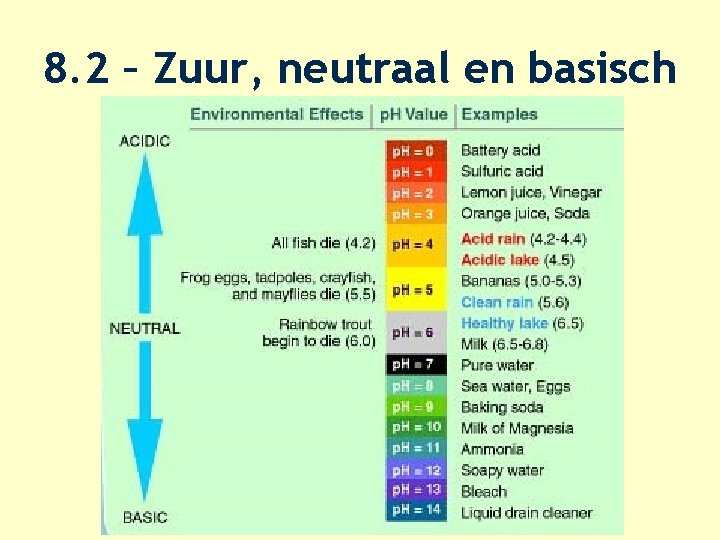
8. 2 – Zuur, neutraal en basisch

8. 2 – Zuur, neutraal en basisch • Indicator (tab 52 A) • Zuurgraad 0 -14? • Lakmoespapier – Rood= zuur – Blauw= basisch – Universeel • Tab 52 A

p. H • Zuurgraad wordt bepaald door concentratie H+ of OH-. • p. H = -log[H+] = 10 -p. H • p. OH = -log[OH-] = 10 -p. OH • p. H + p. OH = 14 (bij T=298 K) – [OH-]*[H+]= 1, 0· 10 -14 mol/l • p. H zuiver water = 7 (vergeet afleiding) • Aantal decimalen in p. H ≙ Aantal significante cijfers in [H+]
![p. H • [H+]= 2, 4· 10 -2 mol/L. p. H=? – p. H=-log p. H • [H+]= 2, 4· 10 -2 mol/L. p. H=? – p. H=-log](http://slidetodoc.com/presentation_image_h2/7cb52b1c4980dab49c01761ddba35e1e/image-6.jpg)
p. H • [H+]= 2, 4· 10 -2 mol/L. p. H=? – p. H=-log [H+]= -log 2, 4· 10 -2= 1, 6197888 – 2 signi wordt 2 decimalen dus p. H = 1, 62 • Bloed, p. H tussen 7, 33 en 7, 42. [H+] = ? – [H+] = 10 -p. H dus 10 -7, 33= 4, 7· 10 -8 mol/l – [H+] = 10 -p. H dus 10 -7, 42= 3, 8· 10 -8 mol/l • 1, 3 mol Na. OH oplossen in 500 m. L. p. H=? – Basisch, dus [OH-]= 1, 3/0, 500 L= 2, 6 mol OH– p. OH= -log[OH-]= -log 2, 6= -0. 41 – p. H= 14 -p. OH = 14— 0, 41= 14, 41!!!!! • Maken opg t/m 7

8. 3 – hoofdkenmerken van zuren en basen • Ethaanzuur, oxaalzuur • Zuur = deel dat 1 of meer H+ kan afstaan – – – Organische zuren Anorganische zuren (fig 8. 9) Instabiele zuren, H 2 CO 3, H 2 SO 3 Stabiele zuren, H 2 SO 4, H 3 PO 4 Ionen als zuren, HCl(g) H+(aq) + Cl-(aq) • Zure oplossing – H 3 O+(aq) • Oxoniumion • Niet stabiel

8. 3 – hoofdkenmerken van zuren en basen • Base = deel dat 1 of meer H+ kan opnemen – CO 32 -, NH 3, OH- • Basische oplossing – OH-(aq) – Metaaloxiden reageren • Ca. O +H 2 O Ca 2+ + 2 OH- – N-atomen zijn basen
Zuur-base reactie • Een reactie waarbij H+ wordt overgedragen – HCl + H 2 O Cl- + H 3 O+ – Na. OH + H 2 O Na+ + OH- + H 2 O – H 3 O+ + OH- 2 H 2 O • Vermindering zuur • Tab 49 – Sterk ioniseert volledig – Zwak ioniseert gedeeltelijk – Geen • 8 -13 maken • Demo 8. 2 zuur base
![Experiment 8. 2 MHCl Mol/L p. H [H 3 O+] Ionisatie MCH 3 COOH Experiment 8. 2 MHCl Mol/L p. H [H 3 O+] Ionisatie MCH 3 COOH](http://slidetodoc.com/presentation_image_h2/7cb52b1c4980dab49c01761ddba35e1e/image-10.jpg)
Experiment 8. 2 MHCl Mol/L p. H [H 3 O+] Ionisatie MCH 3 COOH % Mol/L 1, 0· 10 -1 1, 0· 10 -2 1, 0· 10 -3 1, 0· 10 -4 p. H [H 3 O+] Ionisatie %

8. 4 – sterkte van zuren en basen • Sterk zuur: H 3 O+ + Z- (100% ionisatie) – HCl + H 2 O H 3 O+ + Cl- • Zwak zuur: HZ(aq) (1 -10% ionisatie) – CH 3 COOH + H 2 O CH 3 COO- + H 3 O+ • Sterke base – O 2 - + H 2 O 2 OH- • Zwakke base Deeltje dat H+ opneemt – NH 3 + H 2 O NH 4+ + OH- • K waarde= evenwichtsconstante – Hoe zwakker, hoe kleiner K

8. 4 – sterkte van zuren en basen • K waarde= evenwichtsconstante – – – Hoe zwakker, hoe kleiner K Geen K? Gehydrateerde metaalionen zwak zuur P=-log(K) H 2 SO 4 • Maken opg t/m 18 • Lezen exp 8. 2

8. 5 – geconjugeerde zuur-baseparen • Uitdelen ionenlijst DTM-T • Reactie met water – Na 2 O, KCN, Na 2 CO 3 CH 3 COOH = zuur CH 3 COO= base CO 32= base HCO 3= zuur

Amfolyt = zuur én base • Heeft dus H en is vaak negatief • • • HCO 3 HPO 42 H 2 PO 4 H 2 O Maken t/m 27

8. 6 – enkele berekeningen • 50 m. L HNO 3 met p. H = 1, 30 met water verdund tot 1 L ? Nieuwe p. H = …? • HNO 3 + H 2 O H 3 O+ + NO 3 -
![8. 6 – enkele berekeningen • p. H = -log [H 3 O+] Dus 8. 6 – enkele berekeningen • p. H = -log [H 3 O+] Dus](http://slidetodoc.com/presentation_image_h2/7cb52b1c4980dab49c01761ddba35e1e/image-16.jpg)
8. 6 – enkele berekeningen • p. H = -log [H 3 O+] Dus als ik die weet… • Gegeven: p. H(HNO 3) = 1, 30 [H 3 O+] = 10 -p. H = 10 -1, 30 = 0, 05 mol/L • Maar ik heb 50 m. L dus 0, 05 x 0, 050 = 0, 0025 mol H 3 O+ • Die 0, 0025 mol H+ verdun ik tot 1 L • Dus nieuwe [H 3 O+] = 0, 0025 mol/L • Dus p. H = -log[H+] = -log(0, 0025) = 2, 60 • Maken 28, 29, 30

8. 7 – kwantitatieve analyse • Kwantiteit = hoeveelheid Dus: hoeveel stof zit er in? • Idee: als ik weet hoeveel ik van het A heb en ik weet hoeveel A met B reageert weet ik ook hoeveel B ik heb

8. 7 – kwantitatieve analyse Hoeveel azijnzuur in azijn? • Titratie – Zuur base reactie • zwak zuur, dus met sterke base • CH 3 COOH + OH- CH 3 COO- + H 2 O – Equivalentiepunt • 10, 00 m. L X M CH 3 COOH met 0, 1080 M Na. OHoplossing. Wat is X?
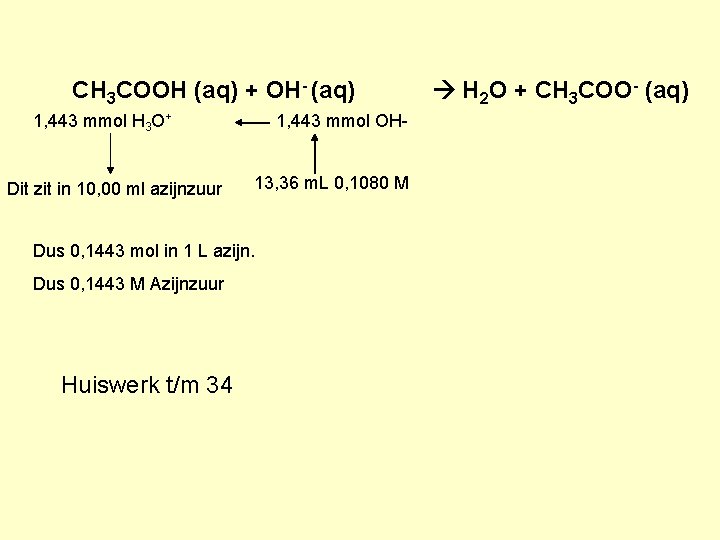
CH 3 COOH (aq) + OH- (aq) 1, 443 mmol H 3 O+ Dit zit in 10, 00 ml azijnzuur 1, 443 mmol OH 13, 36 m. L 0, 1080 M Dus 0, 1443 mol in 1 L azijn. Dus 0, 1443 M Azijnzuur Huiswerk t/m 34 H 2 O + CH 3 COO- (aq)

8. 7 – kwantitatieve analyse • Demotitratie exp 8. 3 – – 2 bladen uitdelen en doorlezen handelingen Demo Zam Uitwerken titratie Doorlezen exp 8. 5

Demotitratie … Voor de titratie van 10, 00 m. L zoutzuur is 11, 02 m. L 0, 0983 M Na. OH nodig. Bereken M HCl • 11, 02 m. L 0, 0983 M Na. OH = 1, 0833 mmol OH • OH- + H 3 O+ 2 H 2 O 1 : 1 • Dan heb ik ook 1, 0833 mmol HCl gehad • 1, 0833 mmol / 10, 00 m. L = 0, 108 mol/L • Maken t/m 40

8. 7 – kwantitatieve analyse • Titratie exp 8. 5 – Wat wordt gevraagd? Wat heb ik nodig? RV? – Uitwerken • Vrijdag bespreken – titratie – Opdrachten • Woensdag – Vragenuur – Repetitie • Vrijdag – titratie voor cijfer

CH 3 COOH (aq) + OH- (aq) 1, 053 *10^-3 mol H 3 O+ Dit zit in 10, 00 ml verdund Azijnzuur H 2 O + CH 3 COO- (aq) 1, 053 *10^-3 mol OH 10, 53 ml 0, 1000 M Dus 1, 053 *10^-1 mol in 1 L verdund azijn. Dus 1, 053 *10^-1 M Azijnzuur Maar, de originele oplossing is 10 keer verdund. Dus de originele molariteit is 10 keer zo groot. 1, 053 M originele azijnzuuroplossing 1, 053 mol in 1 L = (1, 053 * 60. 00 =) 63. 18 gram in 1 L Dus is het goede tafelazijn (6, 318 massa %)
- Slides: 23