5 TEORIJE KISELINA I BAZA 5 1 Arrheniusova

5. TEORIJE KISELINA I BAZA 5. 1. Arrhenius-ova teorija elektrolitičke disocijacije (1887) 5. 2. Brønsted-Lowry-jeva teorija (teorija protona, 1923) 5. 3. Lewis-ova teorija (teorija elektrona, 1923) 5. 4. Relativna jakost kiselina i baza Odjel za kemiju

5. 1. Arrhenius-ova teorija elektrolitičke disocijacije (1887) Svante Arrhenius Odjel za kemiju

1. Kiseline stvaraju vodikov ion u vodenim otopinama. H 2 O HCl ⇋ H+ (aq) + Cl-(aq) a) Anorganske (mineralne) kiseline: HCl, H 2 SO 4, HNO 3 H 3 PO 4, H 2 CO 3 sve jake kiseline sve slabe kiseline b) Organske kiseline: HCHO 2 mravlja kiselina HC 2 H 3 O 2 octena kiselina H 2 C 2 O 4 oksalna kiselina HC 6 H 5 O fenol Odjel za kemiju

2. Baze stvaraju hidroksidni ion u vodenim otopinama. Na. OH H 2 O ⇋ Na+ (aq) + OH-(aq) a) Anorganske baze: Mg(OH)2, Ca(OH)2, Na. OH, Al(OH)3, KOH b) Organske baze ne mogu se objasniti Arrhenius ovom teorijom. Odjel za kemiju

Nedoumice vezane za Arrheniusovu teoriju kiselina i baza: 1. Je li moguće da nevodeni HCl nije kiselina jer znamo da ne disocira na ione (ne provodi električnu struju), ili je ipak kiselina jer nakon dodira s vodom disocira na hidronijeve ione (provodi električnu struju)! 2. Što je s nevodenim otopinama u kojima ne nastaje hidroksidni ion, jer na primjer u metanolu nastaje metoksidni ion (CH 3 O¯) a u amonijaku amidni ion (NH 2¯ )? 3. Ustanovljeno je da H+ ion ne postoji nego je solvatiran s nekoliko molekula otapala (H 3 O+ u vodi, CH 3 OH 2+ u metanolu, NH 4+ u tekućem amonijaku). Odjel za kemiju

4. Neutralizacija, utjecaj na biljne boje, te kiselobazna kataliza su opaženi i u otapalima u kojima nema hidronijevog (aprotična otapala) ni drugih iona (slaba električna provodljivost). 5. U vodenim otopinama kao baze ponašaju se tvari koje disocijacijom ne mogu dati hidroksidni ion (npr. amini). Zbog toga su uvedene alternativne teorije. Odjel za kemiju

5. 2. Brønsted-Lowry-jeva teorija (teorija protona, 1923) Johannes Nicolaus Brønsted Odjel za kemiju Thomas Martin Lowry

1. Kiseline su tvari koje daju proton(e) u kemijskoj reakciji (donori protona). 2. Baze su tvari koje prihvataju proton(e) u kemijskoj reakciji (akceptori protona). Odjel za kemiju

- 1923. godine Brønsted (Danska) i Lowry (Engleska) neovisno jedan o drugome, predložili su teoriju ponašanja kiselina i baza: Kiseline su proton donori (davatelji), a baze su proton akceptori (primatelji). - da bi se neka jedinka ponašala kao kiselina, mora biti prisutan proton akceptor (baza), i obrnuto Odjel za kemiju

Primjer: NH 3 + CN¯ ⇋ NH 2¯ + HCN a) Obratiti pozornost da u gornjoj reakciji nema niti H+ niti OH¯ b) NH 3 je kiselina!! c) CN¯ je baza. d) NH 2¯ je konjugirana baza. (konjugirana baza = anion kiseline). e) HCN je konjugirana kiselina. (konjugirana kiselina = kiselina koja nastaje kad baza prihvati proton izvorne kiseline). Odjel za kemiju

Konjugirane kiseline i baze • kada kiselina daje proton , nastane KONJUGIRANA BAZA kiselina 1 baza 1 + proton kiselina 1 i baza 1 su konjugirani (spregnuti) kiselo/bazni par • kada baza primi proton, nastane KONJUGIRANA KISELINA baza 2 + proton kiselina 2 Odjel za kemiju
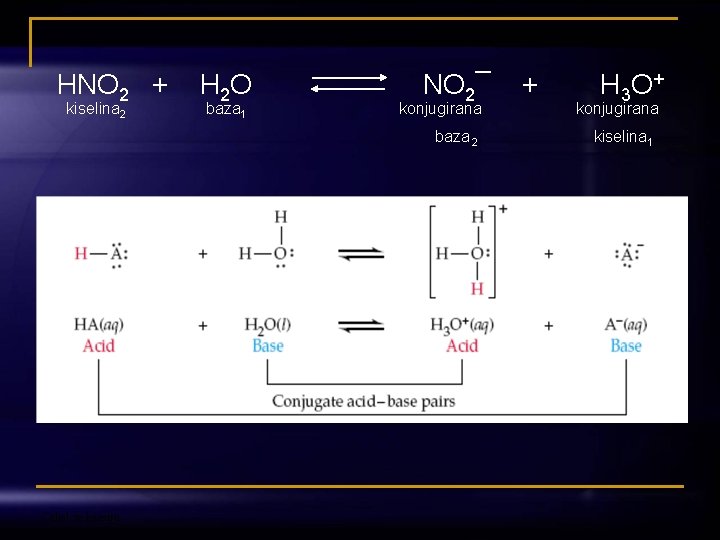
+ HNO + H O NO ¯ + H O 2 2 2 3 kiselina baza konjugirana 2 1 baza 2 kiselina 1 Odjel za kemiju
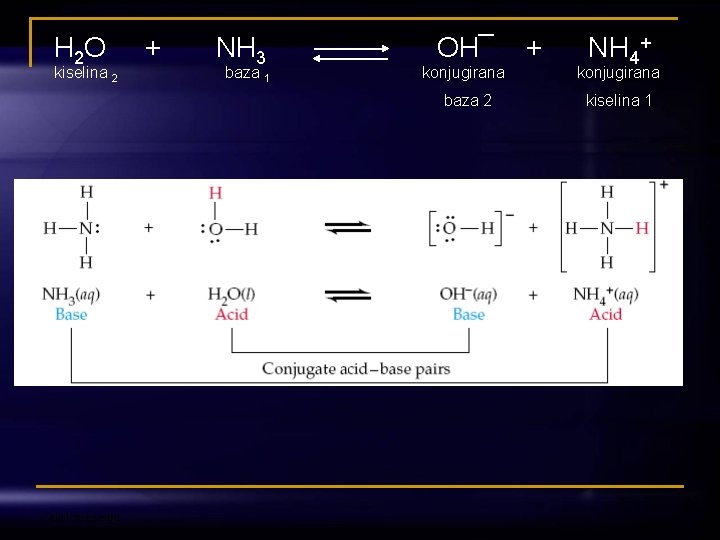
H 2 O + NH 3 OH¯ + NH 4+ kiselina baza konjugirana 2 1 baza 2 kiselina 1 Odjel za kemiju
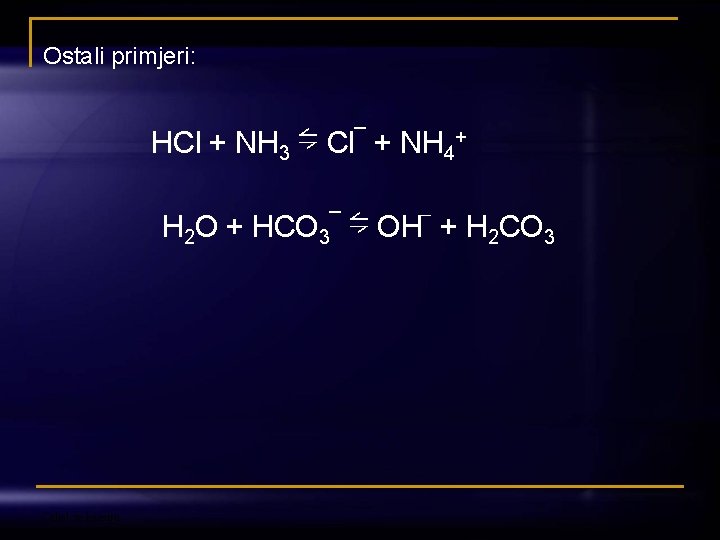
Ostali primjeri: HCl + NH 3 ⇋ Cl¯ + NH 4+ H 2 O + HCO 3¯ ⇋ OH¯ + H 2 CO 3 Odjel za kemiju
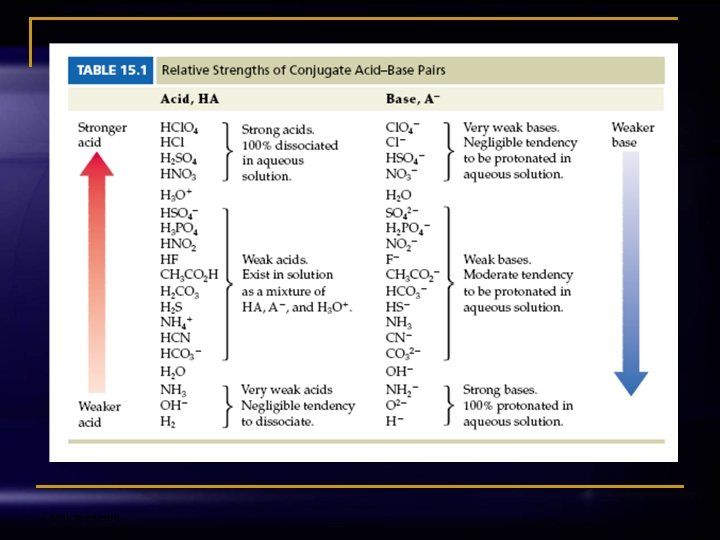
Odjel za kemiju

5. 3. Lewis-ova teorija (teorija elektrona, 1923) Gilbert Newton Lewis Odjel za kemiju

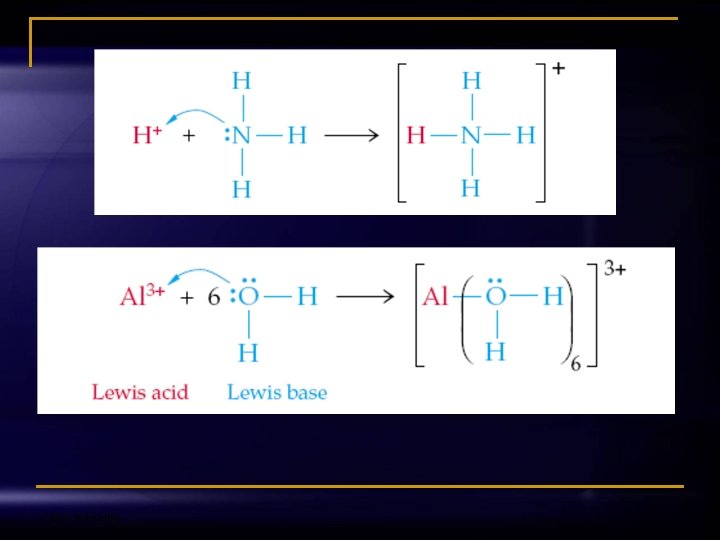
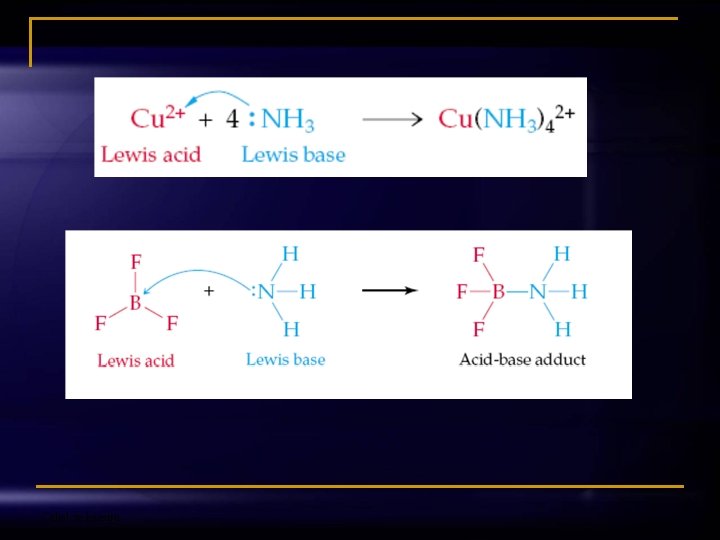
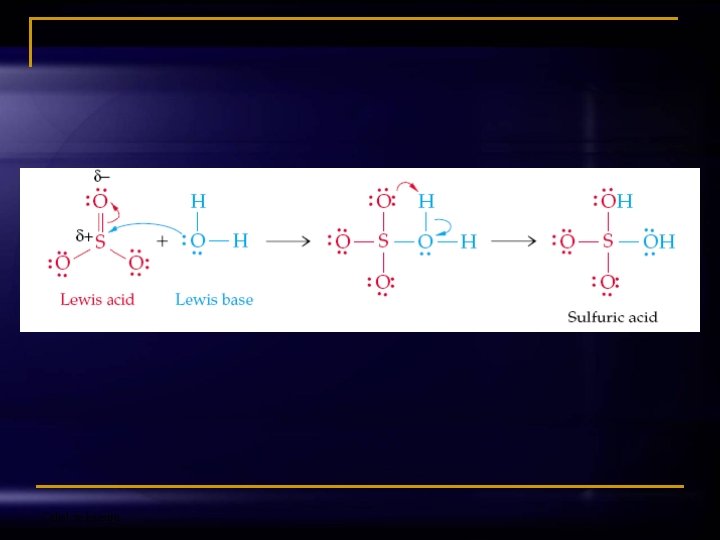
Lewis-ova teorija je najopćenitija teorija 1. Kiseline prihvataju elektrone (elektronske parove) u kemijskoj reakciji (akceptori elektrona). 2. Baze daju elektrone (elektronske parove) u kemijskoj reakciji (donori elektrona). Primjer: BF 3 + : NH 3 ⇋ F 3 B: NH 3 Odjel za kemiju
Odjel za kemiju
Odjel za kemiju
Odjel za kemiju

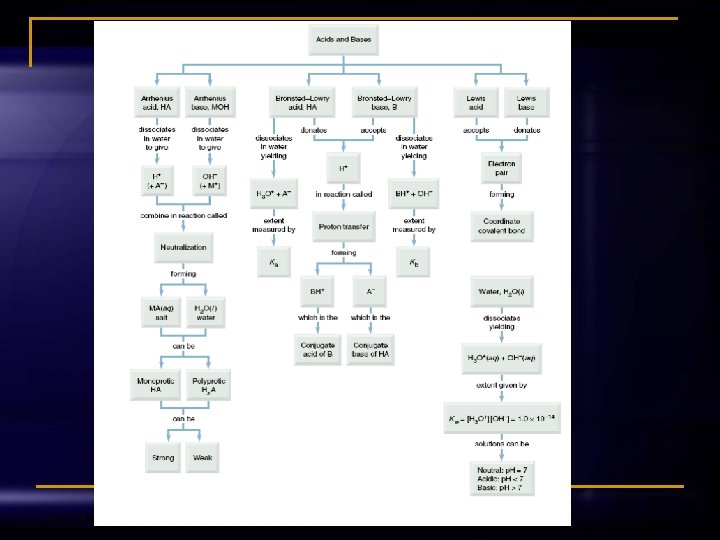
5. 4. Pregled teorija kiselina i baza Odjel za kemiju
Odjel za kemiju

5. 5. Relativna jakost kiselina i baza 1. Definicija "jaka" ili "slaba" nema nikakve veze s korozivnošću. a) "Jaka" = 100 % ionizacija b) "Slaba" = <100 % ionizacija, ali > 0 % 2. Definicija reflektira sposobnost ionizacije kiseline/baze i ništa drugo. 3. Zapamtiti da "jaka" kiselina/baza = jaki elektrolit. Odjel za kemiju

5. 6. Amfiprotična otapala n U prisutnosi baze ponašaju se kao kiselina, a u prisutnosti kiseline kao baza Npr. voda podliježe samoionizaciji 2 H 2 O H 3 O+ + OH¯ (autoprotoliza) U čistoj vodi samo 1 od 107 molekula vode podliježe autoprotolizi. Odjel za kemiju
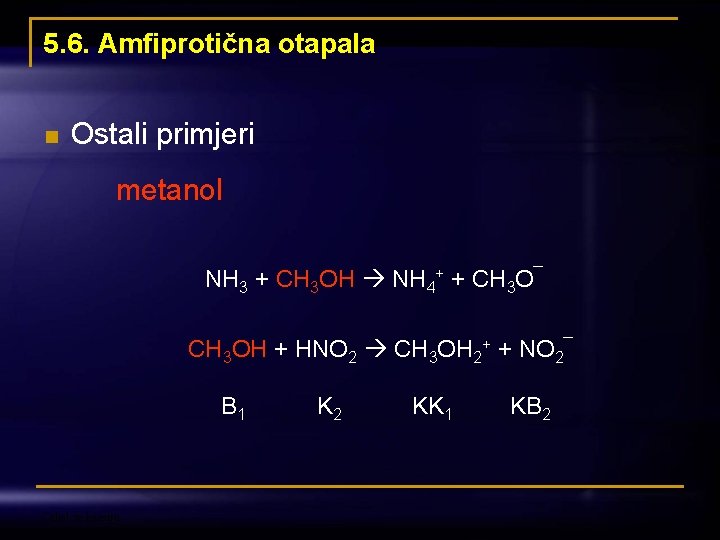
5. 6. Amfiprotična otapala n Ostali primjeri metanol NH 3 + CH 3 OH NH 4+ + CH 3 O¯ CH 3 OH + HNO 2 CH 3 OH 2+ + NO 2¯ B 1 K 2 KK 1 KB 2 Odjel za kemiju

5. 7. Autoprotoliza - amfiprotična otapala podliježu samoionizaciji ili autoprotolizi, čime nastaje par ionskih vrsta baza 1 + kiselina 2 kiselina 1 + baza 2 H 2 O + H 2 O H 3 O+ + OH¯ CH 3 OH + CH 3 OH CH 3 OH 2+ + CH 3 O¯ HCOOH + HCOOH HCOOH 2+ + HCOO¯ NH 3 + NH 3 NH 4+ + NH 2¯ Odjel za kemiju

Relativna jakost nekih kiselina Odjel za kemiju
- Slides: 27