5 Subdomnio Unidade Solues e equilbrio de solubilidade

5 Subdomínio Unidade Soluções e equilíbrio de solubilidade

5. 1 Mineralização das águas e processo de dissolução

70 % Á g u a A água cobre cerca de 70 % da superfície do planeta Terra.

70 % Á g u a Água salgada (97, 3 %) Água doce (2, 7 %) 97, 3 % de toda a água do Planeta é água salgada, e apenas 2, 7 % é água doce.
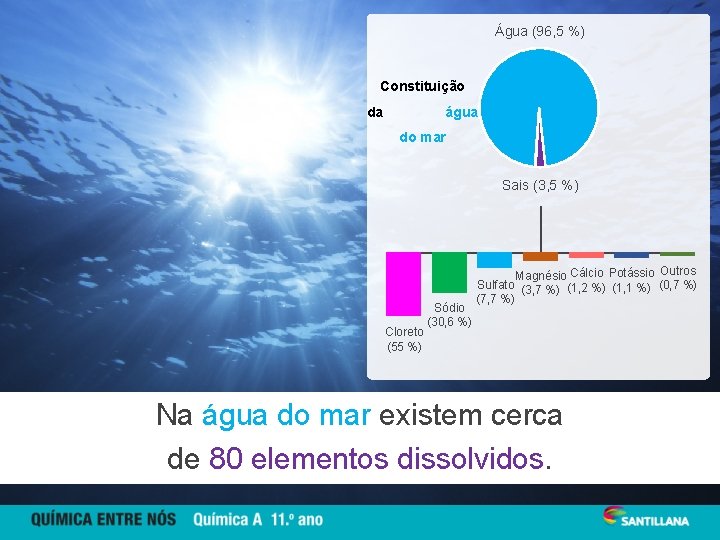
Água (96, 5 %) Constituição da água do mar Sais (3, 5 %) Cloreto (55 %) Sódio (30, 6 %) Magnésio Cálcio Potássio Outros Sulfato (3, 7 %) (1, 2 %) (1, 1 %) (0, 7 %) (7, 7 %) Na água do mar existem cerca de 80 elementos dissolvidos.
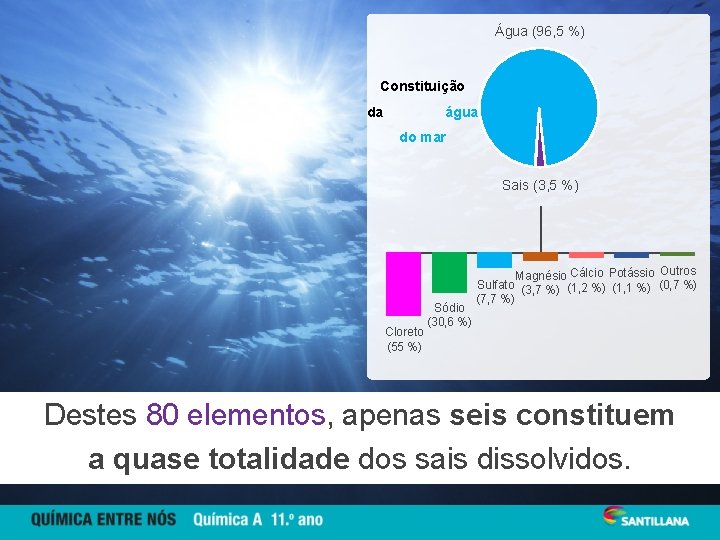
Água (96, 5 %) Constituição da água do mar Sais (3, 5 %) Cloreto (55 %) Sódio (30, 6 %) Magnésio Cálcio Potássio Outros Sulfato (3, 7 %) (1, 2 %) (1, 1 %) (0, 7 %) (7, 7 %) Destes 80 elementos, apenas seis constituem a quase totalidade dos sais dissolvidos.

Os sais dissolvidos na água do mar têm a sua principal origem em erupções vulcânicas, . . .

. . . nas reações químicas entre a água do mar e as rochas vulcânicas recém-formadas. . .

. . . e na lixiviação dos solos.

Além dos sais, encontram-se ainda dissolvidos na água do mar compostos orgânicos e gases.

A água do mar dissolve cerca de 30 % do CO 2 lançado na atmosfera. As moléculas de CO 2 são trocadas de forma contínua e recíproca entre a atmosfera e os oceanos. O processo de dissolução do CO 2 é dado por: CO 2(g) + H 2 O(ℓ) ⇌ HCO 3–(aq) + H 3 O+(aq) HCO 3–(aq) + H 2 O(ℓ) ⇌ CO 32–(aq) + H 3 O+(aq)

O par CO 2/HCO 3– é importante para a manutenção do p. H da água do mar (7, 5 < p. H < 8, 5).

O CO 2 e os iões HCO 3– e CO 32– são vitais para muitas formas de vida marinha.

Quando combinados com iões cálcio, produzem carbonato de cálcio, que constitui conchas e corais.

A água do mar é, por isso, considerada uma solução muito complexa.

A salinidade corresponde à massa total (em gramas) de sais minerais dissolvidos por quilograma de água. A salinidade é expressa habitualmente em partes por mil (‰).

A água do mar tem salinidade média de 35 ‰ (3, 5 %). Contudo, diferentes oceanos e mares apresentam diferentes valores de salinidade média: Oceano/mar Salinidade média (‰) Oceano Atlântico 35, 4 Oceano Índico 34, 8 Oceano Pacífico 34, 5 Mar Mediterrâneo 37, 4 Mar Negro 18 Mar Vermelho 40 Mar Morto 270

A composição média da água dos oceanos iões mais importantes é dada na tabela: Ião Composição (‰) Cloreto (Cℓ–) 19, 3 Sódio (Na+) 10, 6 Sulfato (SO 42–) 2, 7 Magnésio (Mg 2+) 1, 3 Cálcio (Ca 2+) 0, 4 Potássio (K+) 0, 4 Bicarbonato (HCO 3–) 0, 1 O composto dissolvido mais abundante na água dos oceanos é o cloreto de sódio (Na. Cℓ). Os níveis de salinidade da água de um oceano variam de lugar para lugar, mas as proporções relativas dos iões são constantes.

Processo de dissolução e interação soluto-solvente

O fenómeno de dissolução pode ser considerado um processo espontâneo de mistura de duas substâncias (soluto e solvente). Não existe um solvente universal, embora a água dissolva um grande número de substâncias polares e iónicas. Para qualquer solvente, há substâncias que são muito solúveis, enquanto outras substâncias são pouco solúveis.

O fenómeno de dissolução pode ser considerado um processo espontâneo de mistura de duas substâncias (soluto e solvente). A facilidade com que um processo de dissolução ocorre depende sobretudo das intensidades relativas das atrações entre: • as partículas do soluto (interação soluto-soluto); • as partículas do solvente (interação solvente-solvente); • as partículas do soluto e do solvente depois da dissolução (interação soluto-solvente).

Considere a dissolução do cloreto de sódio (Na. Cℓ) em água: Estrutura cristalina de Na. Cℓ Os iões Na+ e Cℓ– encontram-se inicialmente agregados numa estrutura cristalina.
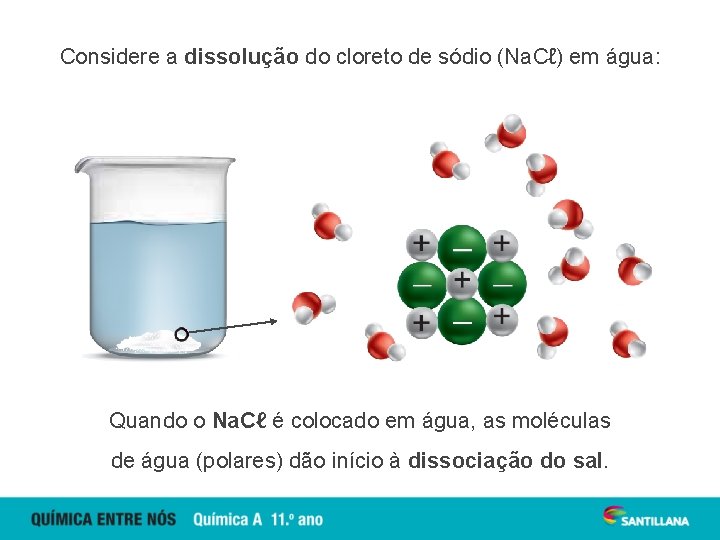
Considere a dissolução do cloreto de sódio (Na. Cℓ) em água: Quando o Na. Cℓ é colocado em água, as moléculas de água (polares) dão início à dissociação do sal.
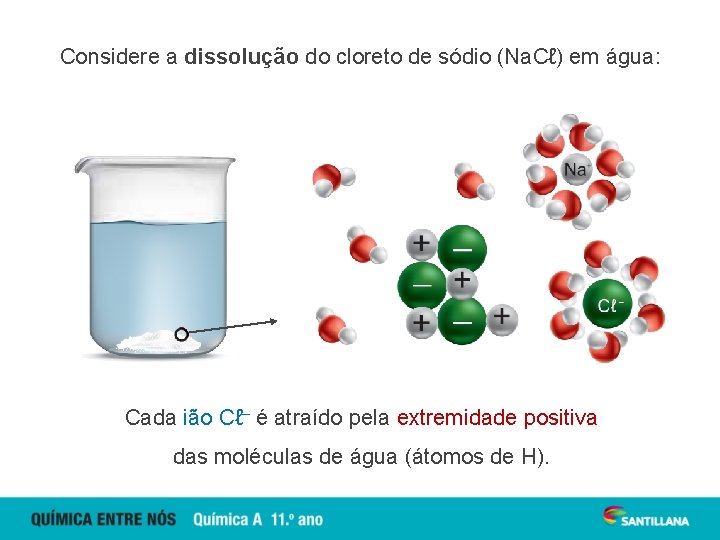
Considere a dissolução do cloreto de sódio (Na. Cℓ) em água: Cada ião Cℓ– é atraído pela extremidade positiva das moléculas de água (átomos de H).
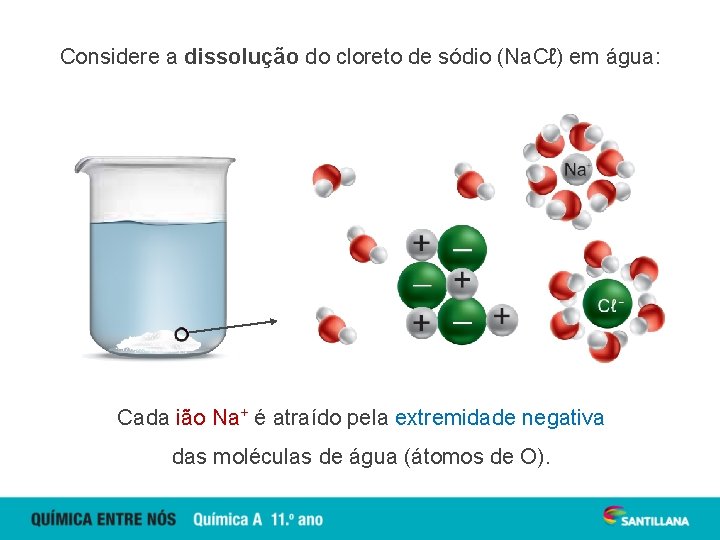
Considere a dissolução do cloreto de sódio (Na. Cℓ) em água: Cada ião Na+ é atraído pela extremidade negativa das moléculas de água (átomos de O).
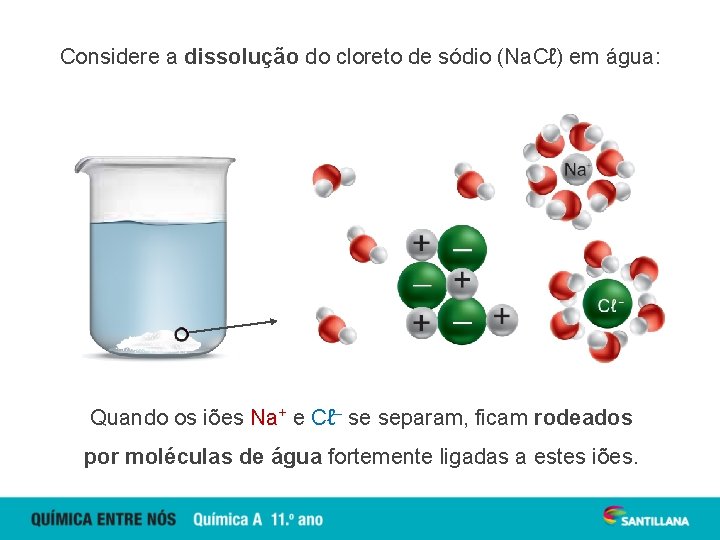
Considere a dissolução do cloreto de sódio (Na. Cℓ) em água: Quando os iões Na+ e Cℓ– se separam, ficam rodeados por moléculas de água fortemente ligadas a estes iões.
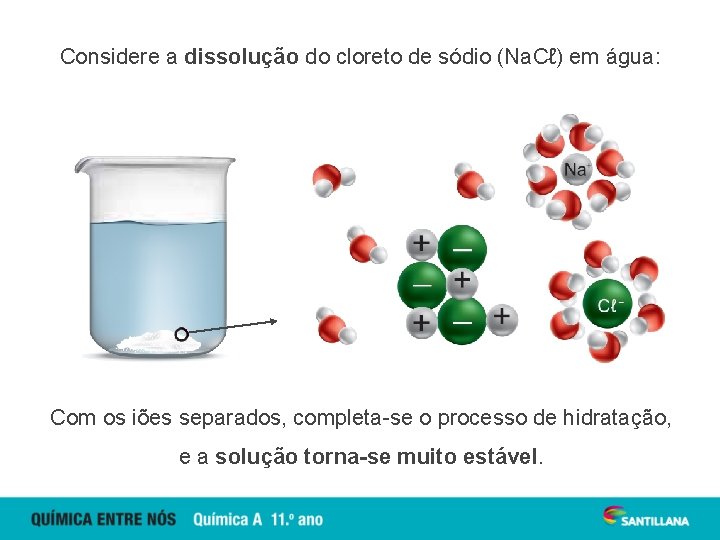
Considere a dissolução do cloreto de sódio (Na. Cℓ) em água: Com os iões separados, completa-se o processo de hidratação, e a solução torna-se muito estável.
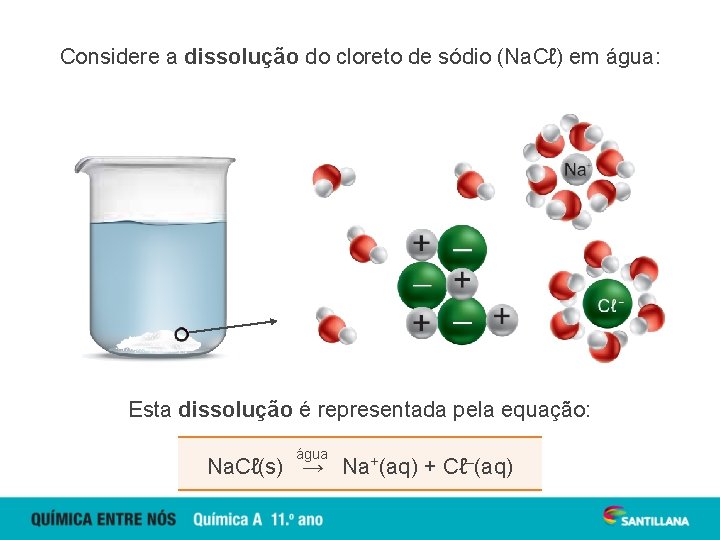
Considere a dissolução do cloreto de sódio (Na. Cℓ) em água: Esta dissolução é representada pela equação: água Na. Cℓ(s) → Na+(aq) + Cℓ–(aq)

Fatores que afetam o tempo de dissolução

Para dada temperatura e pressão, a velocidade de dissolução de um sólido aumenta com: • o estado de divisão do soluto sólido; • o grau de agitação da solução. Estes fatores não alteram a quantidade de soluto que é possível dissolver numa determinada quantidade de solvente, mas interferem no tempo de dissolução do soluto.

Se pretender adoçar uma chávena de chá, . . . Açúcar granulado Açúcar em cubos . . . a dissolução do açúcar será mais rápida se utilizar açúcar granulado ou açúcar em cubos?

Se pretender adoçar uma chávena de chá, . . . Açúcar granulado Açúcar em cubos Maior estado de divisão Menor estado de divisão Dissolução mais rápida Dissolução mais lenta Quanto maior é o estado de divisão do soluto, maior é a área de contacto soluto-solvente; logo, mais rápida é a dissolução.

Considere, agora, que pretende adoçar duas chávenas de chá com a mesma quantidade de açúcar. Sem agitação Com agitação Em qual das chávenas a dissolução do açúcar será mais rápida?

Considere, agora, que pretende adoçar duas chávenas de chá com a mesma quantidade de açúcar. Sem agitação Com agitação Dissolução mais lenta mais rápida A existência de agitação promove um aumento das colisões entre o soluto e o solvente e, por isso, é mais rápida a dissolução.

Conclusão • Na água do mar existem cerca de 80 elementos dissolvidos. • A salinidade corresponde à massa total (em gramas) de sais minerais dissolvidos por quilograma de água e é expressa habitualmente em partes por mil (‰).

Conclusão • O fenómeno de dissolução pode ser considerado um processo espontâneo de mistura de duas substâncias (soluto e solvente).

Conclusão • Para uma dada temperatura e pressão, a velocidade de dissolução de um sólido aumenta com: o o estado de divisão do soluto sólido; o o grau de agitação da solução.
- Slides: 37