5 Stereochemie Chiralitt CIP Regeln Fischerprojektion Buch Hand

5. Stereochemie • Chiralität • CIP Regeln • Fischerprojektion

• Buch & Hand • Hand & Hand

Stereogene Kohlenstoffatome • Video: Salomons • Video: Kinder

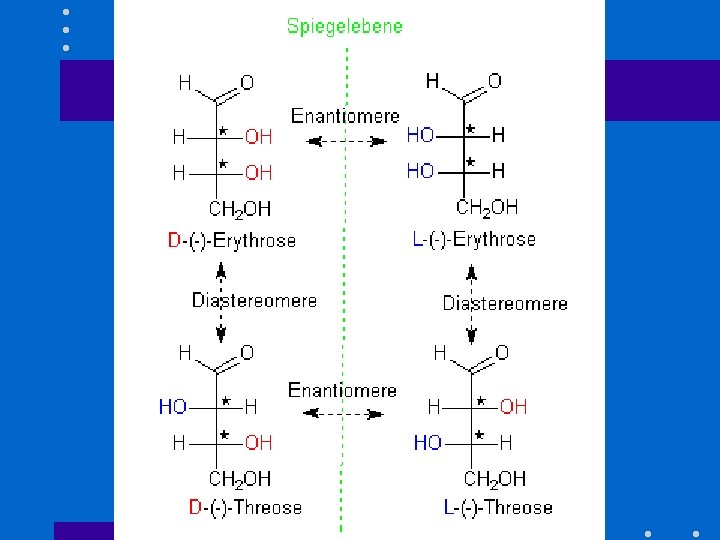
Isomere Substanzen mit der gleichen Summenformel • Strukturisomere – unterschiedliche Atomanordnungen • Stereoisomere – gleiche Atomanordnungen – unterschiedliche räumliche Orientierung • Enantiomere – Bild & Spiegelbild • Diastereomere

Die drei Ks der Chemie • Konstitution – Beschreibung der Atomanordnung • Konfiguration – Beschreibung der Atom-Orientierung • Konformation – Beschreibung der exakten Molekülform (3 D Momentaufnahme)

Messung der Chiralität • Drehung der Polarisationsebene des Lichtes • (optische Aktivität)
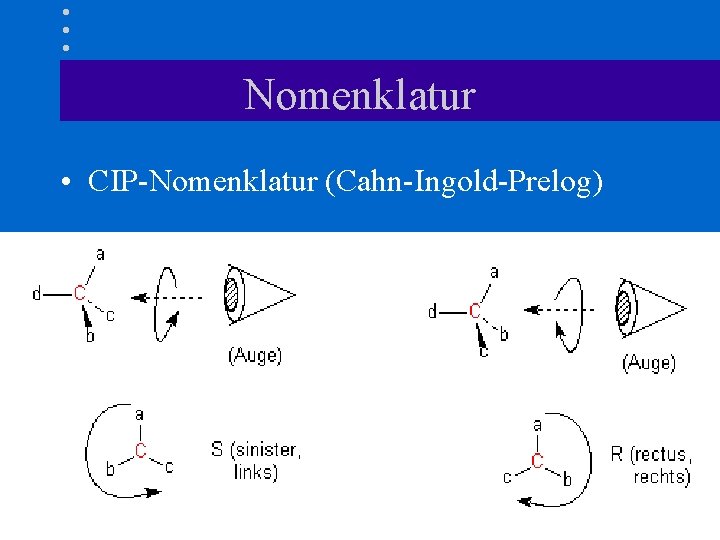
Nomenklatur • CIP-Nomenklatur (Cahn-Ingold-Prelog)

CIP-Prioritätsregeln • 1. Regel – Ordnungszahl der Substituenten – (bei Isotopen: hörer Masse) • 2. Regel – Bindungsordnung • 3. Regel – nächste Substitutionschale bewerten
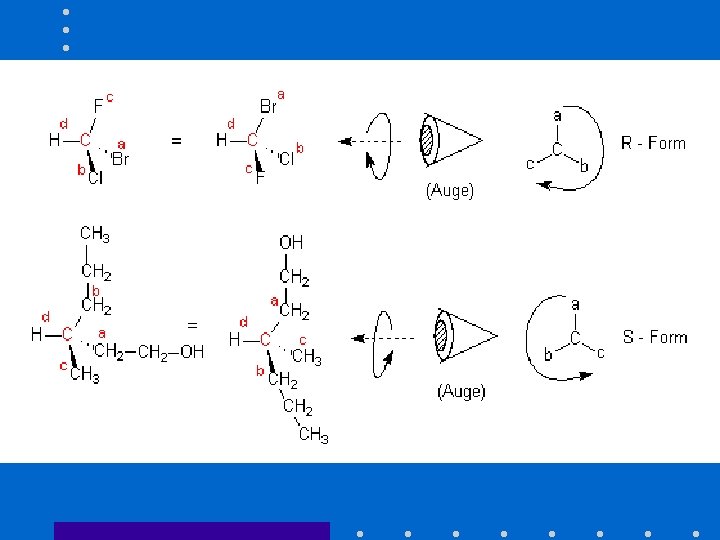
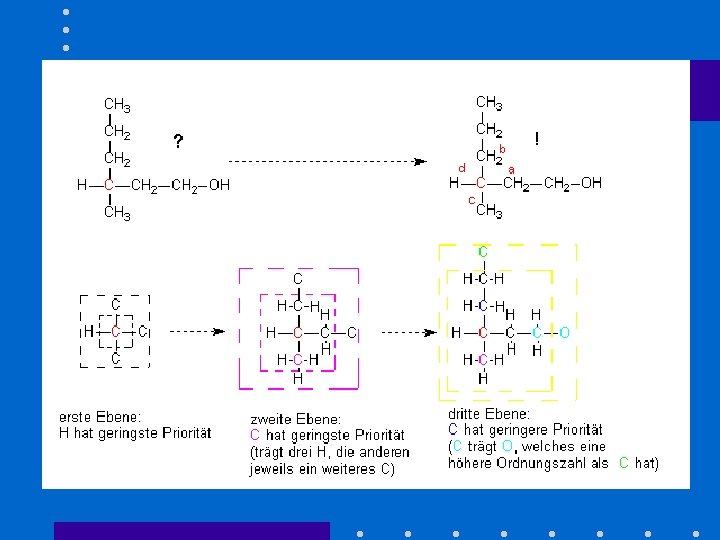

Fischerprojektionen • CHFCl. Br • CH 3 -CHBr. Cl • CH 3 -CH 2 Br-CH 2 F-CH 3
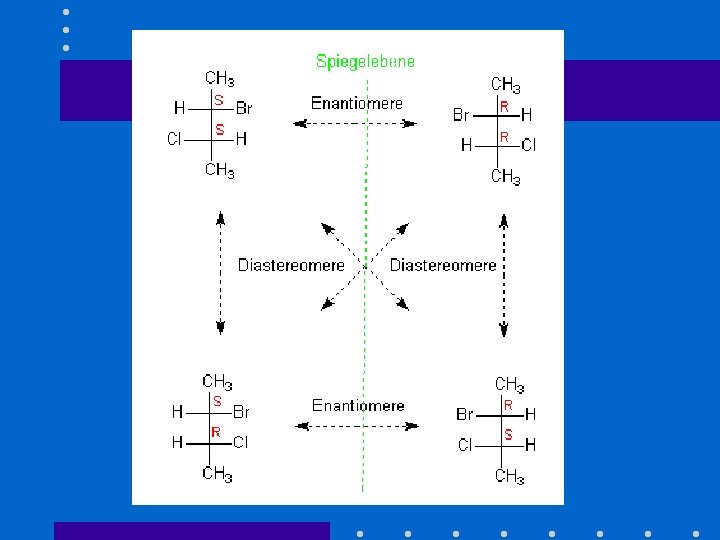
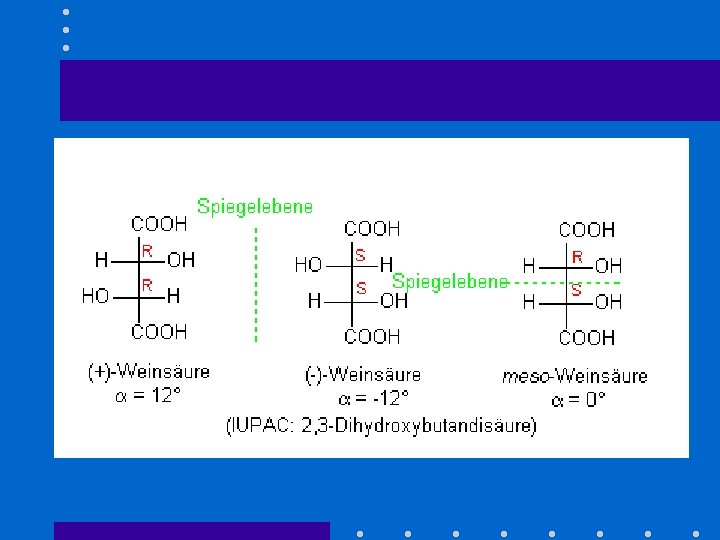

Chiralität = Asymmetrie ? • Symmetrieelemente – Spiegelebenen – Drehachsen – Inversionzentren polare Achsen sind erlaubt • Mesoweinsäure • Quarzkristalle

Begriffe • • Racemat Konglomerat racemische Mischung chirale Verbindung optisch-aktive Verbindung Enantiomere Diastereomere

Chiralität in der Natur • • • Eindeutigkeit von Reaktionen Stabilisierung (Helices) Richtungsabhängige Eigenschaften Entstehung der Chiralität ? ? Quantifizierung von Chiralität

6. Nukleophile Substitution • • • Reaktionswege Übergangszustand / Zwischenprodukte S N 1 / S N 2 Carbeniumionen Nukleophilie <-> Basizität

Beispiele: Nukleophile Subst. • OH- + CH 3 Cl • H-OH + C(CH 3)3 Cl • Video: Salomons • (Eierkarton)

• Reaktionsverläufe Energiediagramme, Reaktionskoordinate • Kinetik / Thermodynamik
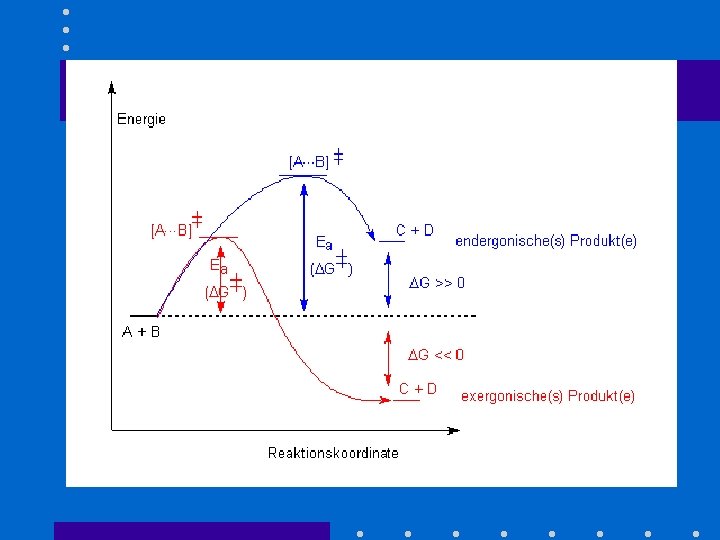
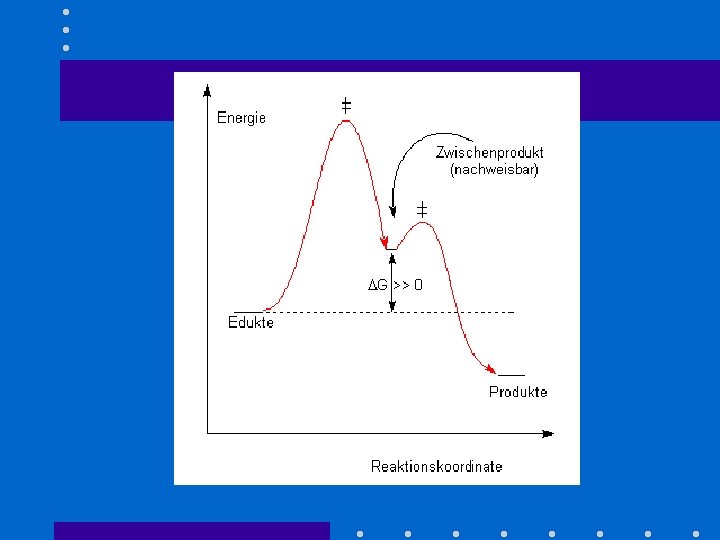

Begriffe • elektrophil = „elektronenliebend“ • nucleophil = „kernliebend“ • SN : Nu- + R-X R-Nu + X • Base Lewis, Brønsted • Nukleophilie Basizität - Target, Polarisierbarkeit, Raumbedarf
![SN 1 -Reaktion • Geschwingkeitsgesetz erster Ordnung -d[RX]/dt = k 1[RX] • Dreibindige, trigonale SN 1 -Reaktion • Geschwingkeitsgesetz erster Ordnung -d[RX]/dt = k 1[RX] • Dreibindige, trigonale](http://slidetodoc.com/presentation_image_h/df5b4f1ed7117ca268f38f408d433bdb/image-24.jpg)
SN 1 -Reaktion • Geschwingkeitsgesetz erster Ordnung -d[RX]/dt = k 1[RX] • Dreibindige, trigonale Zwischenstufe Carbeniumion als Zwischenprodukt • Nebenprodukte – Eliminierungen zu Olefinen – Umlagerungen • Solvatation von Kation + Anion

Carbeniumion • sp 2 • Hyperkonjugation • I-Effekte, M-Effekte
![SN 2 -Reaktion • Geschwingkeitsgesetz zweiter Ordnung -d[RX]/dt = k 2[RX][Y] • Trigonale Bipyramide SN 2 -Reaktion • Geschwingkeitsgesetz zweiter Ordnung -d[RX]/dt = k 2[RX][Y] • Trigonale Bipyramide](http://slidetodoc.com/presentation_image_h/df5b4f1ed7117ca268f38f408d433bdb/image-26.jpg)
SN 2 -Reaktion • Geschwingkeitsgesetz zweiter Ordnung -d[RX]/dt = k 2[RX][Y] • Trigonale Bipyramide als Übergangszustand • Stereospezifisch (Walden-Umkehr) • Nebenprodukte lassen sich besser vermeiden • Solvatisierung des Übergangszustandes (aprotisch)

Geschwindigkeit der SN 2 • Austrittsvermögen der Abgangsgruppe • Nukleophile der Eintrittsgruppe • Sterische Anforderungen des Übergangszustandes • Solvatation

Austrittsvermögen Basenstärke gute Abgangsgruppen = schwache Basen I- > Br- > Cl- > FCl- > Ac. O- > OH- > NH 2 - > CH 3 - Gute Abgangsgruppen Ms, Ts, Sulfate Schlechte Abgangsgruppen OH (-> Ts, H+)

Reaktivität RX RCH 3 R`CH 2 R 2‘CHR 3 C- S N 1 nicht langsam gut S N 2 gut langsam extrem langsam

Nucleophilie • Basenstärke • Polarisierbarkeit HS- > I- > CN- > Br- > NH 3 > F- > CH 3 OH Tabelle Vollhardt, CH 3 I + Nu-

Lösungsmitteleffekte • SN 1 – polar protisch – Solvatation von Anion + Kation • SN 2 – (polar) aprotisch – Solvatation des Übergangszustandes keine Maskierung des

C-C-Verknüpfungen • Umpolung • Grignard-Verbindungen

7 Alkohole • -> nur Folien

8 Ether • Nur Folien

9 Amine • Nur Folien

Zur Organisation • Folien/Internet/Materialien – http: //liqcryst. chemie. uni-hamburg. de/oc 1/ • Elektronische Medien – M. Kinder CD (OC, 2461) – Salomons/Fryhle: Organic Chemistry • Versuche • Vorkommen in der Natur • Englisch: heute Alkohole

10 Alkene • • Elektronische Struktur, Phys. Eigenschaften Nomenklatur Darstellung Reaktionen Allyl-Verbindungen Konjugierte Alkene Vorkommen in der Natur

10. 3 Darstellungen der Alkene • Eliminierungsreaktionen – E 1 – E 2 • Saytzev (Sayzeff) / Hofmann • Crack-Verfahren • Hydrierungen von Alkinen • Wittig (später: -> Carbonyle)

10. 4 Reaktionen der Alkene • Elektrophile Additionen – Markownikow / Anti-Markownikow • • • Hydroborierung Hydroxylierungen Epoxidierungen Ozonolyse Hydrierungen (Salomons-Video)

• Isolierte Doppelbindungen • Allyl-Gruppe (Benzyl-Gruppe) • Kumulierte Doppelbindungen • Konjugierte Doppelbindungen

10. 5 Allylgruppe • Reaktion Br-CH 2 -CH=CH 2 + OH- (Tafel) • Orbitale (Videos aus Salomons)

10. 6 Kumulierte Alkene • • Allene MO, sp / sp 2 Hybridisierung Chiralität („verzerrter Tetraeder“) Stereochemie: cis/trans <-> R/S

10. 7 Konjugierte Alkene • • • Butadien, Hexatrien p-Orbitale 1, 4 -Additionen

10. 8 Diels-Alder-Reaktion • • • Butadien + Ethen (Tafelbild) Videos (Salomons) Erklärung 1: SHOC Erklärung 2: HOMO/LUMO, einfache MOs Erklärung 3: Woodward-Hoffmann, MO Acrolein

Begriffe • • elektrocyclische Reaktionen pericyclische Reaktionen HOMO/LUMO endo/exo

• Zunächst: – Völlig unverständliche Reaktion • Später: – Perfekte Beschreibung durch die Theorie – CASD (Computer Assisted Synthesis Design) • Probleme: – Retrosynthetisch schwer zu erkennen

Ursprung von Reaktivität • Überlappung teilbesetzter Orbitale – (gemeinsamer Raum, gleiche Energie) • Reaktionsklassen – Radikalische Reaktionen – Elektrophile/Nukleophile Reaktionen (‚polar‘) – Elektrocyclische Reaktionen – Redox-Reaktionen • Reaktionssteuerung – Kinetik (Aktivierungsenergie <-> RT) – Thermodynamik

10. 9 natürliche Alkene • (moderate) Reaktivität – Vernetzung (Kauschuk, Leinöl, . . ) • Differenzierung • Signalstoffe – Sphäromone, Hormone • Mechanik: Schmierstoffe, Fette • Optik: Farben, Schalten, Sehen

Olefine in der Natur: Beispiele • • • Ethen Prostaglandine Ölsäure Vitamin A Squalen
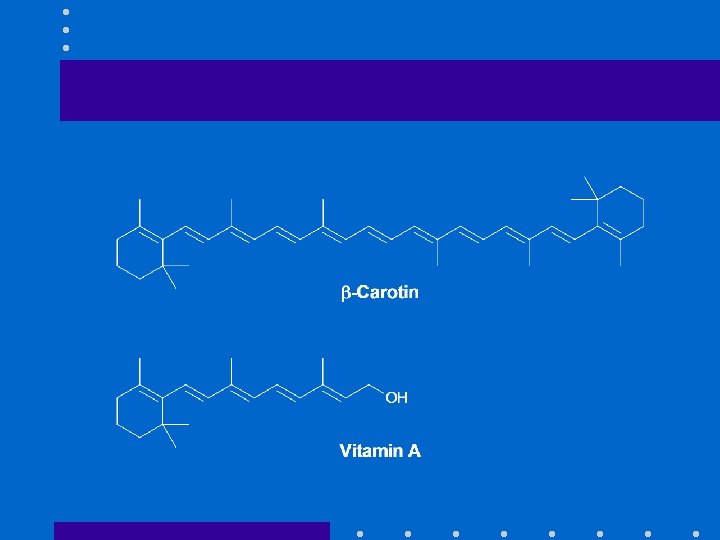

Technische Anwendungen • Polymerisation • Metathese • Photonik

11 Alkine • • Beispiel Ethin M. Kinder CD Nomenklatur Säurestärke, Linearität

11. 2 Darstellung der Alkine • Hydrolyse von Calciumcarbid • Eliminierung von Dihalogeniden – 1, 1 - oder 1, 2 - subst. – Aus Alkene durch Addition/Elimierung • Alkylierungsreaktionen – (Alkinylanionen als Nukleophil)

11. 3 Reaktionen der Alkine • Hydrierungen • Elektrophile Additionen • Cyclisierung zu Benzen – (s. a. Endiiene) • Deprotonierung, Nukleophile Subst.
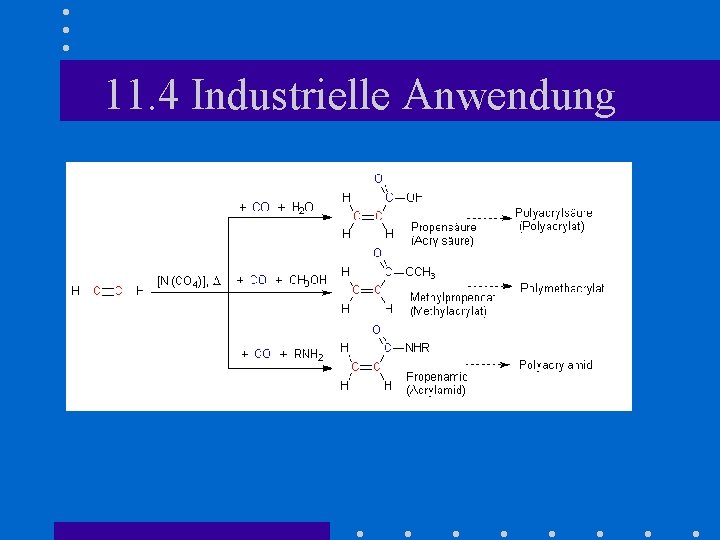
11. 4 Industrielle Anwendung
- Slides: 55