5 OPTIKAI SPEKTROSZKPIA 1 5 1 A BornOppenheimer

5. OPTIKAI SPEKTROSZKÓPIA 1

5. 1 A Born-Oppenheimer közelítés 2

A Born-Oppenheimer közelítést a többatomos molekulák Schrödinger-egyenletére alkalmazzák.
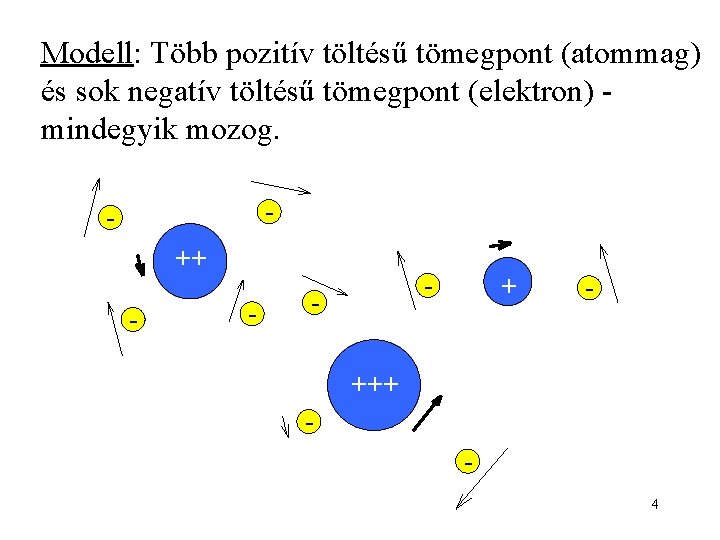
Modell: Több pozitív töltésű tömegpont (atommag) és sok negatív töltésű tömegpont (elektron) mindegyik mozog. - ++ - - + - +++ 4

A Schrödinger-egyenlet általános formában 5
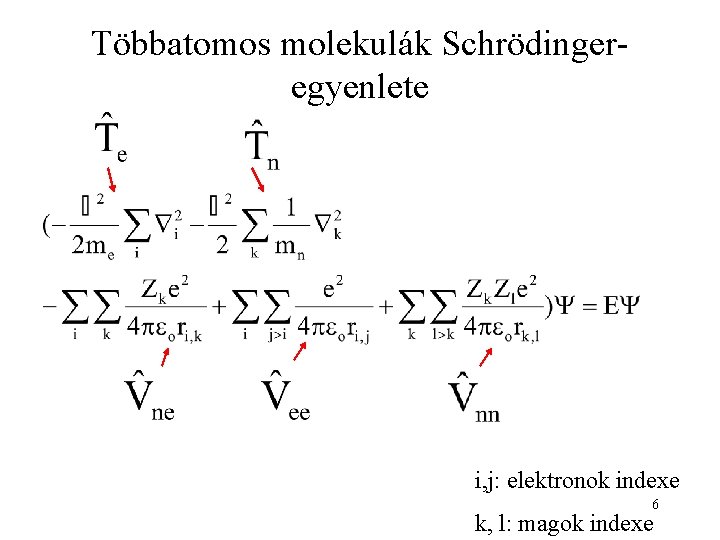
Többatomos molekulák Schrödingeregyenlete i, j: elektronok indexe 6 k, l: magok indexe

A többelektronos atomok Schrödinger-egyenlete sem oldható meg analitikusan, ez még kevésbé. 7

Max Born (1882 -1970) Robert Oppenheimer (1904 -1967) 8


A megoldáshoz használt közelítés • Born-Oppenheimer-közelítés – különválasztjuk az atommagok és az elektronok mozgását (Indoklás: a magok sokkal nehezebbek, így lassabban mozognak, mint az elektronok), és két külön Schrödingeregyenletet írunk fel. – Elektronok mozgása: álló magok terében röpködnek az elektronok – Magok mozgása: a magok a hozzájuk tapasztott elektronokkal mozognak (Elefántcsorda és a legyek…) 10

Elektronok mozgása: rögzített magokat tartalmazó molekula Schrödinger-egyenlete kimarad konstans Egyensúlyi geometria: minimális 11

Magok mozgása: mozgó magokat és tapasztott elektronokat tartalmazó molekula Schrödinger-egyenlete Ez az egyenlet elválaszthatatlan az előzőtől! : a magokhoz csatolt elektronok mozgásának figyelembevétele, azt fejezi ki, hogy a magok elmozdulásával megváltozik az elektronállapot. A magok helyzetét szisztematikusan változtatjuk, az egyes helyzetekben megoldjuk az Ee-re vonatkozó (előző) egyenletet. A magokra vonatkozó egyenlet tehát az elektronmozgásra vonatkozó egyenletek sorát jelenti. 12

További közelítés: a magok mozgására felírt Schrödinger-egyenlet felbontása A forgó mozgás sokkal lassabb, mint a rezgőmozgás. : forgó mozgás (rotáció) : rezgő mozgás (vibráció) 13

Ezek alapján a molekula mozgása felbontható az alábbi összetevőkre: 1. Az elektronok mozgása a rögzített magok terében 2. A magok rezgése 3. A rögzített magok közös forgása 14

Az elektronok mozgásához tartozó kvantált állapotok: Ee 0, Ee 1, Ee 2…. Ezen állapotok közötti átmenet ultraibolya vagy látható fény elnyelésével jár. 15

A rezgőmozgáshoz tartozó kvantált állapotok: Ev 0, Ev 1, Ev 2…. Ezen állapotok közötti átmenet infravörös sugárzás elnyelésével jár. 16

A forgó mozgáshoz tartozó kvantált állapotok: Er 0, Er 1, Er 2…. Ezen állapotok közötti átmenet mikrohullámú sugárzás elnyelésével jár. 17

Elektrongerjesztési /UV-látható spektroszkópia Rezgési / infravörös spektroszkópia Optikai spektroszkópia Forgási / mikrohullámú spektroszkópia 18

5. 2. Az optikai színképek jellemzői 19

A színképek jellemzőit nézzük meg az alábbi példán: „Níluskék A” festék UV-látható színképe oldószer acetonitril, c = 2 10 -5 mol/dm 3. 20
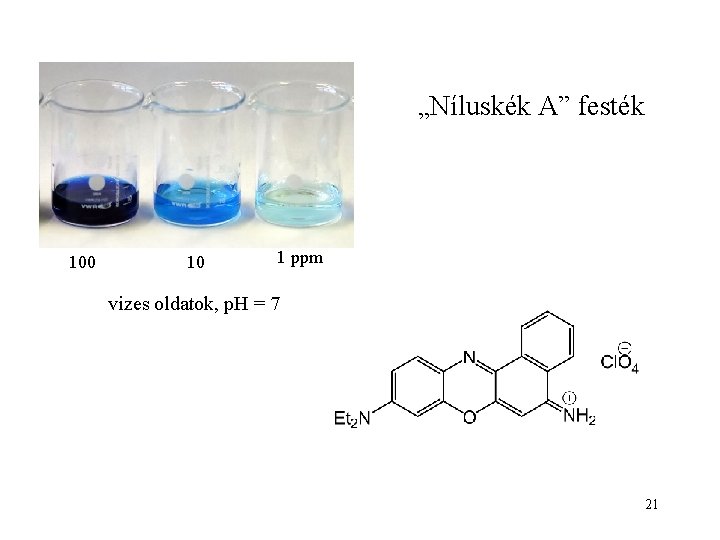
„Níluskék A” festék 100 10 1 ppm vizes oldatok, p. H = 7 21
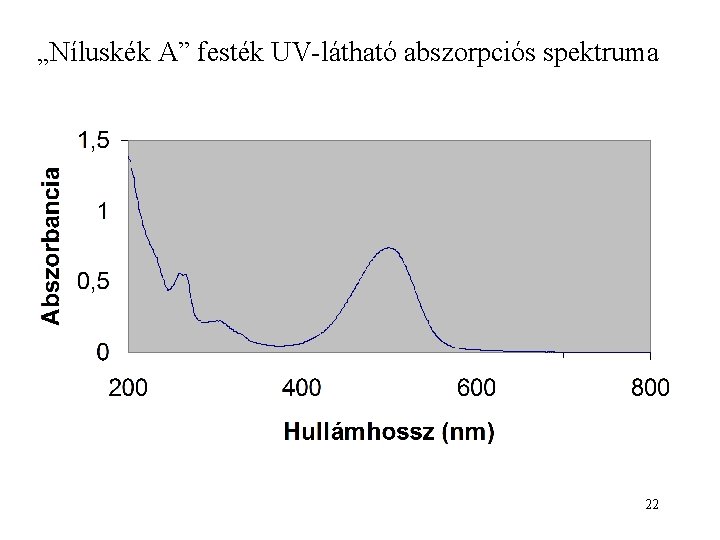
„Níluskék A” festék UV-látható abszorpciós spektruma 22
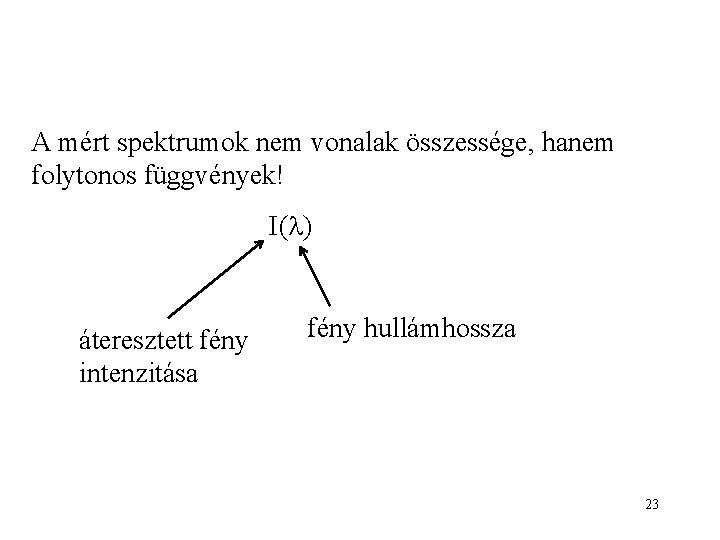
A mért spektrumok nem vonalak összessége, hanem folytonos függvények! I( ) áteresztett fény intenzitása fény hullámhossza 23

A hullámhossz megadása UV-látható színkép: az elnyelt fény hullámhossza ( , nm-ben) Infravörös színkép: az elnyelt fény hullámszáma ( * 1/ , cm-1 -ben) Mikrohullámú színkép: az elnyelt fény frekvenciája ( MHz, GHz-ben) 24
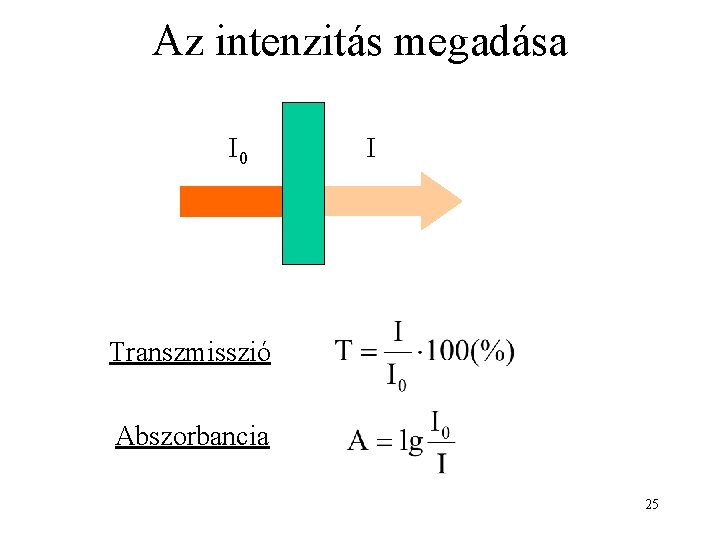
Az intenzitás megadása I 0 I Transzmisszió Abszorbancia 25

Lambert - Beer törvény abszorciós koefficiens (dm 3 mol-1 cm-1) c koncentráció (mol/dm 3) úthossz (küvettavastagság) (cm) Az abszorbancia arányos a koncentrációval! 26

A spektrumsávok jellemzői - a sávmaximum adatai - a sávok intenzitása - a sávok szélessége 27

A sávok jellemzőinek megadása A sávmaximumok adatait tüntetik fel max, vagy *max — Amax, vagy max formájában max független a koncentrációtól! A sávintenzitást a sáv alatti területként értelmezik: A sáv szélességét félértékszélesség formájában adják meg: 1/2, ill. *1/2 az Amax/2 -höz tartozó két spektrumpont távolsága 28
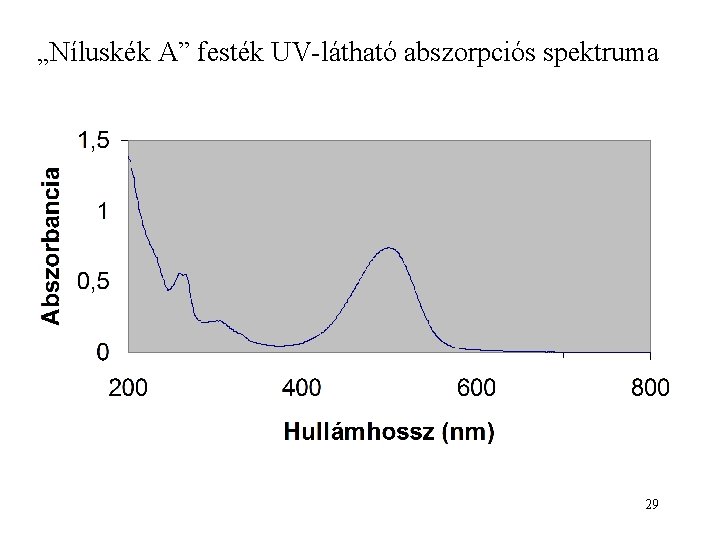
„Níluskék A” festék UV-látható abszorpciós spektruma 29
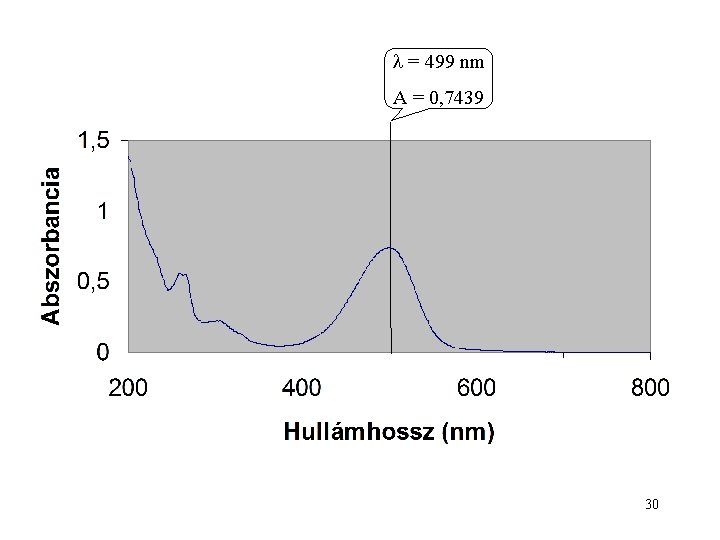
= 499 nm A = 0, 7439 30
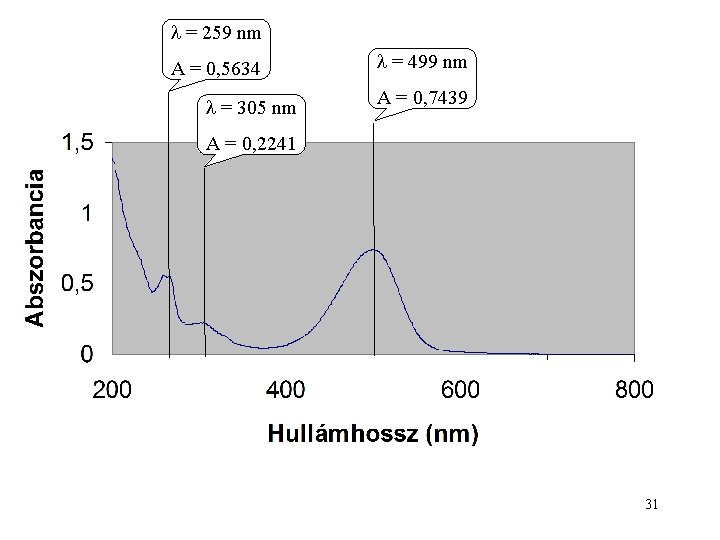
= 259 nm A = 0, 5634 = 305 nm = 499 nm A = 0, 7439 A = 0, 2241 31
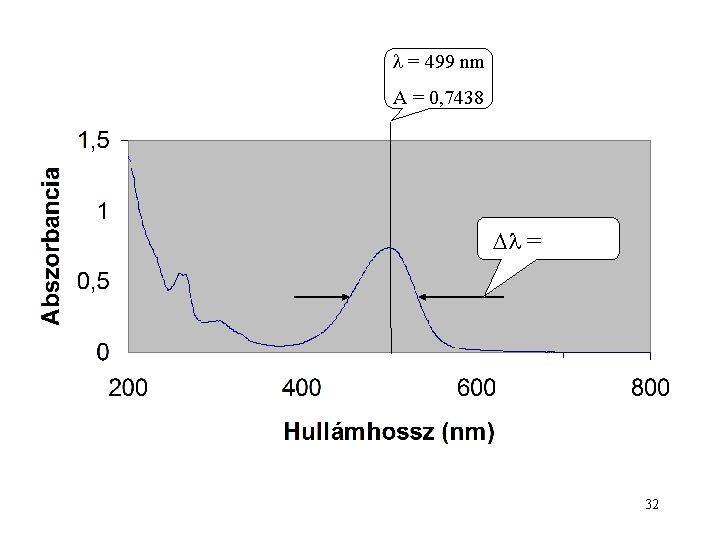
= 499 nm A = 0, 7438 = 32
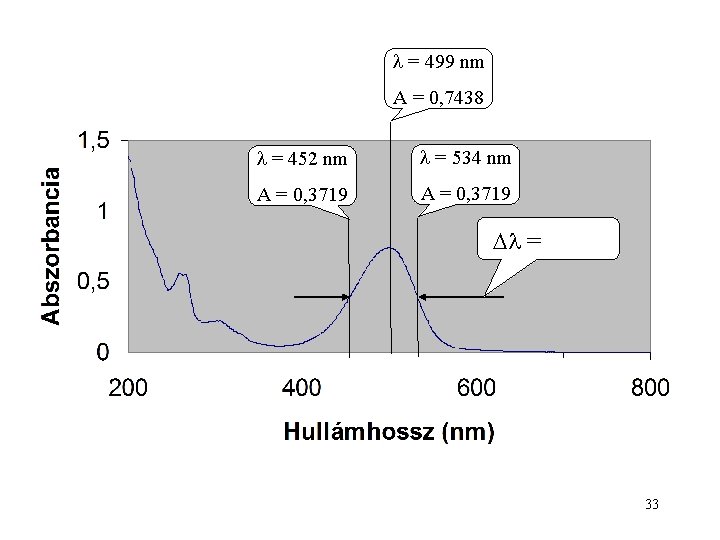
= 499 nm A = 0, 7438 = 452 nm = 534 nm A = 0, 3719 = 33
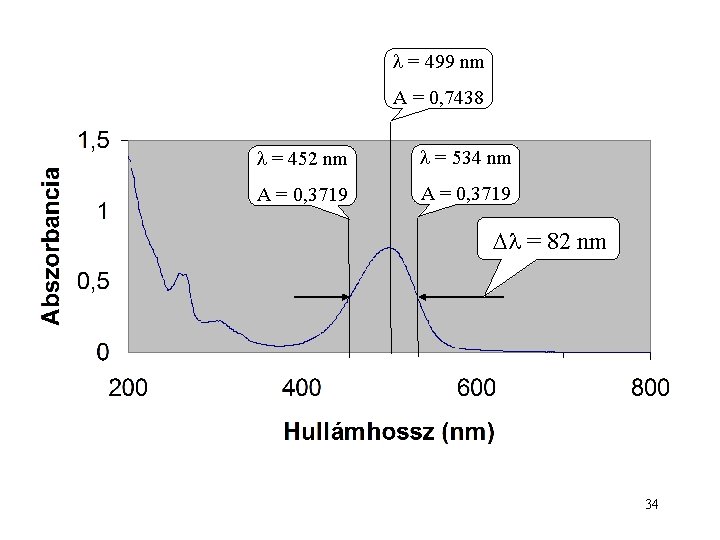
= 499 nm A = 0, 7438 = 452 nm = 534 nm A = 0, 3719 = 82 nm 34

5. 3. Az optikai színképek értelmezése A kísérleti spektrum adatai és a molekula Schrödinger-egyenletének megoldásával kapott sajátértékek/sajátfüggvények kapcsolata 35
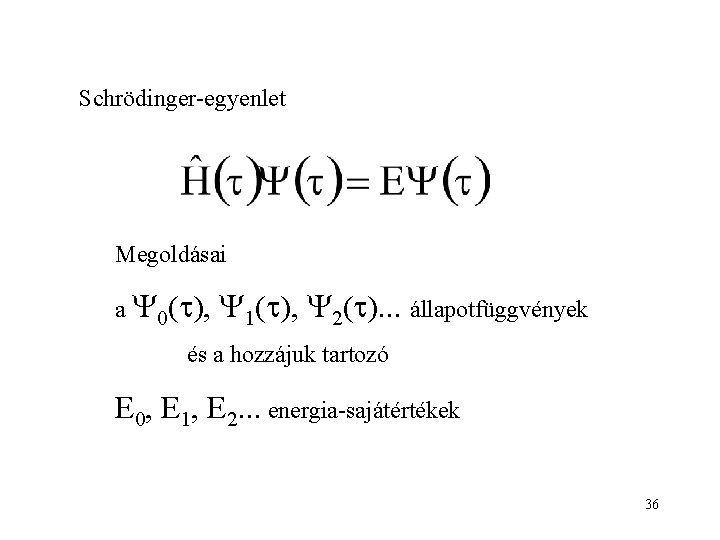
Schrödinger-egyenlet Megoldásai a 0( ), 1( ), 2( ). . . állapotfüggvények és a hozzájuk tartozó E 0, E 1, E 2. . . energia-sajátértékek 36
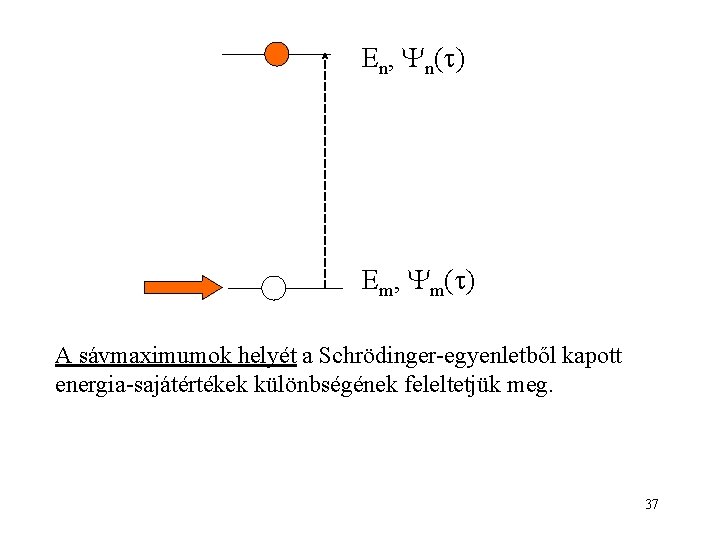
En, n( ) Em, m( ) A sávmaximumok helyét a Schrödinger-egyenletből kapott energia-sajátértékek különbségének feleltetjük meg. 37
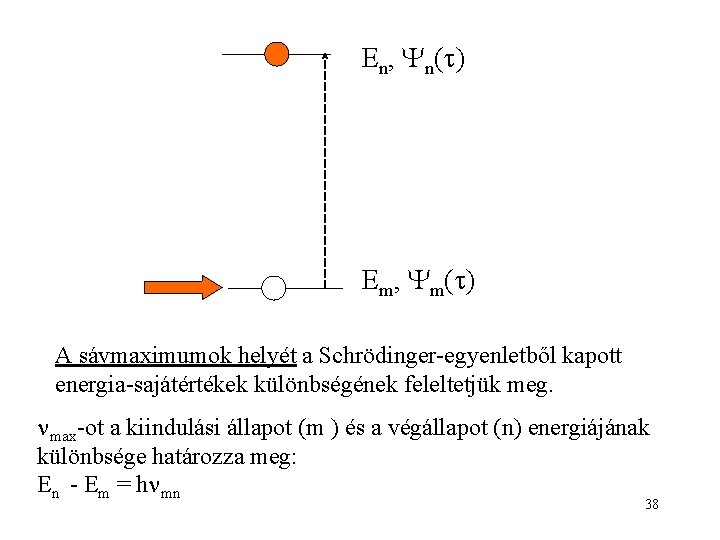
En, n( ) Em, m( ) A sávmaximumok helyét a Schrödinger-egyenletből kapott energia-sajátértékek különbségének feleltetjük meg. max-ot a kiindulási állapot (m ) és a végállapot (n) energiájának különbsége határozza meg: En - Em = h mn 38
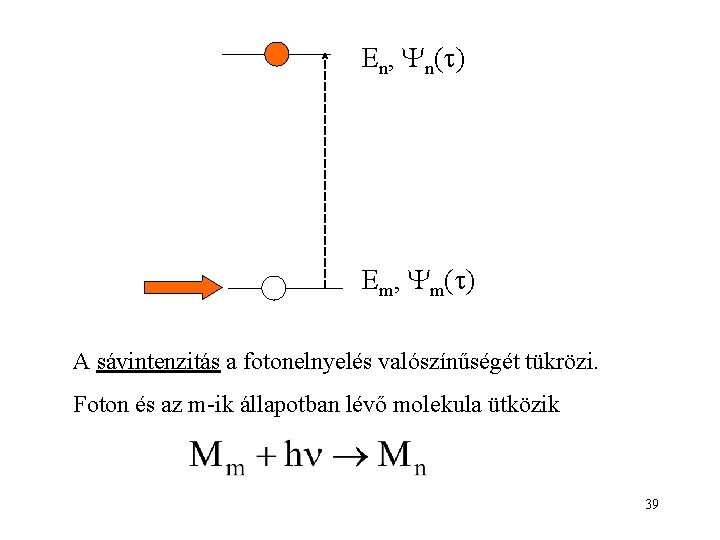
En, n( ) Em, m( ) A sávintenzitás a fotonelnyelés valószínűségét tükrözi. Foton és az m-ik állapotban lévő molekula ütközik 39

„Bimolekuláris reakció!” 40

„Bimolekuláris reakció!” Sebességi egyenlet: Nm : kisebb energiájú molekulák koncentrációja : a fotonok koncentrációja Amn : az abszorpció sebességi állandója 41

Amn összekapcsolja a mért sávintenzitásokat a Schrödingeregyenletből kapott ( ) állapotfüggvényekkel! Kapcsolat a sávintenzitással: NA Avogadro-szám h Planck-állandó c fénysebesség 42

Kapcsolat az állapotfüggvényekkel: Rmn a ún. átmeneti momentum 43

Az átmeneti momentum és a dipólusmomentum , ahol a dipólusmomentum operátora qi az i-edik részecske töltése, xi, yi, zi az i-edik részecske helykoordinátái 44

A sávszélesség A Schrödinger-egyenlet modellje olyan molekula, amely - izolált a többi molekulától, - forog, rezeg, stb. de a tömegközéppontja rögzített, - állapotainak élettartama végtelennek tekinthető („stacionárius állapotok”). 45

A spektrumvonalak kiszélesedése sávvá az alábbi okokra vezethető vissza: 1. Molekulák közötti kölcsönhatások. A térben egymáshoz közel elhelyezkedő molekulák perturbálják egymás energiaszintjeit, ezért az éles energiaszintek kiszélesednek. A hatás nem kvantált. Szilárd, folyadék és nagynyomású gáz állapotban ez a hatás szabja meg a sávszélességet. 46

2. Doppler-effektus: a gázminták molekulái különböző irányokban, különböző sebességgel mozognak. A detektorhoz viszonyított sebességük módosítja az abszorpciós frekvenciát: A sáv alakja a molekulák (nem kvantált) sebességeloszlását tükrözi. 47


3. Természetes vonalkiszélesedés (Fourier-limit) A molekula állapotainak véges élettartama korlátozza a hozzájuk tartozó energiaértékek pontosságát: Kiindulási állapot kiszélesedése: m Em h Végállapot kiszélesedése: n En h A határozatlansági reláció egyik megnyilvánulása! Ez határozza meg az elvileg elérhető minimális sávszélességet! Impulzusüzemű (gáz)lézerek vonalszélességét határozhatja meg. 49
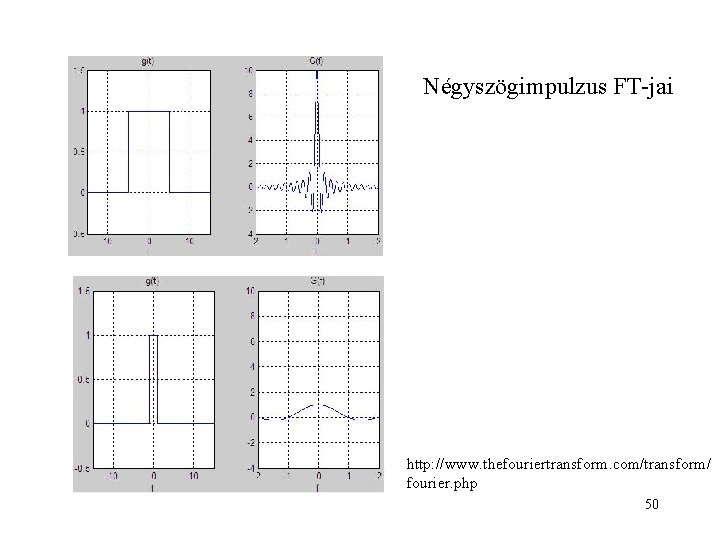
Négyszögimpulzus FT-jai http: //www. thefouriertransform. com/transform/ fourier. php 50

Joseph Fourier (1768 – 1830) 51
- Slides: 51