5 5 Mlange acide faible base faible Soit

5. 5) Mélange acide faible base faible. Soit une solution contenant de l ’acide méthanoïque et du méthanoate de sodium aux concentrations apportées respectivement égales à C 1 et C 2. Donnée : HCOOH/HCOO- : p. Ka = 3, 8 Dissolution de HCOONa : Recherche R. P. : p. Ka OH- 14, 0 H 2 O HCOONa (s) n H 2 O = HCOO- (aq) + Na+ (aq) Réactions : R 1 : HCOOH + HCOO- = HCOO- + HCOOH R 2 : HCOOH + H 2 O = HCOO- + H 3 O+ R 3 : HCOO- + H 2 O= HCOOH + OH- R 4 : 2 H 2 O = H 3 O+ + OH- HCOOH 2 O 3, 8 0 HCOOH H 3 O+ Constantes : 1 1, 6 10 -4 6, 3 10 -11 Ke
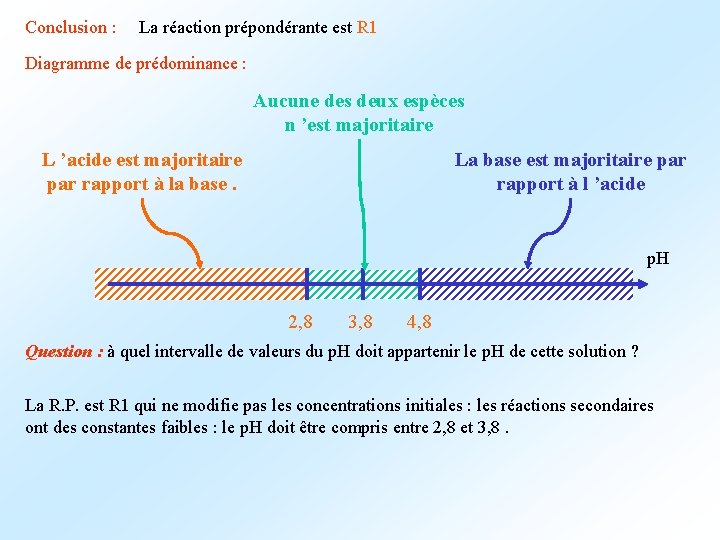
Conclusion : La réaction prépondérante est R 1 Diagramme de prédominance : Aucune des deux espèces n ’est majoritaire L ’acide est majoritaire par rapport à la base. La base est majoritaire par rapport à l ’acide p. H 2, 8 3, 8 4, 8 Question : à quel intervalle de valeurs du p. H doit appartenir le p. H de cette solution ? La R. P. est R 1 qui ne modifie pas les concentrations initiales : les réactions secondaires ont des constantes faibles : le p. H doit être compris entre 2, 8 et 3, 8.

Calcul : C 1 = C 2 = 0, 10 mol. L-1. Rappel La R. P. est R 1 qui ne modifie pas les concentrations initiales. Si les constantes K A 0 et KB 0 très inférieures à 1 : les concentrations de l ’acide faible et de la base faible demeurent inchangées. p. H ? La concentration des ions oxonium est contrôlée par l ’équilibre : HCOOH + H 2 O = HCOO- + H 3 O+ avec équilibre de contrôle. [H 3 O+] = p. H = d ’où - log([H 3 O+]) = p. H = soit

A. N. : p. H = 3, 8 Question : des deux réactions secondaires R 2 et R 3 , laquelle peut poser problème ? Celle qui a la constante la plus élevée , c ’est à dire R 2 Question : comment vérifier que cette réaction est négligeable ? Une réaction secondaire est négligeable si les produits qu ’elle forme sont minoritaires par rapport aux produits de la R. P. Ici, celà revient à vérifier que les ions oxonium sont minoritaires par rapport à l ’acide méthanoïque et aux ions méthanoate. [H 3 O+] = soit 1, 6 10 -4 mol. L-1 [H 3 O+] << [HCOOH] et [HCOO-] Application : Calculer p. H pour C 1 = C 2 = 5, 0 10 -4 mol. L-1

5. 6) Application : R. P. quantitative. Solution A : acide méthanoïque de concentration CA = 0, 100 mol. L-1 Solution B : hydroxyde de sodium de concentration CB = 0, 100 mol. L-1 On mélange un volume VA = 20, 0 m. L de solution A et un volume VB = 10, 0 m. L de solution B. Calculer le p. H de la solution obtenue. Données : p. KA(HCOOH/HCOO-) = 3, 8 n H 2 O dissolution de Na. OH : Na. OH (s) = Na+ (aq) + OH- (aq) l’acide méthanoïque est un acide faible Calcul des concentrations apportées dans le mélange : CA ’ = 6, 67 10 -2 mol. L-1 CB ’ = 3, 33 10 -2 mol. L-1
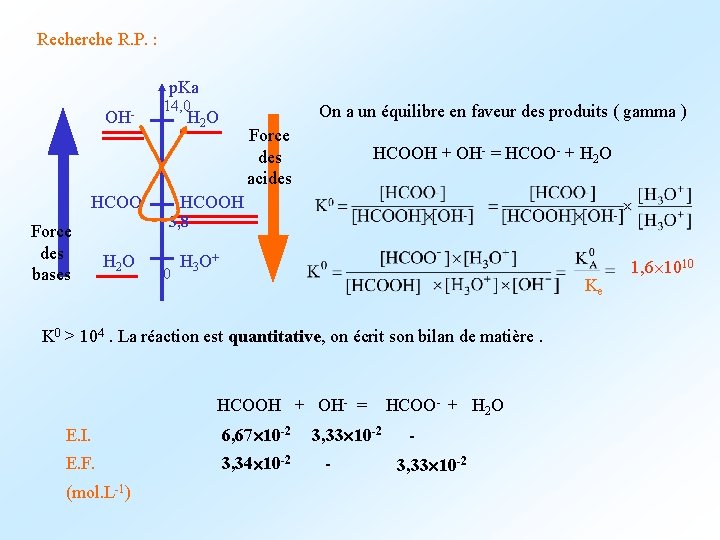
Recherche R. P. : p. Ka OH- HCOOForce des bases H 2 O 14, 0 On a un équilibre en faveur des produits ( gamma ) H 2 O Force des acides HCOOH + OH- = HCOO- + H 2 O HCOOH 3, 8 0 H 3 O+ Ke K 0 > 104. La réaction est quantitative, on écrit son bilan de matière. HCOOH + OH- = HCOO- + H 2 O E. I. 6, 67 10 -2 E. F. 3, 34 10 -2 (mol. L-1) 3, 33 10 -2 - 3, 33 10 -2 1, 6 1010

Recherche R. P. sur le nouveau système : On a une solution de l ’acide faible HCOOH et de sa base faible conjuguée HCOO- , p. Ka solution dite ? solution tampon OH- HCOOForce des bases H 2 O 14, 0 H 2 O Force des acides HCOOH + HCOO- = HCOO- + HCOOH de constante K 10 = 1 HCOOH réactions secondaires ? 2 acide avec l ’eau : HCOOH + H 2 O = HCOO- + H 3 O+ H 3 O+ 3 base avec l ’eau : HCOO- + H 2 O = HCOOH + OH- 3, 8 0 R. P. ? 4 autoprotolyse de l ’eau : parmi ces trois réactions , laquelle doit éventuellement être prise en compte ? 2 car Calcul du p. H : conséquence ? formule ? 1, 58 10 -4 hypothèse ? 6, 31 10 -11 les réactions secondaires et surtout R 2 sont négligeables la composition du système n ’est pas modifiée ou les concentrations de l ’acide et de la base restent inchangées. A. N. : p. H = 3, 8

Validité de ce résultat ? Il est cohérent avec la composition du système ( [HCOOH] [HCOO-] ) puisque : p. H est compris entre 2, 8 et 4, 8. R 2 négligeable ? R 2 est négligeable si les produits qu’elle formes ont minoritaires par rapport aux produits de la R. P. Comment le vérifier ? [H 3 O+] = Conclusion ? 10 -p. H = En comparant [H 3 O+] à [HCOOH] et [HCOO-] 1, 58 10 -4 mol. L-1 le résultat est valide puisque les ions oxonium sont minoritaires par rapport à HCOOH et HCOO-.

5. 5) Mélange acide faible base faible. Retour Soit une solution contenant de l ’acide méthanoïque et du méthanoate de sodium aux concentrations apportées respectivement égales à C 1 et C 2. Donnée : HCOOH/HCOO- : p. Ka = 3, 8 Dissolution de HCOONa : Recherche R. P. : p. Ka OH- 14, 0 H 2 O HCOONa (s) n H 2 O = HCOO- (aq) + Na+ (aq) Réactions : R 1 : HCOOH + HCOO- = HCOO- + HCOOH R 2 : HCOOH + H 2 O = HCOO- + H 3 O+ R 3 : HCOO- + H 2 O= HCOOH + OH- R 4 : 2 H 2 O = H 3 O+ + OH- HCOOH 2 O 3, 8 0 HCOOH H 3 O+ Constantes : 1 1, 6 10 -4 6, 3 10 -11 Ke

- Slides: 10