5 10 Les composs binaires molculaires 5 10

5. 10 - Les composés binaires moléculaires

5. 10 Les composés moléculaire Donc que ce passe-t-il lorsqu’un non-métal réagis avec un autre non-métal?

Les composés avec les liaisons covalentes sont appelés des composés moléculaires ex: eau, sucre , CO 2, … Liaisons covalentes: covalentes Les atomes partagent les électrons ex: Cl – Cl O=O H–O–H Composé moléculaire = non-métal + non-métal (ex: NO 2)

Propriétés des Composés moléculaire: -Points de fusion et d’ébullition bas (ils ne forment pas de réseau cristallin, et les molécules individuels bougent plus rapidement) -Basse solubilité (car les atomes des composés moléculaire partagent des couches de valence, et sont moins attirés aux molécules d’eau) -Basse conductivité (car il n’y a pas d’ions, et les électrons ne voyagent pas facilement d’une molécule à l’autre. )

Nommer les composés moléculaires • C’est la mème que les composés ioniques. • Écrivez le moins métallique non-métal première (plus à droite sur la table périodique), puis ajouter «URE» . • Ajoutez les préfixes indiquant le nombre de chaque type d'atome dans le molécule, sauf quand le 1 er élément a un seul atome Ex : H 2 O P 2 O 3 CO N’écrit pas le préfixe “mono” ici
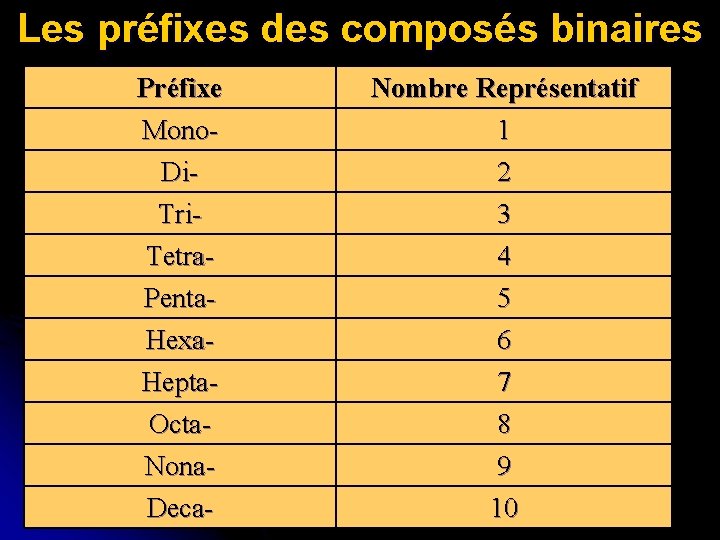
Les préfixes des composés binaires Préfixe Mono. Di. Tri. Tetra- Nombre Représentatif 1 2 3 4 Penta. Hexa. Hepta. Octa. Nona. Deca- 5 6 7 8 9 10
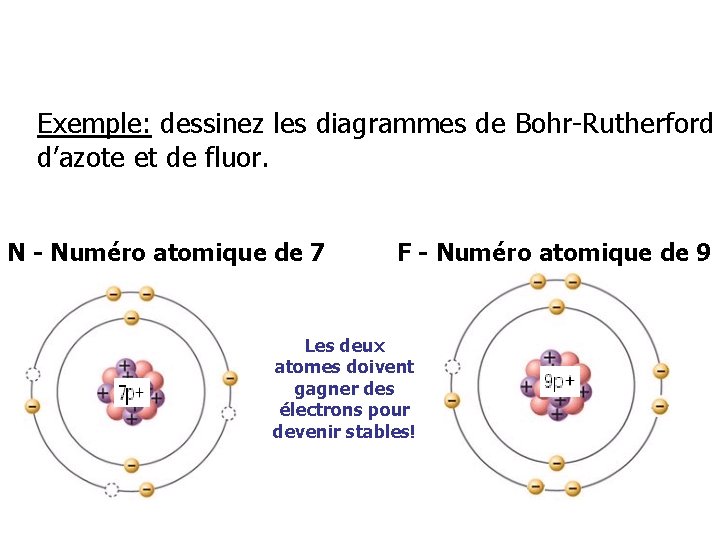
Exemple: dessinez les diagrammes de Bohr-Rutherford d’azote et de fluor. N - Numéro atomique de 7 F - Numéro atomique de 9 Les deux atomes doivent gagner des électrons pour devenir stables!

Pour que les deux atomes deviennent stables, ils doivent partager des électrons. (Cela nécessite parfois plus qu’un atome d’un ou des deux éléments. )

Travail l Questions: p. 212 #1 -10 l Feuilles de travail
- Slides: 9