4 COURS DE STRUCTURE DE LA MATIRE Module













![Atome de Lithium Li, Z=3 : 1 s 2 2 s 1 ou [He] Atome de Lithium Li, Z=3 : 1 s 2 2 s 1 ou [He]](https://slidetodoc.com/presentation_image_h2/001ca8957a2165a4fd93be77f42ec789/image-18.jpg)
![4 Atome de Béryllium Be, Z=4 : 1 s 22 s 2 ou [He] 4 Atome de Béryllium Be, Z=4 : 1 s 22 s 2 ou [He]](https://slidetodoc.com/presentation_image_h2/001ca8957a2165a4fd93be77f42ec789/image-19.jpg)













- Slides: 37

4 COURS DE STRUCTURE DE LA MATIÈRE (Module Ph 13) 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 1

4 3) Les atomes polyélectroniques a) L’atome polyélectronique b) Règles de remplissage des couches et souscouches c) Règles de Slater 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 2

a) L’atome polyélectronique 4 Dans le cas d’un atome polyélectronique la résolution de l’équation de Schrödinger est impossible. Une méthode appelé méthode de Slater permet de déterminer les principales propriétés de l‘atome. on fait alors les approximations suivantes : Ø le noyau est immobile Ø on néglige les interactions entre les électrons Ø on affecte le noyau d’un numéro atomique effectif Z*eff en tenant compte du champ électrique des électrons. Z*eff = Z - i : coefficient de l’écran d’électron i 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 3

4 b) Règles de remplissage des couches et sous couches d’un atome polyélectronique La structure électronique d'un atome correspond à l'arrangement des électrons dans ses différentes orbitales atomiques. Deux principes régissent la structure électronique des atomes: Principe de stabilité: les électrons vont se placer le plus près possible du noyau dans les orbitales de plus basses énergies. Dans son état fondamental, la stabilité de l’atome est maximale. Principe d'exclusion de Pauli : dans un atome, chaque électron doit posséder un jeu de quatre nombres quantiques différents. En conséquence, une orbitale définie par les nombres quantiques n, l, l, m ne peut contenir que deux électrons au maximum qui différent par leur quatrième nombre quantique et donc s = + 1/2 ou s = - 1/2. 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 4

4 Règle de Hund Les électrons occupent un maximum d'orbitales définies par le nombre quantique azimutal l avant de s’apparier c’est à dire avant de les compléter par un deuxième électron de spin opposé. Il y’a donc deux types d’électrons: ü Electron célibataire: électron seul dans une orbitale. ü Electrons appariés : ou doublet d’électrons, deux électrons dans une même orbitale ne différent que par leur nombre quantique s (doublet électronique: un électron avec s = +1/2 et l'autre avec s = -1/2). 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 5

4 Si, dans une sous-couche p, d ou f, on a le choix entre deux électrons appariés ( un doublet d’électrons ) dans la même orbitale et deux électrons célibataires (non-appariés) dans deux orbitales de même énergie, la règle de Hund indique c'est la seconde solution qui est la moins énergétique. Exemple Soit deux électrons dans une sous-couche p. Il existe deux possibilités: Dans le cas (1), les électrons sont appariés (un électron avec s = +1/2 et l'autre électron avec s = -1/2), Dans le cas (2), ils sont parallèles (les deux valeurs de s sont égales). La règle de Hund indique la deuxième possibilité est la plus stable. 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 6

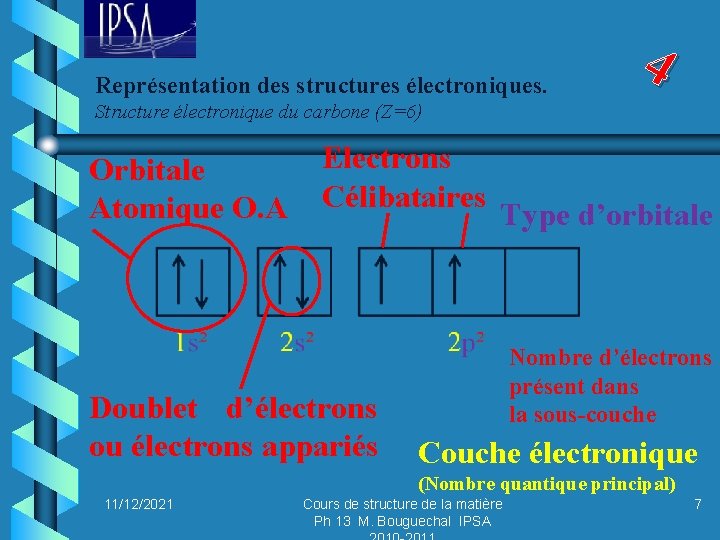
Représentation des structures électroniques. 4 Structure électronique du carbone (Z=6) Orbitale Atomique O. A Electrons Célibataires Doublet d’électrons ou électrons appariés Type d’orbitale Nombre d’électrons présent dans la sous-couche Couche électronique (Nombre quantique principal) 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 7

4 Ordre de remplissage des orbitales Les électrons d'un atome donné vont remplir les orbitales d'énergie croissante. Cette dernière dépendant des nombres quantiques n et l, 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 8

4 Pour retenir l'ordre de remplissage, il est commode d'utiliser la méthode proposée par Klechkowski Les sous couches d’un atome poly 6électronique sont occupés par les électrons par ordre croissants de l’énergie. Les électrons remplissent d’abord les niveaux de plus faibles énergie c’est à dire les niveaux les plus liés (plus proches du noyau). Ordre de remplissage : 1 s 2 s 2 p 3 s 3 p 4 s 3 d 4 p 5 s 4 d 5 p 6 s etc. … Règle de l’octet: Le nombre d’électrons maximum sur une couche de rang n est 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 2 n² 9

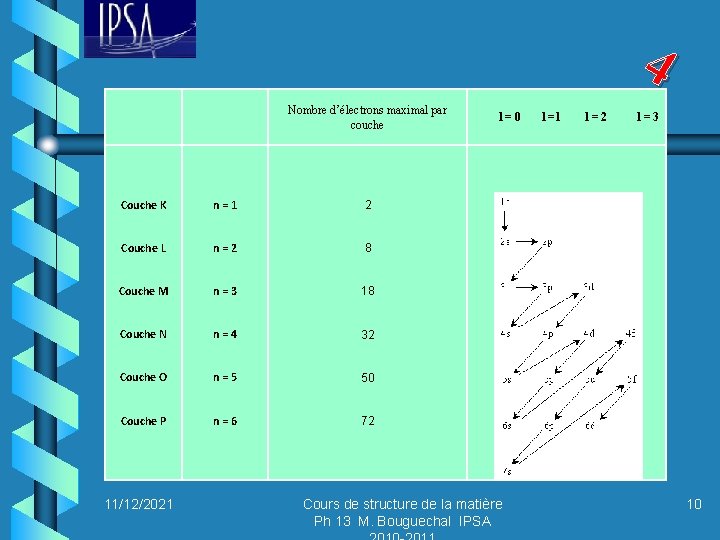
4 Nombre d’électrons maximal par couche Couche K n=1 2 Couche L n=2 8 Couche M n=3 18 Couche N n=4 32 Couche O n=5 50 Couche P n=6 72 11/12/2021 l=0 Cours de structure de la matière Ph 13 M. Bouguechal IPSA l =1 l=2 l=3 10

4 Nombre d’électrons maximal par orbitale atomique O. A s 2 électrons maximum et donc une case quantique 1 s 2 2 s 2 3 s 2 Si l’O. A contient un seul électron : 1 s 1 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 11

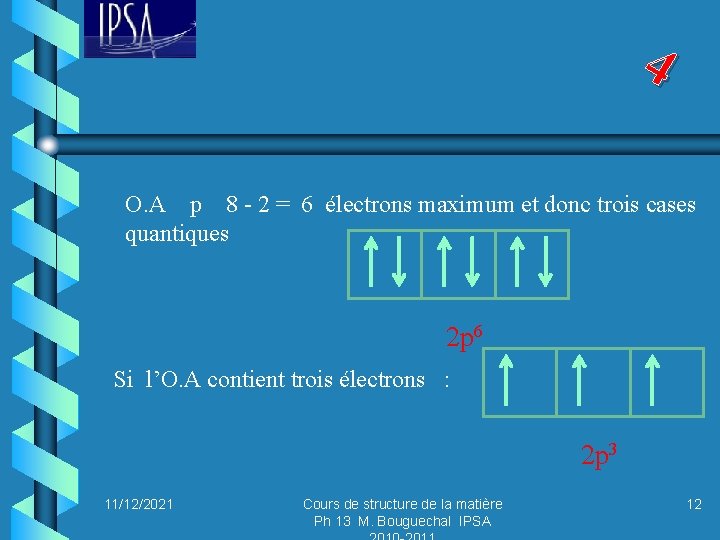
4 O. A p 8 - 2 = 6 électrons maximum et donc trois cases quantiques 2 p 6 Si l’O. A contient trois électrons : 2 p 3 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 12

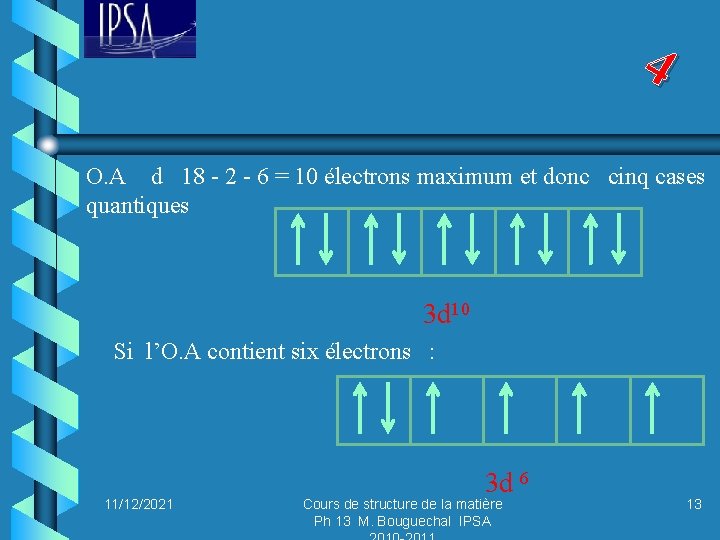
4 O. A d 18 - 2 - 6 = 10 électrons maximum et donc cinq cases quantiques 3 d 10 Si l’O. A contient six électrons : 11/12/2021 3 d 6 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 13

4 O. A f 32 -2 -6 -10 = 14 électrons maximum et donc sept cases quantiques 4 f 14 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 14

4 O. A g 50– 2 -6 -10 -14 = 18 électrons maximum et donc neuf cases quantiques 5 g 18 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 15

4 Ordre de remplissage, Méthode de Klechkowski 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 16

4 Atome d’hydrogène H, Z=1 : 1 s 1 Atome d’hélium He, Z=2 : 1 s 2 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 17
![Atome de Lithium Li Z3 1 s 2 2 s 1 ou He Atome de Lithium Li, Z=3 : 1 s 2 2 s 1 ou [He]](https://slidetodoc.com/presentation_image_h2/001ca8957a2165a4fd93be77f42ec789/image-18.jpg)
Atome de Lithium Li, Z=3 : 1 s 2 2 s 1 ou [He] 2 s 1 4 1 s 2 2 s 1 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 18
![4 Atome de Béryllium Be Z4 1 s 22 s 2 ou He 4 Atome de Béryllium Be, Z=4 : 1 s 22 s 2 ou [He]](https://slidetodoc.com/presentation_image_h2/001ca8957a2165a4fd93be77f42ec789/image-19.jpg)
4 Atome de Béryllium Be, Z=4 : 1 s 22 s 2 ou [He] 2 s 2 1 s 2 2 s 2 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 19

Atome de Bore B, Z=5: 1 s 2 2 s 22 p 1 4 ou [He] 2 s 2 p 2 1 1 s 2 2 s² 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 2 p 1 20

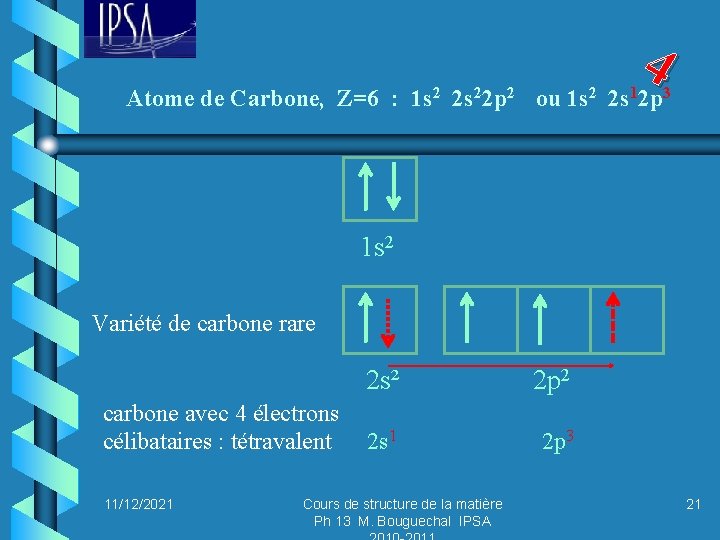
4 Atome de Carbone, Z=6 : 1 s 2 2 s 22 p 2 ou 1 s 2 2 s 12 p 3 1 s 2 Variété de carbone rare carbone avec 4 électrons célibataires : tétravalent 11/12/2021 2 s² 2 p 2 2 s 1 2 p 3 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 21

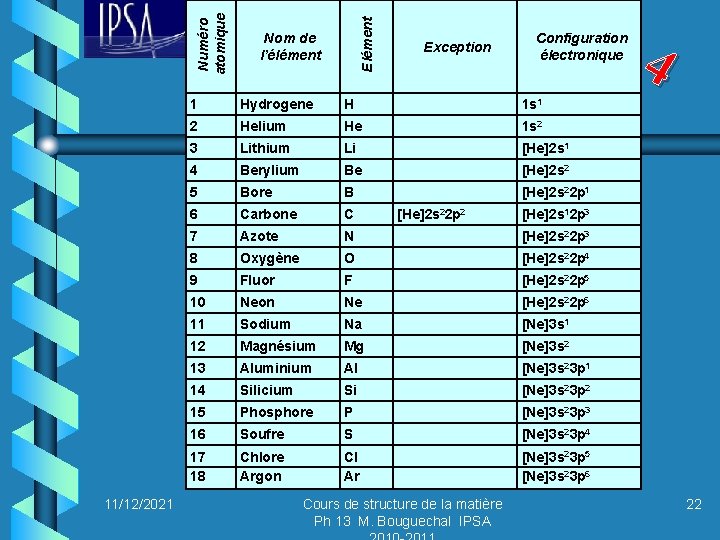
Elément Numéro atomique 11/12/2021 Nom de l’élément Exception Configuration électronique 1 Hydrogene H 1 s 1 2 Helium He 1 s 2 3 Lithium Li [He]2 s 1 4 Berylium Be [He]2 s 2 5 Bore B [He]2 s 22 p 1 6 Carbone C 7 Azote N [He]2 s 22 p 3 8 Oxygène O [He]2 s 22 p 4 9 Fluor F [He]2 s 22 p 5 10 Neon Ne [He]2 s 22 p 6 11 Sodium Na [Ne]3 s 1 12 Magnésium Mg [Ne]3 s 2 13 Aluminium Al [Ne]3 s 23 p 1 14 Silicium Si [Ne]3 s 23 p 2 15 Phosphore P [Ne]3 s 23 p 3 16 Soufre S [Ne]3 s 23 p 4 17 18 Chlore Argon Cl Ar [Ne]3 s 23 p 5 [Ne]3 s 23 p 6 [He]2 s 22 p 2 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 4 [He]2 s 12 p 3 22

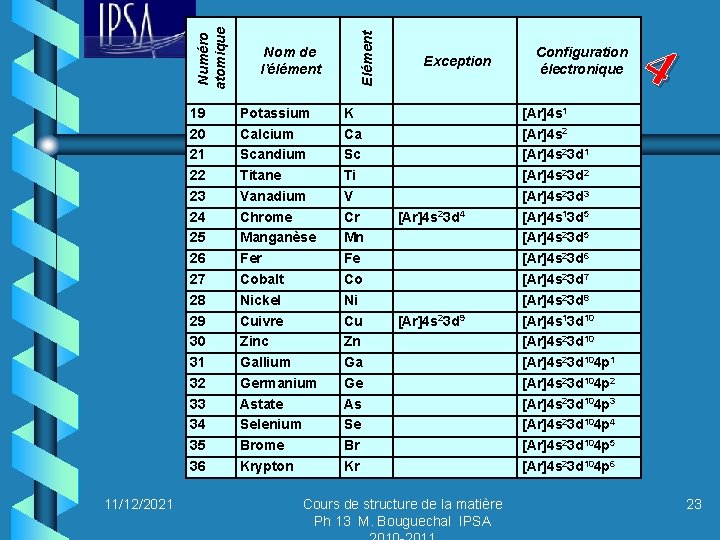
11/12/2021 Potassium Calcium Scandium Titane Vanadium Chrome Manganèse Fer Cobalt Nickel Cuivre Zinc Gallium Germanium Astate Selenium Brome Krypton Elément Numéro atomique 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 Nom de l’élément K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr Exception [Ar]4 s 23 d 4 [Ar]4 s 23 d 9 Cours de structure de la matière Ph 13 M. Bouguechal IPSA Configuration électronique 4 [Ar]4 s 1 [Ar]4 s 23 d 2 [Ar]4 s 23 d 3 [Ar]4 s 13 d 5 [Ar]4 s 23 d 6 [Ar]4 s 23 d 7 [Ar]4 s 23 d 8 [Ar]4 s 13 d 10 [Ar]4 s 23 d 104 p 1 [Ar]4 s 23 d 104 p 2 [Ar]4 s 23 d 104 p 3 [Ar]4 s 23 d 104 p 4 [Ar]4 s 23 d 104 p 5 [Ar]4 s 23 d 104 p 6 23

c) Règles de Slater 4 John Slater (1930): Physicien américain Atome polyélectronique La répulsion inter-électronique ne permet pas l’utilisation du modèle de Bohr pour les atomes polyélectroniques. Il existe une méthode qui permet l’étude d’un atome polyélectronique mise au point par J. S. Slater en 1930 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 24

1. Généralités sur la méthode de Slater 4 Méthode de calcul de la charge effective: On considère que les nombreuses interactions électrostatiques dans un atome peuvent être ramenées à un petit nombre d’interactions simples à quantifier. Soit l’attraction entre les Z protons du noyau et un électron étudié E quelconque. L’attraction est perturbée par les électrons situés entre le noyau et l’électron E. On dit alors que ces électrons forment un écran. La charge Z du noyau de l’atome devient alors une charge effective Z* relative à l’électron E : Z* = Z - Σσ Σσ : constante d’écran (de tous les autres électrons). 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 25

4 La charge effective du noyau Z* dépend de l’électron E choisi Le coefficient d’écran total Σσ est celui de tous les autres électr 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 26

2. Coefficient d’écran σ 4 Selon la proposition de Slater les coefficients d’écran sont déterminés de la manière suivante : ü Les orbitales atomiques sont séparés en plusieurs groupes : 1 s 1 s 2 s 2 p 3 s 3 p 3 d 3 d 4 s 4 p 4 d 4 d 4 f 4 f 5 s 5 p … ü Le coefficient d’écran i relatif à l’électron E est égale à la somme des coefficients ij dus à tous les électrons autres que E. 11/12/2021 Cours de structure de la matière 27 Ph 13 M. Bouguechal IPSA

4 Le calcul s’effectue grâce aux règles suivantes : pour un électron occupant: Orbital atomique 1 s le coefficient d’écran de l’autre électron 1 s est égale à 0, 31 Orbitale atomique s ou p le coefficient d’écran dû à un électron d’une orbitale atomique de nombre quantique principal n’ vaut ij = 1 si n’ < n-1 ij = 0, 85 si n’ = n-1 ij = 0, 35 si n’ = n ij = 0 si n’ > n Orbitale atomique d ou f le coefficient d’écran vaut 0, 35 pour un électron du même groupe et 1 pour tous les autres ( quelques exceptions) 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 28

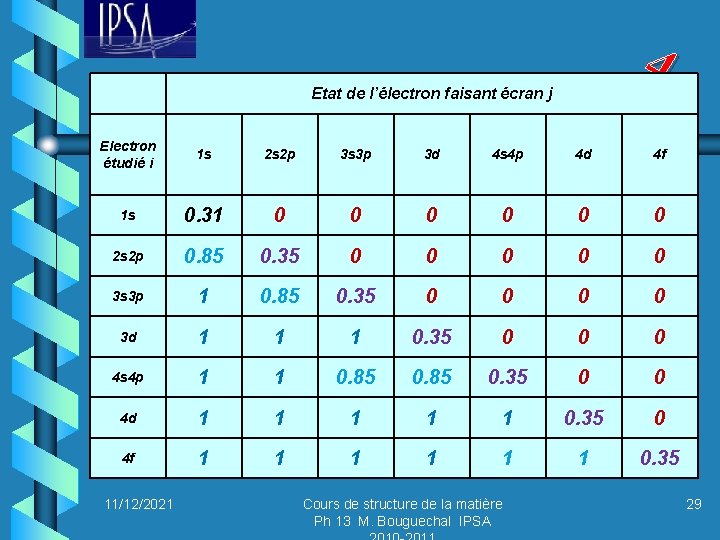
4 Etat de l’électron faisant écran j Electron étudié i 1 s 2 s 2 p 3 s 3 p 3 d 4 s 4 p 4 d 4 f 1 s 0. 31 0 0 0 2 s 2 p 0. 85 0. 35 0 0 0 3 s 3 p 1 0. 85 0. 35 0 0 3 d 1 1 1 0. 35 0 0 0 4 s 4 p 1 1 0. 85 0. 35 0 0 4 d 1 1 1 0. 35 0 4 f 1 1 1 0. 35 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 29

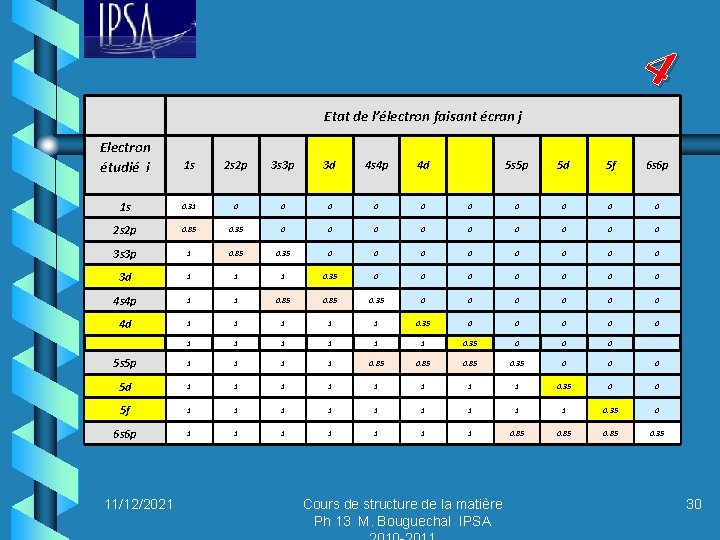
4 Etat de l’électron faisant écran j Electron étudié i 1 s 2 s 2 p 3 s 3 p 3 d 4 s 4 p 4 d 1 s 0. 31 0 0 0 2 s 2 p 0. 85 0. 35 0 0 0 3 s 3 p 1 0. 85 0. 35 0 3 d 1 1 1 4 s 4 p 1 1 4 d 1 5 s 5 p 5 d 5 f 6 s 6 p 0 0 0 0 0. 35 0 0 0 0. 85 0. 35 0 0 0 1 1 1 0. 35 0 0 0 5 s 5 p 1 1 0. 85 0. 35 0 0 0 5 d 1 1 1 1 0. 35 0 0 5 f 1 1 1 1 1 0. 35 0 6 s 6 p 1 1 1 1 0. 85 0. 35 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 30

4 En 1960 Slater introduit un nombre quantique apparent n* pour diminuer les différences entre les valeurs expérimentales et les valeurs calculées. Il est nécessaire d’introduire n* à partir de la 4 ème période. n 1 2 3 4 5 6 n* 1 2 3 3. 7 4. 0 4. 2 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 31

Hydrogène 1 H : 1 s 1 1 groupe de Slater Coefficient d’écran pour l’unique électron 1 s = 0 Charge effective du noyau pour cet électron Z*eff = Z - = 1 - 0 = 1 4 Hélium 2 He : 1 s² 1 groupe de Slater Coefficient d’écran pour un électron 1 s = 0, 31 Charge effective du noyau pour un électron 1 s Z*eff = 2 – 0, 31 = 1, 69 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 32

4 Carbone 6 C = 1 s² 2 p² 2 groupes de Slater ü Coefficient d’écran pour un électron 1 s 1 = Σ σ = 0, 31 + 0 = 0, 31 Charge effective du noyau pour un électron 1 s Z*eff 1 = 6 - 1 = 5, 69 ü Coefficient d’écran pour un électron 2 s 2 p 2 = Σ σ = 0, 85 x 2 + 0, 35 x 3 = 2, 75 Charge effective du noyau pour un électron 2 s 2 p Z*eff 2 = 6 - 2 = 3, 25 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 33

Soufre 16 S = 1 s² 2 p 6 3 s² 3 p 4 3 groupes de Slater ü Coefficient pour un électron 1 s 1 = Σ σ = 0, 31 + 0 = 0, 31 Charge effective du noyau pour un électron 1 s Z*eff 1 = 16 - 1 = 15, 69 4 Coefficient pour un électron 2 s 2 p 2 = Σ σ = 0, 85 x 2 2 + 0, 35 x 7 7 = 4, 15 Charge effective du noyau pour un électron 2 s 2 p Z*eff 2 = 16 - 2 = 11, 85 ü Coefficient pour un électron 3 s 3 p 3 = Σ σ = 2 + 8 x 0, 85 + 5 x 0, 35 = 10, 55 Charge effective du noyau pour un électron 3 s 3 p Z*eff 3 = 16 - 3 = 5, 45 ü 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 34

L’énergie d’un électron i d’un atome donné est donnée par : 4 L’énergie totale de tous les électrons est donc : pi représente le nombre d’électrons ayant l’énergie Ei 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 35

4 Le rayon de l’orbite atomique ou de l’ atome est donné par la formule : 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 36

4 Fin de la leçon 4 11/12/2021 Cours de structure de la matière Ph 13 M. Bouguechal IPSA 37