3 Subdomnio Unidade Reaes cidobase 3 1 cidos

3 Subdomínio Unidade Reações ácido-base

3. 1 Ácidos e bases

Os ácidos e as bases são substâncias com propriedades características.

Estas substâncias são conhecidas desde a Antiguidade.

Muitas dessas substâncias são utilizadas com frequência no nosso quotidiano.

O sumo de limão tem características ácidas, . . .

. . . tal como o sumo de maçã. . .

. . . e o vinagre.

Por outro lado, o champô tem características básicas (ou alcalinas), . . .

. . . tal como o sabonete e o sabão. . .

. . . e muitos dos produtos de limpeza doméstica.

Durante séculos, ácidos e bases foram reconhecidos apenas pelos sentidos. Ácidos Bases Sabor azedo. Sabor amargo. Modificam a cor de alguns vegetais. Escorregadias ao tato. Estes critérios eram puramente empíricos. Não permitiam explicar os efeitos observados.

Antoine Lavoisier, químico francês, foi o primeiro cientista a tentar identificar os elementos Antoine Lavoisier (1743 -1794) químicos comuns aos ácidos. Lavoisier define ácido como uma substância que contém oxigénio na sua composição. Segundo Lavoisier, a acidez estava diretamente relacionada com o elemento químico oxigénio.

Humphry Davy, químico britânico, provou que havia ácidos que Humphry Davy (1778 -1829) não continham oxigénio. Ao estudar o ácido muriático (ácido clorídrico — HCℓ), notou que este não continha oxigénio. Segundo Davy, a acidez estava diretamente relacionada com o elemento químico hidrogénio.

Svante Arrhenius, químico sueco, desenvolveu, em 1884, a Teoria Svante Arrhenius (1859 -1927) da Dissociação Eletrolítica. Segundo Arrhenius, as características ácidas e básicas de certas soluções estavam relacionadas com a presença de iões H+ e OH–. A Teoria da Dissociação Eletrolítica valeu a Arrhenius o Prémio Nobel da Química em 1903.

Segundo Arrhenius: Ácido Bases Substância que contém hidrogénio Substância que contém o grupo (H) e se dissocia, dando origem hidroxilo (OH) e se dissocia, a io es H+ em soluc a o aquosa. originando OH– em soluc a o aquosa. De um modo geral: HA(aq) → A–(aq) + H+(aq) MOH(aq) → M+(aq) + OH–(aq) Exemplos: HCℓ(aq) → Cℓ–(aq) + H+(aq) KOH(s) → K+(aq) + OH–(aq) H 2 SO 4(aq) → SO 42–(aq) + 2 H+(aq) Mg(OH)2(s) → Mg 2+(aq) + 2 OH–(aq)

Ácidos e bases, reagindo entre si, neutralizam os seus efeitos. A reação entre H+ e OH– é uma reação de neutralização: H+(aq) + OH–(aq) → H 2 O (l)

Apesar da enorme importância da Teoria de Arrhenius, esta apresentava algumas limitações: • Não explicava o comportamento de um grande número de substâncias que se comportavam como bases mas que não possuíam o grupo OH. Exemplos: amoníaco (NH 3) e carbonato de sódio (Na 2 CO 3). • Aplicava-se apenas a soluções aquosas e não conseguia explicar a existência de H+ em soluções não aquosas.

Ácidos e bases segundo Brönsted e Lowry

Em 1923, o químico dinamarquês Johannes Brönsted e o químico inglês Thomas Lowry propuseram, de forma independente, Johannes Brönsted (1879 -1947) definições para ácidos e bases. A teoria de ambos, conhecida como a Teoria de Brönsted-Lowry, definia ácidos e bases em termos da sua capacidade Thomas Lowry (1874 -1936) de transferência de protões.

Segundo a Teoria de Brönsted-Lowry: Ácido Johannes Brönsted (1879 -1947) Ácido é toda a espécie química (molécula ou ião) capaz de ceder protões (H+). Base é toda a espécie química (molécula Thomas Lowry (1874 -1936) ou ião) capaz de aceitar protões (H+).
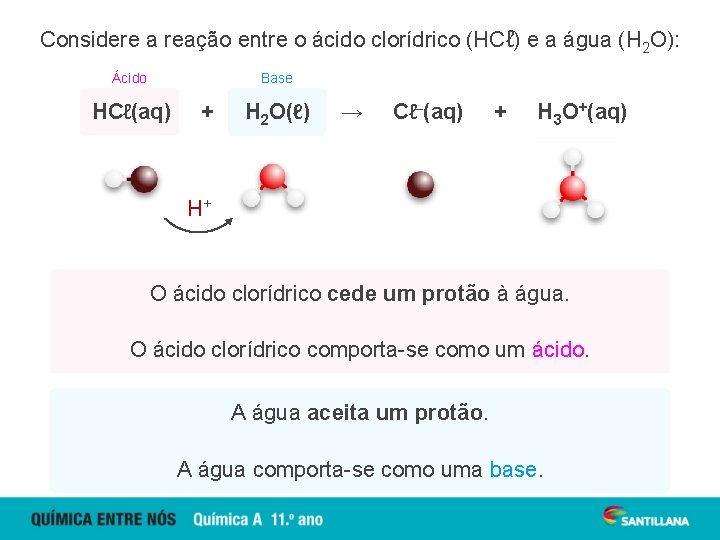
Considere a reação entre o ácido clorídrico (HCℓ) e a água (H 2 O): Ácido Base HCℓ(aq) + H 2 O(ℓ) → Cℓ–(aq) + H 3 O+(aq) H+ O ácido clorídrico cede um protão à água. O ácido clorídrico comporta-se como um ácido. A água aceita um protão. A água comporta-se como uma base.
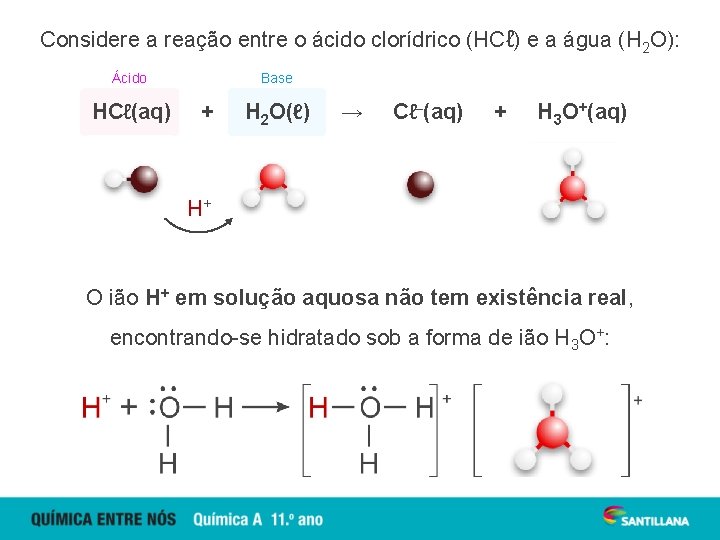
Considere a reação entre o ácido clorídrico (HCℓ) e a água (H 2 O): Ácido HCℓ(aq) Base + H 2 O(ℓ) → Cℓ–(aq) + H 3 O+(aq) H+ O ião H+ em solução aquosa não tem existência real, encontrando-se hidratado sob a forma de ião H 3 O+:
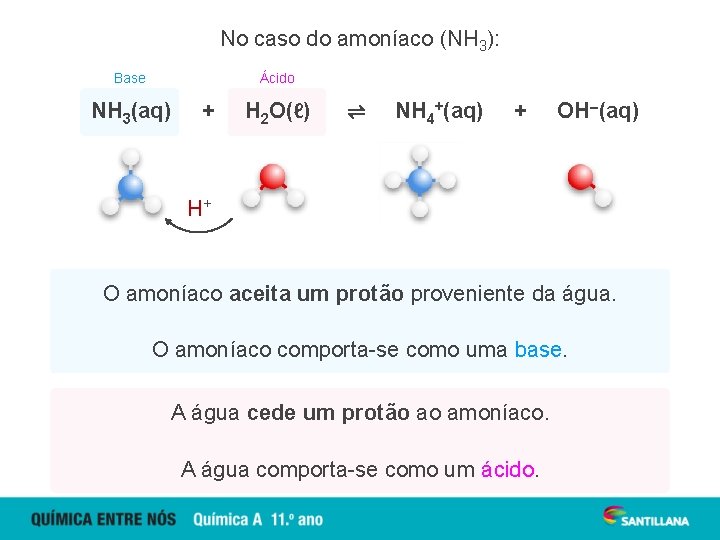
No caso do amoníaco (NH 3): Base Ácido NH 3(aq) + H 2 O(ℓ) ⇌ NH 4+(aq) + OH–(aq) H+ O amoníaco aceita um protão proveniente da água. O amoníaco comporta-se como uma base. A água cede um protão ao amoníaco. A água comporta-se como um ácido.
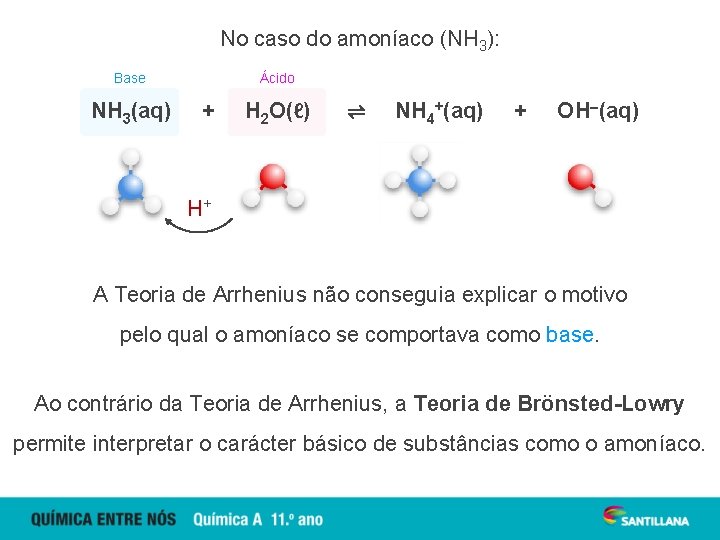
No caso do amoníaco (NH 3): Base NH 3(aq) Ácido + H 2 O(ℓ) ⇌ NH 4+(aq) + OH–(aq) H+ A Teoria de Arrhenius não conseguia explicar o motivo pelo qual o amoníaco se comportava como base. Ao contrário da Teoria de Arrhenius, a Teoria de Brönsted-Lowry permite interpretar o carácter básico de substâncias como o amoníaco.
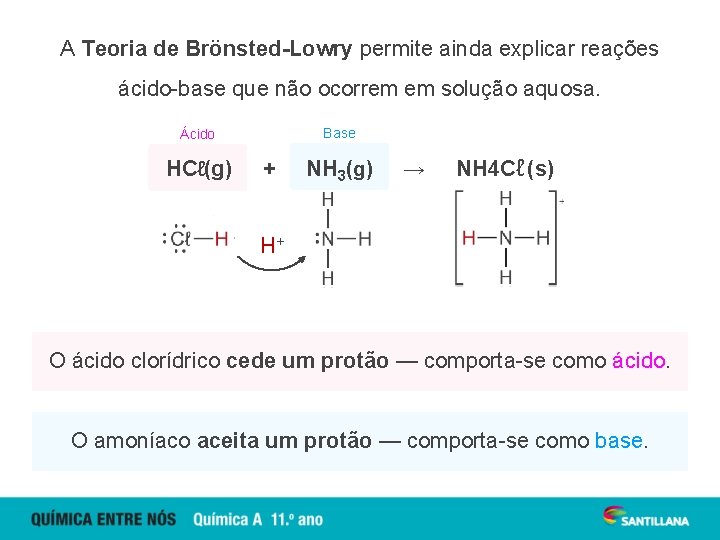
A Teoria de Brönsted-Lowry permite ainda explicar reações ácido-base que não ocorrem em solução aquosa. Base Ácido HCℓ(g) + NH 3(g) → NH 4 Cℓ (s) H+ O ácido clorídrico cede um protão — comporta-se como ácido. O amoníaco aceita um protão — comporta-se como base.
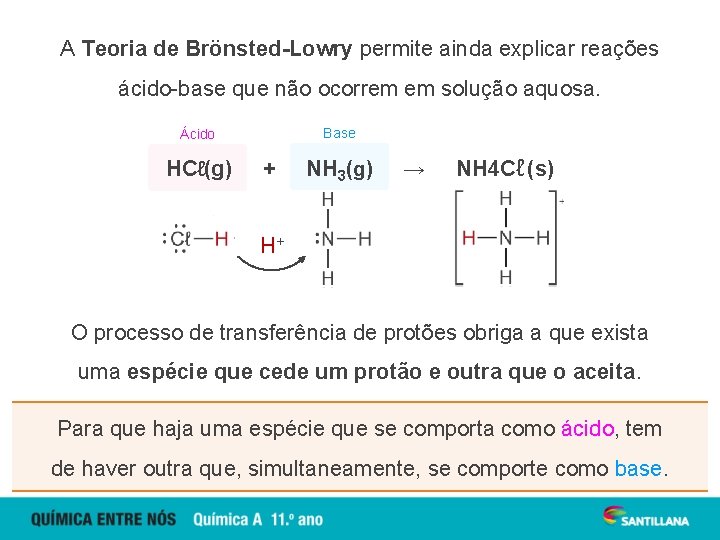
A Teoria de Brönsted-Lowry permite ainda explicar reações ácido-base que não ocorrem em solução aquosa. Base Ácido HCℓ(g) + NH 3(g) → NH 4 Cℓ (s) H+ O processo de transferência de protões obriga a que exista uma espécie que cede um protão e outra que o aceita. Para que haja uma espécie que se comporta como ácido, tem de haver outra que, simultaneamente, se comporte como base.

Pares ácido-base conjugados e espécies químicas anfotéricas

No equilíbrio ácido-base genérico: Ácido HA(aq) Base + H+ H 2 O(ℓ) ⇌ A–(aq) + H 3 O+(aq) Na reação direta, de acordo com a Teoria de Brönsted-Lowry: • HA cede um protão — comporta-se como ácido; • a água aceita um protão — comporta-se como base.

No equilíbrio ácido-base genérico: Ácido HA(aq) Base + H 2 O(ℓ) Base ⇌ A–(aq) Ácido + H 3 O+(aq) H+ Na reação inversa, de acordo com a Teoria de Brönsted-Lowry: • H 3 O+ cede um protão — comporta-se como ácido; • A– aceita um protão — comporta-se como base.
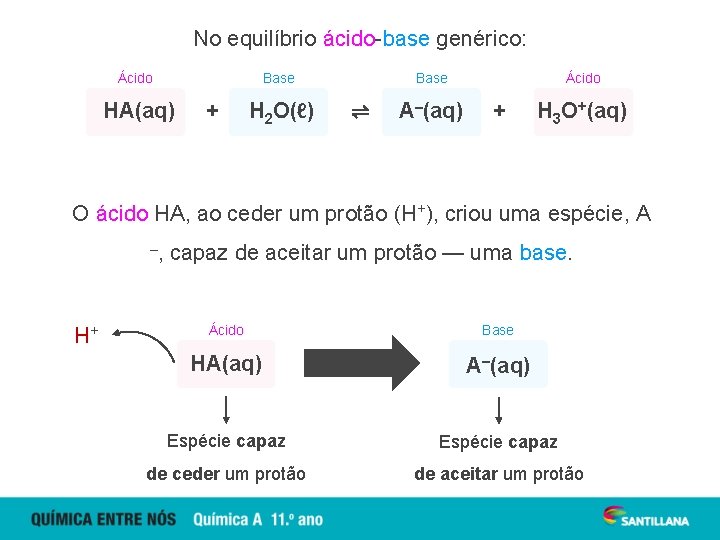
No equilíbrio ácido-base genérico: Ácido Base HA(aq) + H 2 O(ℓ) Base ⇌ A–(aq) Ácido + H 3 O+(aq) O ácido HA, ao ceder um protão (H+), criou uma espécie, A –, H+ capaz de aceitar um protão — uma base. Ácido Base HA(aq) A–(aq) Espécie capaz de ceder um protão de aceitar um protão
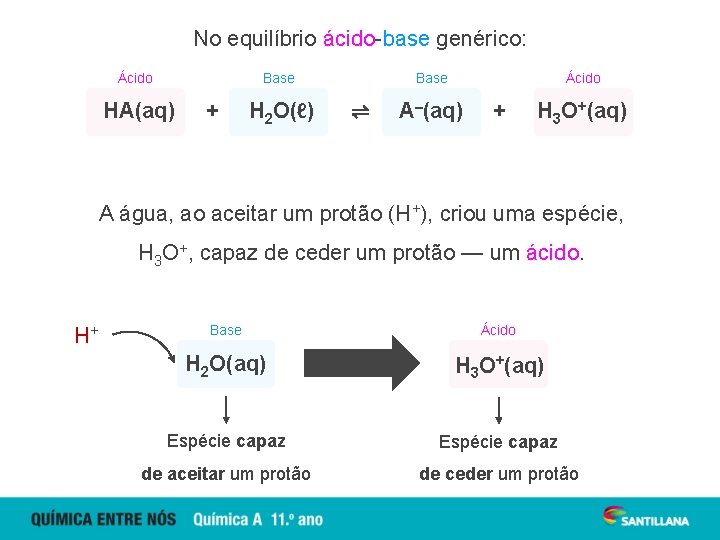
No equilíbrio ácido-base genérico: Ácido Base HA(aq) + H 2 O(ℓ) Base ⇌ Ácido A–(aq) + H 3 O+(aq) A água, ao aceitar um protão (H+), criou uma espécie, H 3 O+, capaz de ceder um protão — um ácido. H+ Base Ácido H 2 O(aq) H 3 O+(aq) Espécie capaz de aceitar um protão de ceder um protão

No equilíbrio ácido-base genérico: Ácido HA(aq) Base + H 2 O(ℓ) Base ⇌ A–(aq) Ácido + H 3 O+(aq) Estes pares de espécies, que entre si só diferem num protão, denominam-se pares ácido-base conjugados: Ácido Base HA / A– Ácido Base H 3 O + / H 2 O O ácido HA, ao ceder um protão, A base água, ao aceitar um protão, transforma-se na base A–. transforma-se no ácido H 3 O+.

No equilíbrio ácido-base genérico: Ácido HA(aq) Base + H 2 O(ℓ) Base ⇌ A–(aq) Ácido + H 3 O+(aq) Em qualquer reação de ácido-base, podem ser identificados dois pares ácido-base conjugados. Na escrita dos pares ácido-base conjugados, deve escrever-se em primeiro lugar o ácido e só depois a base.
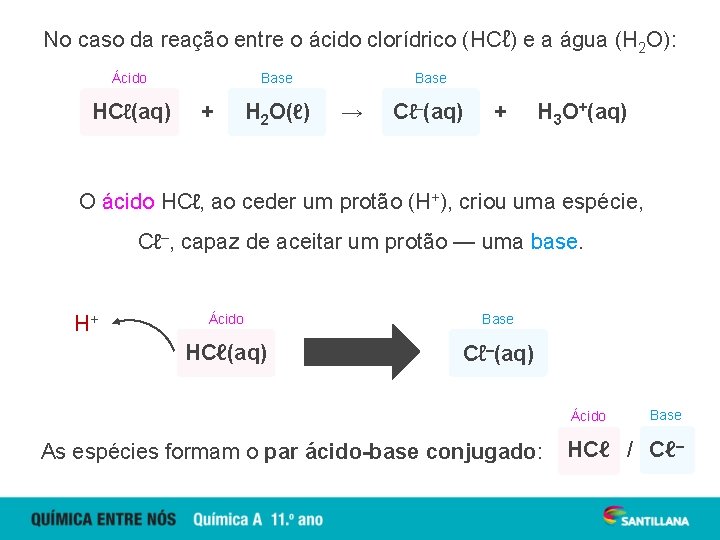
No caso da reação entre o ácido clorídrico (HCℓ) e a água (H 2 O): Ácido HCℓ(aq) Base + H 2 O(ℓ) Base → Cℓ–(aq) + H 3 O+(aq) O ácido HCℓ, ao ceder um protão (H+), criou uma espécie, Cℓ–, capaz de aceitar um protão — uma base. H+ Ácido Base HCℓ(aq) Cℓ–(aq) Ácido As espécies formam o par ácido-base conjugado: Base HCℓ / Cℓ–
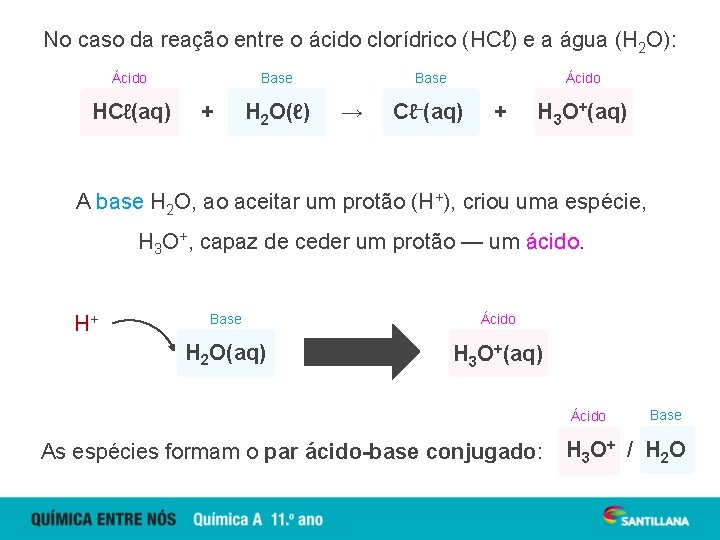
No caso da reação entre o ácido clorídrico (HCℓ) e a água (H 2 O): Ácido HCℓ(aq) Base + H 2 O(ℓ) Base → Ácido Cℓ–(aq) + H 3 O+(aq) A base H 2 O, ao aceitar um protão (H+), criou uma espécie, H 3 O+, capaz de ceder um protão — um ácido. H+ Base Ácido H 2 O(aq) H 3 O+(aq) Ácido As espécies formam o par ácido-base conjugado: Base H 3 O + / H 2 O
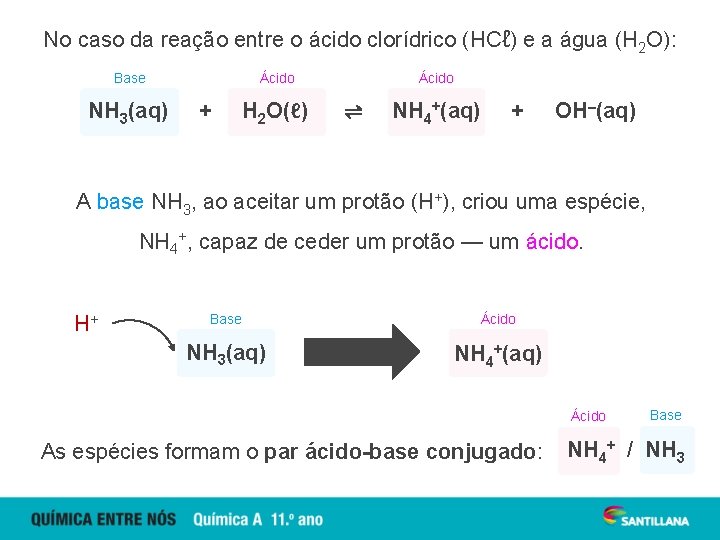
No caso da reação entre o ácido clorídrico (HCℓ) e a água (H 2 O): Base NH 3(aq) Ácido + H 2 O(ℓ) Ácido ⇌ NH 4+(aq) + OH–(aq) A base NH 3, ao aceitar um protão (H+), criou uma espécie, NH 4+, capaz de ceder um protão — um ácido. H+ Base Ácido NH 3(aq) NH 4+(aq) Ácido As espécies formam o par ácido-base conjugado: Base NH 4+ / NH 3
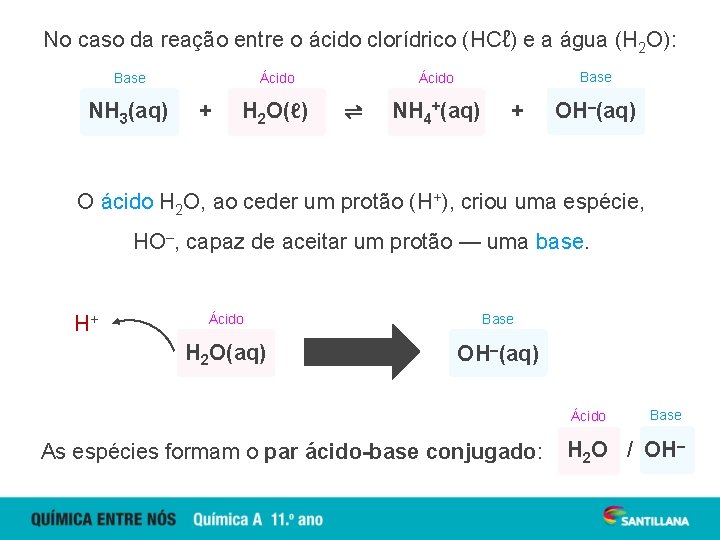
No caso da reação entre o ácido clorídrico (HCℓ) e a água (H 2 O): Base NH 3(aq) Ácido + H 2 O(ℓ) Base Ácido ⇌ NH 4+(aq) + OH–(aq) O ácido H 2 O, ao ceder um protão (H+), criou uma espécie, HO–, capaz de aceitar um protão — uma base. H+ Ácido Base H 2 O(aq) OH–(aq) Ácido As espécies formam o par ácido-base conjugado: Base H 2 O / OH–

A água (H 2 O) pode comportar-se: • como um ácido, capaz de ceder um protão, quando está na presença de uma base; Base NH 3(aq) Ácido + H 2 O(ℓ) ⇌ NH 4+(aq) + OH–(aq) • como uma base, capaz de aceitar um protão, quando está na presença de um ácido. Ácido HCℓ(aq) Base + H 2 O(ℓ) → Cℓ–(aq) + H 3 O+(aq)

As substâncias que se comportam como ácidos ou bases, dependendo da espécie com a qual reagem, denominam-se substâncias anfotéricas ou anfipróticas. Exemplos: • Água (H 2 O); • Ião hidrogenossulfato (HSO 4–).

Conclusão • Ácido é toda a espécie química (molécula ou ião) capaz de ceder protões (H+). • Base é toda a espécie química (molécula ou ião) capaz de aceitar protões (H+).

Conclusão • As substâncias que se comportam como ácidos ou bases, dependendo da espécie com a qual reagem, denominam-se substâncias anfotéricas ou anfipróticas.
- Slides: 42