3 Dstructure of bacterial ribsoomes Components required for
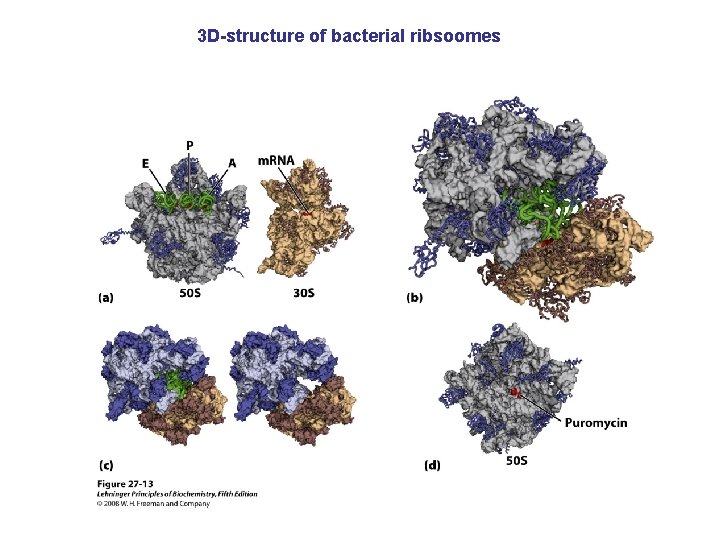
3 D-structure of bacterial ribsoomes

Components required for protein-synthesis in E. coli
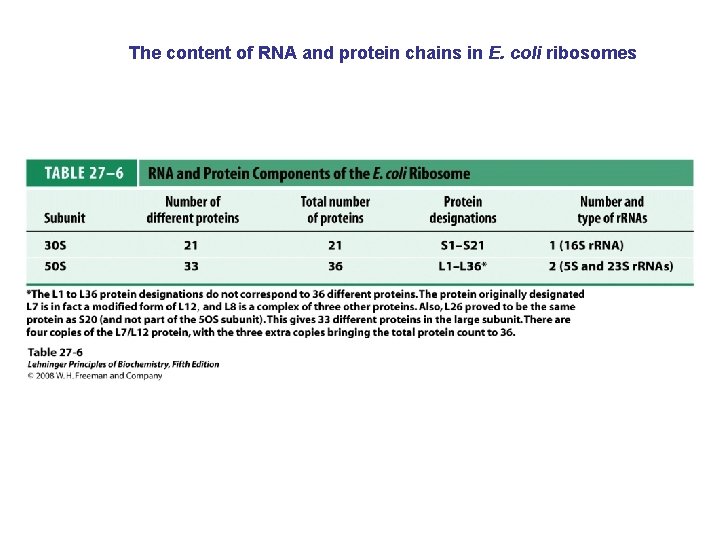
The content of RNA and protein chains in E. coli ribosomes
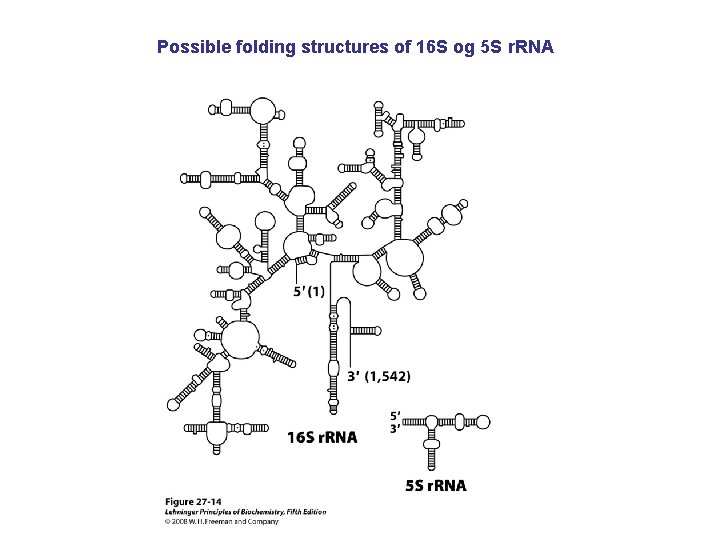
Possible folding structures of 16 S og 5 S r. RNA
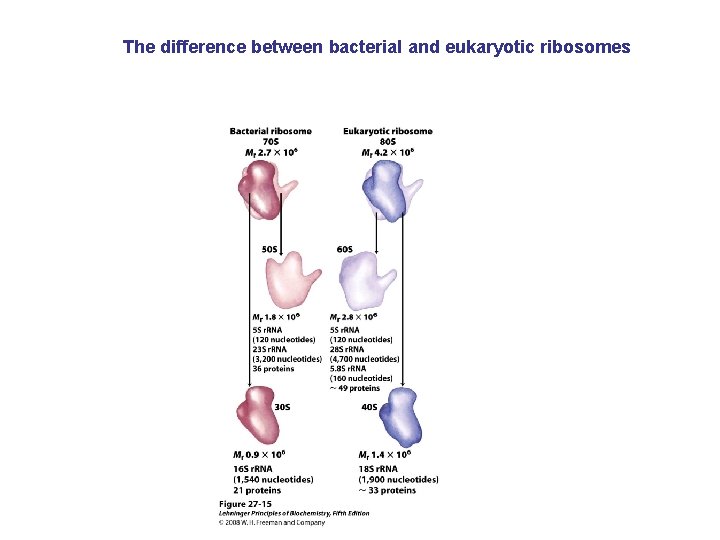
The difference between bacterial and eukaryotic ribosomes
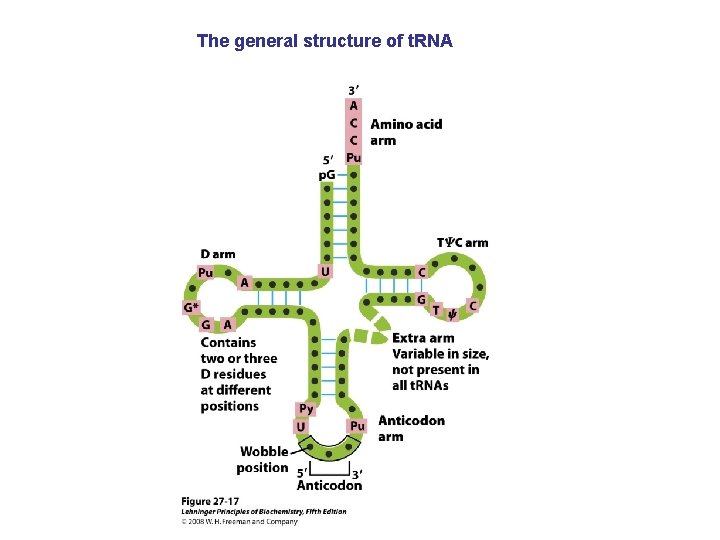
The general structure of t. RNA
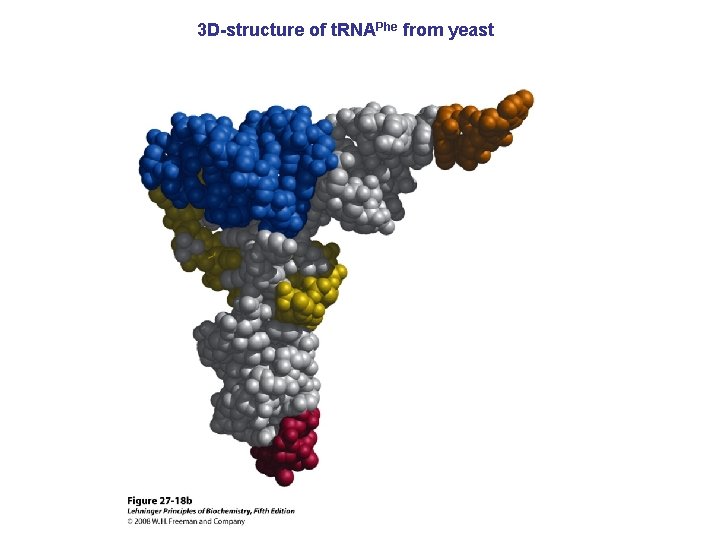
3 D-structure of t. RNAPhe from yeast
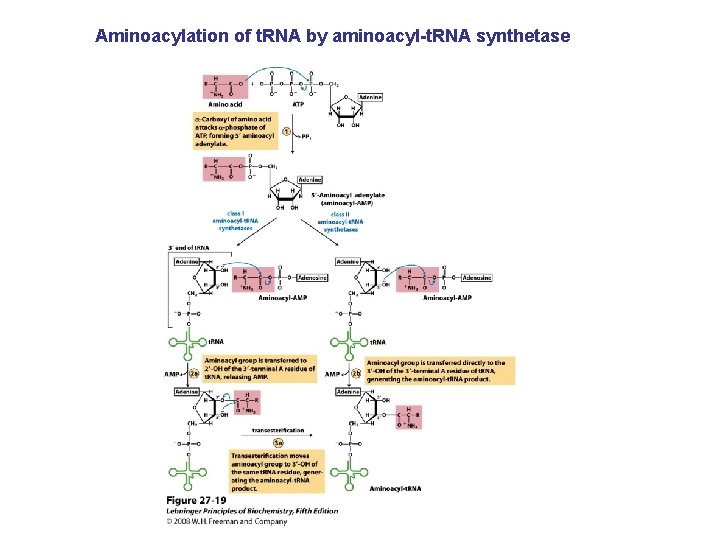
Aminoacylation of t. RNA by aminoacyl-t. RNA synthetase
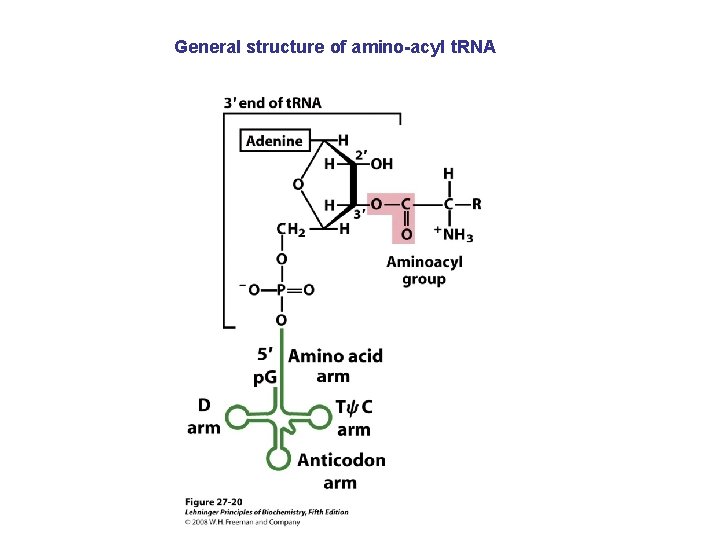
General structure of amino-acyl t. RNA
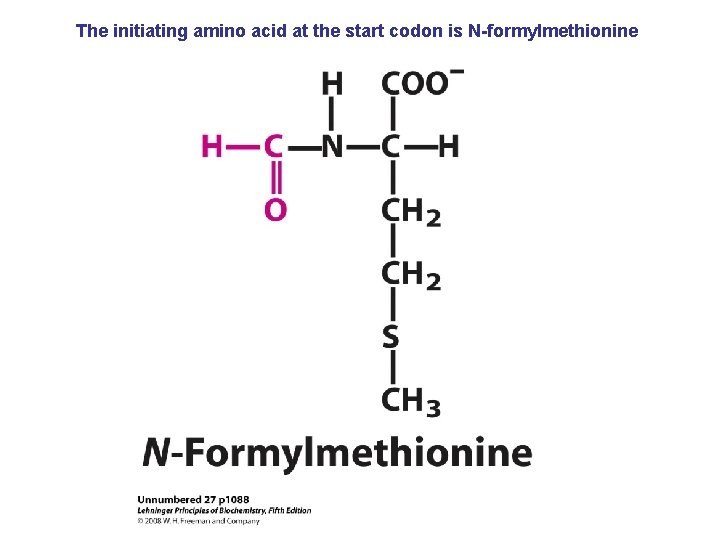
The initiating amino acid at the start codon is N-formylmethionine
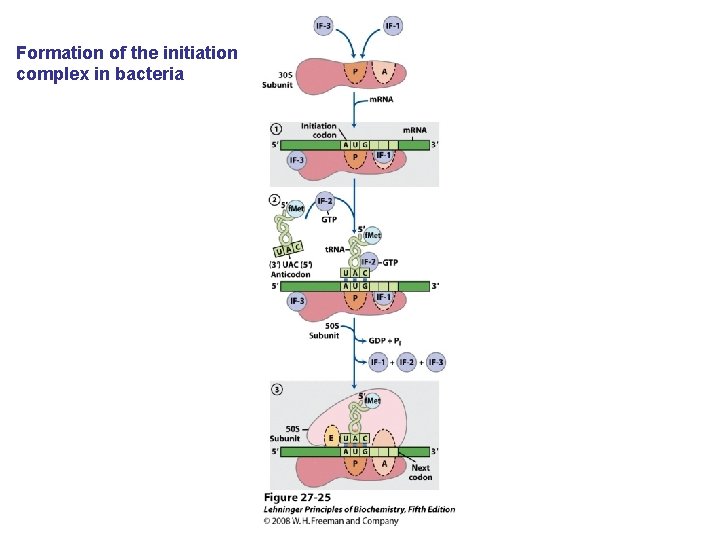
Formation of the initiation complex in bacteria
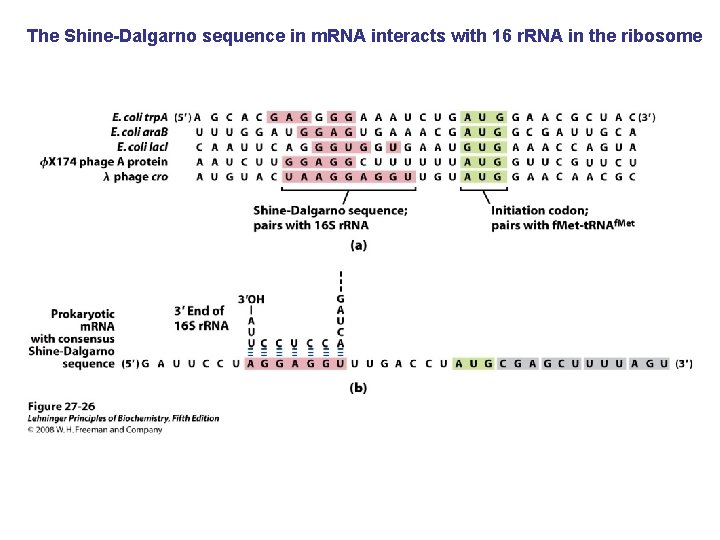
The Shine-Dalgarno sequence in m. RNA interacts with 16 r. RNA in the ribosome







De viktigste punktene i proteinsyntesen i bakterier: • Den første aminosyra er alltid formylmetionin, uavhengig av hva startkodonet (nesten alltid AUG eller GUG) er. • Før peptidbindinger lages må aminosyrene aktiveres ved å kondensere med ATP. Denne reaksjonen drives av spalting av en fosfodiesterbinding i ATP slik at PP frigjøres. Etter dette kobles aminosyren på sitt aktuelle t. RNA ved hjelp av aminoacyl t. RNA syntetase. • 30 S subenheten av ribosomet bindes til m. RNA slik at AUG blir posisjonert i P-setet (peptidylsetet). Husk at det er her Shine-Dalgarno sekvensen i m. RNA kommer inn ved å basepare med en del av 16 S r. RNA. • t. RNA med formylmetionin rekrutteres til P-setet ved binding til AUG i m. RNA. • 50 S subenheten rekrutteres til komplekset. • Neste aminosyre rekrutteres via sitt t. RNA til kodon 2 i m. RNA ved A-setet (aminoacylsetet) i ribosomet. • En peptidbinding dannes ved at formylmetionin linkes til aminosyren i A-setet. • t. RNA med dipeptidet translokeres fra A-setet til P-setet. • En tredje aminosyre rekrutteres via sitt t. RNA til kodon 3 i m. RNA ved A-setet. Ny peptidpinding dannes som over. • Prosessen fortsetter til stopp-kodonet. Dette senses av release faktor og proteinet forlater ribosomet i Exit site. Ribosomet spaltes i 30 S og 50 S subenheter igjen. • Det inngår mange proteinfaktorer (initieringsfaktorer, elongeringsfaktorer etc) i de ulike stegene, men dere trenger ikke å huske navnene på disse eller hvor de inngår. Derimot er det svært viktig å være klar over at det forbrukes veldig mye GTP. Siden det lages veldig mye proteiner i levende celler blir dermed proteinsyntesen en energimessig sett veldig kostbar prosess.

Proteins and folding and posttranslatoric modification Proteins can be denatured, i. e by heating. This means that the folding structure collapses, resulting in loss of functionality Proteins from thermofilic organisms can resist boiling Some proteins fold correctly by themselves after retransfer to low temperatures, but most proteins don’t During production many proteins can only obtain correct folding if assisted by other proteins (chaperones) during production in living cells If large quantities of a specific chaperone-dependent protein is produced in a cell, it may become misfolded. This represents a very serious problem in biotechnology If a protein is misfolded during production it may in some, but not all cases, be correctly refolded in the laboratory Many proteins, particularly from eukaryotes, are further modified in the cells after translation. This can involve phosphorylation, glycosylation etc. The modifications have various biolological functions, and this is also very important in biotechnology.
- Slides: 20