3 COURS DE THERMODYNAMIQUE Module Ph 21 11012022



































































- Slides: 74

3 COURS DE THERMODYNAMIQUE (Module Ph 21) 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 1

3 Chapitre trois Echanges de travail et de chaleur 3. 1 Echange de travail 11/01/2022 3. 1. 1 Notion de travail 3. 1. 2 Convention de signe 3. 1. 3 Travail lors d’un cycle 3. 1. 4 Travail lors d’une transformation isobare 3. 1. 5 Travail lors d’une transformation isochore 3. 1. 6 Travail lors d’une transformation isotherme d’un gaz parfait Cours de thermodynamique M. Bouguechal Ph 21 2

3 3. 2 11/01/2022 Echange de chaleur 3. 2. 1 Notion de chaleur 3. 2. 2 Formules d’échange de chaleur 3. 2. 3 Relations entre les coefficients calorimétriques 3. 2. 3 Applications aux gaz parfaits Cours de thermodynamique M. Bouguechal Ph 21 3

3 3. 1 Echange de travail, 3. 1. 1 Notion de travail Le travail est un mode de transfert de l’énergie. C’est un autre mode de transfert de l’énergie. La chaleur, est aussi un mode de transfert de l’énergie. Le travail est aussi appelé de l’énergie mécanique. C'est l'énergie qui intervient dès qu'il y a un mouvement comme un piston qui se déplace ou une déformation d'un corps comme une paroi mobile ou déformable. 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 4

3 La formule infinitésimale du travail est donnée par : 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 5

3 Si le système subit une transformation ou un changement qui l’amène de l’état (1) à l’état (2), au cours de laquelle le point d’application de la force se déplace, cette force fournit alors le travail : 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 6

3 La pression P et la force sont liées par la relation : Si dl et F sont de même sens F. dl > 0. Le système reçoit du travail (+) et son volume diminue (-), on peut donc écrire : 3 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 7

3 Si la transformation est irréversible, le travail est alors donné par : 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 8

En résumé, le travail fourni à un système au cours d’une transformation réversible s’exprime en fonction de ses variables d’état internes. 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 9

3 Le travail réversible échangée entre le système et le milieu extérieur quand le système passe d’un état initial i à un état final f est donné par : 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 10

3 P Etat initial Etat final V Cette intégrale est représentée en valeur absolue par la surface sous la courbe, surface qui dépend du chemin suivi. 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 11

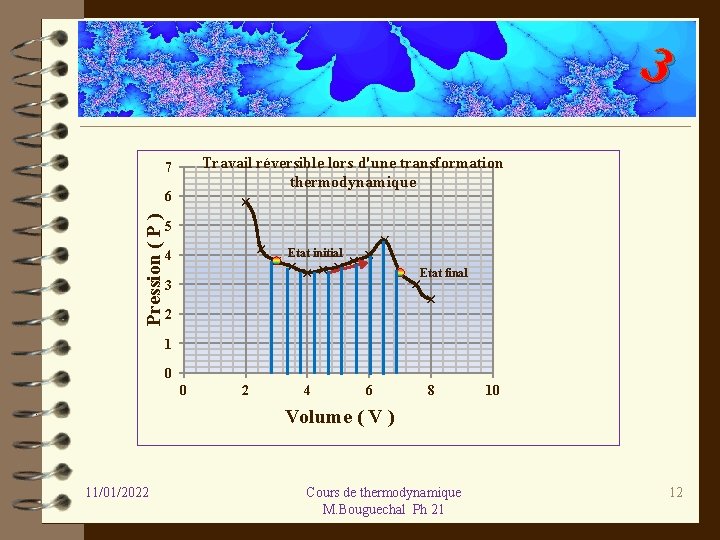
3 Travail réversible lors d'une transformation thermodynamique 7 Pression ( P ) 6 5 Etat initial 4 Etat final 3 2 1 0 0 2 4 6 8 10 Volume ( V ) 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 12

3 Le travail accompli par la transformation thermodynamique, sur la figure, lors du passage de l’état initial à l’état final est donné par la surface hachurée sous la courbe. Ce travail est négatif d’après la formule, présence du signe – et c’est donc un travail cédé à l’extérieur. Si on inverse le sens de la transformation, le signe du travail change. 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 13

3 Convention de signe : le travail reçu par le système est positif, le travail cédé par le système est négatif. Cette convention est aussi valable pour la chaleur échangée Q. W > 0 ou Q > 0 11/01/2022 W < 0 ou Q < 0 Cours de thermodynamique M. Bouguechal Ph 21 14

3 3. 1. 2 Travail lors d’un cycle thermodynamique 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 15

3 Le travail total échangé lors de cette transformation cyclique est négatif, le système fournit du travail à l’extérieur, il s’agit d’un cycle moteur. Pour connaitre le signe du travail, il faut raisonner en utilisant les aires sous la courbe. L’aire totale est la somme de deux aires de signes opposés, l’aire négative est plus grande en valeur absolue. 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 16

3 MOTEUR 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 17

3 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 18

3 Le travail total échangé lors de cette transformation cyclique est positif, le système reçoit du travail de l’extérieur, il s’agit d’un cycle récepteur. Pour connaitre le signe du travail, il faut raisonner en utilisant les aires sous la courbe. L’aire totale est la somme de deux aires de signes opposés, l’aire positive est plus grande en valeur absolue. 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 19

3 RECEPTEUR 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 20

3 Que le cycle soit récepteur ou moteur, on a toujours : 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 21

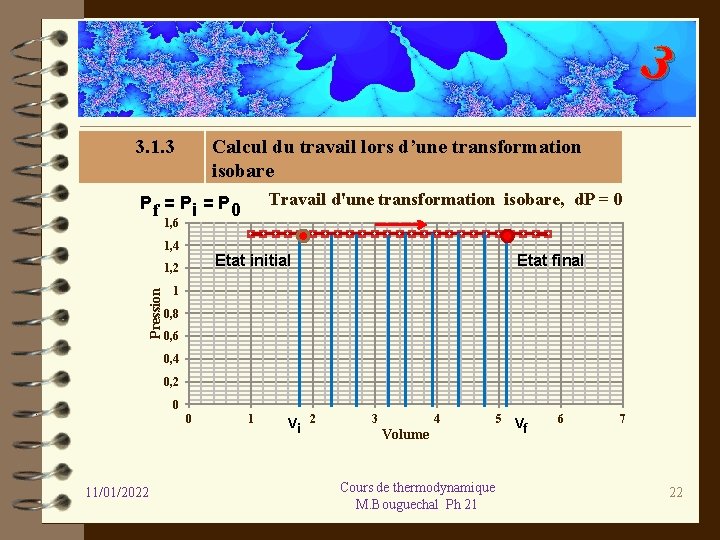
3 3. 1. 3 Calcul du travail lors d’une transformation isobare Travail d'une transformation isobare, d. P = 0 Pf = P i = P 0 1, 6 1, 4 Pression Etat final Etat initial 1, 2 1 0, 8 0, 6 0, 4 0, 2 0 0 11/01/2022 1 Vi 2 3 4 Volume Cours de thermodynamique M. Bouguechal Ph 21 5 Vf 6 7 22

3 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 23

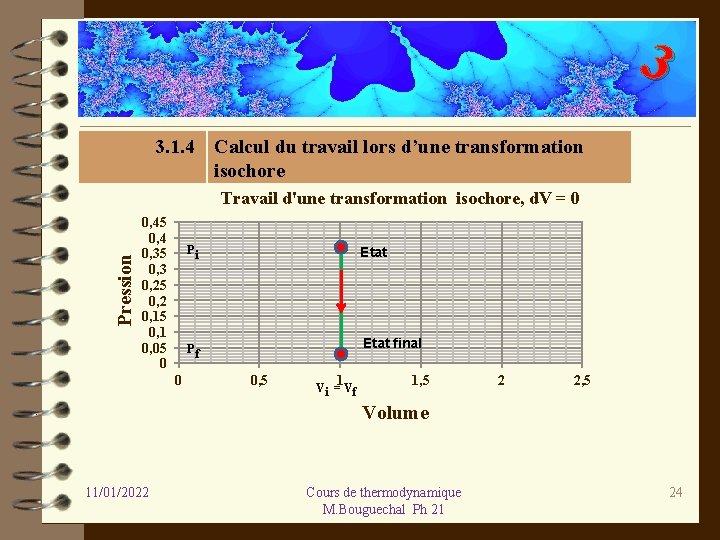
3 4. Calcul du travail lors d’une transformation isochore. 3. 1. 4 Calcul du travail lors d’une transformation isochore Pression Travail d'une transformation isochore, d. V = 0 0, 45 0, 4 0, 35 0, 3 0, 25 0, 2 0, 15 0, 1 0, 05 0 0 Pi Etat Pf Etat final 0, 5 1 Vi = V f 1, 5 2 2, 5 Volume 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 24

3 4. Calcul du travail lors d’une transformation isochore. Dans le cas d’une transformation isochore il n’y a pas d’aire sous la courbe. Le travail est donc égal à : 0. On peut aussi utiliser la formule et on obtient : 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 25

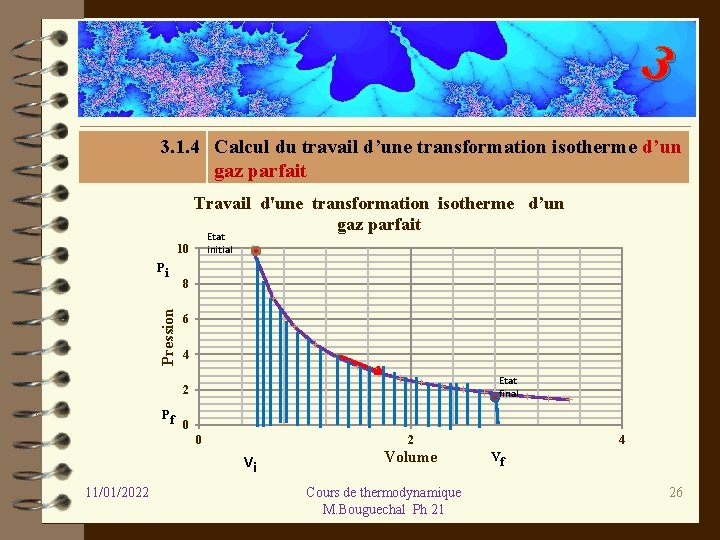
3 3. 1. 4 Calcul du travail d’une transformation isotherme d’un 4. Calcul du travail lors d’une transformation isotherme d’un gaz parfait Travail d'une transformation isotherme d’un gaz parfait Etat initial 10 Pression Pi 8 6 4 Etat final 2 Pf 0 0 2 Vi 11/01/2022 Volume Cours de thermodynamique M. Bouguechal Ph 21 4 Vf 26

3 Pour calculer cette intégrale, il faut connaitre la relation entre P et V et donc l’équation d’état du gaz. Dans le cas d’un gaz parfait, on a : 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 27

3 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 28

3 3. 2 Echange de chaleur 3. 2. 1 Notion de chaleur L’énergie peut être transférée sous d’autres formes, autre que le travail, elle peut être transférée sous forme de chaleur. Prenons un exemple pour comprendre le mécanisme d’un transfert d’énergie sous forme de chaleur et supposant qu’un système solide, par exemple un morceau de métal, soit en contact avec de l’air : le métal ayant une température par exemple inférieure à son environnement, les molécules de l’air vont entrer en contact avec le système et vont échanger de l’énergie avec ce solide : il y a transfert de chaleur. 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 29

3 L’agitation thermique dans l’air correspond translation et de rotation des molécules. à un mouvement de Les molécules de l’air viennent frapper la surface du solide : à chaque impact, les molécules de la surface extérieure reçoivent une certaine quantité de mouvement qui induit un mouvement de vibration du solide qui se transmet au fur et à mesure vers les atomes proches. Progressivement, l’agitation thermique passe dans le solide dont la température augmente : cette énergie s’est transférée sous forme de chaleur, c’est un transfert de l’agitation thermique des molécules Contrairement au travail, l’énergie transférée ici se fait de manière désordonnée, désordonnée car le mouvement des molécules et l’agitation des molécules est désordonnés. 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 30

3 ü Le l’énergie. ü La de l’énergie. 11/01/2022 est un mode de transfert de est un mode de transfert Cours de thermodynamique M. Bouguechal Ph 21 31

3 • Modèles d’échange de chaleur Il existe trois types d’échange de chaleur. ü Transfert de chaleur par conduction 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 32

3 ü Transfert de chaleur par convection 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 33

3 ü Transfert de chaleur par rayonnement 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 34

3 3. 2. 2 Formules d’échange de chaleur Comme le travail, la chaleur n’est pas une fonction d’état, ce n’est pas une différentielle totale exacte et son intégration dépend du chemin, elle peut s’écrire sous les formes suivantes, en utilisant deux variables parmi les trois variables P, V, T, la troisième n’est pas nécessaire car elle est liée aux autres par une équation d’état. 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 35

3 sont appelés coefficients calorimétriques. sont des coefficients extensifs. sont des coefficients intensifs. 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 36

3 Cv : Capacité calorifique massique (molaire)ou chaleur massique ( molaire ) à volume constant. Unités : J. K – 1. Kg – 1 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 37

3 CP : Capacité calorifique massique (molaire) ou chaleur massique ( molaire ) à pression constante. Unités : J. K – 1. Kg – 1 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 38

3 l : coefficient calorimétrique massique appelé chaleur latente de dilatation à température constante. Unités : Pa. h : coefficient calorimétrique massique appelé chaleur latente de compression à température constante. Unités : m 3. Kg – 1 ou m 3. mol-1 λ : coefficient calorimétrique massique de conductivité thermique à volume constant. Unités : m 3. Kg – 1 ou m 3. mol-1 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 39

3 ü Capacités calorifiques des solides et des liquides Les solides et les liquides subissent de faibles variations de volume et de pression quand on les chauffe, on définit alors de la capacité calorifique C massique d’un solide : 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 40

3 ü Capacités calorifiques des gaz Dans le cas des gaz, les variations de volume et de pression sont importantes lors de variation de température, il existe donc deux capacités calorifiques pour caractériser l’échange de chaleur : CV et CP. 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 41

3 Il y a six coefficients à déterminer, mais comme il y a des relations entre ces coefficients, on n’a pas besoin de connaitre tous les coefficients. Cherchons les relations entre ces coefficients. 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 42

3 3. 2. 3 Relations entre les coefficients calorimétriques Il suffit d’écrire que P = P( T, V ) ou T = T ( P, V ) ou encore V = V( P, T ), de remplacer de l’une des expressions de la chaleur et d’identifier avec une équation parmi les trois. 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 43

3 Ecrivons que : T = T ( P, V ) et déterminons la différentielle totale de T : 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 44

3 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 45

3 On identifie : 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 46

3 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 47

3 Ecrivons que : P = P ( V, T ) et déterminons la différentielle totale de P : Injectons 11/01/2022 cette relation dans la deuxième équation ( 2 ) de la chaleur Cours de thermodynamique M. Bouguechal Ph 21 48

3 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 49

3 On identifie : 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 50

3 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 51

3 Ecrivons que : V = V ( P, T ) et déterminons la différentielle totale de V : Injectons cette relation dans l’équation ( 3 ) de la chaleur 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 52

3 On identifie : 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 53

3 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 54

3 1 3 4 2 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 55

3 La connaissance de CP et CV permet de déterminer les autres coefficients calorimétriques. 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 56

3 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 57

3 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 58

3 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 59

3 La connaissance de CV et CP permet de déterminer tous les coefficients calorimétriques à condition de connaitre l’équation d’état du fluide. Si on ne connait pas l’équation d’état du fluide, il faut utiliser les coefficients thermoélastiques. 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 60

3 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 61

3 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 62

3 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 63

3 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 64

3 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 65

3 Autre méthode : Il est possible d’obtenir les formules précédentes en utilisant une méthode plus rapide. On prend nos équations, et on considère des transformations particulières : isobare, isotherme ou isochore. 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 66

3 Si on considère un échange de chaleur à pression constante, c’est-àdire une transformation isobare on peut donc écrire : 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 67

3 Si on considère un échange de chaleur à pression constante, c’est-àdire une transformation isochore on peut donc écrire : 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 68

3 3. 2. 3 Applications aux gaz parfaits L’équation d’état des gaz parfait étant connu, on peut alors déterminer les coefficients calorimétriques, signalons que ce calcul peut se faire pour n’importe quel fluide dont on connait l’équation d’état et les capacités calorifiques. 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 69

3 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 70

3 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 71

3 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 72

3 Fin de la leçon 3 11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 73

11/01/2022 Cours de thermodynamique M. Bouguechal Ph 21 74