3 Cintique des gaz et arosols 1 2



![Pression et température m = masse d’une molécule n = concentration en molécules [m-3] Pression et température m = masse d’une molécule n = concentration en molécules [m-3]](https://slidetodoc.com/presentation_image/0054bf85159a8ecb00a9a59a14f631c6/image-4.jpg)
![Libre parcours moyen n Molécule de diamètre d. n = concentration en molécules [m-3] Libre parcours moyen n Molécule de diamètre d. n = concentration en molécules [m-3]](https://slidetodoc.com/presentation_image/0054bf85159a8ecb00a9a59a14f631c6/image-5.jpg)


















- Slides: 25

3. Cinétique des gaz et aérosols 1. 2. Rappels et définitions Milieu constitué de 2 espèces

Vitesses Vitesse la plus probable Vp (équilibre de Boltzmann) n Vitesse moyenne : n n Vitesse quadratique moyenne :

Flux n C’est le nombre de molécules qui traversent à l’équilibre l’unité de surface par unité de temps. n = concentration en molécules [L-3]
![Pression et température m masse dune molécule n concentration en molécules m3 Pression et température m = masse d’une molécule n = concentration en molécules [m-3]](https://slidetodoc.com/presentation_image/0054bf85159a8ecb00a9a59a14f631c6/image-4.jpg)
Pression et température m = masse d’une molécule n = concentration en molécules [m-3] k = constante de Boltzmann 1, 380× 10 -23 J. K-1
![Libre parcours moyen n Molécule de diamètre d n concentration en molécules m3 Libre parcours moyen n Molécule de diamètre d. n = concentration en molécules [m-3]](https://slidetodoc.com/presentation_image/0054bf85159a8ecb00a9a59a14f631c6/image-5.jpg)
Libre parcours moyen n Molécule de diamètre d. n = concentration en molécules [m-3]

Libre parcours moyen pour un gaz S = constante de Sutherland P en k. Pa T en K 760 mm Hg = 1 atm = 1, 013× 105 Pa

Viscosité dynamique d’un gaz (Pa. s) 1 micropoise = 10 -7 Pa. s m = masse d’une molécule n = concentration en molécules [m-3]

3. Cinétique des gaz et aérosols 1. 2. Rappels et définitions Milieu constitué de 2 espèces

n n n 2 espèces (molécules ou molécules-particules) assimilables à des sphères rigides, sans interactions à distance. Température identique en tout point du système. Chocs élastiques n 1 et n 2 sont les concentrations respectives de chaque espèce m 1 et m 2 sont les masses respectives de chaque espèce

Libre parcours moyen

Cas d’un aérosol n Si n 2 << n 1 et m 2 >> m 1 (cas d’une particule dans un gaz) d 12 rayon de la particule

Coefficient de diffusion n n 1 et n 2 : concentrations indépendantes de t La répartition est uniforme dans chaque plan // au plan xy n La diffusion se fait // à z n Equilibre de T et P dans tout le volume considéré. n

n n = n 1+ n 2 ne dépend pas de z x p n 2 Flux des 2 o Flux des 1 n 1 z

Flux 1 Flux 2 (en général) n Pour conserver n : n D 12 = coefficient de diffusion = [L 2 T-1]

n Si 1 et 2 sont identiques : coefficient de diffusion simple. n On peut écrire :

Formule de Maxwell Chapman n m 1 et m 2 : masse des molécules

n Si m 2 >> m 1 (cas de particules dans un gaz)

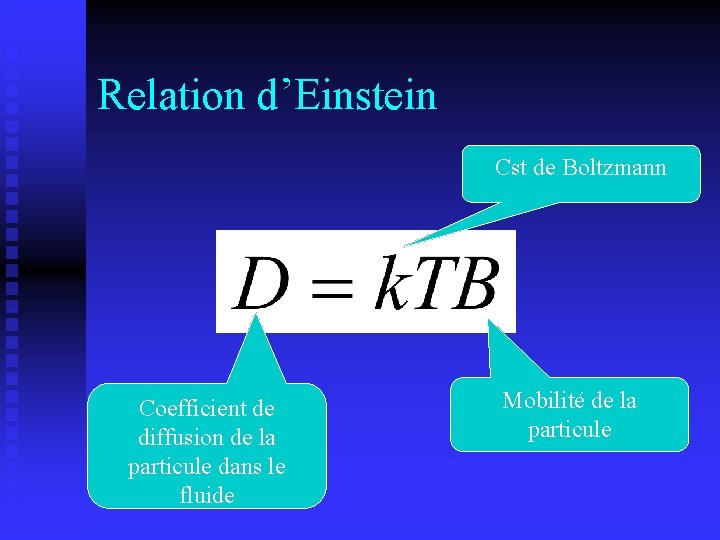
Relation d’Einstein Cst de Boltzmann Coefficient de diffusion de la particule dans le fluide Mobilité de la particule

Libre parcours moyen apparent d’un aérosol n Distance parcourue par la particule avant que sa direction change de /2. Vm= vitesse thermique moyenne de la particule

Temps de relaxation n Les particules sont soumises en permanence à des chocs. V 0 = vitesse moyenne (dans la direction oz) des particules à l’instant t 0 = temps de relaxation de l’aérosol

Distance d’arrêt d’un aérosol de vitesse initiale V 0 : n n A l’instant t la molécule à parcouru : Distance parcourue par la particule avant que sa direction ne change de /2.

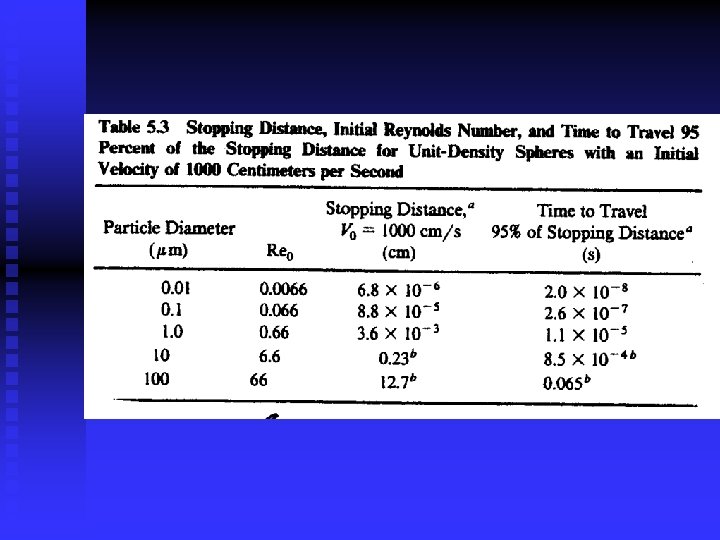
Distance d’arrêt d’une particule n Mercer (1973) : pour 1 < Rep 0< 400


Fuchs (1964) n Particules de masse volumique 1000 kg/m 3 dans de l’air à pression atmosphérique et à 20 °C.

Equations de la diffusion : lois de Fick n 1ère loi de Fick : n 2ème loi de Fick :