3 BLM Kuantum Dalga Mekaniinin Tarihsel Boyutu Elektronun

3. BÖLÜM Kuantum Dalga Mekaniğinin Tarihsel Boyutu Elektronun ikili davranışı Elektronların dalga özelliği 1

Atomun yapısı 3. Bölüm Kazanımlar 3. Atomun kuantum modeli ile ilgili olarak öğrenciler; 3. 1. Atomlar/ iyonlar için, ‘orbital’ kavramını, elektronların bulunma olasılığı ile ilişkilendirerek tanımlar. 3. 2. Orbitallerin sembol gösterimlerini, geometrilerini, yönlenmelerini ve elektronun enerjisini kuantum sayıları ile ilişkilendirir. 3. 3. Çok elektronlu sistemlerde orbitallerin enerji sırasını belirler. 3. 4. Atomlar ve iyonlar için elektron dizilimlerini yazar.

Elektronların dalga özelliği Elektronlar bir atom içinde belirli bir enerji değerine sahiptir. Kuantum mekaniğine göre elektronlar hem tanecik hem de dalga gibi davranmaktadırlar. Normalde bir parçacık olan atomlar dalga gibi davranmaktadır. 3

Dalga – Tanecik Özelliği Louise de Broglie ve Schrödinger ışığın dalga ve tanecik teorilerini birleştirerek bugünkü dalga mekaniğinin temelini oluşturdular. Broglie bir fotonun enerjisini hesaplayabilmek için Plank bağıntısını ve Einstein enerji eşitliğini birlikte kullandı. 4
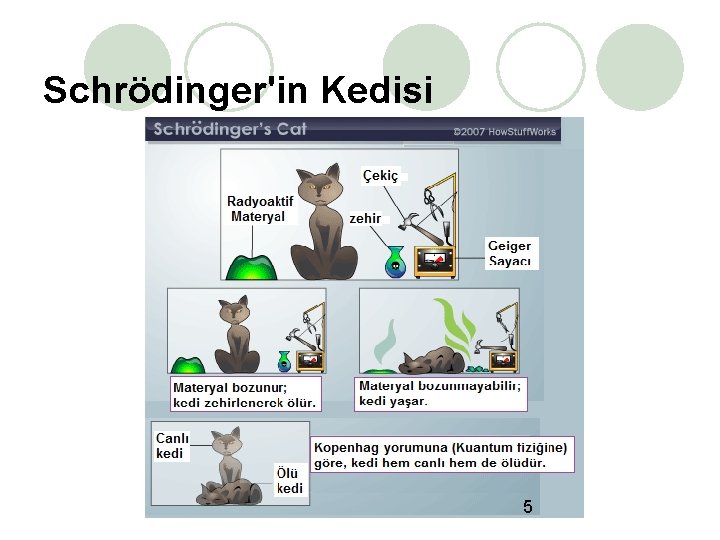
Schrödinger'in Kedisi 5

Schrödinger'in Kedisi Deneyde kapalı bir kutunun içinde bir düzenek ve başlangıçta canlı olan bir kedi vardır. (Kutunun içinin hiçbir şekilde gözlemlenememesi çok önemli bir noktadır. Bunun sebebi Kopenhag Yorumu'dur. ) Düzeneğin içeriği şöyledir: Bozunma olasılığı %50 olan bir parçacık, bu parçacığın bozunmasıyla ortama yayılacak olan zehirli 6 gazdır.

Einstein E= mc 2 Plank E= hⱱ mc 2 = hⱱ ⱱ=c/ʎ olduğundan mc 2 = h. c/ʎ 7

De Broglie'ye göre Bir taneciğin dalga boyu taneciğin hızı, kütlesi ve Planck sabiti h’a bağlıdır. X-ışınları kırınımından yola çıkarak hareket eden maddesel parçacıkların dalga gibi davranabileceğini söyledi. 8

De Broglie Maddesel taneciklere bir arada kabul edilen dalgalara madde dalgaları denir. Küçük tanecikler için madde dalgaları varsa elektron gibi taneciklerin demetleri de dalgaların özelliklerini taşımalıdır. 9

Elektronların dalga özelliği Işık bir dalga mıdır, yoksa bir parçacık mıdır? Bu soruya de Brogli'nin kuramından sonra "Işık bir dalgadır. " dalgadır şeklinde yanıt verebiliriz. Ancak soruyu gözlenmekte olan olaya göre yanıtlamak daha doğrudur. Bazı olaylar, foton kavramı temeline dayalı olarak daha iyi açıklanabilirken, bazıları ise dalga modeliyle daha iyi açıklanabilir. Sonuçta foton ve dalga kuramı birbirinin tamamlayıcısıdır. 10

Elektronların dalga özelliği gösterdiğinin kanıtı a) İnce bir Alüminyum tabakasının elektron kırınımı görüntüsü b) İnce bir Alüminyum tabakasının X ışınları kırınımı görüntüsü Bu iki şeklin arasındaki benzerliklere dikkat edildiğinde elektronların da X- ışınları gibi dalga özelliği gösterdiği anlaşılır. 11

HEISENBERG BELİRSİZLİK İLKESİ a) Elektronu gözlemlemek için uzun dalga boylu ışın kullandığımızda elektronun hızı ve konumundaki belirsizlik yüksektir. b) Kısa dalga boylu ışın kullandığımızda (yüksek enerji) hızdaki belirsizlik yüksektir. Kısa dalga boylu ışın kullanmanın sonucunda foton ile çarpışan elektrona enerji aktarılır ve hareket yönü değişebilir. 12

HEISENBERG BELİRSİZLİK İLKESİ Bir parçacığın konumu ve hızı aynı anda tam olarak ölçülemez. Buna Heisenberg belirsizlik ilkesi denir. 13

HEISENBERG BELİRSİZLİK İLKESİ Bu belirsizlik ölçü aletlerinin yetersizliğinden kaynaklanmamaktadır. Bu yapısal bir belirsizliktir. 14
Elektronun yörüngesi var mı? Heisenberg belirsizlik ilkesini hidrojen atomuna uyguladığımız zaman, Bohr'un düşündüğü gibi, elektronun belirli bir yörünge üzerinde hareket etmediğini görürüz. 15

BOHR MODELİNİN YETERSİZLİĞİ Dalga-tanecik ikiliğinin sonucunun belirsizlik ilkesi olduğu anlaşıldığında Bohr atom modelindeki temel hatanın, bir elektronun yörünge dışında hareket edemeyeceğini kabul etmek olduğu anlaşılacaktır. Bu açıklamadan sonra atomdaki elektronların davranışı farklı bir yaklaşımla ele alınabilir. 16
17


Atomun Kuantum Modeli Schrödinger Atom modelinde yörünge yerine atomik orbitallerden bahsedilir. Orbital: Orbital Bir elektronun çekirdeğin çevresinde bulunma olasılığının en çok olduğu hacme denir.
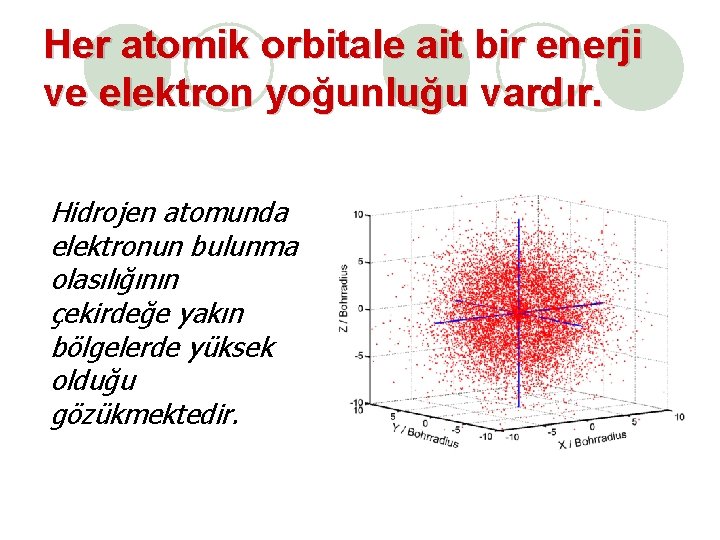
Her atomik orbitale ait bir enerji ve elektron yoğunluğu vardır. Hidrojen atomunda elektronun bulunma olasılığının çekirdeğe yakın bölgelerde yüksek olduğu gözükmektedir.

KUANTUM SAYILARI Kuantum mekaniğinde, elektronların hidrojen ve diğer atomlarda dağılımlarını vermek için üç kuantum sayısı gerekmektedir. Bu sayılar; 1. Baş kuantum sayısı (n) 2. Açısal momentum kuantum sayısı (l) 3. Manyetik kuantum sayısı (ml) 4. Elektron spin kuantum sayısı (ms)

1. BAŞ KUANTUM SAYISI (n) Baş kuantum (n) 1, 2, 3 gibi tamsayıdır. Baş kuantum sayısı, belirli bir orbitaldeki elektronun çekirdeğe olan ortalama uzaklığı ile ilgilidir.

Açısal Momentum (ikincil) Kuantum Sayısı (l) l ile gösterilir. n-1 kadardır. n=4 ise l=4 -1=3’tür. l’nin aldığı değerler: s, p, d, f l 0 1 2 3 Orbitalin sembolü s p d f

Manyetik Kuantum Sayısı ml ile gösterilir. 2 l+1 kadardır. l=0 olursa ml= 1 olur (s). l=1 olursa ml=3 olur. m=-1, 0, 1 değerlerini alır. (px, py, pz) l=2 olursa ml=5 olur. m=-2, -1, 0, 1, 2 değerlerini alır. (dx 2 -y 2, dz 2, dxy, dxz, dyz, ) ml

Kuantum sayıları ve orbitaller
Orbital Çeşitleri 1 s
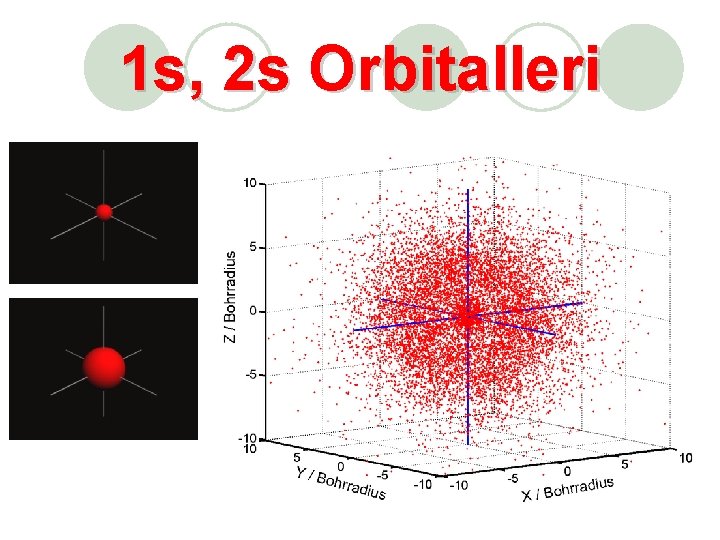
1 s, 2 s Orbitalleri

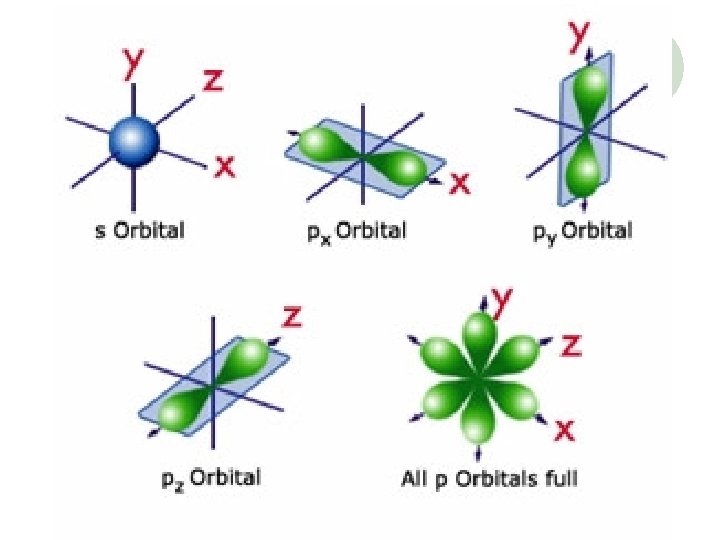
2 p orbitalleri 2 py 2 p x 2 p z
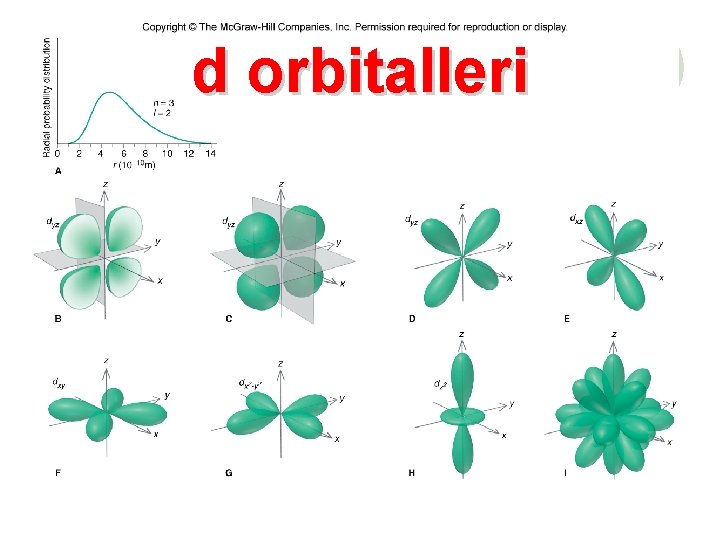
d orbitalleri

ORBİTALLER

1 orbital en fazla 2 e- alır. • • s orbitali 1 tanedir. En fazla 1 x 2=2 e- alır. p orbitali 3 tanedir. En fazla 3 x 2=6 e- alır. d orbitali 5 tanedir. En fazla 5 x 2=10 e- alır. f orbitali 7 tanedir. En fazla 7 x 2=14 e- alır.
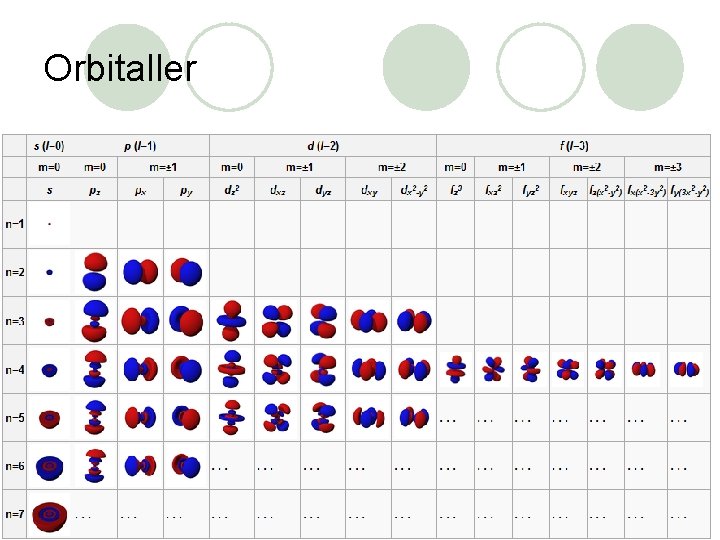
Orbitaller
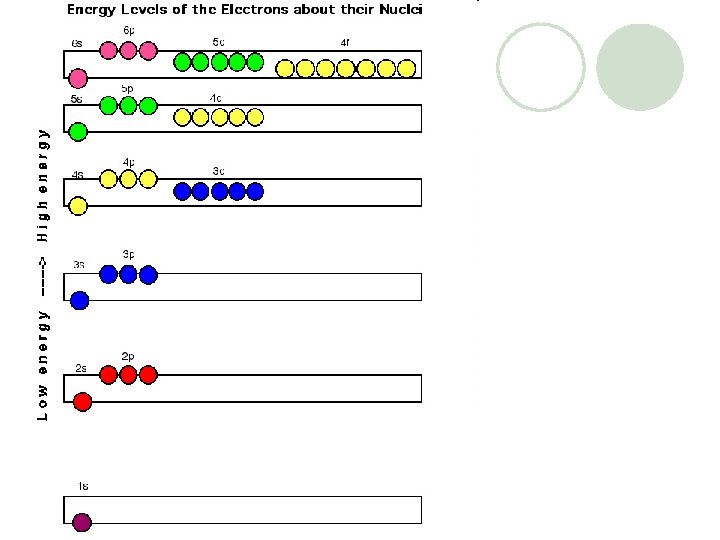
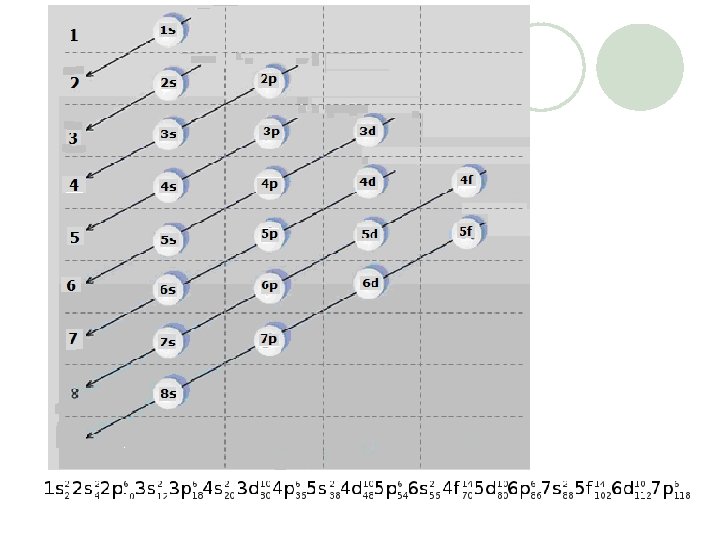
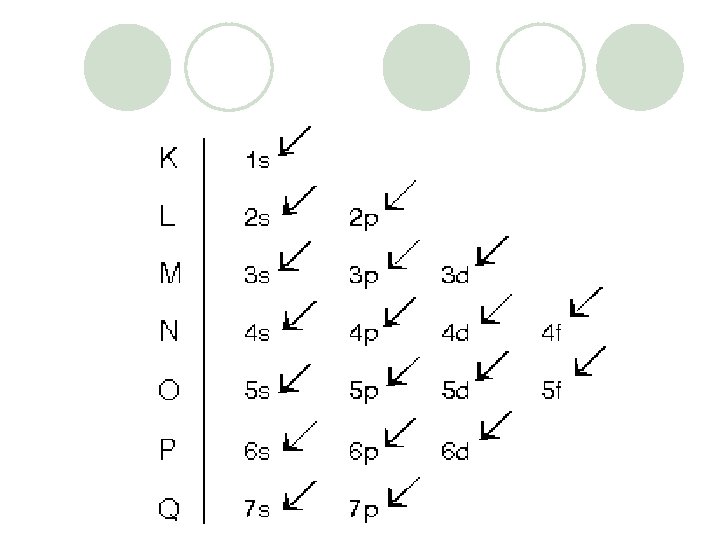



Pauli Kuralı: Elektronlar çekirdeğin çevresinde dönerken aynı zamanda kendi eksenleri etrafında da dönerler. Birisi saat ibresi yönünde dönerken diğeri onun tersi yönünde döner. (+1/2, -1/2)

Elektronların orbitallere yerleşmesi 1 H: 1 s 1 2 He: 1 s 2 3 Li: 1 s 2 / 2 s 1 2 / 2 s 2 Be: 1 s 4

Elektronların orbitallere yerleşmesi 5 B 1 s 2/2 s 22 px 1
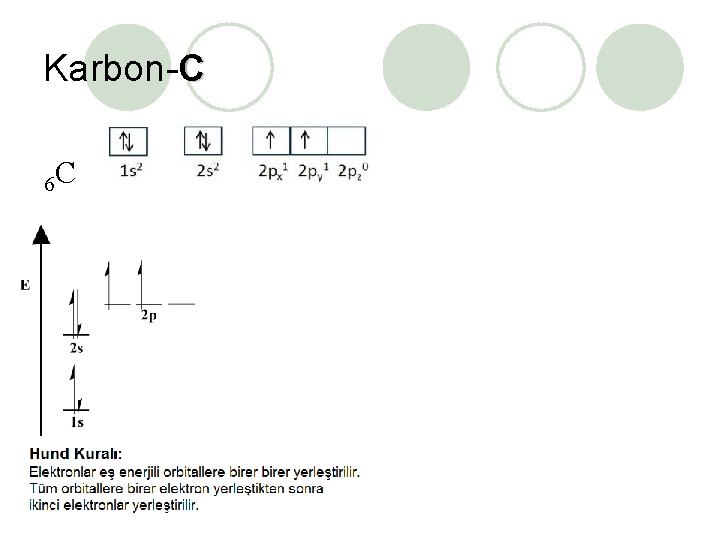
Karbon-C 6 C

Azotun elektronlarının orbitallere yerleşmesi 7 N: 2 1 s / 2 1 1 1 2 s 2 px 2 py 2 pz

Oksijenin elektronlarının orbitallere yerleşmesi 8 O: 2 2 2 1 1 1 s /2 s 2 px 2 py 2 pz

Elektronların orbitallere yerleşmesi F 9 2 2 1 1 s /2 s 2 px 2 py 2 pz 10 Ne 2 2 2 1 s /2 s 2 px 2 py 2 pz

Elektronların orbitallere yerleşmesi 12 Mg 1 s 2/2 s 22 p 6/3 s 2 [Ne]3 s 2 16 S 1 s 2/2 s 22 p 6/3 s 23 px 23 py 13 pz 1 [Ne]3 s 23 px 23 py 13 pz 1 18 Ar 1 s 2/2 s 22 p 6/3 s 23 px 23 py 23 pz 2 [Ne]3 s 23 px 23 py 23 pz 2



Elektronların orbitallere yerleşmesi Atom Numarası Sembol Elektron Dizilimi 1 H 1 s 1 2 He 1 s 2 = [He] 3 Li [He] 2 s 1 4 Be [He] 2 s 2 5 B [He] 2 s 2 2 p 1 6 C [He] 2 s 2 2 p 2
![7 N [He] 2 s 2 2 p 3 8 O [He] 2 s 7 N [He] 2 s 2 2 p 3 8 O [He] 2 s](http://slidetodoc.com/presentation_image/46ce97238dbe5968c8380974550266d8/image-52.jpg)
7 N [He] 2 s 2 2 p 3 8 O [He] 2 s 2 2 p 4 9 F [He] 2 s 2 2 p 5 10 Ne [He] 2 s 2 2 p 6 = [Ne] 11 Na [Ne] 3 s 1 12 Mg [Ne] 3 s 2
![13 Al [Ne] 3 s 2 3 p 1 14 Si [Ne] 3 s 13 Al [Ne] 3 s 2 3 p 1 14 Si [Ne] 3 s](http://slidetodoc.com/presentation_image/46ce97238dbe5968c8380974550266d8/image-53.jpg)
13 Al [Ne] 3 s 2 3 p 1 14 Si [Ne] 3 s 2 3 p 2 15 P [Ne] 3 s 2 3 p 3 16 S [Ne] 3 s 2 3 p 4 17 Cl [Ne] 3 s 2 3 p 5 18 Ar [Ne] 3 s 2 3 p 6 = [Ar] 19 K [Ar] 4 s 1
![20 Ca [Ar] 4 s 2 21 Sc [Ar] 4 s 2 3 d 20 Ca [Ar] 4 s 2 21 Sc [Ar] 4 s 2 3 d](http://slidetodoc.com/presentation_image/46ce97238dbe5968c8380974550266d8/image-54.jpg)
20 Ca [Ar] 4 s 2 21 Sc [Ar] 4 s 2 3 d 1 22 Ti [Ar] 4 s 2 3 d 2 23 V [Ar] 4 s 2 3 d 3 24 Cr [Ar] 4 s 1 3 d 5 25 Mn [Ar] 4 s 2 3 d 5 26 Fe [Ar] 4 s 2 3 d 6 27 Co [Ar] 4 s 2 3 d 7 28 Ni [Ar] 4 s 2 3 d 8
![30 Zn [Ar] 4 s 2 3 d 10 31 Ga [Ar] 4 s 30 Zn [Ar] 4 s 2 3 d 10 31 Ga [Ar] 4 s](http://slidetodoc.com/presentation_image/46ce97238dbe5968c8380974550266d8/image-55.jpg)
30 Zn [Ar] 4 s 2 3 d 10 31 Ga [Ar] 4 s 2 3 d 10 4 p 1 32 Ge [Ar] 4 s 2 3 d 10 4 p 2 33 As [Ar] 4 s 2 3 d 10 4 p 3 34 Se [Ar] 4 s 2 3 d 10 4 p 4 35 Br [Ar] 4 s 2 3 d 10 4 p 5 36 Kr [Ar] 4 s 2 3 d 10 4 p 6 = [Kr]


Aynı grupta bulunan elementlerin orbitallerinde aynı sayıda elektron vardır. IA Grubu 7 A Grubu 1 H 1 s 1 3 Li [He] 2 s 1 9 F [He] 2 s 2 2 p 5 11 Na [Ne] 3 s 1 17 Cl [Ne] 3 s 2 3 p 5
![Li (Z = 3): [He] 2 s 1 Be (Z = 4): [He] 2 Li (Z = 3): [He] 2 s 1 Be (Z = 4): [He] 2](http://slidetodoc.com/presentation_image/46ce97238dbe5968c8380974550266d8/image-58.jpg)
Li (Z = 3): [He] 2 s 1 Be (Z = 4): [He] 2 s 2 B (Z = 5): [He] 2 s 2 2 p 1 C (Z = 6): [He] 2 s 2 2 p 2 N (Z = 7): [He] 2 s 2 2 p 3 O (Z = 8): [He] 2 s 2 2 p 4 F (Z = 9): [He] 2 s 2 2 p 5 2 6

Orbitallerde Elektronların Yerleşim Kuralları Pauli İlkesi • Bir atomda kuantum sayıları birbirinin aynı olan iki elektron yoktur. • n, l, ml ve ms kuantum sayıları hiçbir zaman birbirinin aynısı olamaz. • n, l, ml aynı olsa bile ms leri farklıdır. • Yani bir orbitaldeki iki elektronun dönme yönleri (spinleri) farklıdır.

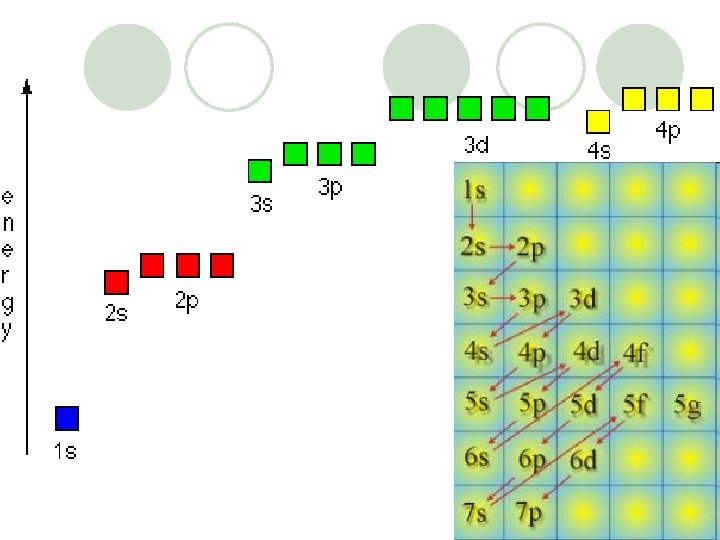
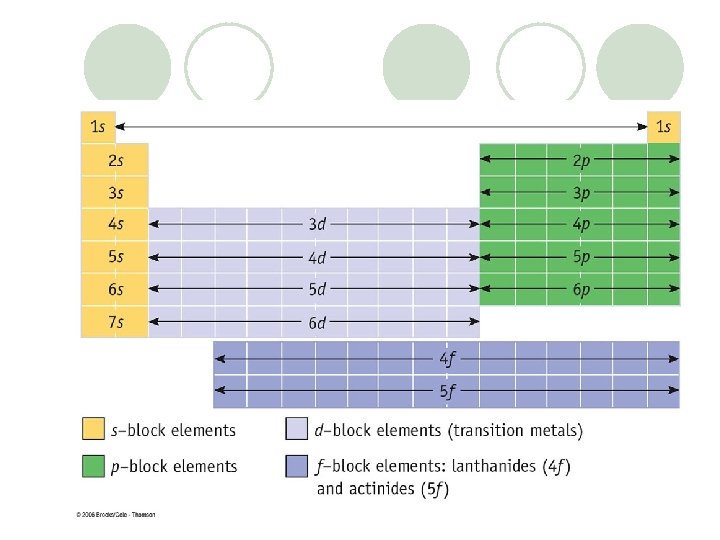
Orbitallerde Elektronların Yerleşim Kuralları Aufbau Yöntemi • Elektronlar orbitallere atomun enerjisi en az olacak şekilde yerleşir. • 1 s 2 s 2 p 3 s 3 p 4 s 3 d 4 p 5 s 4 d 5 p 6 s 4 f 5 d 6 p 7 s 5 f • Bu sırada yerleşir.

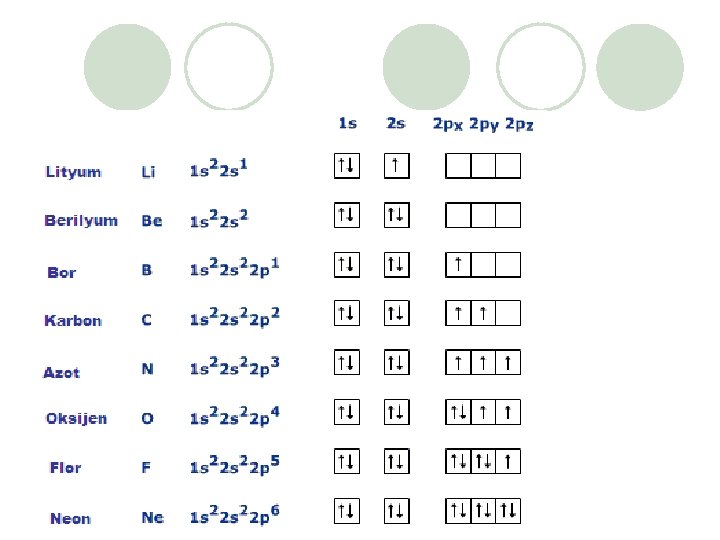
Orbitallerde Elektronların Yerleşim Kuralları Hund Kuralı • Aynı enerjiye sahip farklı orbitallerin (alt kabuk orbitallerine) eş enerjili orbitaller denir. Örneğin 2 px, 2 py, 2 pz orbitalleri eş enerjilidir. • Elektronlar eş enerjili orbitallere teker yerleştirilir, eş enerjili orbitallerin tamamı birer elektron aldıktan sonra diğer elektronları ters spinli olarak almaya başlar. Buna Hund Kuralı denir.

Küresel Simetri Bir atomun elektron dizilişindeki en son orbitalin tam dolu ya da yarı dolu olması atoma küresel simetrik durum kazandırır. Bu durumdaki atom daha çok kararlıdır. Bir atomun elektron dizilişi s 1, s 2, p 3, p 6, d 5, d 10, f 7, f 14 ile bitiyorsa o atom küresel simetri özelliği gösterir.

Soru: 15 X, 13 Y ve 25 Z atomlarından hangisi ya da hangileri küresel simetri gösterir? 1 s 2 2 p 6 3 s 2 3 p 3 (P 3 ile bittiği için küresel simetri) Çözüm: 15 X: 2 2 s 2 2 p 6 3 s 2 3 p 1 Y: 1 s 13 (p 1 ile bittiği için küresel simetri değil) 2 2 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 5 Z: 1 s 25 (d 5 ile bittiği için küresel simetri)

6 C küresel simetrik mi? Küresel simetriden kazanılan kararlılık sebebi ile elektronların atom içinde yer değiştirme olayı s orbitalinden d orbitaline olduğu halde, d orbitalinden p orbitaline olmaz.
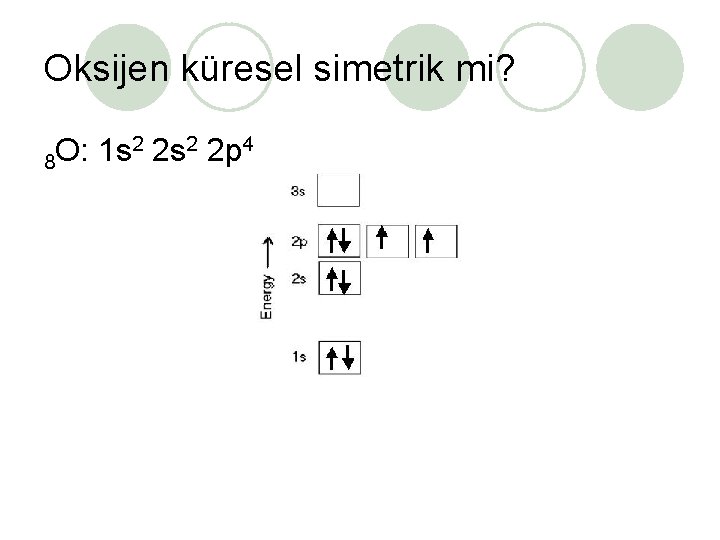
Oksijen küresel simetrik mi? 2 2 s 2 2 p 4 O: 1 s 8

![Cr ve Cu atomlarında küresel simetri var mı? Cr (Z = 24): [Ar] 4 Cr ve Cu atomlarında küresel simetri var mı? Cr (Z = 24): [Ar] 4](http://slidetodoc.com/presentation_image/46ce97238dbe5968c8380974550266d8/image-68.jpg)
Cr ve Cu atomlarında küresel simetri var mı? Cr (Z = 24): [Ar] 4 s 2 3 d 4 Cr (Z = 24): [Ar] 4 s 1 3 d 5 Cu (Z = 29): [Ar] 4 s 2 3 d 9 Cu (Z = 29): [Ar] 4 s 1 3 d 10
![SORU : Kromun temel hal elektron dizilişi, Cr: [Ar]4 s 2 3 d 4 SORU : Kromun temel hal elektron dizilişi, Cr: [Ar]4 s 2 3 d 4](http://slidetodoc.com/presentation_image/46ce97238dbe5968c8380974550266d8/image-69.jpg)
SORU : Kromun temel hal elektron dizilişi, Cr: [Ar]4 s 2 3 d 4 yerine, Cr: [Ar]4 s 1 3 d 5 dir. Niçin? daha kararlı
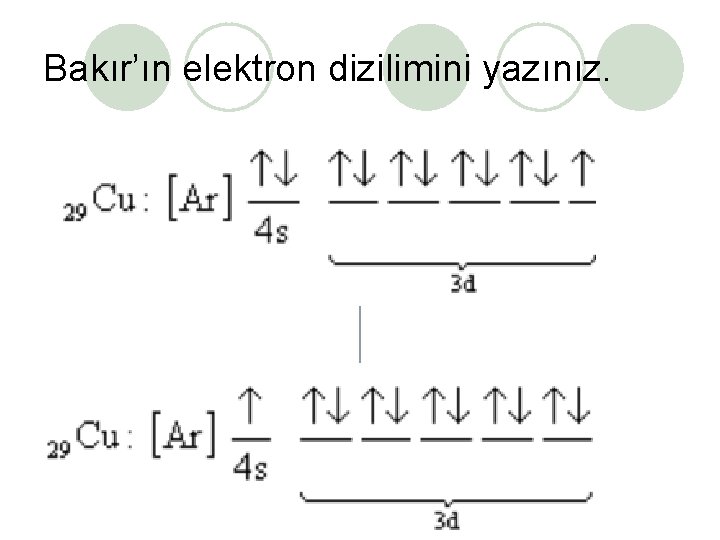
Bakır’ın elektron dizilimini yazınız.

Atomun Yapısı 5. Bölüm: Mol 4. Bağıl atom kütlesi ve mol kavramı ile ilgili olarak öğrenciler; 4. 1. İkili hidrojen bileşiklerinde, 1 g hidrojen ile birleşen diğer element kütleleri temelinde bağıl atom kütlesini tanımlar. 4. 2. Hidrojen ile bileşik yapmayan elementlerin bağıl atom kütlelerinin nasıl bulunabileceğini açıklar. 4. 3. Elementler ve bileşikler için mol kavramını açıklar.
- Slides: 71