3 A HIDROGNATOM SZERKEZETE 1 3 1 A















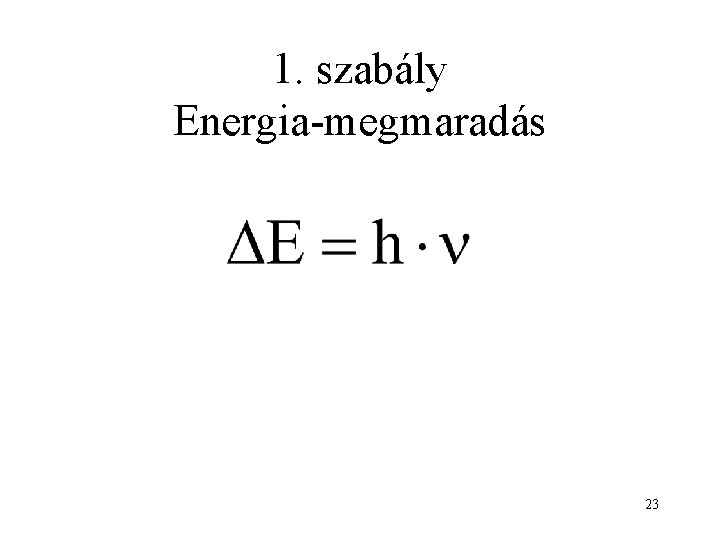











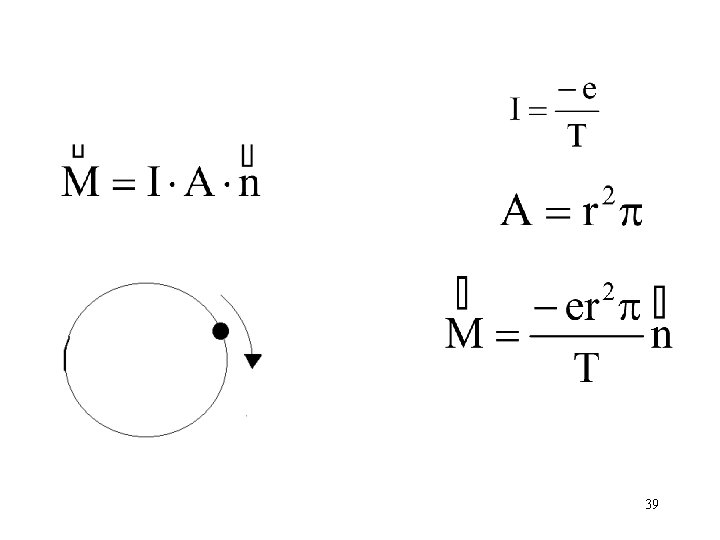















- Slides: 57

3. A HIDROGÉNATOM SZERKEZETE 1

3. 1. A hidrogénatom Schrödinger -egyenlete 2

A hidrogénatom klasszikus mechanikai modellje + Pozitív töltésű részecske, amely körül egy negatív töltésű részecske mozog („kering”). 3

A kvantummechanika Schrödinger-egyenlete általános formában 4

A hidrogénatom Schrödinger-egyenlete Megj. : alsó indexben e és p elektronra és protonra utal, e elemi töltés (1, 602 x 10 -19 C), elektron töltése -e r az elektron protontól való távolsága, vákuum permittivitás (8, 854 10 -12 Fm-1). 5

A hidrogénatom Schrödingeregyenlete megoldható! A megoldás trükkje: polár-koordináta rendszert alkalmazunk. 6

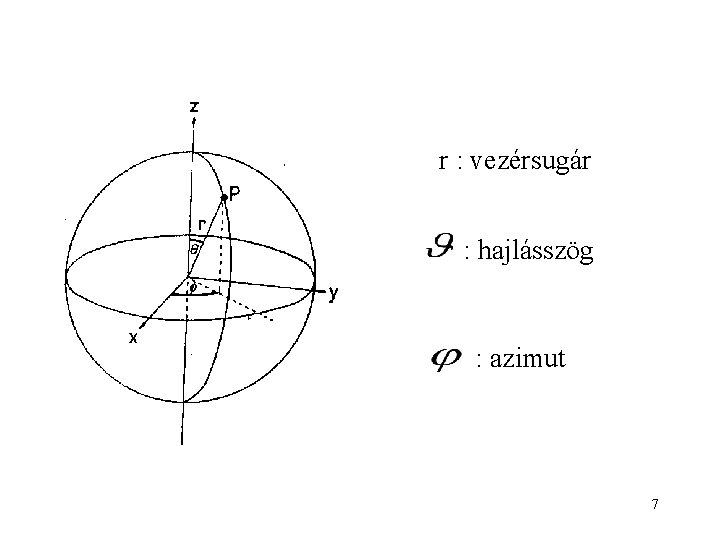
r : vezérsugár : hajlásszög : azimut 7

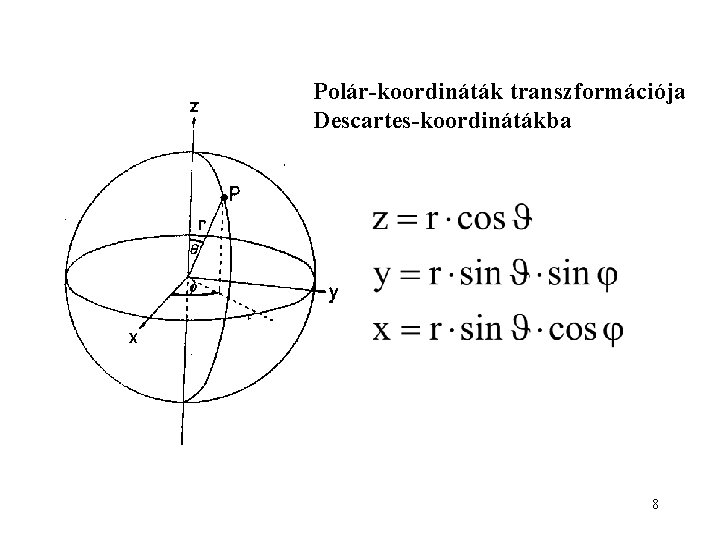
Polár-koordináták transzformációja Descartes-koordinátákba 8

A Schrödinger-egyenlet megoldása Sajátérték n: főkvantumszám 1, 2, 3. . . 9

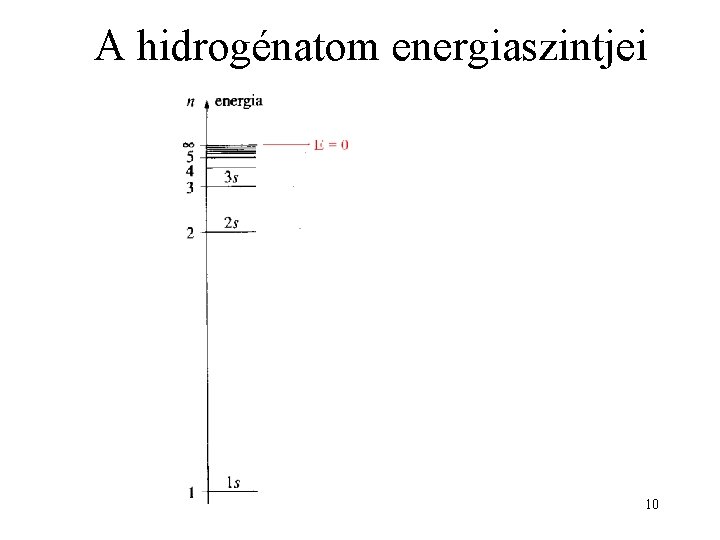
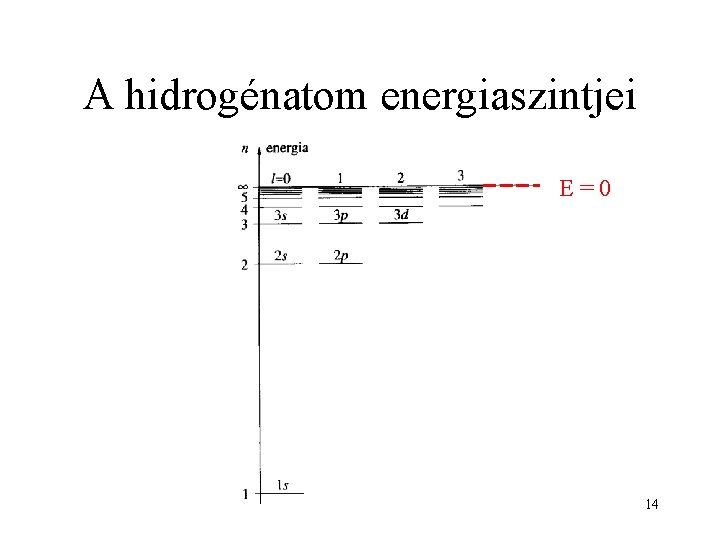
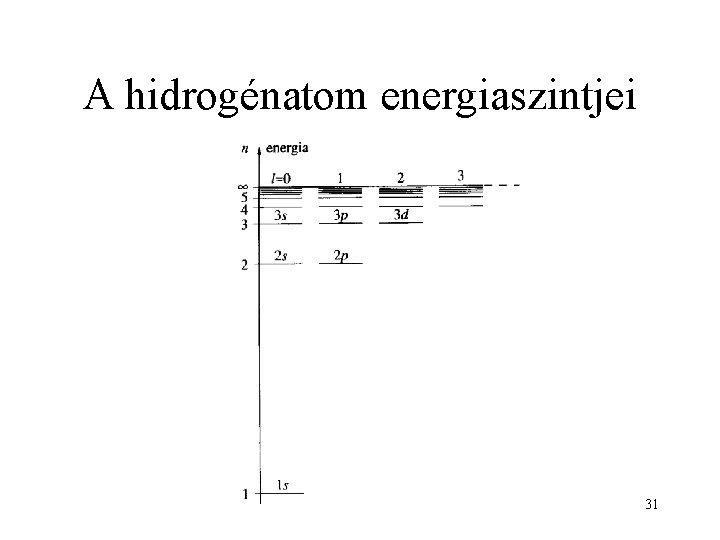
A hidrogénatom energiaszintjei 10

A Schrödinger-egyenlet megoldása Sajátfüggvények („atompályák”) Három egész számot tartalmaznak 11

A Schrödinger-egyenlet megoldása Degenerált állapotok 12

A Schrödinger-egyenlet megoldása Degenerált állapotok Ha n megegyezik, de és/vagy m nem, azok a H-atom degenerált állapotai 13

A hidrogénatom energiaszintjei E=0 14

A sajátfüggvények alakja radiális rész anguláris (szögtől függő) rész 15

A hidrogénatom komplex hullámfüggvényei 16

Lineár-kombinációk (ábrázolhatóság miatt) 17

A hidrogénatom valós hullámfüggvényei 18

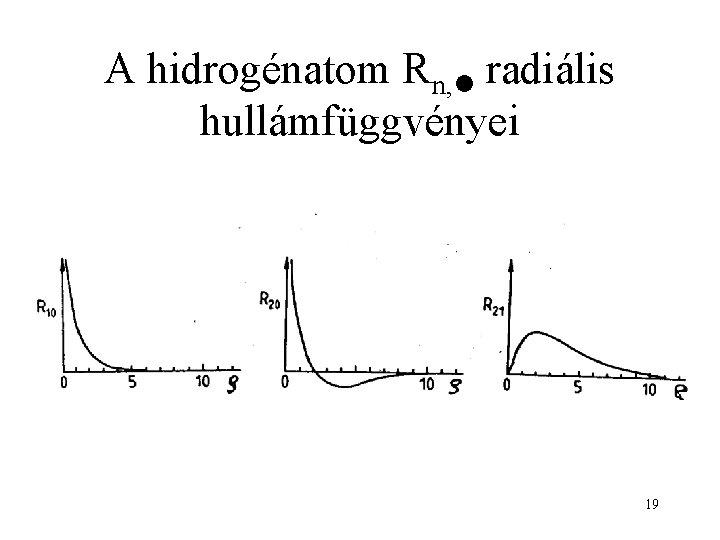
A hidrogénatom Rn, radiális hullámfüggvényei 19

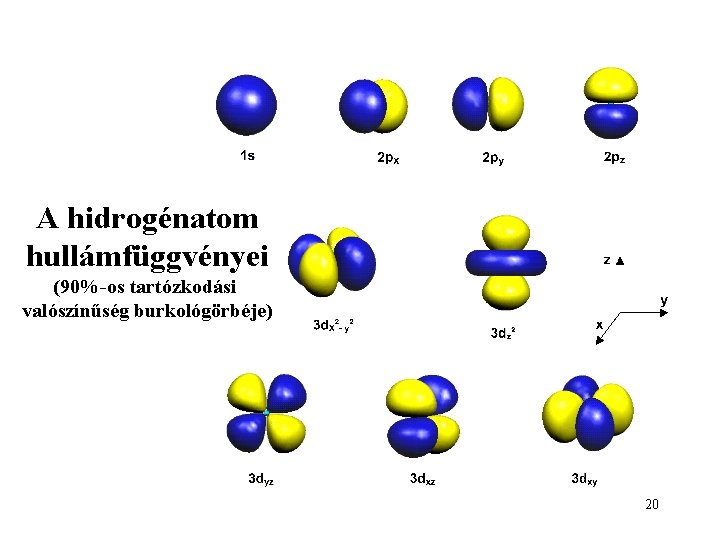
A hidrogénatom hullámfüggvényei (90%-os tartózkodási valószínűség burkológörbéje) 20

3. 2 A hidrogénatom színképe 21

Kiválasztási szabályok: az elektromágneses sugárzás elnyelésének/kibocsátásának feltételei (Levezethető kvantum-mechanika axiómából) 22
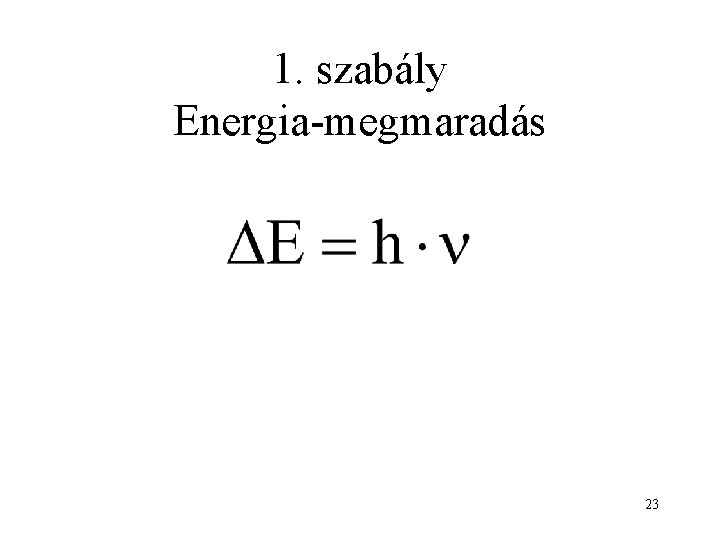
1. szabály Energia-megmaradás 23

2. szabály: az átmeneti momentumhoz kapcsolódik Átmeneti momentum és állapotfüggvény 1 -es index: kiindulási állapotban dipólus-momentum operátor 2 -es index: végállapotban 24

Dipólus momentum d - + egy pozitív és egy negatív töltés q : a töltés d: a távolság; a negatív töltéstől a pozitív töltés irányába mutat 25

Több töltés esetén q : a töltés 26

Hidrogénatomra vonatkozó kiválasztási szabályok bármennyi 28

A hidrogénatom színképe diszkrét vonalak! 29

Az atomos hidrogén spektruma 30

A hidrogénatom energiaszintjei 31

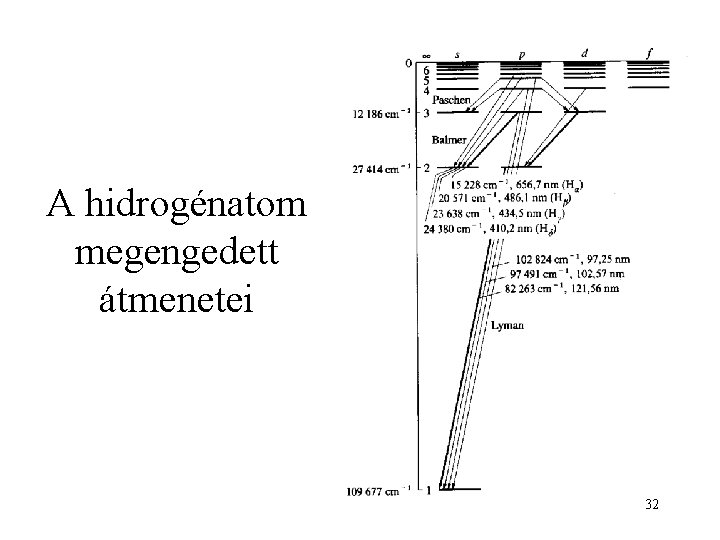
A hidrogénatom megengedett átmenetei 32

A hidrogénatom vonalszériái 33

3. 3 -3. 4 A hidrogénatom elektronjának impulzusmomentuma, mágneses momentuma (Előadás alapján) 34

Mikrorészecskék kvantált fizikai mennyiségei • • • E energia L impulzus-momentum absz. értéke Lz impulzus-momentum z-irányú vetülete M mágneses momentum abszolút értéke Mz mágneses momentum z-irányú vetülete 35

A klasszikus mechanikában körmozgást végző testre m: tömeg 36

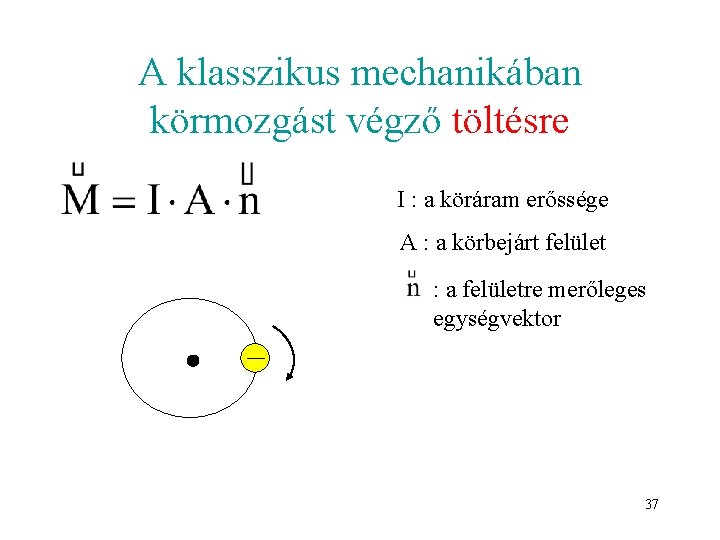
A klasszikus mechanikában körmozgást végző töltésre I : a köráram erőssége A : a körbejárt felület : a felületre merőleges egységvektor 37

Próbáljuk meg összefüggésbe hozni az impulzus-momentummal! 38
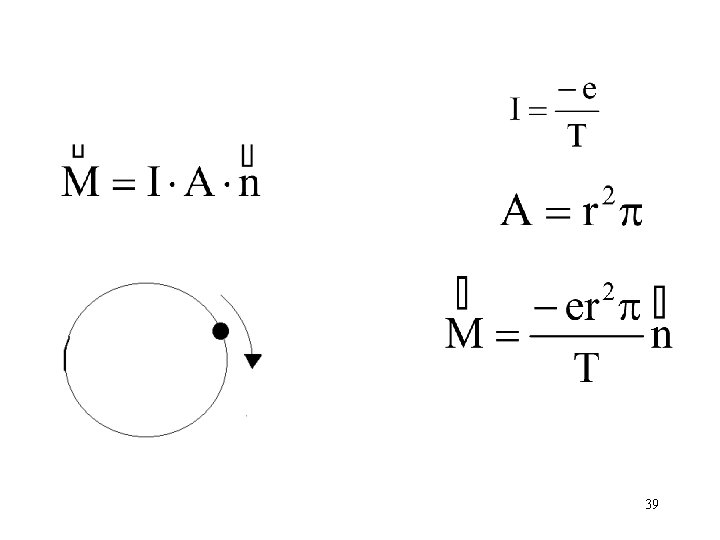
39

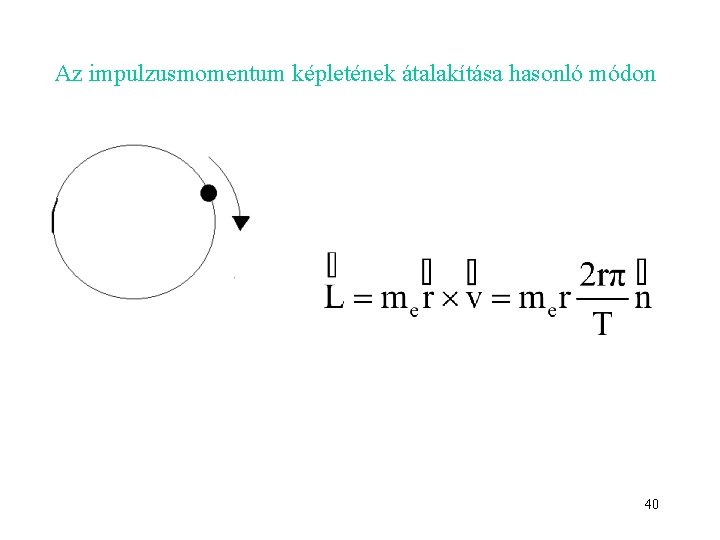
Az impulzusmomentum képletének átalakítása hasonló módon 40

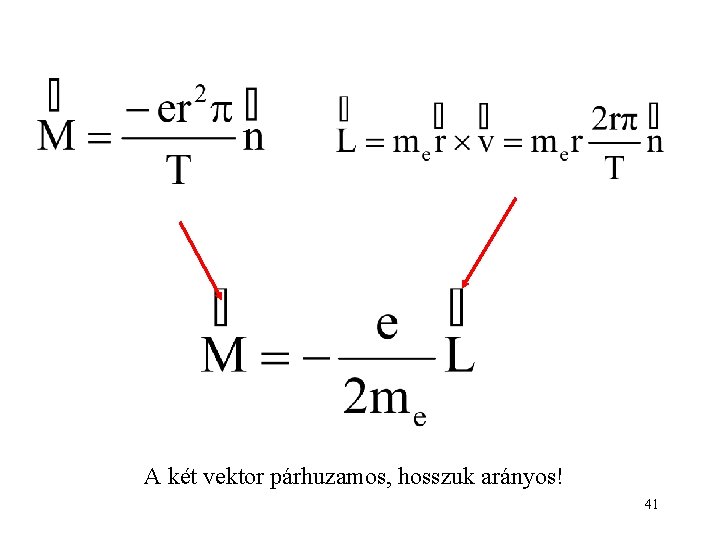
A két vektor párhuzamos, hosszuk arányos! 41

H-atomra kvantum-mechanikai levezetéssel (sajátérték-egyenletből) mellék-kvantumszám m: mágneses kvantumszám 42

H-atomra az M és L közötti arányosság alapján Bohr-magneton 43

H-atomra az M és L közötti arányosság alapján m : mágneses kvantumszám 44

Mágneses térben levő részecske potenciális energiája Klasszikus fizika: Kvantummechanika : mágneses indukció 45

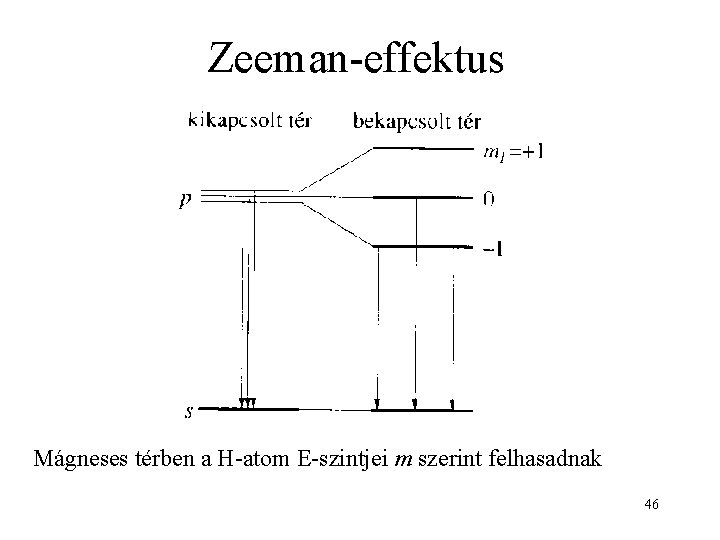
Zeeman-effektus Mágneses térben a H-atom E-szintjei m szerint felhasadnak 46

3. 5 Az elektronspin 47

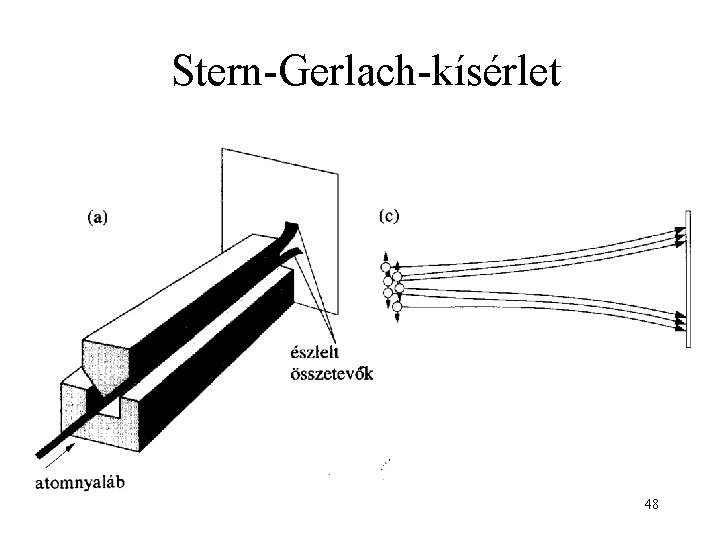
Stern-Gerlach-kísérlet 48

Ezüst-atom sugár kísérlet (hidrogénatommal a kísérlet nehezebb, de az eredmény hasonló. ) Alapáll. : n =1; és m csak 0 lehet! Nem hat az atomra erő, nem térül el Eredmény: két irányba eltérül!! 49

Értelmezés Alapállapotban is van impulzusmomentum, amelyből mágneses momentum adódik. Ez az impulzusmomentum a spin. Jele: abszolút értéke: S z-irányú vetülete: Sz 50

Az elektron spinje : spinre utaló mellék-kvantumszám s spin-kvantumszám (spinre utaló mágneses kvantumszám) 51

Spinből származó mágneses momentum abszolút érték z irányú komponens ge : Lande-faktor hidrogénatomban ge=2, 0023 52

A spinból származó mágneses momentum magyarázza a Stern-Gerlach kísérletet! 53

Spin értelmezése: Paul Dirac (1902 -1984) Relativisztikus kvantummechanika 54

Relativitáselmélet • Olyan mozgások leírása, ahol a sebesség összemérhető a fénysebességgel. • Az elektron sebessége is összemérhető a fénysebességgel. • Dirac-egyenlet: Schrödinger egyenlet módosítva a relativitáselmélettel. 55

A hidrogénatom Diracegyenletének megoldása Újabb kvantumszám: belső kvantumszám : az elektronpálya impulzusmomentumát jell. kvantumszám : a spin impulzusmomentumát jell. kvantumszám ha s pálya p pálya d pálya E függ n-től nagyon és j-től picit 56

Spin-pálya felhasadás p pálya d pálya Ha 0 -től eltér a mellék-kvantumszám, a belső kvantumszám szerint az energiaszintek kétfelé hasadnak. 57

A Dirac-egyenlet sajátfüggvényei „spin-koordináta” 58