21 st International AIDS Conference AIDS 2016 Durban

21 st International AIDS Conference (AIDS 2016) Durban, Sudáfrica 18 -22 de Julio 2016

Advertencia de ACC VIH sobre el uso de estas diapositivas • Estas diapositivas se han realizado, bajo la coordinación de un grupo de colaboradores independientes, que han revisado los estudios más relevantes presentados en el Congreso AIDS 2016, que ha tenido lugar del 18 al 22 de julio de 2016 en Durban (Sudáfrica). • • Expresamos nuestro agradecimiento a los autores de los trabajos presentados. • • El contenido de este material refleja el punto de vista de los autores y no el de ACC VIH. Estas diapositivas pueden ser utilizadas, con fines docentes y de formación, en sus presentaciones por aquellos médicos o investigadores que lo deseen. Sin embargo, se ruega no cambiar el contenido ni la atribución de las mismas. Esta actividad docente puede contener datos sobre fármacos o productos que no estén aprobados por la EMEA y las autoridades sanitarias españolas o de otros países. ACC VIH no recomienda utilizar ningún fármaco fuera de las recomendaciones realizadas por dichos organismos. Por ello, ACC VIH advierte a los lectores que deben consultar las recomendaciones y las informaciones que proporcionan las autoridades sanitarias, los comités de expertos y los fabricantes de los diferentes productos sobre la correcta utilización de los fármacos (indicaciones, dosificaciones, contraindicaciones, efectos adversos, interacciones, etc).

ÍNDICE • Pr. EP y TAR como prevención • Tratamiento antirretroviral • Comorbilidades-VHC AIDS 2016, Durban, 18 -22 Julio 2016.

AIDS 2016 Pr. EP y TAR como prevención
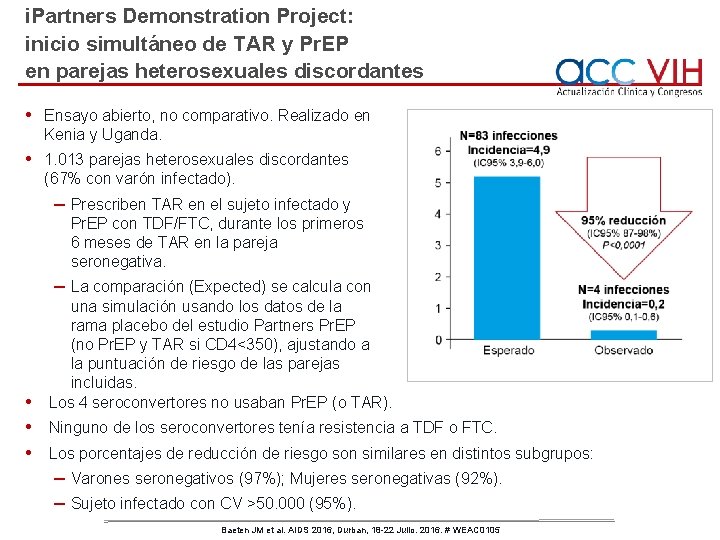
i. Partners Demonstration Project: inicio simultáneo de TAR y Pr. EP en parejas heterosexuales discordantes • Ensayo abierto, no comparativo. Realizado en Kenia y Uganda. • 1. 013 parejas heterosexuales discordantes (67% con varón infectado). – Prescriben TAR en el sujeto infectado y Pr. EP con TDF/FTC, durante los primeros 6 meses de TAR en la pareja seronegativa. – La comparación (Expected) se calcula con una simulación usando los datos de la rama placebo del estudio Partners Pr. EP (no Pr. EP y TAR si CD 4<350), ajustando a la puntuación de riesgo de las parejas incluidas. Los 4 seroconvertores no usaban Pr. EP (o TAR). • • Ninguno de los seroconvertores tenía resistencia a TDF o FTC. • Los porcentajes de reducción de riesgo son similares en distintos subgrupos: – Varones seronegativos (97%); Mujeres seronegativas (92%). – Sujeto infectado con CV >50. 000 (95%). Baeten JM et al. AIDS 2016, Durban, 18 -22 Julio. 2016. # WEAC 0105
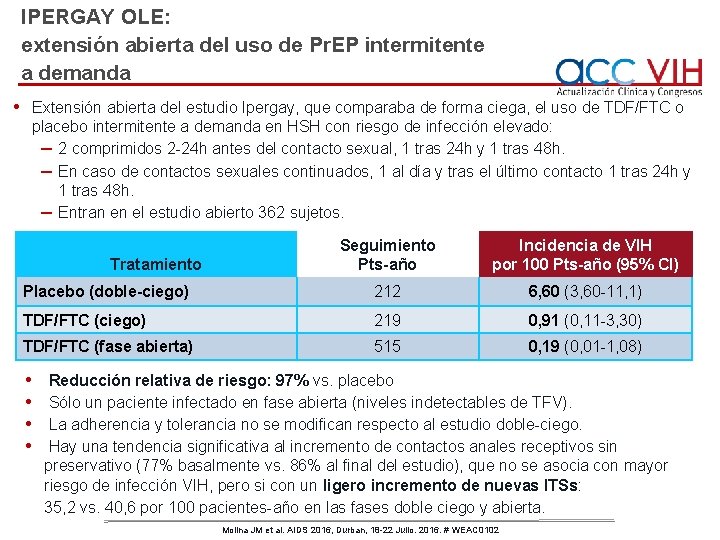
IPERGAY OLE: extensión abierta del uso de Pr. EP intermitente a demanda • Extensión abierta del estudio Ipergay, que comparaba de forma ciega, el uso de TDF/FTC o placebo intermitente a demanda en HSH con riesgo de infección elevado: – 2 comprimidos 2 -24 h antes del contacto sexual, 1 tras 24 h y 1 tras 48 h. – En caso de contactos sexuales continuados, 1 al día y tras el último contacto 1 tras 24 h y 1 tras 48 h. – Entran en el estudio abierto 362 sujetos. Seguimiento Pts-año Incidencia de VIH por 100 Pts-año (95% CI) Placebo (doble-ciego) 212 6, 60 (3, 60 -11, 1) TDF/FTC (ciego) 219 0, 91 (0, 11 -3, 30) TDF/FTC (fase abierta) 515 0, 19 (0, 01 -1, 08) Tratamiento • • Reducción relativa de riesgo: 97% vs. placebo Sólo un paciente infectado en fase abierta (niveles indetectables de TFV). La adherencia y tolerancia no se modifican respecto al estudio doble-ciego. Hay una tendencia significativa al incremento de contactos anales receptivos sin preservativo (77% basalmente vs. 86% al final del estudio), que no se asocia con mayor riesgo de infección VIH, pero si con un ligero incremento de nuevas ITSs: 35, 2 vs. 40, 6 por 100 pacientes-año en las fases doble ciego y abierta. Molina JM et al. AIDS 2016, Durban, 18 -22 Julio. 2016. # WEAC 0102
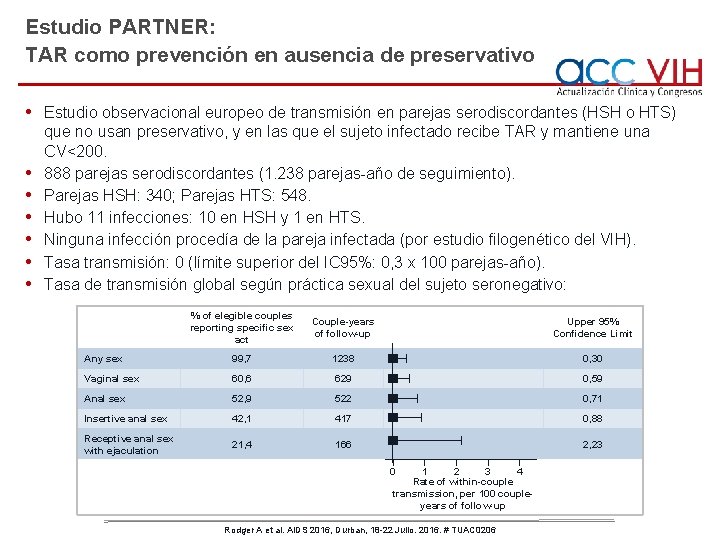
Estudio PARTNER: TAR como prevención en ausencia de preservativo • Estudio observacional europeo de transmisión en parejas serodiscordantes (HSH o HTS) • • • que no usan preservativo, y en las que el sujeto infectado recibe TAR y mantiene una CV<200. 888 parejas serodiscordantes (1. 238 parejas-año de seguimiento). Parejas HSH: 340; Parejas HTS: 548. Hubo 11 infecciones: 10 en HSH y 1 en HTS. Ninguna infección procedía de la pareja infectada (por estudio filogenético del VIH). Tasa transmisión: 0 (límite superior del IC 95%: 0, 3 x 100 parejas-año). Tasa de transmisión global según práctica sexual del sujeto seronegativo: % of elegible couples reporting specific sex act Couple-years of follow-up Upper 95% Confidence Limit Any sex 99, 7 1238 0, 30 Vaginal sex 60, 6 629 0, 59 Anal sex 52, 9 522 0, 71 Insertive anal sex 42, 1 417 0, 88 Receptive anal sex with ejaculation 21, 4 166 2, 23 0 1 2 3 4 Rate of within-couple transmission, per 100 coupleyears of follow-up Rodger A et al. AIDS 2016, Durban, 18 -22 Julio. 2016. # TUAC 0206

AIDS 2016 Tratamiento antirretroviral
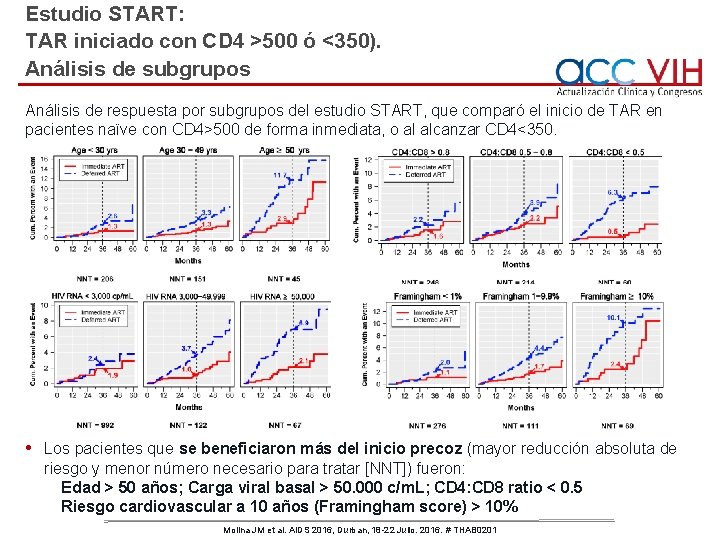
Estudio START: TAR iniciado con CD 4 >500 ó <350). Análisis de subgrupos Análisis de respuesta por subgrupos del estudio START, que comparó el inicio de TAR en pacientes naïve con CD 4>500 de forma inmediata, o al alcanzar CD 4<350. • Los pacientes que se beneficiaron más del inicio precoz (mayor reducción absoluta de riesgo y menor número necesario para tratar [NNT]) fueron: Edad > 50 años; Carga viral basal > 50. 000 c/m. L; CD 4: CD 8 ratio < 0. 5 Riesgo cardiovascular a 10 años (Framingham score) > 10% Molina JM et al. AIDS 2016, Durban, 18 -22 Julio. 2016. # THAB 0201
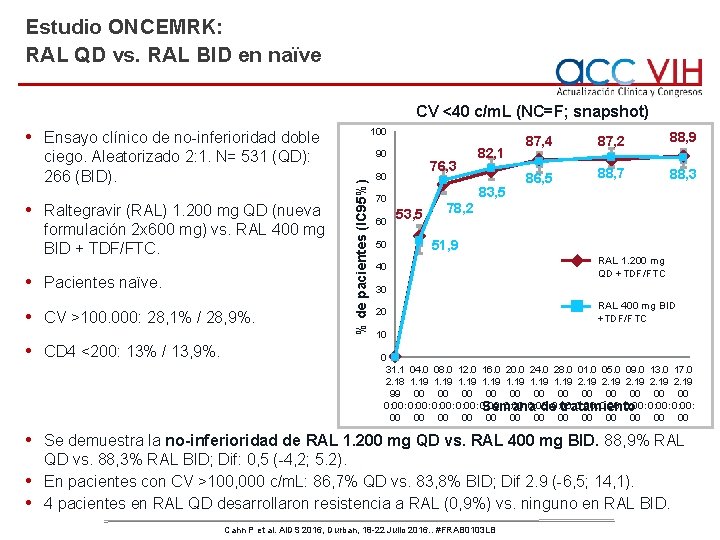
Estudio ONCEMRK: RAL QD vs. RAL BID en naïve CV <40 c/m. L (NC=F; snapshot) 100 • Ensayo clínico de no-inferioridad doble • Raltegravir (RAL) 1. 200 mg QD (nueva formulación 2 x 600 mg) vs. RAL 400 mg BID + TDF/FTC. • Pacientes naïve. • CV >100. 000: 28, 1% / 28, 9%. • CD 4 <200: 13% / 13, 9%. 90 % de pacientes (IC 95%) ciego. Aleatorizado 2: 1. N= 531 (QD): 266 (BID). 76, 3 80 83, 5 70 60 50 82, 1 53, 5 87, 4 87, 2 88, 9 86, 5 88, 7 88, 3 78, 2 51, 9 40 RAL 1. 200 mg QD +TDF/FTC 30 20 RAL 400 mg BID +TDF/FTC 10 0 31. 1 04. 0 08. 0 12. 0 16. 0 20. 0 24. 0 28. 0 01. 0 05. 0 09. 0 13. 0 17. 0 2. 18 1. 19 1. 19 2. 19 99 00 00 00 0: 00: 0: 00: 0: 00: Semana de 0: 00: tratamiento 00 00 00 00 • Se demuestra la no-inferioridad de RAL 1. 200 mg QD vs. RAL 400 mg BID. 88, 9% RAL QD vs. 88, 3% RAL BID; Dif: 0, 5 (-4, 2; 5. 2). • En pacientes con CV >100, 000 c/m. L: 86, 7% QD vs. 83, 8% BID; Dif 2. 9 (-6, 5; 14, 1). • 4 pacientes en RAL QD desarrollaron resistencia a RAL (0, 9%) vs. ninguno en RAL BID. Cahn P et al. AIDS 2016, Durban, 18 -22 Julio 2016. . #FRAB 0103 LB
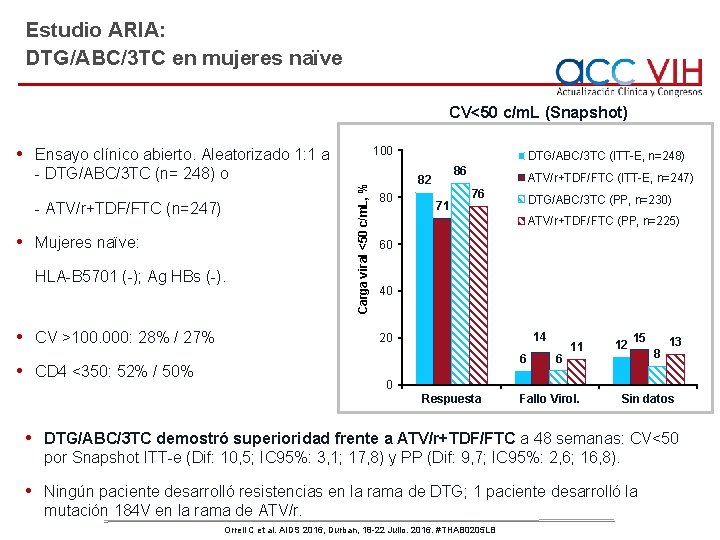
Estudio ARIA: DTG/ABC/3 TC en mujeres naïve CV<50 c/m. L (Snapshot) • Ensayo clínico abierto. Aleatorizado 1: 1 a - ATV/r+TDF/FTC (n=247) • Mujeres naïve: HLA-B 5701 (-); Ag HBs (-). • CV >100. 000: 28% / 27% Carga viral <50 c/m. L, % - DTG/ABC/3 TC (n= 248) o 100 DTG/ABC/3 TC (ITT-E, n=248) 86 82 80 71 ATV/r+TDF/FTC (ITT-E, n=247) 76 DTG/ABC/3 TC (PP, n=230) ATV/r+TDF/FTC (PP, n=225) 60 40 14 20 6 • CD 4 <350: 52% / 50% 6 11 12 15 8 13 0 Respuesta Fallo Virol. Sin datos • DTG/ABC/3 TC demostró superioridad frente a ATV/r+TDF/FTC a 48 semanas: CV<50 por Snapshot ITT-e (Dif: 10, 5; IC 95%: 3, 1; 17, 8) y PP (Dif: 9, 7; IC 95%: 2, 6; 16, 8). • Ningún paciente desarrolló resistencias en la rama de DTG; 1 paciente desarrolló la mutación 184 V en la rama de ATV/r. Orrell C et al. AIDS 2016, Durban, 18 -22 Julio. 2016. #THAB 0205 LB
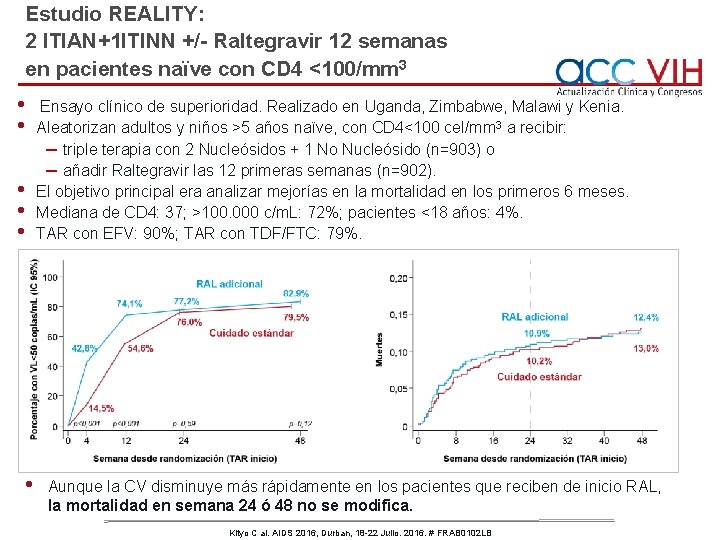
Estudio REALITY: 2 ITIAN+1 ITINN +/- Raltegravir 12 semanas en pacientes naïve con CD 4 <100/mm 3 • • • Ensayo clínico de superioridad. Realizado en Uganda, Zimbabwe, Malawi y Kenia. Aleatorizan adultos y niños >5 años naïve, con CD 4<100 cel/mm 3 a recibir: – triple terapia con 2 Nucleósidos + 1 No Nucleósido (n=903) o – añadir Raltegravir las 12 primeras semanas (n=902). El objetivo principal era analizar mejorías en la mortalidad en los primeros 6 meses. Mediana de CD 4: 37; >100. 000 c/m. L: 72%; pacientes <18 años: 4%. TAR con EFV: 90%; TAR con TDF/FTC: 79%. Aunque la CV disminuye más rápidamente en los pacientes que reciben de inicio RAL, la mortalidad en semana 24 ó 48 no se modifica. Kityo C al. AIDS 2016, Durban, 18 -22 Julio. 2016. # FRAB 0102 LB
![Estudio LATTE-2: Cabotegravir [CAB]+Rilpivirina [RPV] I. M. en pacientes naïve. 48 semanas • • Estudio LATTE-2: Cabotegravir [CAB]+Rilpivirina [RPV] I. M. en pacientes naïve. 48 semanas • •](http://slidetodoc.com/presentation_image_h2/d629f9bb7687623f479a3f10074a36f8/image-13.jpg)
Estudio LATTE-2: Cabotegravir [CAB]+Rilpivirina [RPV] I. M. en pacientes naïve. 48 semanas • • CV<50 c/m. L (Snapshot) Ensayo clínico abierto. Fase II. Pacientes naïve. Se tratan con CAB+ABC/3 TC oral 20 semanas, + RPV oral las últimas 4 semanas. Tras confirmar CV<50 c/m. L se aleatorizan 2: 2: 1 a: - Q 4 W: CAB+RPV IM/4 semanas (n= 115); - Q 8 W: CAB+RPV IM/8 semanas (n= 115); o - CAB+ABC/3 TC oral (n=56) CV >100. 000: 18%. Ambos regímenes IM demuestran no inferioridad respecto a la pauta oral: Q 4 W vs. oral: Dif: 2%; (IC 95%: -7, 6; 11, 6) y Q 8 W vs. oral: Dif: 2, 9%; (IC 95%: -6, 6; 12, 4). La rama Q 8 W presentó más fracasos virológicos y un paciente (en Q 8 W) desarrolló resistencia a CAB y RPV: NNRTI: K 103 N, E 138 G y K 238 T; INI: Q 148 R. 2 pacientes (<1%) discontinuaron por intolerancia a las inyecciones. La dosis IM seleccionada para continuar la fase III es cada 4 semanas. Margolis D et al. AIDS 2016, Durban, 18 -22 Julio. 2016. #THAB 0206 LB
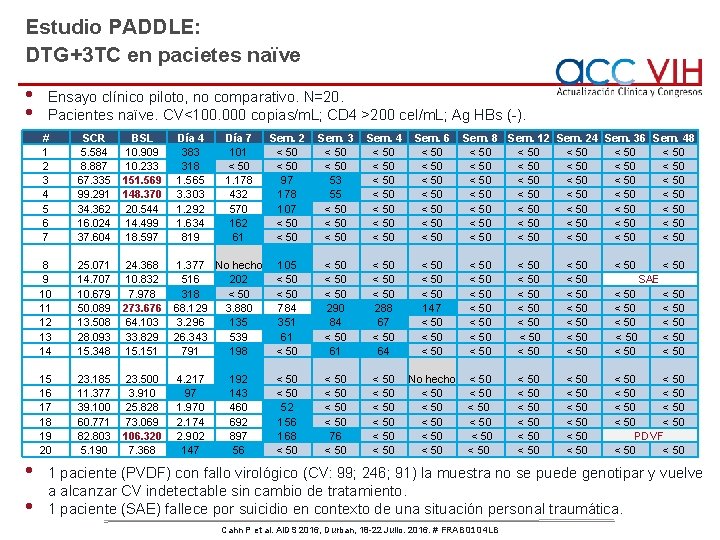
Estudio PADDLE: DTG+3 TC en pacietes naïve • • Ensayo clínico piloto, no comparativo. N=20. Pacientes naïve. CV<100. 000 copias/m. L; CD 4 >200 cel/m. L; Ag HBs (-). # 1 2 3 4 5 6 7 SCR 5. 584 8. 887 67. 335 99. 291 34. 362 16. 024 37. 604 BSL 10. 909 10. 233 151. 569 148. 370 20. 544 14. 499 18. 597 Día 4 383 318 1. 565 3. 303 1. 292 1. 634 819 8 9 10 11 12 13 14 25. 071 14. 707 10. 679 50. 089 13. 508 28. 093 15. 348 24. 368 10. 832 7. 978 273. 676 64. 103 33. 829 15. 151 15 16 17 18 19 20 23. 185 11. 377 39. 100 60. 771 82. 803 5. 190 23. 500 3. 910 25. 828 73. 069 106. 320 7. 368 Día 7 101 < 50 1. 178 432 570 162 61 Sem. 2 < 50 97 178 107 < 50 Sem. 3 < 50 53 55 < 50 Sem. 4 < 50 < 50 Sem. 6 < 50 < 50 1. 377 No hecho 516 202 318 < 50 68. 129 3. 880 3. 296 135 26. 343 539 791 198 105 < 50 784 351 61 < 50 290 84 < 50 61 < 50 288 67 < 50 64 < 50 147 < 50 < 50 < 50 < 50 < 50 < 50 < 50 4. 217 97 1. 970 2. 174 2. 902 147 < 50 52 156 168 < 50 < 50 76 < 50 < 50 No hecho < 50 < 50 < 50 < 50 < 50 < 50 < 50 < 50 PDVF < 50 192 143 460 692 897 56 Sem. 8 Sem. 12 Sem. 24 Sem. 36 Sem. 48 < 50 < 50 < 50 < 50 < 50 < 50 < 50 < 50 < 50 SAE < 50 < 50 < 50 1 paciente (PVDF) con fallo virológico (CV: 99; 246; 91) la muestra no se puede genotipar y vuelve a alcanzar CV indetectable sin cambio de tratamiento. 1 paciente (SAE) fallece por suicidio en contexto de una situación personal traumática. Cahn P et al. AIDS 2016, Durban, 18 -22 Julio. 2016. # FRAB 0104 LB
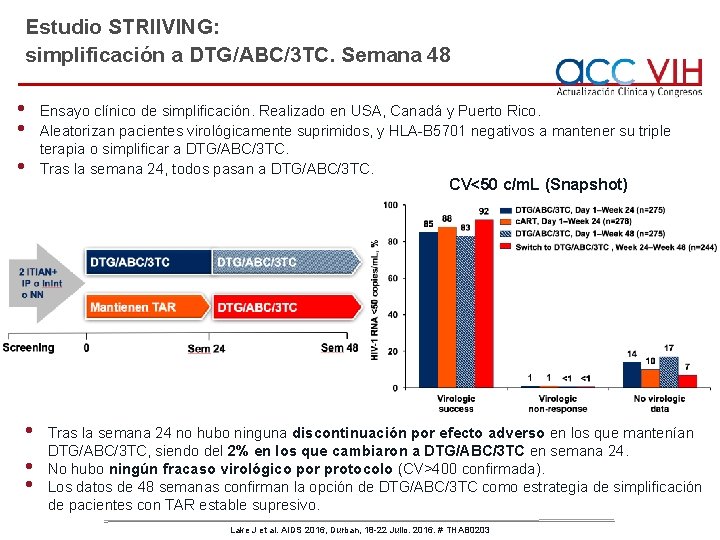
Estudio STRIIVING: simplificación a DTG/ABC/3 TC. Semana 48 • • • Ensayo clínico de simplificación. Realizado en USA, Canadá y Puerto Rico. Aleatorizan pacientes virológicamente suprimidos, y HLA-B 5701 negativos a mantener su triple terapia o simplificar a DTG/ABC/3 TC. Tras la semana 24, todos pasan a DTG/ABC/3 TC. CV<50 c/m. L (Snapshot) Tras la semana 24 no hubo ninguna discontinuación por efecto adverso en los que mantenían DTG/ABC/3 TC, siendo del 2% en los que cambiaron a DTG/ABC/3 TC en semana 24. No hubo ningún fracaso virológico por protocolo (CV>400 confirmada). Los datos de 48 semanas confirman la opción de DTG/ABC/3 TC como estrategia de simplificación de pacientes con TAR estable supresivo. Lake J et al. AIDS 2016, Durban, 18 -22 Julio. 2016. # THAB 0203

DTG+RPV como simplificación de pacientes muy pretratados con viremia suprimida • • Estudio de cohorte en práctica clínica habitual. Analizan 38 pacientes con CV suprimida e historia de múltiples tratamientos previos que se simplifican a Dolutegravir (DTG)+Rilpivirina (RPV), ambos administrados una vez al día. Excluyen pacientes con historia de resistencia a DTG o RPV. • Características de los pacientes (n=38): - CD 4 basales: 592 cel/mm 3 Tiempo con CV <50: 6, 7 años Número de pastillas en el tratamiento previo: 4, 3 Tomando ITIAN+ITINN+IP: 85%; ITIAN+ITINN+IP+INI: 53% Historia de fracaso con 3 o más familias de antirretrovirales: 55% Historia de resistencia a ITIAN: 65%; a ITINN 37%; a IP: 32%. Motivos de cambio: - Interacciones: 38% Toxicidad: 33% Simplificación: 25% • 3 pacientes discontiuaron el nuevo régimen: - 1 por toxicidad gastrointestinal - 1 por interacción con omeprazol - 1 por decisión del médico • Ningún fracaso virológico: - CV <35 c/m. L en 100% (38/38) en semana 4, y en 100% (35/35) en semana 48. Con respecto al basal, se apreció un descenso significativo de triglicéridos (173 a 133 mg/d. L); de colesterol (de 202 a 188 mg/d. L); y del filtrado glomerular estimado (CKD-EPI; de 85 a 76 m. L/min). • Diaz A et al. AIDS 2016, Durban, 18 -22 Julio. 2016. # TUPEDB 0106

AIDS 2016 Comorbilidades
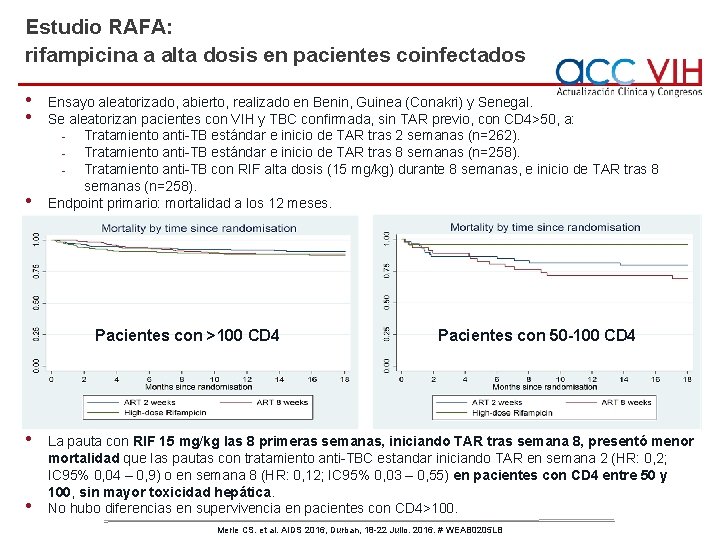
Estudio RAFA: rifampicina a alta dosis en pacientes coinfectados • • • Ensayo aleatorizado, abierto, realizado en Benin, Guinea (Conakri) y Senegal. Se aleatorizan pacientes con VIH y TBC confirmada, sin TAR previo, con CD 4>50, a: - Tratamiento anti-TB estándar e inicio de TAR tras 2 semanas (n=262). - Tratamiento anti-TB estándar e inicio de TAR tras 8 semanas (n=258). - Tratamiento anti-TB con RIF alta dosis (15 mg/kg) durante 8 semanas, e inicio de TAR tras 8 semanas (n=258). Endpoint primario: mortalidad a los 12 meses. Pacientes con >100 CD 4 • • Pacientes con 50 -100 CD 4 La pauta con RIF 15 mg/kg las 8 primeras semanas, iniciando TAR tras semana 8, presentó menor mortalidad que las pautas con tratamiento anti-TBC estandar iniciando TAR en semana 2 (HR: 0, 2; IC 95% 0, 04 – 0, 9) o en semana 8 (HR: 0, 12; IC 95% 0, 03 – 0, 55) en pacientes con CD 4 entre 50 y 100, sin mayor toxicidad hepática. No hubo diferencias en supervivencia en pacientes con CD 4>100. Merle CS. et al. AIDS 2016, Durban, 18 -22 Julio. 2016. # WEAB 0205 LB
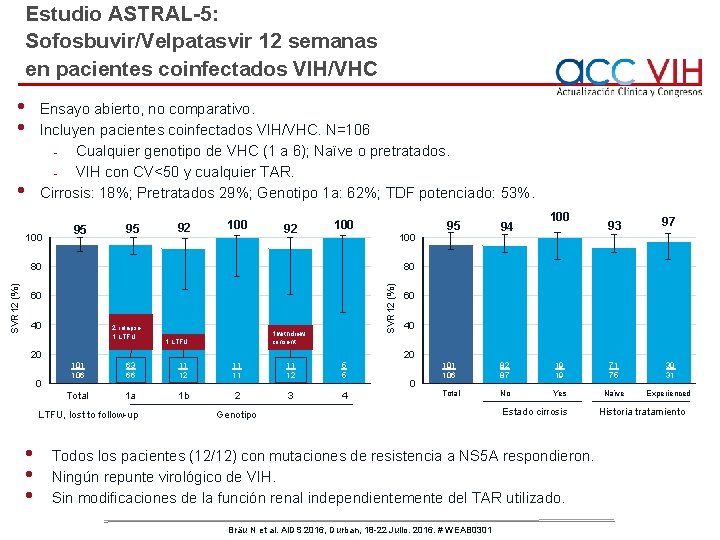
Estudio ASTRAL-5: Sofosbuvir/Velpatasvir 12 semanas en pacientes coinfectados VIH/VHC • • Ensayo abierto, no comparativo. Incluyen pacientes coinfectados VIH/VHC. N=106 - Cualquier genotipo de VHC (1 a 6); Naïve o pretratados. - VIH con CV<50 y cualquier TAR. Cirrosis: 18%; Pretratados 29%; Genotipo 1 a: 62%; TDF potenciado: 53%. • 100 95 95 92 100 100 60 40 2 relapse 1 LTFU 1 withdrew consent 1 LTFU 20 0 100 93 97 60 40 20 101 106 63 66 11 12 11 11 11 12 5 5 Total 1 a 1 b 2 3 4 LTFU, lost to follow-up • • • 94 80 SVR 12 (%) 80 95 0 101 106 82 87 19 19 71 75 30 31 Total No Yes Naïve Experienced Genotipo Estado cirrosis Todos los pacientes (12/12) con mutaciones de resistencia a NS 5 A respondieron. Ningún repunte virológico de VIH. Sin modificaciones de la función renal independientemente del TAR utilizado. Bräu N et al. AIDS 2016, Durban, 18 -22 Julio. 2016. # WEAB 0301 Historia tratamiento
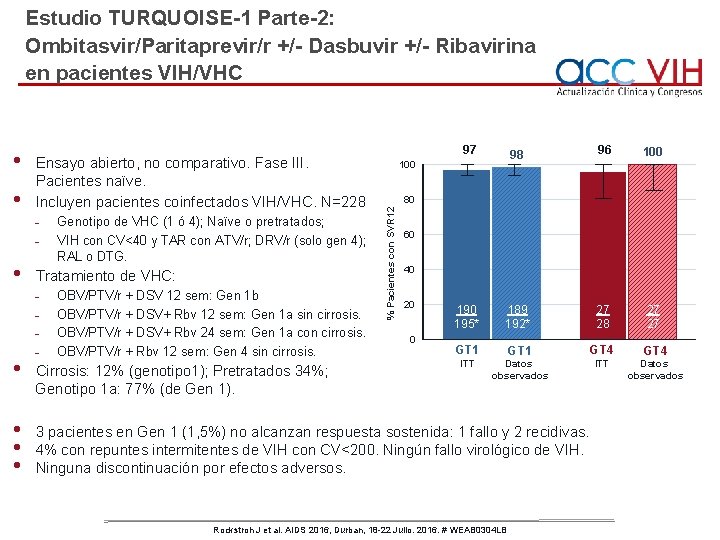
Estudio TURQUOISE-1 Parte-2: Ombitasvir/Paritaprevir/r +/- Dasbuvir +/- Ribavirina en pacientes VIH/VHC • Ensayo abierto, no comparativo. Fase III. Pacientes naïve. Incluyen pacientes coinfectados VIH/VHC. N=228 - • • • Genotipo de VHC (1 ó 4); Naïve o pretratados; VIH con CV<40 y TAR con ATV/r; DRV/r (solo gen 4); RAL o DTG. Tratamiento de VHC: - OBV/PTV/r + DSV 12 sem: Gen 1 b OBV/PTV/r + DSV+ Rbv 12 sem: Gen 1 a sin cirrosis. OBV/PTV/r + DSV+ Rbv 24 sem: Gen 1 a con cirrosis. OBV/PTV/r + Rbv 12 sem: Gen 4 sin cirrosis. Cirrosis: 12% (genotipo 1); Pretratados 34%; Genotipo 1 a: 77% (de Gen 1). 98 96 100 195* 189 192* 27 28 27 27 GT 1 GT 4 ITT Datos observados 80 % Pacientes con SVR 12 • 97 100 60 40 20 0 3 pacientes en Gen 1 (1, 5%) no alcanzan respuesta sostenida: 1 fallo y 2 recidivas. 4% con repuntes intermitentes de VIH con CV<200. Ningún fallo virológico de VIH. Ninguna discontinuación por efectos adversos. Rockstroh J et al. AIDS 2016, Durban, 18 -22 Julio. 2016. # WEAB 0304 LB

21 st International AIDS Conference (AIDS 2016) Durban, Sudáfrica 18 -22 de Julio 2016
- Slides: 21