2018 Lezione 2 Atomi Molecole e Ioni Teoria

















- Slides: 37

2018 Lezione 2. Atomi, Molecole e Ioni

Teoria Atomica di Dalton (1808) 1. Gli elementi sono composti da particelle estremamente piccole, gli atomi. 2. Tutti gli atomi di un certo elemento sono identici. Hanno la stessa dimensione, massa e proprietà chimiche. Gli atomi di un elemento differiscono da quelli degli altri elementi. 3. I composti sono costituiti da atomi di differenti elementi. Gli atomi che li costituiscono sempre presenti in un rapporto numerico definito. 4. Una reazione chimica comporta una differente associazione/combinazione di atomi, non la loro creazione o distruzione. 2

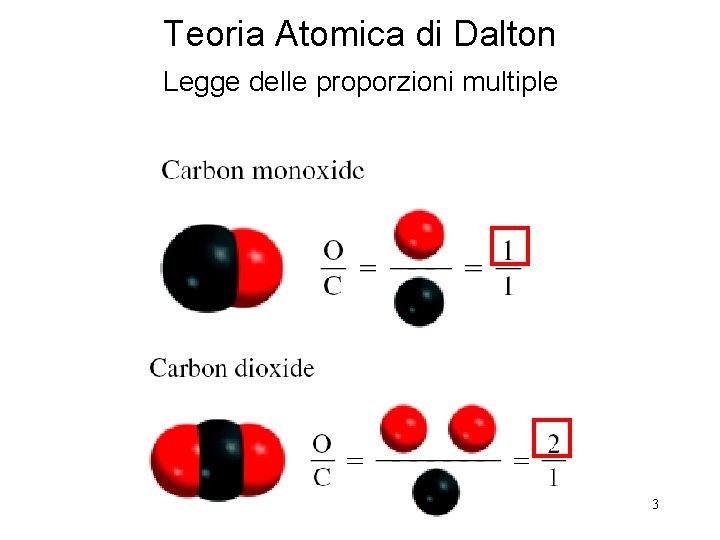
Teoria Atomica di Dalton Legge delle proporzioni multiple 3

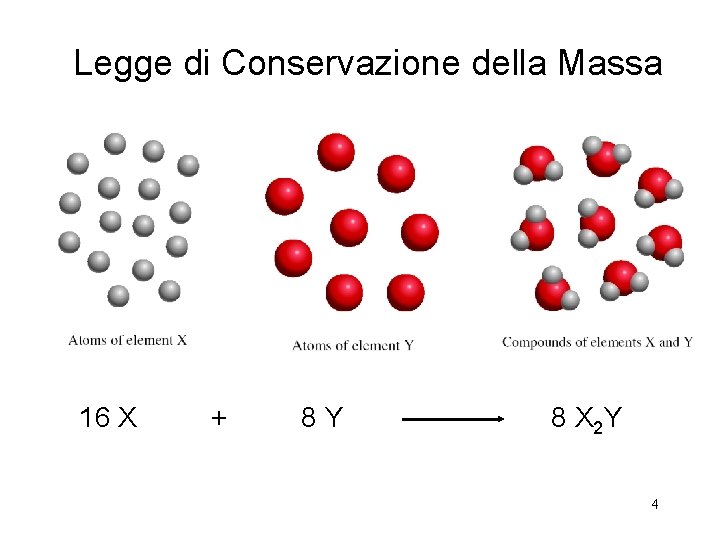
Legge di Conservazione della Massa 16 X + 8 Y 8 X 2 Y 4

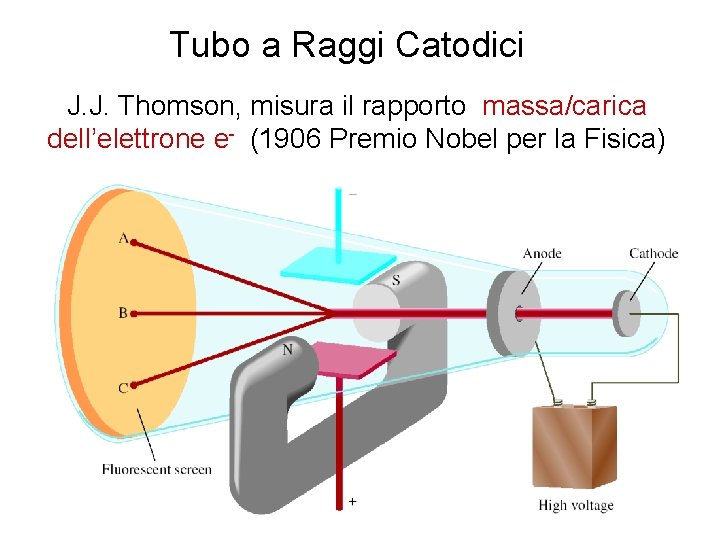
Tubo a Raggi Catodici J. J. Thomson, misura il rapporto massa/carica dell’elettrone e- (1906 Premio Nobel per la Fisica) 5

Tubo a Raggi Catodici 6

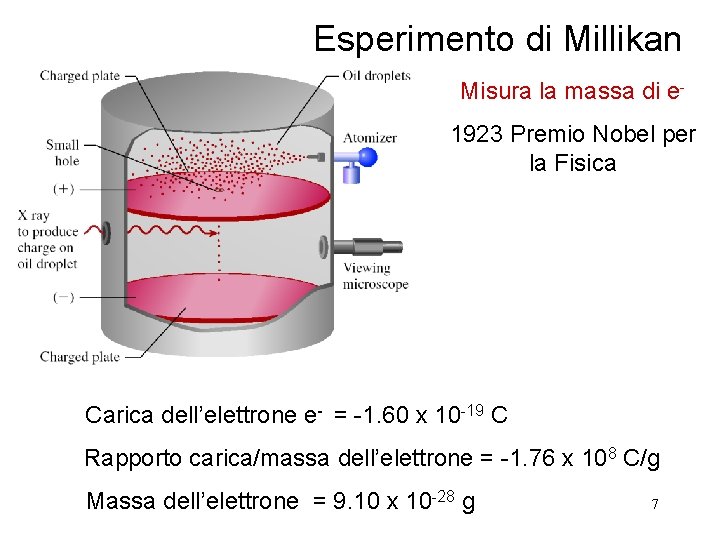
Esperimento di Millikan Misura la massa di e 1923 Premio Nobel per la Fisica Carica dell’elettrone e- = -1. 60 x 10 -19 C Rapporto carica/massa dell’elettrone = -1. 76 x 108 C/g Massa dell’elettrone = 9. 10 x 10 -28 g 7

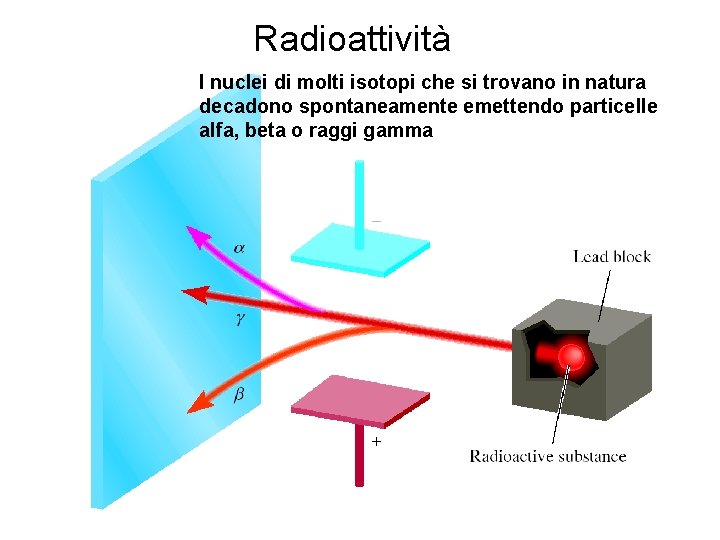
Radioattività I nuclei di molti isotopi che si trovano in natura decadono spontaneamente emettendo particelle alfa, beta o raggi gamma 8

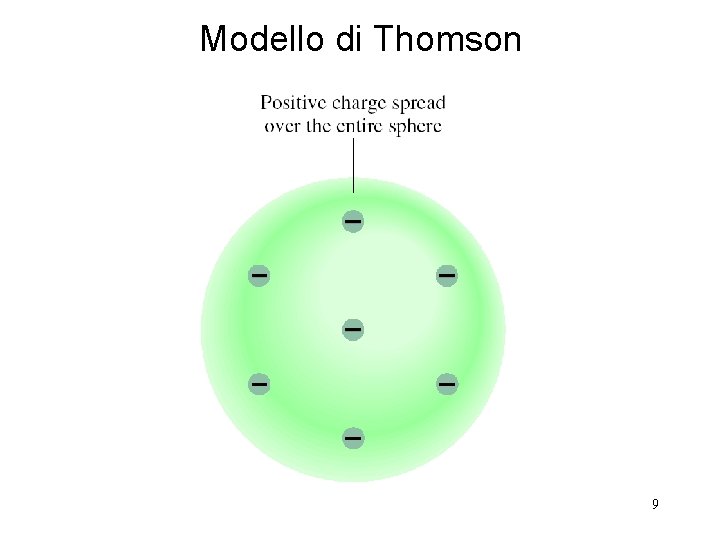
Modello di Thomson 9

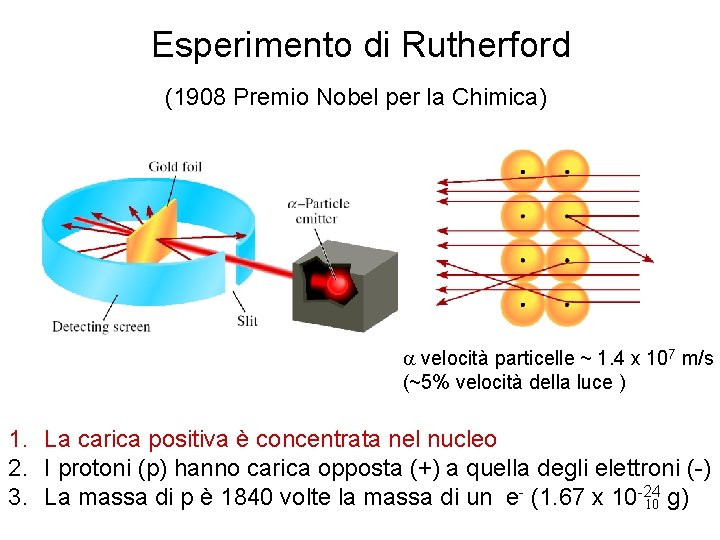
Esperimento di Rutherford (1908 Premio Nobel per la Chimica) a velocità particelle ~ 1. 4 x 107 m/s (~5% velocità della luce ) 1. La carica positiva è concentrata nel nucleo 2. I protoni (p) hanno carica opposta (+) a quella degli elettroni (-) 3. La massa di p è 1840 volte la massa di un e- (1. 67 x 10 -24 10 g)

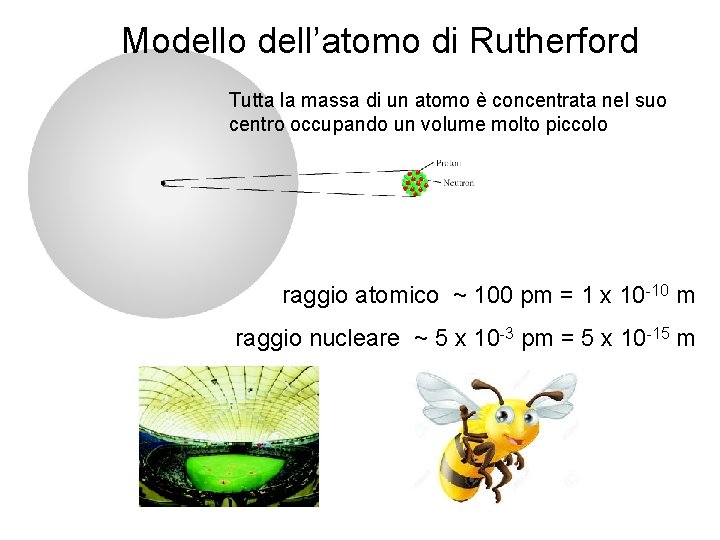
Modello dell’atomo di Rutherford Tutta la massa di un atomo è concentrata nel suo centro occupando un volume molto piccolo raggio atomico ~ 100 pm = 1 x 10 -10 m raggio nucleare ~ 5 x 10 -3 pm = 5 x 10 -15 m

Chadwick’s Experiment (1932) (1935 Noble Prize in Physics) H atoms - 1 p; He atoms - 2 p mass He/mass H should = 2 measured mass NO He/mass H = 4 a + 9 Be 1 n + 12 C + energy neutron (n) is neutral (charge = 0) n mass ~ p mass = 1. 67 x 10 -24 g 12

Proprietà delle particelle subatomiche massa p ≈ massa n ≈ 1840 x massa e 13

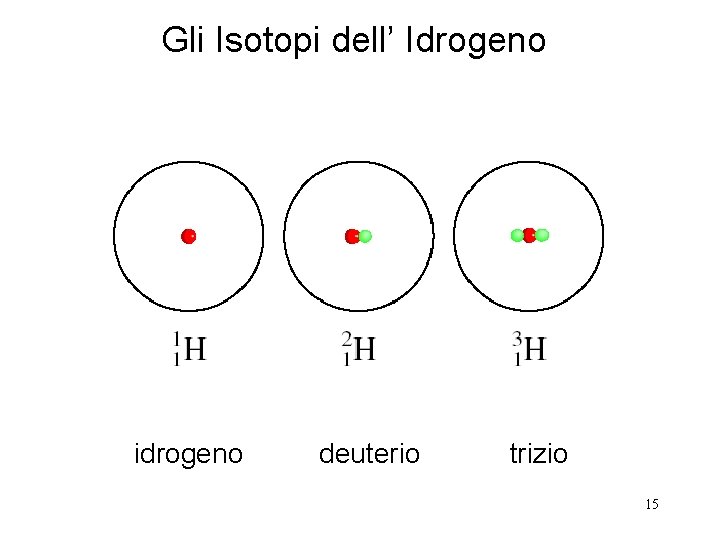
Numero Atomico, Numero di Massa e Isotopi Numero Atomico (Z) = numero di protoni nel nucleo Numero di Massa (A) = numero di protoni + numero di neutroni = numero atomico (Z) + numero di neutroni Isotopi sono atomi di uno stesso elemento (X) aventi un differente numero di neutroni nei loro nuclei Numero di Massa A ZX Numero Atomico 1 1 H 235 92 2 1 H U Simbolo dell’elemento (D) 238 92 3 1 H U (T) 14

Gli Isotopi dell’ Idrogeno idrogeno deuterio trizio 15

esempi Quanti protoni, neutroni, ed elettroni ci sono nel 14 6 C ? 6 protoni, 8 (14 - 6) neutroni, 6 elettroni Quanti protoni, neutroni, ed elettroni ci sono nel 11 6 C ? 6 protoni, 5 (11 - 6) neutroni, 6 elettroni 16

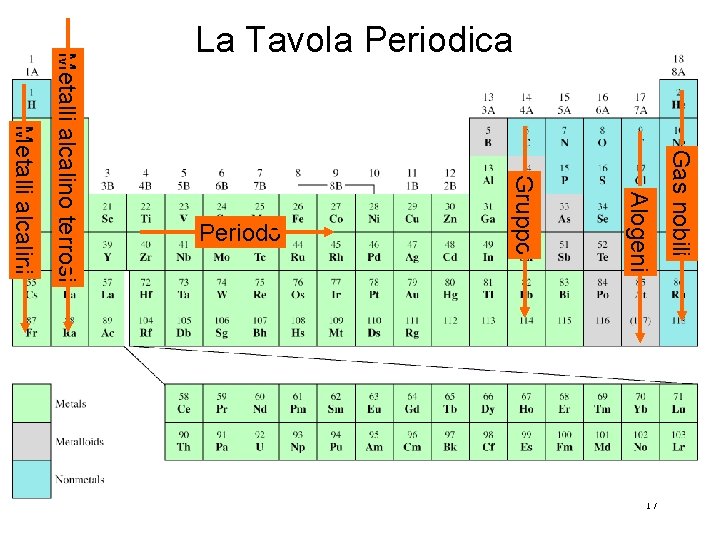
Metalli alcalini 17 Gas nobili Alogeni Gruppo Periodo Metalli alcalino terrosi La Tavola Periodica

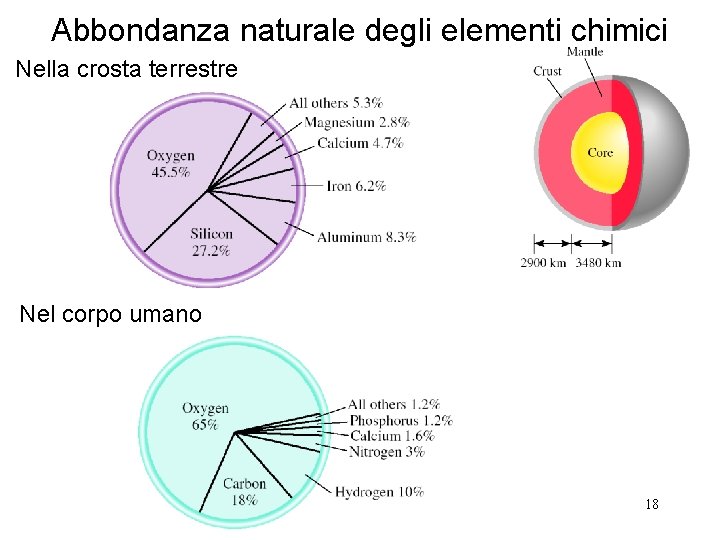
Abbondanza naturale degli elementi chimici Nella crosta terrestre Nel corpo umano 18

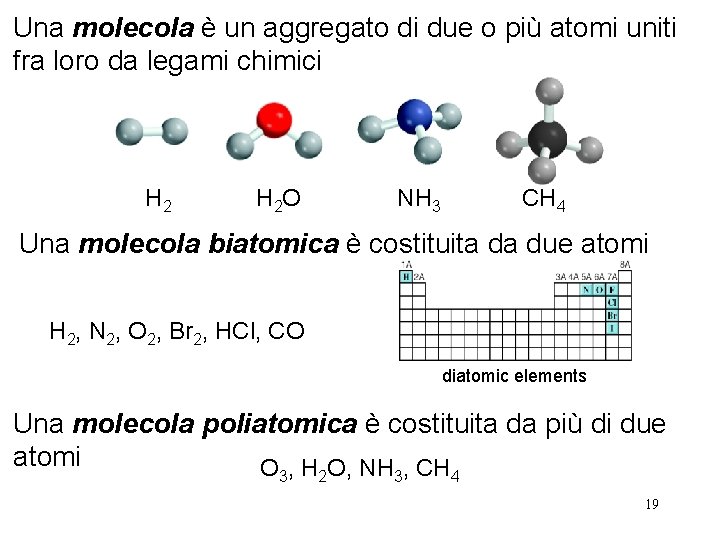
Una molecola è un aggregato di due o più atomi uniti fra loro da legami chimici H 2 O NH 3 CH 4 Una molecola biatomica è costituita da due atomi H 2, N 2, O 2, Br 2, HCl, CO diatomic elements Una molecola poliatomica è costituita da più di due atomi O , H O, NH , CH 3 2 3 4 19

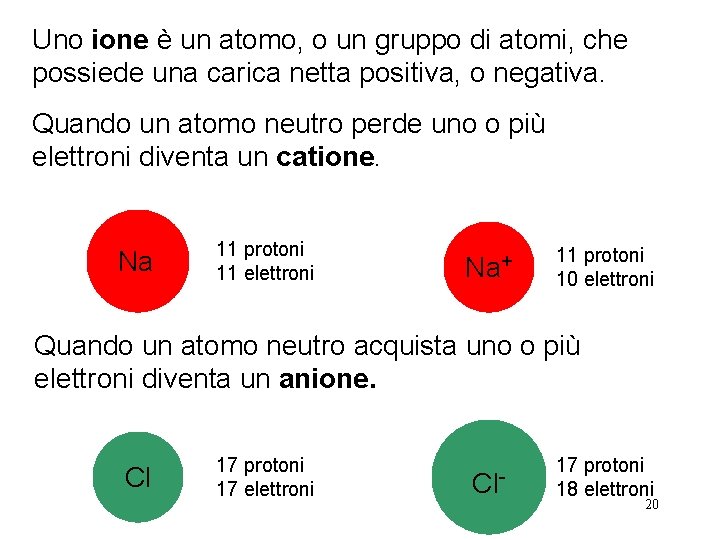
Uno ione è un atomo, o un gruppo di atomi, che possiede una carica netta positiva, o negativa. Quando un atomo neutro perde uno o più elettroni diventa un catione. Na 11 protoni 11 elettroni Na+ 11 protoni 10 elettroni Quando un atomo neutro acquista uno o più elettroni diventa un anione. Cl 17 protoni 17 elettroni Cl- 17 protoni 18 elettroni 20

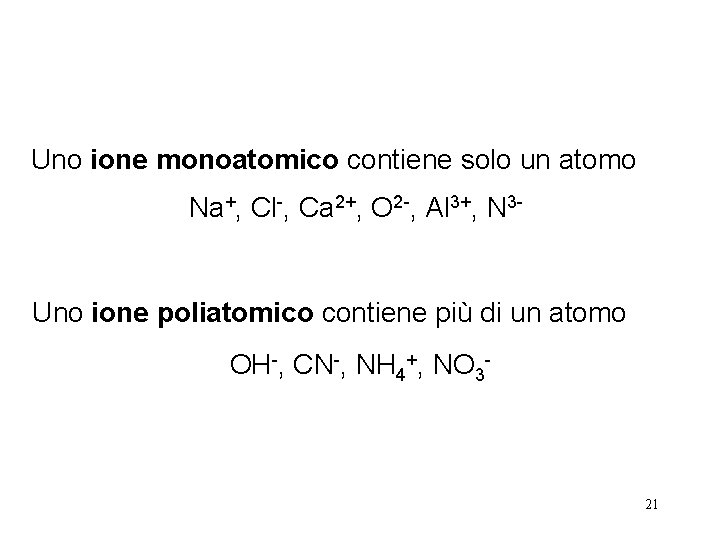
Uno ione monoatomico contiene solo un atomo Na+, Cl-, Ca 2+, O 2 -, Al 3+, N 3 - Uno ione poliatomico contiene più di un atomo OH-, CN-, NH 4+, NO 3 - 21

Gli Ioni più comuni e loro posizione nella Tavola Periodica 22

esempi Quanti protoni ed elettroni sono presenti 27 3+ 13 Al 13 protoni, 10 elettroni (13 – 3) Quanti protoni ed elettroni sono presenti 78 2 Se 34 34 protoni, 36 (34 + 2) elettroni 23

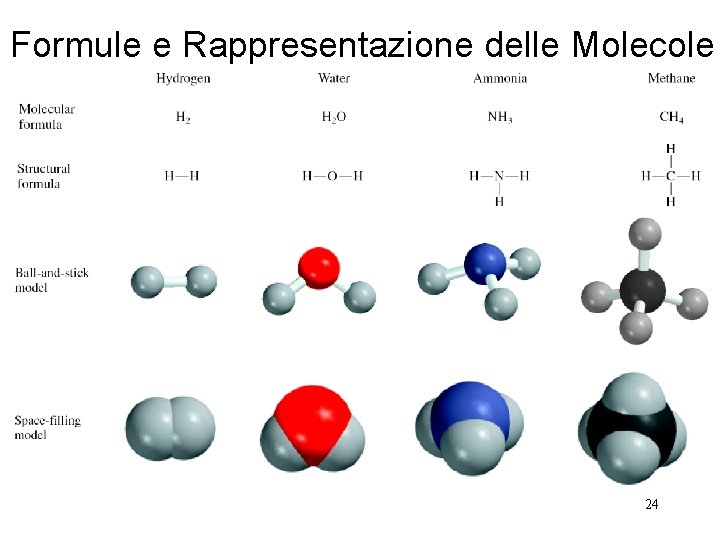
Formule e Rappresentazione delle Molecole 24

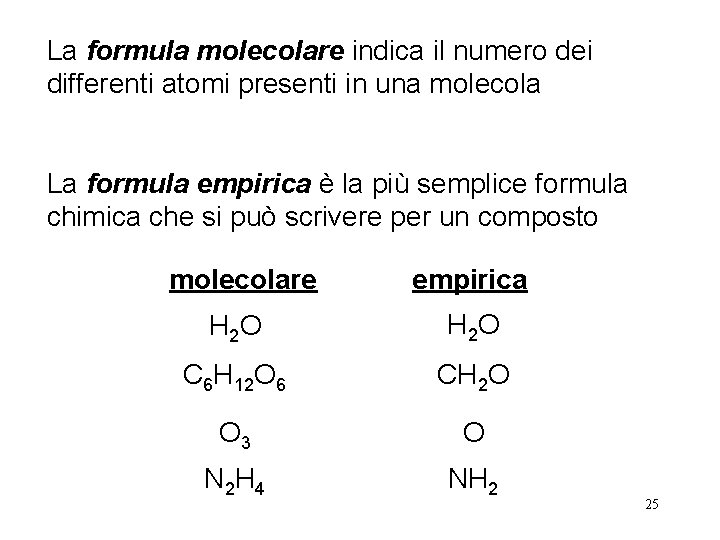
La formula molecolare indica il numero dei differenti atomi presenti in una molecola La formula empirica è la più semplice formula chimica che si può scrivere per un composto molecolare empirica H 2 O C 6 H 12 O 6 CH 2 O O 3 O N 2 H 4 NH 2 25

I composti ionici sono formati da cationi ed anioni • La formula è la medesima della formula empirica • La somma delle cariche dovute ai cationi è pari a quella dovuta agli anioni Il composto ionico Na. Cl 26

NO The most reactive metals (green) and the most reactive nonmetals (blue) combine to form ionic compounds. 27

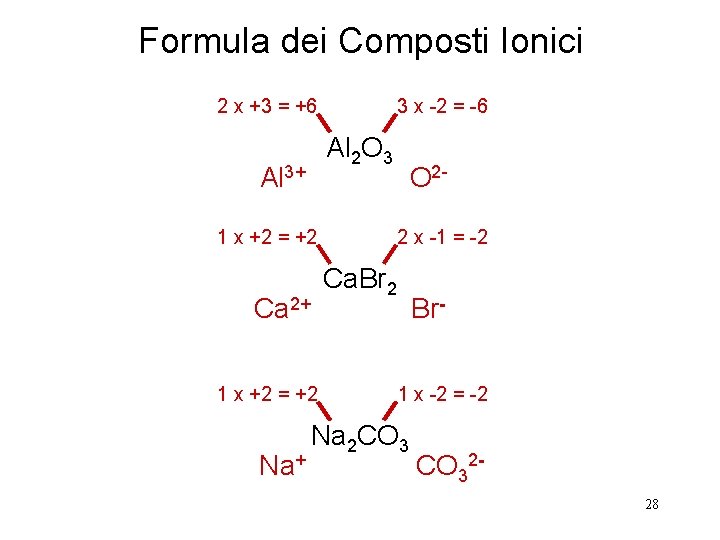
Formula dei Composti Ionici 2 x +3 = +6 3 x -2 = -6 Al 2 O 3 Al 3+ 1 x +2 = +2 Ca 2+ 1 x +2 = +2 Na+ O 22 x -1 = -2 Ca. Br 2 Br 1 x -2 = -2 Na 2 CO 3228

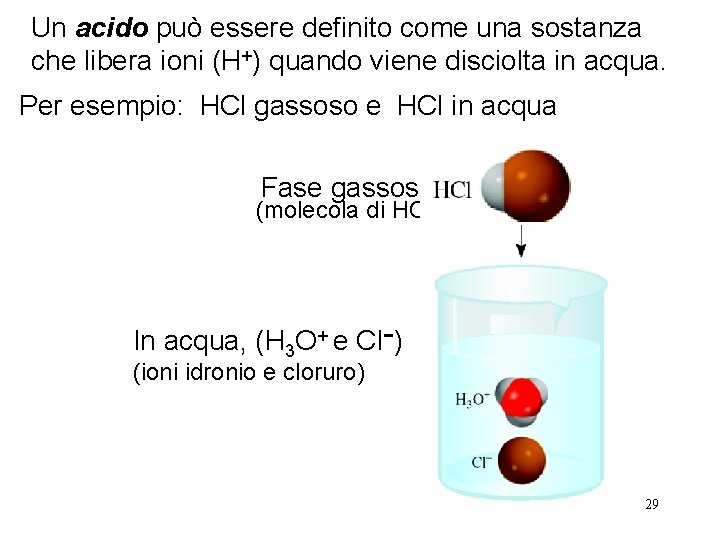
Un acido può essere definito come una sostanza che libera ioni (H+) quando viene disciolta in acqua. Per esempio: HCl gassoso e HCl in acqua Fase gassosa (molecola di HCl) In acqua, (H 3 O+ e Cl−) (ioni idronio e cloruro) 29

Idracidi 30

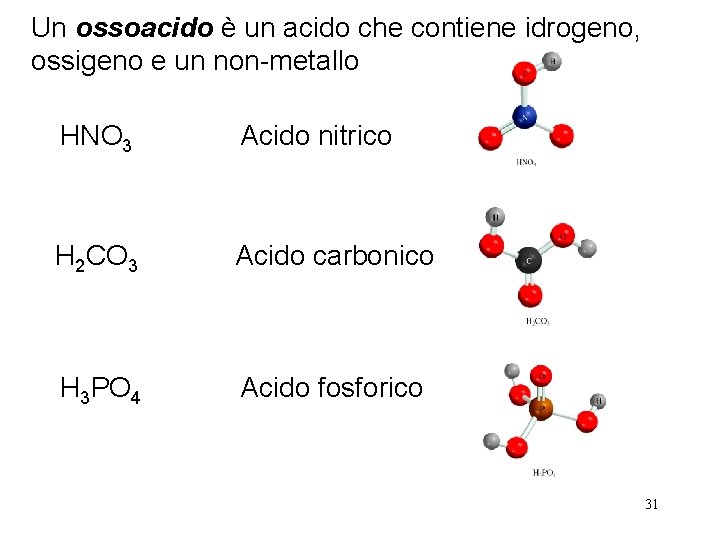
Un ossoacido è un acido che contiene idrogeno, ossigeno e un non-metallo HNO 3 Acido nitrico H 2 CO 3 Acido carbonico H 3 PO 4 Acido fosforico 31

Ossiacidi e relativi anioni che contengono atomi di cloro Acido Anione HCl. O 4 (acido perclorico) Cl. O 4– (perclorato) HCl. O 3 (acido clorico) Cl. O 3– (clorato) HCl. O 2 (acido cloroso) Cl. O 2– (clorito) HCl. O (acido ipocloroso) Cl. O– (ipoclorito) 32

Una base è una sostanza che disciolta in acqua libera ioni idrossido (OH-). Na. OH Idrossido di sodio KOH Idrossido di potassio Ba(OH)2 Idrossido di bario 33

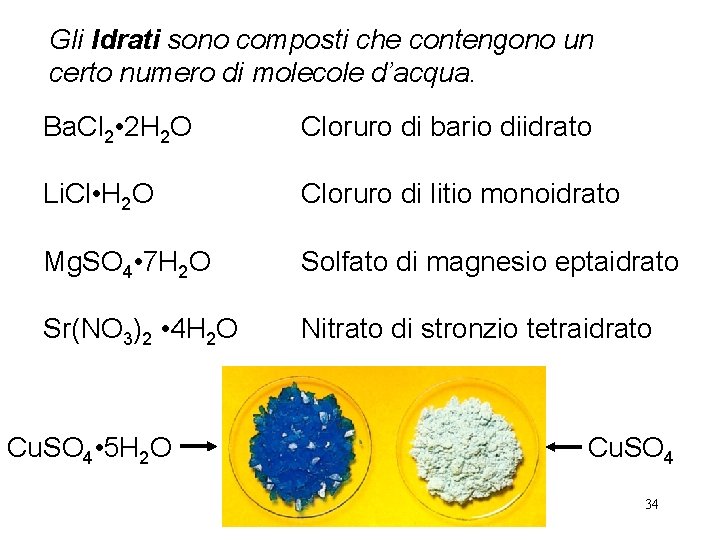
Gli Idrati sono composti che contengono un certo numero di molecole d’acqua. Ba. Cl 2 • 2 H 2 O Cloruro di bario diidrato Li. Cl • H 2 O Cloruro di litio monoidrato Mg. SO 4 • 7 H 2 O Solfato di magnesio eptaidrato Sr(NO 3)2 • 4 H 2 O Nitrato di stronzio tetraidrato Cu. SO 4 • 5 H 2 O Cu. SO 4 34

Nomenclatura composti inorganici Sono due i principali sistemi di nomenclatura: - IUPAC (International Union of Pure and Applied Chemistry), più razionale mette in evidenza i vari atomi di ciascun composto -TRADIZIONALE che mette in evidenza la distinzione tra metalli e non metalli

esempi
