2018 FARMACOLOGIA FARMACOCINETICA 1 Dra Mnica L Freile
















































- Slides: 69

2018 FARMACOLOGIA FARMACOCINETICA 1 Dra Mónica L. Freile

2 FARMACOCINÉTICA Es la rama de la Farmacología que estudia el paso de los fármacos a través del organismo en función del tiempo y de la dosis. Comprende los procesos de Liberación, Absorción, Distribución, Metabolismo y Excreción de fármacos. 2018

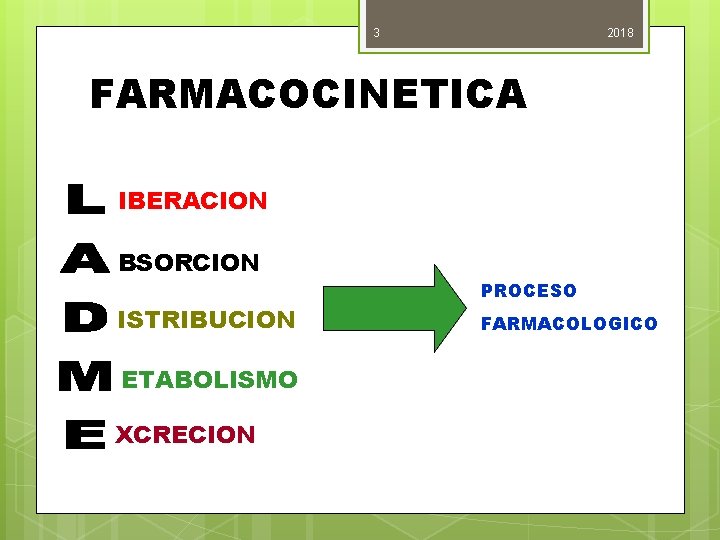
3 2018 FARMACOCINETICA IBERACION BSORCION ISTRIBUCION ETABOLISMO XCRECION PROCESO FARMACOLOGICO

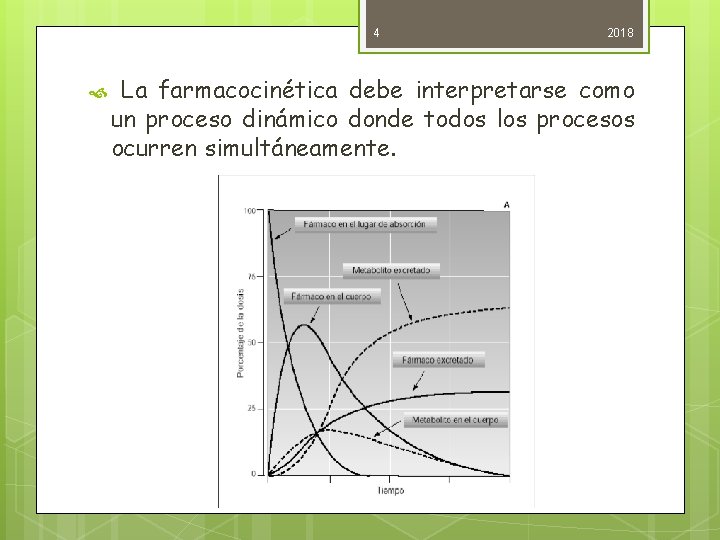
4 2018 La farmacocinética debe interpretarse como un proceso dinámico donde todos los procesos ocurren simultáneamente.

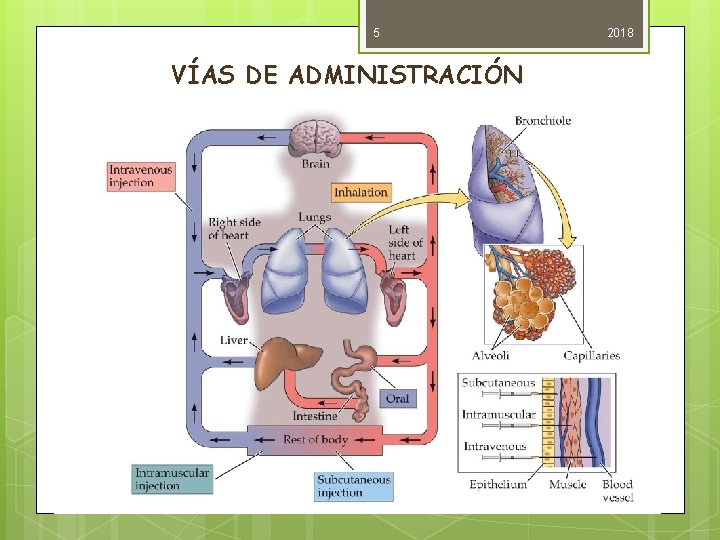
5 VÍAS DE ADMINISTRACIÓN 2018

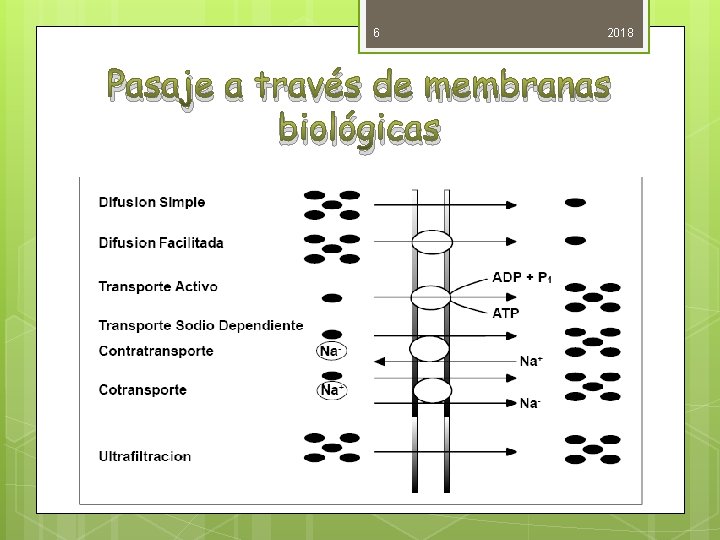
6 2018 Pasaje a través de membranas biológicas

7 2018 Movilización de las moléculas de una droga desde el sitio de mayor al de menor cc, a través de los lípidos de la membrana, sin consumo de ATP ni utilización de mecanismos de transporte. La velocidad de pasaje en la difusión simple depende de: la Liposolubilidad, el Tamaño y la Ionización Molecular.

8 2018 Liposolubilidad: > liposolubilidad, > v. de difusión y viceversa Para medirla se utiliza el coeficiente de partición lípido/H 20 Tamaño molecular Ionización Molecular: Las membranas biológicas son 108 veces más permeables a las moléculas no ionizadas. A = liposolubilidad, la FNI es el principal determinante de la velocidad de difusión. La FNI depende de: Si el fármaco es un ácido o una base El p. Ka del fármaco El p. H del medio orgánico

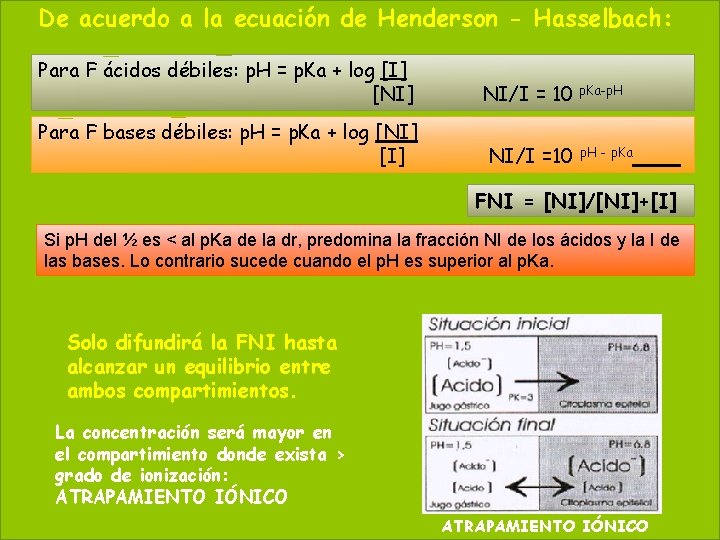
De acuerdo a la ecuación de 9 Henderson - Hasselbach: 2018 Para F ácidos débiles: p. H = p. Ka + log [I] [NI] NI/I = 10 Para F bases débiles: p. H = p. Ka + log [NI] [I] NI/I =10 p. Ka-p. H - p. Ka FNI = [NI]/[NI]+[I] Si p. H del ½ es < al p. Ka de la dr, predomina la fracción NI de los ácidos y la I de las bases. Lo contrario sucede cuando el p. H es superior al p. Ka. Solo difundirá la FNI hasta alcanzar un equilibrio entre ambos compartimientos. La concentración será mayor en el compartimiento donde exista > grado de ionización: ATRAPAMIENTO IÓNICO

10 2018 Permite la difusión de sustancias prácticamente insolubles en lípidos (glucosa) mediante el empleo de transportadores o carriers específicos en la membrana. Difunde a favor de un gradiente de cc, sin incorporación o utilización de energía. • Saturabilidad • Selectividad • Competición • Reversibilidad • Bidireccionalidad

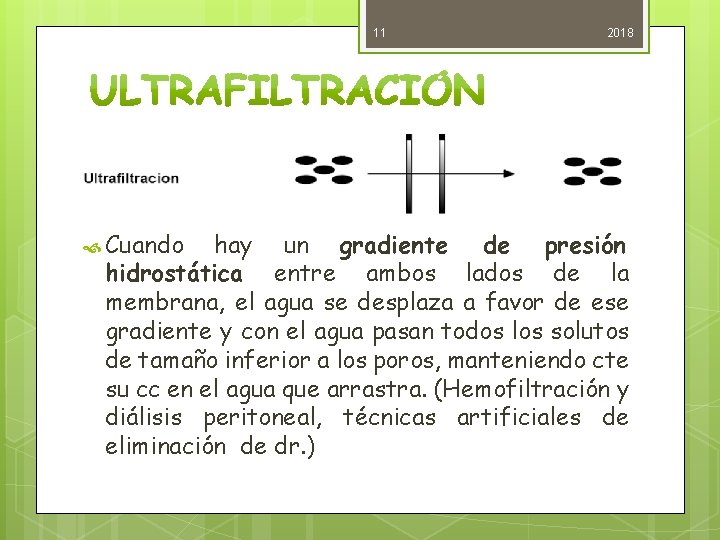
11 Cuando 2018 hay un gradiente de presión hidrostática entre ambos lados de la membrana, el agua se desplaza a favor de ese gradiente y con el agua pasan todos los solutos de tamaño inferior a los poros, manteniendo cte su cc en el agua que arrastra. (Hemofiltración y diálisis peritoneal, técnicas artificiales de eliminación de dr. )

12 2018 Pasaje por difusión a través de poros, sin movimiento de agua. Compuestos ionizados forman complejos de pares iónicos neutros combinándose con sustancias endógenas (mucina), que difunden a favor de su gradiente de cc

13 Es 2018 un transporte contra gradiente de una droga, que utiliza un portador y cuya fuente de energía es el gradiente de sodio entre ambos lados de la membrana. El sentido del pasaje del sodio es el que determina el sentido de transporte de la droga. Cuando la droga y el sodio se transportan en el mismo sentido se habla de cotransporte; si lo hacen en sentido contrario de contratransporte.

14 El 2018 transporte activo, directamente ligado a hidrólisis del ATP, es un mecanismo utilizado solamente por algunos fármacos (sodio, litio). En la endocitosis, el fármaco se une a un sitio receptor de una membrana celular, la que forma una vesícula que se incorpora al citoplasma. El proceso inverso se denomina exocitosis. Para algunos fcos (insulina) se ha documentado la existencia de endocitosis en un lado de una célula y exocitosis en el otro polo.

15 2018 ABSORCIÓN Es el pasaje de una droga desde un compartimiento en comunicación con el exterior al compartimiento presistémico. Se considera que un fármaco llega a la circulación sistémica cuando llega a las venas pulmonares. Compartimiento presistémico: es el conjunto de elementos ubicados entre el sitio de absorción y las venas pulmonares. A todo sitio de absorción le corresponde una vía de administración, pero hay vías de administración que no tienen sitio de absorción ya que no implican mecanismos de absorción (por ej. : la vía intravenosa).

16 2018 ABSORCIÓN Depende de: Características fisicoquímicas del fármaco Características de la preparación fcéutica Características del lugar de absorción • Eliminación presistémica y fenómeno de “primer paso”

17 2018 Características de la superficie absorbente • Area de absorción : TGI • Irrigación • TGI : por presencia de alimentos. • Factores fisiológicos o patológico : velocidad de vaciamiento gástrico, motilidad intestinal etc. BIODISPONIBILIDAD: Representa la fracción de dosis administrada (por cualquier vía) que alcanza la circulación general en forma inalterada (activa) • Via EV : la disponibilidad es de 100% • Vía oral : la biodisponibilidad no alcanza el 100% : Efecto de primer paso o metabolismo pre sistémico

18 May 20, 2021

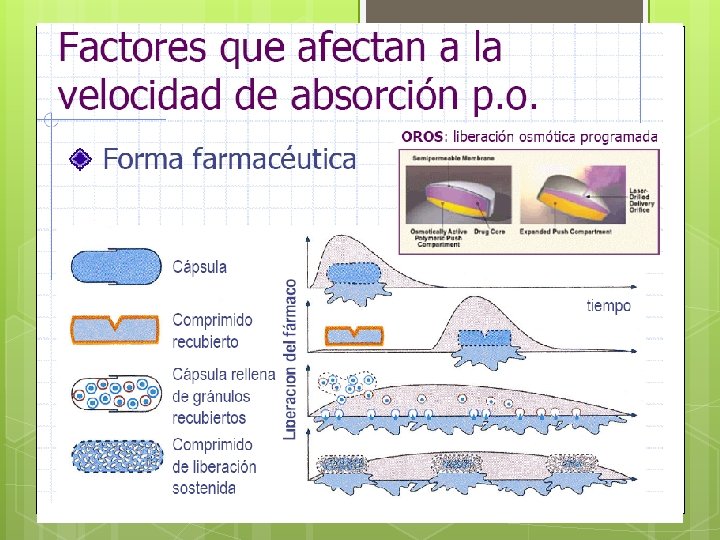
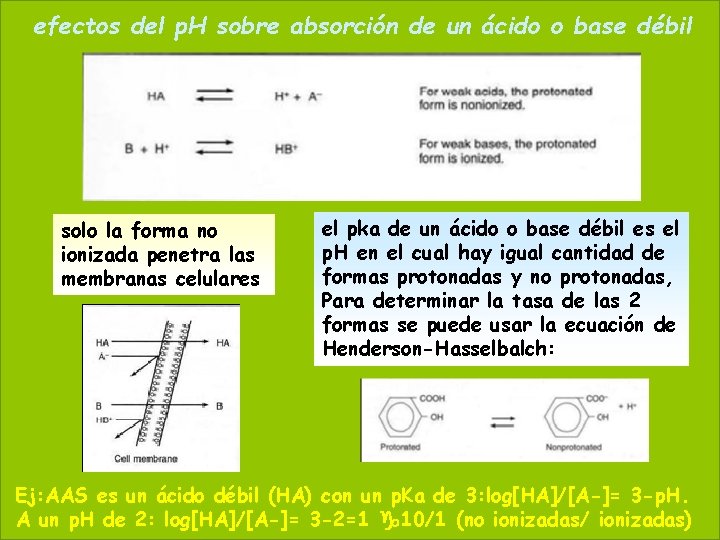
efectos del p. H sobre absorción de un ácido o. Maybase 19 20, 2021 débil solo la forma no ionizada penetra las membranas celulares el pka de un ácido o base débil es el p. H en el cual hay igual cantidad de formas protonadas y no protonadas, Para determinar la tasa de las 2 formas se puede usar la ecuación de Henderson-Hasselbalch: Ej: AAS es un ácido débil (HA) con un p. Ka de 3: log[HA]/[A-]= 3 -p. H. A un p. H de 2: log[HA]/[A-]= 3 -2=1 10/1 (no ionizadas/ ionizadas)

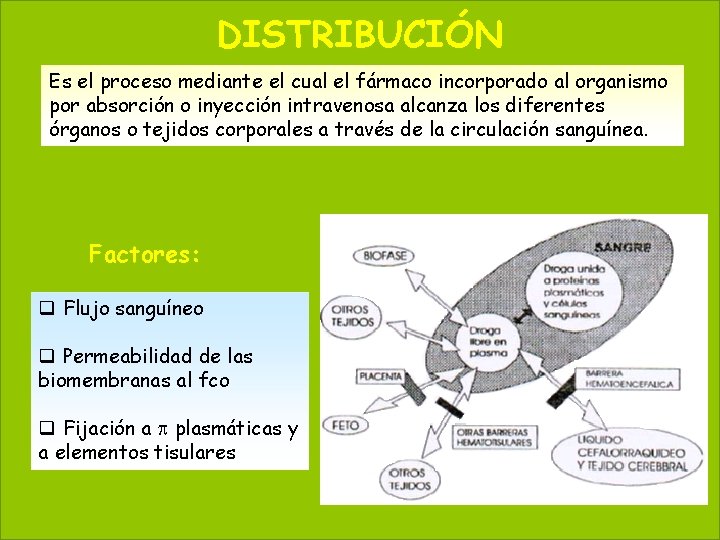
DISTRIBUCIÓN 20 May 20, 2021 Es el proceso mediante el cual el fármaco incorporado al organismo por absorción o inyección intravenosa alcanza los diferentes órganos o tejidos corporales a través de la circulación sanguínea. Factores: q Flujo sanguíneo q Permeabilidad de las biomembranas al fco q Fijación a p plasmáticas y a elementos tisulares

21 2018 MECANISMOS DE DISTRIBUCIÓN Los fármacos circulan en la plasma en dos formas: Fracción libre: Constituye la fracción fcológicamente activa, pues es la que puede difundir hasta los tejidos donde ejerce su acción (fracción difusible); sin embargo, por esta misma razón, también está disponible para el metabolismo y excreción pues puede alcanzar los órganos donde se metaboliza y excreta. Fracción ligada a las proteínas plasmáticas: Se halla unida principalmente a las albúminas, por lo cual no puede difundir hacia los tejidos (fracción no difusible): Es la fracción fcológicmanete inactiva (carece de acción), pues es incapaz de alcanzar los tejidos en donde ejerce sus efectos. Atraviesa poco las membranas, por lo cual: No llega a los tejidos. No cruza la BHE (no alcanza concentraciones adecuadas en el LCR). Se metaboliza con dificultad. Sirve como reservorio del fármaco en la sangre que se libera con lentitud.

22 • • 2018 En general, los fármacos de naturaleza ácida se ligan en mayor proporción a la albúmina plasmática, en tanto que los de naturaleza básica se unen más a las alfa-1 -glucoproteínas ácidas. Ambas formas del fármaco en la sangre (ligada y libre) se encuentran en equilibrio dinámico pues, a medida que la porción libre cumple su acción y se va consumiendo, la fracción ligada se separa de las proteínas, restableciendo la proporción de fracción libre, con lo cual se mantiene el equilibrio. Como la unión a las proteínas es poco específica, existen casos en que varios fármacos compiten por unirse a una misma proteína plasmática (por ej, la fenilbutazona puede desplazar a las warfarinas de su unión, aumentando su efecto anticoagulante). Para algunas sustancias endógenas, existen p específicas (transcortina para los glucocorticoides, transferrina para el hierro).

23 2018 TIPO DE UNIÓN A LAS PROTEINAS PLASMÁTICAS Reversible: Puede hacerse mediante dos tipos de enlace Enlace iónico o electrovalente: entre iones de carga opuesta. Es el tipo de enlace más común. Enlaces de hidrógeno Dipolar y de Van der Waals, para los fármacos no ionizados liposolubles (ej: esteroides hormonales). Irreversibles Enlace covalente por ej, entre los metales pesados (Hg, As) y los grupos sulfhidrilo de las proteínas plasmáticas.

24 2018 FACTORES QUE MODIFICAN LA DISTRIBUCION PROPIEDADES FISICO QUIMICAS DEL FARMACO Se distribuyen mejor los fármacos Liposolubles, No ionizado y los de Bajo peso molecular GASTO CARDIACO alcanzan concentraciones elevadas en los órganos más irrigados. PERMEABILIDAD CAPILAR a mayor permeabilidad mejor distribución de los fármacos. CONTENIDO LIPIDICO DEL TEJIDO existen fármacos que son muy Liposolubles quedando atrapados en los Tejidos grasos y no aptos para distribución GRADO DE UNION A LAS PROTEINAS PLASMATICAS Sólo la fracción libre (la no unida a la proteínas) pueden difundir libremente. BARRERAS CORPORALES *Barrera Hematoencefálica *Barrera Placentaria

25 2018 BARRERAS CORPORALES BARRERA HEMATOENCEFALICA Es permeable a Sustancias Liposolubles e Hidrosolubles muy pequeñas (Urea, Alcohol) Las sustancias muy Ionizadas son incapaces de pasarlos (Penicilina y Aminas cuaternarias), pero si hay inflamación de las Meninges (MENINGITIS) aumenta la vasodilatación y permite el pasaje de los antibióticos. BARRERA PLACENTARIA Los fármacos la atraviesan por Difusión pasiva, facilitada y Pinocitosis (Inmunoglobulinas tipo gammaglobulinas) Es permeable a fracciones no ionizadas, a los no electrolitos liposolubles (cloroformo, Eter y sustancias volátiles) Es permeable a Hormonas esteroideas, alcohol, salicilatos, atropina, Barbitúricos, antibióticos , alcaloides y antihistaminicos.

26 2018 MODELOS DE DISTRIBUCIÓN El agua corporal total, que en el adulto representa un 60% del peso corporal total, está distribuido de la siguiente manera: En el espacio intracelular: 40% del peso corporal. En el espacio extracelular: Intravascular (plasma): 5% Intersticial: 15% Por ej. en un sujeto de 70 kg. , el agua corporal total será de 42 litros, el agua intravascular 3, 5 litros y el agua intersticial alrededor de 10, 5 litros. La farmacocinética considera al organismo dividido en compartimiento, acuosos o no, pero siempre, “sectores virtuales del organismo en los cuales el medicamento se considera distribuido uniformemente”.

27 2018 MODELOS DE COMPARTIMENTOS A) MODELO UNICOMPARTAMENTAL En este caso, la depuración de un compuesto se produce siguiendo una cinética de primer orden, es decir, la cantidad de fármaco eliminada por unidad de tiempo depende de la cantidad (concentración) del compuesto presente en el comportamiento. ABSORCION Compartimento Central EXCRECION

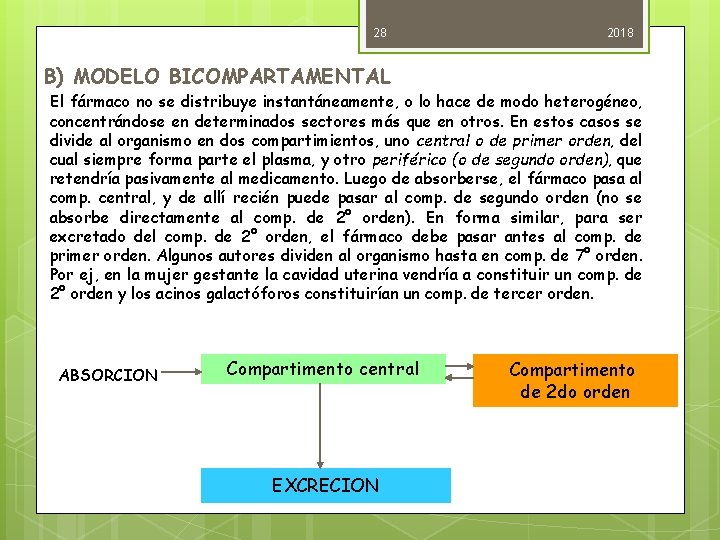
28 2018 B) MODELO BICOMPARTAMENTAL El fármaco no se distribuye instantáneamente, o lo hace de modo heterogéneo, concentrándose en determinados sectores más que en otros. En estos casos se divide al organismo en dos compartimientos, uno central o de primer orden, del cual siempre forma parte el plasma, y otro periférico (o de segundo orden), que retendría pasivamente al medicamento. Luego de absorberse, el fármaco pasa al comp. central, y de allí recién puede pasar al comp. de segundo orden (no se absorbe directamente al comp. de 2° orden). En forma similar, para ser excretado del comp. de 2° orden, el fármaco debe pasar antes al comp. de primer orden. Algunos autores dividen al organismo hasta en comp. de 7° orden. Por ej, en la mujer gestante la cavidad uterina vendría a constituir un comp. de 2° orden y los acinos galactóforos constituirían un comp. de tercer orden. ABSORCION Compartimento central EXCRECION Compartimento de 2 do orden

29 2018 REDISTRIBUCION � � Cdo se administra por vía IV un fco muy lipo. S, se diluirá en la sangre e irá distribuyéndose, alcanza mayores niveles en los órganos con mayor flujo sanguíneo absoluto (cerebro, riñón, pulmón) que en los de menor flujo (celular subcutáneo). A medida que pasa el tiempo, tenderá a aproximarse a un estado estacionario, pasando desde los tejidos con mayor flujo al plasma y, del plasma, a otros tejidos. A este proceso se lo llama redistribución. La redistribución de una droga puede significar el fin de su efecto terapéutico (tiopental).

30 2018 DISTRIBUCION DE DROGAS EN EL SNC � � En el SNC, sus células endoteliales están muy estrechamente unidas entre sí y forman parte de lo que se denomina barrera hematoencefálica. La barrera hematoencefálica no es uniforme. Por ej, no hay barrera en la zona quimiorreceptora gatillo (ZQG). En el tratamiento de la enfermedad de Parkinson con levodopa: esta se transforma en dopamina, que ejerce el efecto antiparkinsoniano en el cuerpo estriado y produce vómitos a nivel de la ZQG; si se administra carbidopa (no atraviesa la BHE) se inhibe la transformación de levodopa en dopamina a nivel de la ZQG, pero no en el cuerpo estriado, pudiendo de esta manera, aliviarse el efecto adverso sin afectarse el terapéutico.

31 DISTRIBUCIÓN � La distribución de los fármacos permite su acceso a los órganos en los que debe actuar y a los órganos que los van a eliminar y condiciona las concentraciones que alcanzan en cada tejido. � Tiene especial importancia en la elección del fármaco más adecuado para tratar enfermedades localizadas en áreas especiales, como el SNC, y en la valoración del riesgo de los fármacos durante el embarazo y la lactancia. 2018

32 2018 Volumen de Distribución El volumen aparente de distribución de un fármaco es el volumen en que tendría que haberse disuelto la dosis administrada de un fármaco para alcanzar la concentración plasmática observada. Este volumen aparente dependerá del volumen real en que se distribuya el fármaco, de su unión a las proteínas del plasma y de su unión a los tejidos. Cantidad de fármaco Vd = —————— Concentración plasmática

33 2018 METABOLISMO El metabolismo o biotransformación de fármacos es la modificación de sus moléculas catalizada por enzimas. Conjunto de reacciones que transforman al fco. en una sustancia mas fácilmente eliminable por las vías fisiológicas normales.

34 2018 MECANISMO DE BIOTRANFORMACION Se realiza mediante 2 tipos reacciones químicas : Reacciones de funcionalización Fase I: no sintéticas o de Oxidación, reducción, hidroxilación e hidrólisis Las reacciones de fase I suelen transformar el fármaco original en un metabolito mas polar, introduciendo o desenmascarando u grupo funcional (-OH, -NH 2, -SH). Con frecuencia estos metabolitos son inactivos, aunque en cierto casos solo se modifica su actividad. Reacciones de Fase II: sintéticas o de biosíntesis Conjugación, Acetilación, Metilación y Glutationización El fármaco o sus metabolitos se acoplan a un compuesto endógeno (ácido glucorónico, sulfato, acetato o un aminoácido). Este proceso conduce habitualmente a la inactivación del fármaco.

35 METABOLISMO o BIOTRANFORMACION REACCIONES DE FASE I Oxidaciones dependientes de citocromo P 450: Propranolol, Fenobarbital, Fenitoína, Fenibutazona, Anfetamina, Warfarina. Hidroxilaciones alifáticas: Pentobarbital, Amobarbital, Ibuprofeno, Digitoxina Reducción: Cloramfenicol, Clorazepam. Metadona Hidrólisis: Procaína, Succinilcolina, 2018

36 2018 REACCIONES DE FASE II Conjugación Reactivo endógeno Glucoronización UDP: ac. Glucorónico Morfina, Acetaminofén, Diazepam. Sufatiazol, Digoxina. Acetilación : Acetil-co. A Sulfonamidas Isoniazida, Mezcalina. Glutationización: Glutation Ac. Etacrínico, Bromobenceno Metilación : S-Adenosilmetionina Dopamina, Adrenalina, Histamina.

37 2018 FACTORES QUE MODIFICAN LA BIOTRANSFORMACIÓN Factores genéticos: Determinan que el metabolismo de un mismo fármaco pueda ser distinto en individuos de la misma especie. Esto explica la hipersusceptibilidad a ciertos fármacos. Por ej, la isoniazida se metaboliza en el hígado por procesos de acetilación. Por razones genéticas, existen sujetos con deficiencia de enzimas acetiladoras, a los que se conoce como “acetiladores lentos”, que son más propensos a la toxicidad por isoniazida. Otro ej. es la anemia hemolítica que ocurre en sujetos con deficiencia de la enzima G-6 -P-D que reciben antimaláricos (esta afección es de origen genético y se da más en la raza negra). Factores fisiológicos: Edad. La biotransformación es acelerada en jóvenes y lenta en neonatos (debido a la inmadurez de los sistemas enzimáticos), y en los ancianos (en quienes las funciones renal y hepática se hallan disminuidas). Sexo. ej, en la rata hembra el metabolismo de los barbitúricos es más lento que en el macho, debido a que el estradiol (hormona sexual femenina) inhibe la biotransformación de los barbitúricos. Gestación: la placenta constituye un órgano que participa activamente en la biotransformación de fármacos. Estrés: incrementa la biotransformación que inducen la biosíntesis de enzimas metabolizadoras.

38 2018 Factores patológicos: Desnutrición Los mecanismos de biotransformación están alterados por falta de los sustratos orgánicos indispensables para tal fin. Insuficiencia hepática cualquier alteración de la función hepática disminuye la capacidad de este órgano para metabolizar los fármacos. Insuficiencia renal puede alterar el metabolismo de algunos fármacos que se metabolizan a este nivel. Factores farmacológicos Vía de administración Los fármacos administrados por VO sufren metabolismo de primer paso, no así los que se administran por vía sublingual o intravascular. Gradientes de p. H Los fármacos existen bajo dos formas (ácidos y bases). Las formas ácidas se excretan en mayor proporción cuando se hallan en medio básico. Si se varía el p. H la excreción disminuye y el fármaco tiene mayor posibilidad de metabolizarse.

39 2018 Inductores enzimáticos: Algunos fármacos estimulan la síntesis de enzimas microsomales, aumentando su propia biotransformación o la de otros fármacos, lo que origina múltiplres interacciones y efectos tóxicos. Por ej, los barbitúricos (considerados entre los más potentes inductores enzimáticos) aceleran su propio metabolismo y el de otros medicamentos. Interacción farmacológica. Los fármacos pueden interactuar entre sí, acelerando o retardando su biotransformación, lo cual puede originar efectos tóxicos. Por ej, la fenilbutazona acelera la biotransformación de los anticoagulantes, inhibiendo su efecto.

40 2018 FUNCIONALIDAD DEL CITOCROMO P 450 � Familias de Citocromo P 450 �Involucradas en la síntesis de esteroides y ácidos biliares �Las que metabolizan xenobióticos �Localizado en el REL del hígado �Metaboliza sustratos liposolubles �Es inespecífico, saturable e inducible*

41 2018 Reacciones No Sintéticas o de Fase I Oxidorreducciones Son catalizadas por : Deshidrogenasas. Transfieren el e- a un aceptor diferente del O 2, (NAD, NADP). Oxidasas. Enzimas que utilizan al O 2 como aceptor de e-. 2 subtipos: - Oxidasas. No introducen O 2, en la molécula oxidada. - Oxigenasas. Introducen O 2, en la molécula oxidada. Las de f(x) mixta, oxidan un sustrato (introduciendo un átomo de O 2, ) y reducen al otro átomo de O 2, formando agua y utilizan para el transporte de electrones al citocromo P 450. Reductasas. Son enzimas que catalizan reducciones de sustratos. Las desalquilaciones, desaminaciones y decarboxilaciones de fármacos son reacciones oxidativas, canalizadas por oxigenasas. Hidrólisis droga reacciona con agua, dando dos moléculas de menor PM. Catalizadas por hidrolasas. Las hidrólisis de los ésteres son catalizadas por esterasas y los productos son un ácido y un alcohol. Las amidasas catalizan la hidrólisis de amidas, dando origen a un ácido y una amina.

42 2018 Reacciones Sintéticas o de Fase II Aquellas que agregan un radical químico a una droga. Conjugación con ácido glucurónico. Catalizada por la UDPglucuroniltransferasa, actuando como dador el ácido UDP-glucurónico. el compuesto formado es un βglucurónido. Las bacterias intestinales poseen β-glucuronidasas que pueden liberar la droga activa y permitir que se reabsorba. Sulfoconjugación. Conjugación con ácido sulfúrico, catalizada por sulfotransferasas. El dador de sulfatos es la fosfoadenosinafosfosulfato (PAPS). Algunas fenolsulfotransferasas se encuentran en las bacterias intestinales. Acetilaciones. Son N-acetilaciones catalizadas por N-acetiltransferasas siendo dador de acetilos la acetilcoenzima A. Metilaciones. Son reacciones catalizadas por metiltransferasas, siendo dador de metilos la Sadenosilmetionina. Conjugación con glicina. Es catalizada por la glicina-aciltransferasa. La glicina reacciona, generalmente, con sustancias aromáticas y los productos obtenidos se denominan ácidos hipúricos. Formación de ácidos mercaptúricos. Inicialmente, la droga reacciona con el glutatión (gamma-glutamil-cisteinil-glicina) con intervención de glutatión-S-transferasas. Posteriormente, en pasos sucesivos, se separan el ácido glutámico y la glicina, quedando la droga unida a la cisteína (compuesto denominado ácido mercaptúrico).

METABOLISMO 43 May 20, 2021 biotransformación, primer paso Los fármacos que se absorben en el intestino pueden ser biotransformados por enzimas en la pared intestinal y en el hígado antes de llegar a la circulación general Muchos fármacos son convertidos a metabolitos inactivos durante el fenómeno del primer paso, disminuyendo la biodisponibilidad

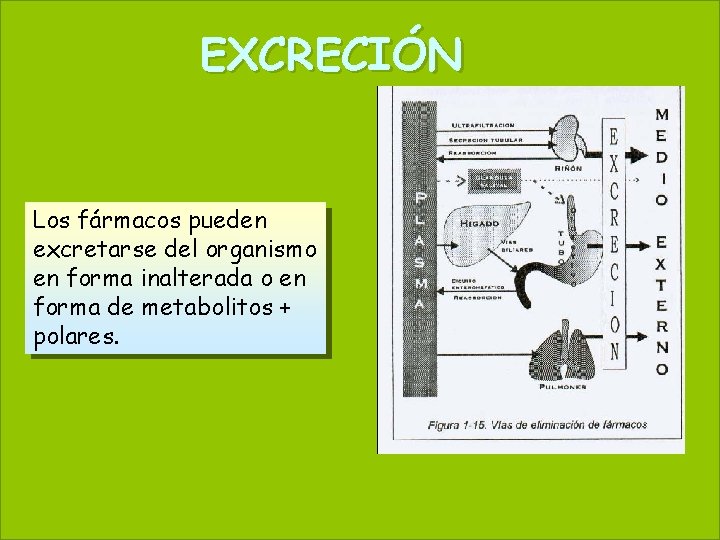
EXCRECIÓN 44 Los fármacos pueden excretarse del organismo en forma inalterada o en forma de metabolitos + polares. May 20, 2021

EXCRECIÓN 45 2018 El nefrón es el principal sistema de excreción de drogas. Es el resultado de la combinación de procesos de Ultrafiltración, Reabsorción y Secreción. En el glomérulo se produce la Ultrafiltración de plasma. También pasa una pequeña fracción de la albúmina que, luego, es casi totalmente reabsorbida. En el túbulo renal tienen lugar la Reabsorción, Secreción, Acumulación y Biotransformación de drogas Secreción tubular Es el pasaje de droga desde el plasma a la luz tubular, a través del epitelio del túbulo. se efectúa por medio de mecanismos concentrativos sodio dependientes, y muchas veces la unión a proteínas plasmáticas no impide este proceso. El segmento 2 del túbulo proximal es el principal sitio de secreción tubular. Reabsorción tubular Se habla de reabsorción cuando una droga biodisponible pasa a un compartimiento de excreción (colon, túbulo renal) y es nuevamente absorbida desde él. Una molécula reabsorbida puede o no volver a la circulación sistémica.

EXCRECIÓN p. H 46 2018 urinario y Excreción de drogas Tanto el túbulo proximal como el distal tienen capacidad de modificar el p. H urinario; como consecuencia, varían la fracción de droga no ionizada, la reabsorción y la excreción de las drogas. Si se alcaliniza la orina, excreción de ácidos (barbitúricos, salicilatos), pq su fracción ionizada, por lo que su reabsorción. Si se acidifica la orina, la reabsorción de bases (anfetamina) Acumulación tubular de drogas Ciertas drogas, como las polimixinas y los aminoglucósidos, tienden a acumularse en el túbulo proximal, y esta acumulación estaría relacionada con su toxicidad.

47 2018

OTRAS VÍAS DE EXCRECIÓN 48 May 20, 2021 EXCRECIÓN RENAL: a) Filtración Glomerular: Fcos libres y Metabolitos. b) Reabsorción Tubular Pasiva: Túbulos Prox. y Distal. Influencia del p. H. c) Secreción Tubular Activa: Bomba de secreción de ác. débiles y bases débiles. EXCRECIÓN BILIAR Y FECAL: Fármacos inalterados no absorbidos. Metabolitos en Bilis: ác. y bases orgánicas incorporadas a la bilis por transporte activo. Circulación Enterohepática, eventual eliminación renal. EXCRECIÓN PULMONAR: a) Anestésicos Generales: líquidos volátiles y gases. b) Alcohol. c) Otros líquidos volátiles: gasolina, kerosene. EXCRECIÓN LACTEA: Importante por posible efectos en el niño lactante (ansiolíticos, antibióticos, alcohol, depresores del SNC, otros). OTRAS VIAS DE EXCRECIÓN. Saliva: difusión simple fármacos no ionizados. Conveniente para determinación Cp fcos. Sudor. Lágrimas. Piel, pelos: (Determinación de algunos metales pesados tóxicos: arsénico, mercurio)

BIODISPONIBILIDAD 49 May 20, 2021 Biodisponibilidad: la fracción de la dosis administrada de un fármaco y a la velocidad con que éste llega a la circulación sistémica despues de los procesos de absorción y está disponible para cumplir su efecto farmacológico. Bioequivalentes: dos preparados con igual pa pero de distinto origen y tienen = biodisponibilidad.

50 2018 EQUIVALENTES FARMACÉUTICOS: contienen el mismo pa o fármaco, la misma sal o éster, la misma cantidad del fármaco, ff, son administrados por la misma vía, cumplen idénticos o comparables estándares de calidad, aunque posean diferencias en los excipientes o formas de elaboración. ALTERNATIVA TERAPÉUTICA: Medicamentos similares al original, que contienen el mismo pa, aunque diferente sal, o éster, se presentan en diferentes ff o concentraciones, pero c/ la misma vía de administración, indicación terapéutica y posología.

51 FARMACOCINETICA CUANTITATIVA 2018

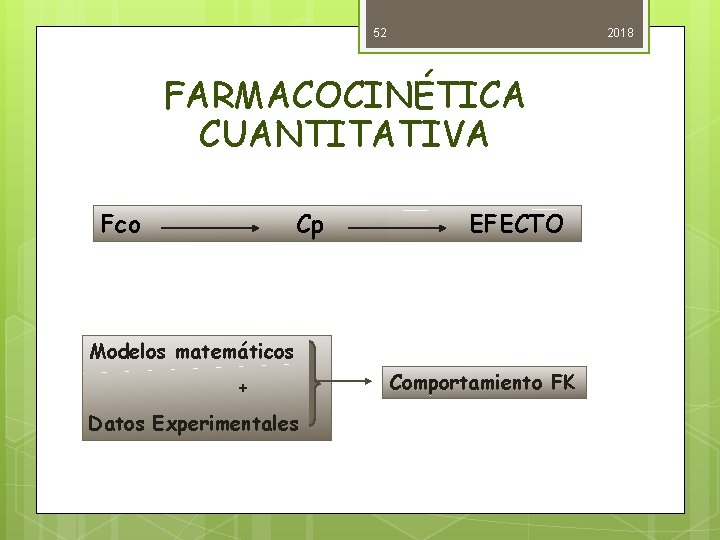
52 2018 FARMACOCINÉTICA CUANTITATIVA Fco Cp EFECTO Modelos matemáticos + Datos Experimentales Comportamiento FK

CINETICA DE PRIMER ORDEN 53 Cp May 20, 2021 Log Cp Cpo Pdte: -Ke/2, 303 Tpo d. C = - K cte dt Cp = Cpo Tpo Log Cp = log Cpo – K t 2, 303 * e –Kt Ln Cp = ln Cpo – K t

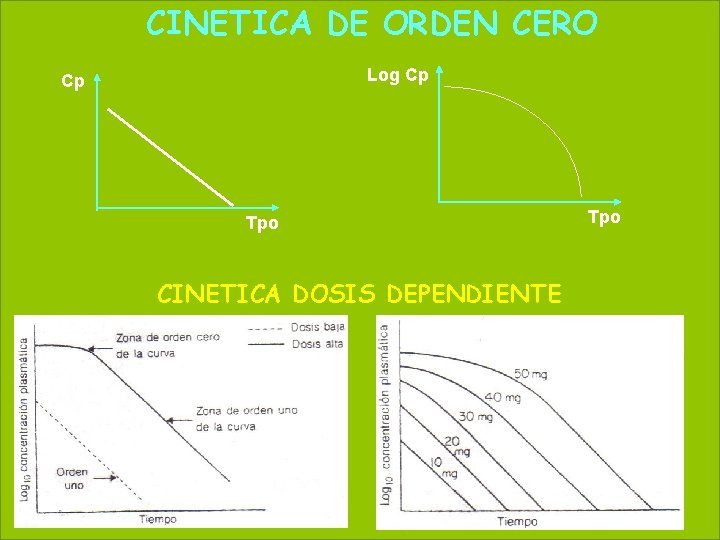
CINETICA DE ORDEN CERO 54 May 20, 2021 Log Cp Cp Tpo CINETICA DOSIS DEPENDIENTE Tpo

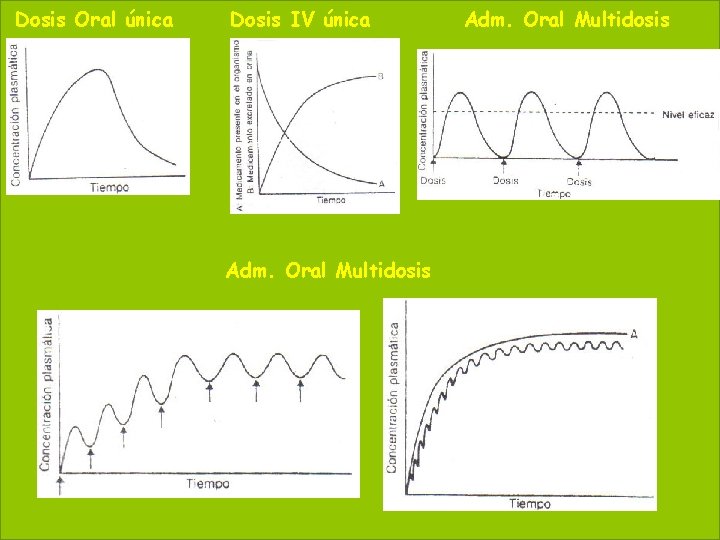
Dosis Oral única Dosis IV única 55 Adm. Oral Multidosis May 20, 2021

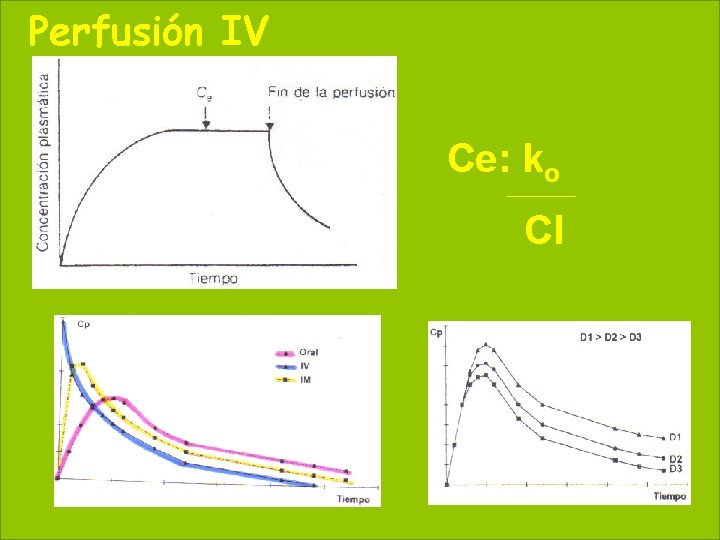
Perfusión IV 56 May 20, 2021 Ce: ko Cl

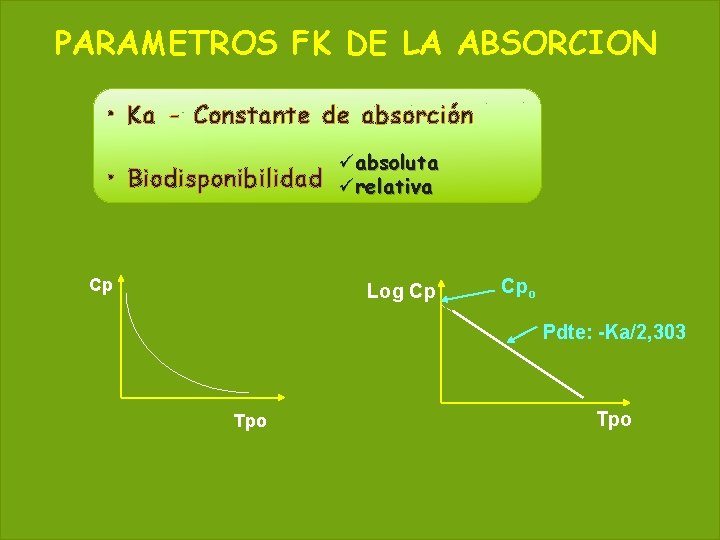
PARAMETROS FK DE LA ABSORCION 57 May 20, 2021 • Ka - Constante de absorción üabsoluta • Biodisponibilidad ürelativa Cp Log Cp Cpo Pdte: -Ka/2, 303 Tpo

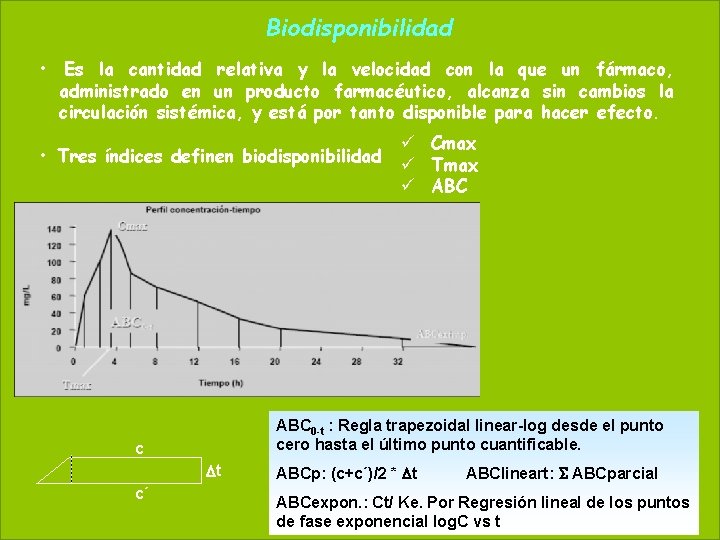
Biodisponibilidad 58 May 20, 2021 • Es la cantidad relativa y la velocidad con la que un fármaco, administrado en un producto farmacéutico, alcanza sin cambios la circulación sistémica, y está por tanto disponible para hacer efecto. • Tres índices definen biodisponibilidad ABC 0 -t : Regla trapezoidal linear-log desde el punto cero hasta el último punto cuantificable. c Dt c´ ü Cmax ü Tmax ü ABCp: (c+c´)/2 * Dt ABClineart: S ABCparcial ABCexpon. : Ct/ Ke. Por Regresión lineal de los puntos de fase exponencial log. C vs t

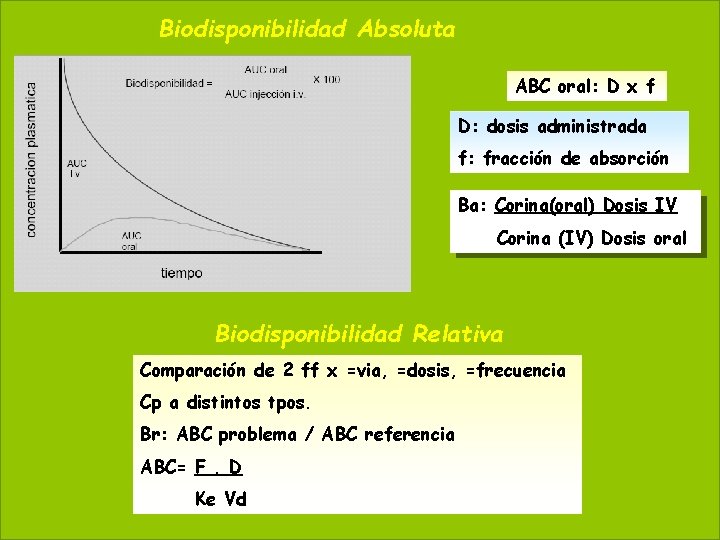
Biodisponibilidad Absoluta 59 May 20, 2021 ABC oral: D x f D: dosis administrada f: fracción de absorción Ba: Corina(oral) Dosis IV Corina (IV) Dosis oral Biodisponibilidad Relativa Comparación de 2 ff x =via, =dosis, =frecuencia Cp a distintos tpos. Br: ABC problema / ABC referencia ABC= F. D Ke Vd

60 2018 CINETICA DE ABSORCION La Ka representa probabilidad que tiene una molécula de absorberse por unidad de tiempo. Ø La mayoría de los procesos de absorción son de 1 er orden. La velocidad del proceso es entonces proporcional al número de moléculas disponibles para absorberse. Ø En los procesos de orden cero, la velocidad del proceso es constante e independiente de la concentración. Ø La biodisponibilidad indica la cantidad y la forma en que un fármaco llega a la circulación sistémica. Ø La biodisponibilidad suele valorarse mediante el área bajo la curva de los niveles plasmáticos.

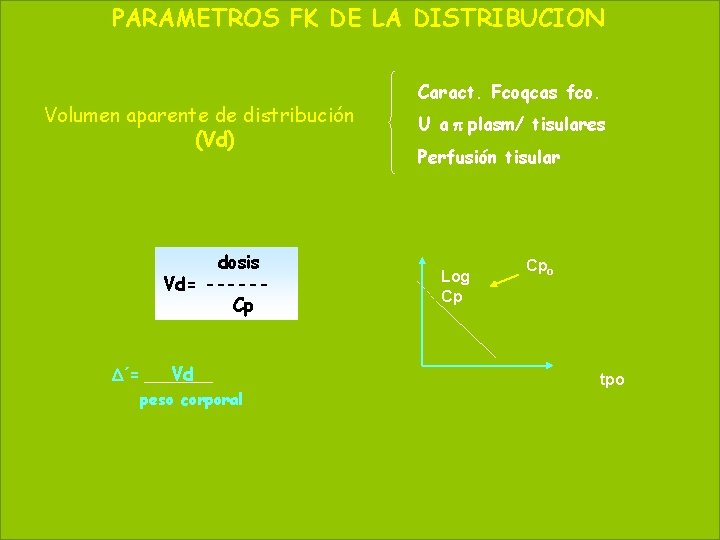
PARAMETROS FK DE LA DISTRIBUCION 61 May 20, 2021 Volumen aparente de distribución (Vd) dosis Vd= -----Cp D´= Vd peso corporal Caract. Fcoqcas fco. U a p plasm/ tisulares Perfusión tisular Log Cp Cpo tpo

Metabolismo y eliminación de fármacos. 62 May 20, 2021 Terminación de la acción de los fármacos Ø Metabolismo (Biotransformacion) - Higado Ø Excreción – Riñones – Higado, bilis – Pulmones Ø Redistribucion Eliminación de fármacos. Parámetros farmacocinéticos • Ke - Constante de eliminación. • Vida media de eliminación • Aclaramiento. ü Tipos de cinética de eliminación Eliminación de primer orden o lineal Eliminación de orden 0

Eliminación de fármacos. Parámetros farmacocinéticos 63 May 20, 2021 • Ke, Constante de eliminación: indica en términos porcentuales la velocidad a la que se elimina un fármaco. • Vida media de eliminación: tiempo que tarda una determinada concentración plasmática en reducirse a la mitad. • Aclaramiento: Volumen aparente de plasma queda depurado por unidad de tiempo.

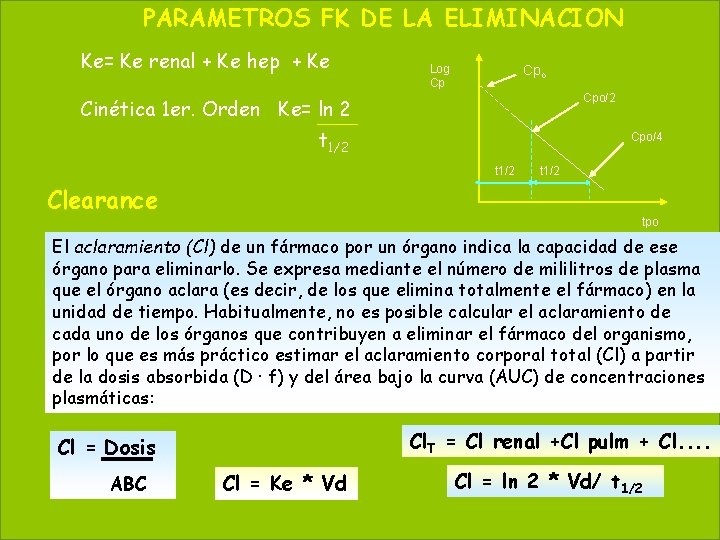
PARAMETROS FK DE LA ELIMINACION 64 May 20, 2021 Ke= Ke renal + Ke hep + Ke Log Cp Cpo/2 Cinética 1 er. Orden Ke= ln 2 t 1/2 Cpo/4 t 1/2 Clearance tpo El aclaramiento (Cl) de un fármaco por un órgano indica la capacidad de ese órgano para eliminarlo. Se expresa mediante el número de mililitros de plasma que el órgano aclara (es decir, de los que elimina totalmente el fármaco) en la unidad de tiempo. Habitualmente, no es posible calcular el aclaramiento de cada uno de los órganos que contribuyen a eliminar el fármaco del organismo, por lo que es más práctico estimar el aclaramiento corporal total (Cl) a partir de la dosis absorbida (D · f) y del área bajo la curva (AUC) de concentraciones plasmáticas: Cl. T = Cl renal +Cl pulm + Cl. . Cl = Dosis ABC Cl = Ke * Vd Cl = ln 2 * Vd/ t 1/2

65 May 20, 2021 Ejemplo de Eliminación de fármacos

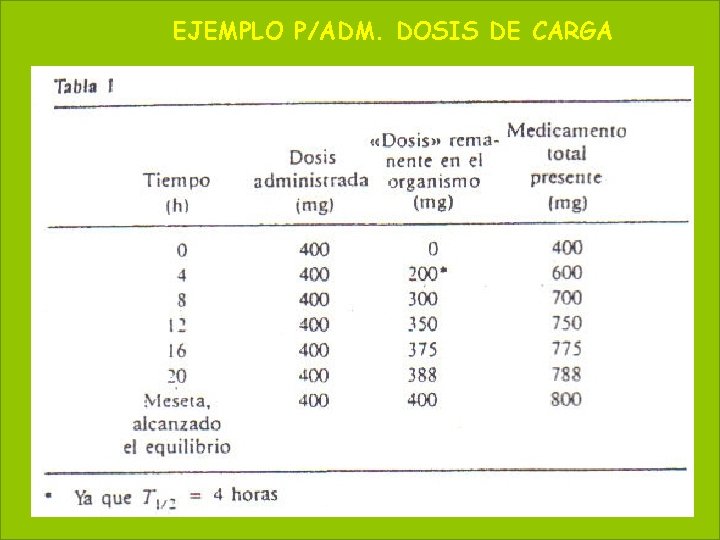
66 DOSIS DE CARGA May 20, 2021 EJEMPLO P/ADM.

67 May 20, 2021

La cinética de eliminación cuantifica la velocidad con que los 68 May 20, 2021 fármacos se eliminan del organismo. Se expresa mediante dos constantes farmacocinéticas: t 1/2 e= 0. 5 Cp 0 k • Aclaramiento o Clearence (Cl) • Constante de Eliminacion (Ke) Cp=Cp 0 - k. t t 1/2 e = 0, 693/Ke Cp = Cp 0 · e -K e · t CLEARENCE El aclaramiento (Cl) de un fármaco por un órgano indica la capacidad de ese órgano para eliminarlo. Se expresa mediante el número de mililitros de plasma que el órgano aclara (es decir, de los que elimina totalmente el fármaco) en la unidad de tiempo. Habitualmente, no es posible calcular el aclaramiento de cada uno de los órganos que contribuyen a eliminar el fármaco del organismo, por lo que es más práctico estimar el aclaramiento corporal total (Cl) a partir de la dosis absorbida (D · f) y del área bajo la curva (AUC) de concentraciones plasmáticas: D·f Cl = ——— AUC El aclaramiento es una constante no compartimental, es decir, independiente del comportamiento monocompartimental, bicompartimental o tricompartimental del fármaco.

FORMULAS 69 May 20, 2021