2010 QUIMICA SEMANA No 1 ESTRUCTURA ATMICA TABLA

2010 QUIMICA SEMANA No. 1 ESTRUCTURA ATÓMICA TABLA PERIÓDICA

QUIMICA: ES LA RAMA DE LA CIENCIA QUE ESTUDIA LAS CARACTERÍSTICAS Y COMPOSICIÓN DE TODOS LOS MATERIALES, ASI COMO LOS CAMBIOS QUE ÉSTOS SUFREN. CADA SUSTANCIA QUÍMICA TIENE CARACTERÍSTICAS ESPECÍFICAS.
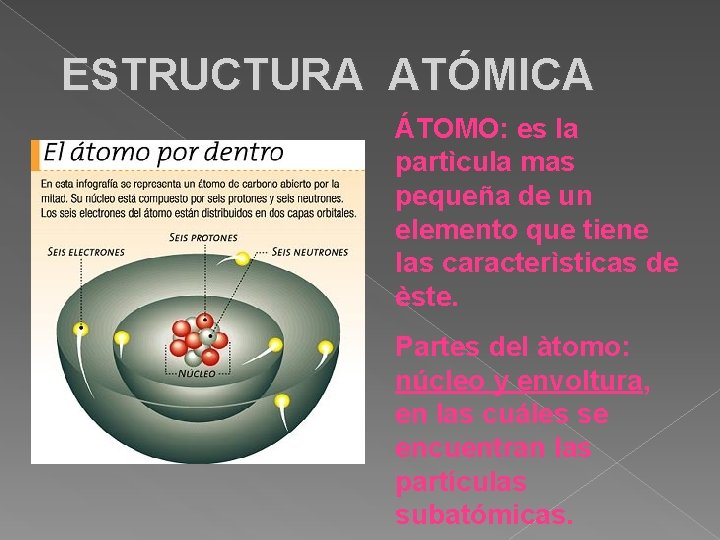
ESTRUCTURA ATÓMICA ÁTOMO: es la partìcula mas pequeña de un elemento que tiene las caracterìsticas de èste. Partes del àtomo: núcleo y envoltura, en las cuáles se encuentran las partículas subatómicas.
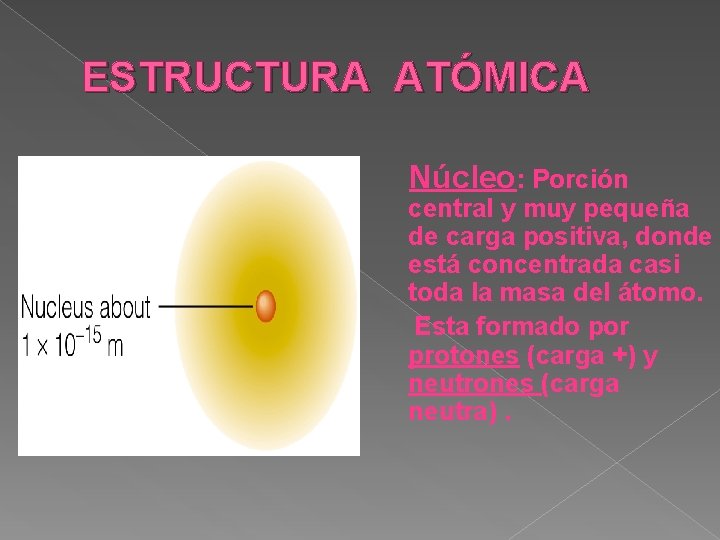
ESTRUCTURA ATÓMICA Núcleo: Porción central y muy pequeña de carga positiva, donde está concentrada casi toda la masa del átomo. Esta formado por protones (carga +) y neutrones (carga neutra).


Nube Electrónica, Envoltura o Corona. Región difusa alrededor del núcleo. Tiene carga negativa, en la cual encontramos los electrones (-) girando a gran velocidad. Todo átomo es electricamente neutro. PROTONES = ELECTRONES (+) (-)

SIMBOLOS DE PARTICULAS SUBATÓMICAS. Partícula electrón Protón Neutrón Símbolo ep+ o p n Carga 11+ 0 Masa (g) 9. 10953 x 10 -28 g 1. 67265 x 10 -24 g 1. 678495 x 1024 g

NUMERO DE MASA (A) Es la suma de protones + neutrones. A= p + n Ej. Ca 40=20+20 Na 23 = 11+12

NÚMERO ATÓMICO (Z) Es el número de protones que hay en el núcleo de cada átomo de ese elemento. Ej. (Z) Co 27 (Z) F 9 El número de protones determina la identidad de cada elemento.

Ej. Elemento C No. Protones Atómico (Z) 6 6 O 8 8 Ca 20 20 Fe 26 26

En la tabla periódica los elementos están ordenados por el No. atómico. Ej. El Nitrógeno tiene 7 protones y 7 electrones y un No. Masa (A) 14. 01 uma. 1 uma = 1. 6606 x 10 -24 g Cuál es el carga eléctrica total del átomo? Cuántos neutrones tiene el átomo? Cual es el no. Atómico del nitrógeno? Ejercicio: Mg, Co, P

ISOTOPOS: Atomos de un elemento específico, que contiene diferente No. de neutrones, por lo tanto diferente número de Masa. La mayor parte de los elementos tienen varios isótopos. El Estaño (Sn) es el elemento con mayor número de isótopos. Todos los isótopos tienen prácticamente las mismas propiedades químicas.
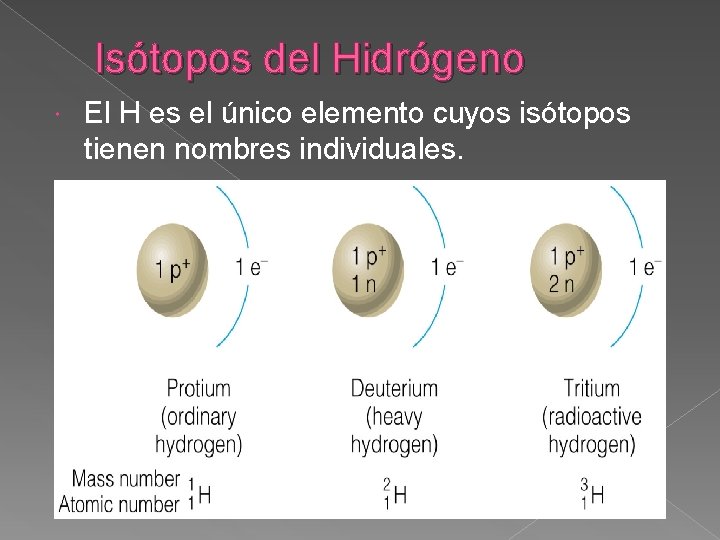
Isótopos del Hidrógeno El H es el único elemento cuyos isótopos tienen nombres individuales.

Algunas formas de nombrar isótopos: Co 60 (60 indica el no. de masa). 27 protones + 33 neutrones. X Az X= símbolo del elemento. A = no. de masa Z= no. Atómico. 60 Co 27 Ej. Mg

Aplicación médica: El Co 60 es un isótopo radiactivo que se emplea en el tratamiento del Cáncer por radioterapia. Peso atómico o masa atómica media: es el promedio de las masas de todos los isótopos naturales de ese elemento.
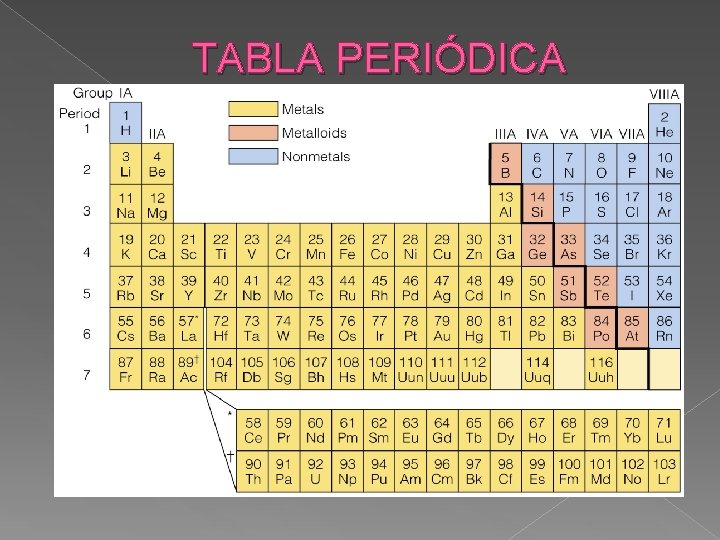
TABLA PERIÓDICA

METALES: • La mayor parte adquiere un lustre metálico brillante cuando se pulen. • No se combinan unos con otros. • Reaccionan con los no metales. • Conducen electricidad NO METALES • Se combinan con metales. • Se combinan con ellos mismos para formar compuestos como CO , SO 2 , CH 4

• No conducen la electricidad. METALOIDES: • Sus propiedades tienen un carácter intermedio. • Semiconductores de la electricidad.

Períodos: son las filas horizontales de la tabla (7). Grupos o Familias: Son las columnas verticales de elementos. Se numeran de I a VIII, de acuerdo a sus electrones de valencia, y se dividen en A y B. Pueden también numerarse de 1 a 18 (nueva tendencia). A: Elementos representativos. B: Elementos de transición.

NOMBRES DE LOS GRUPOS: IA: Metales alcalinos. IIA: Metales alcalinoterreos. IIIA: Familia del Boro. IV: Familia del Carbono V: Familia del Nitrógeno. VI: Familia del Oxígeno. VII: Halógenos VIII: Gases Nobles
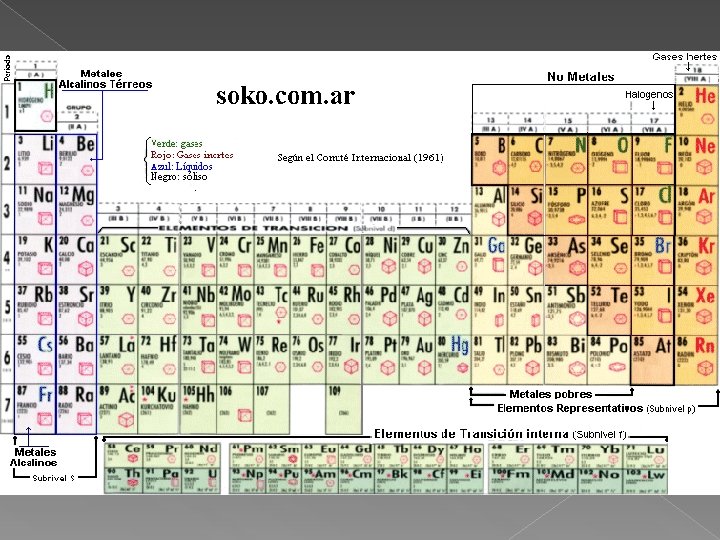

v. Entre los no metales se encuentran dos gases muy conocidos N y O que están presentes en la atmósfera. v. Los metales del Grupo IA son los más reactivos. Ej. K, Na.

§LANTANIDOS: Grupo de 14 elementos no. atómico de 58 -71. §ACTINIDOS: Grupo de elementos de No. Atómico de 90 – 103. §TRANSURÁNICOS: Sintéticos con más 92 protones.
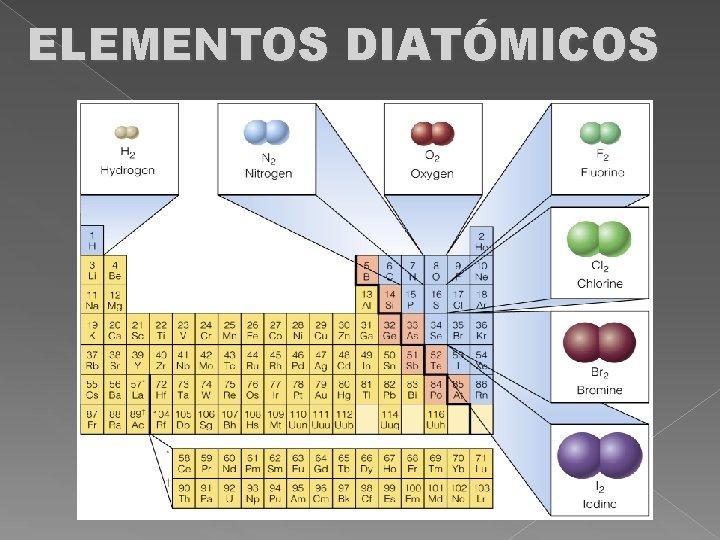
ELEMENTOS DIATÓMICOS

Elemento más abundante en la naturaleza.
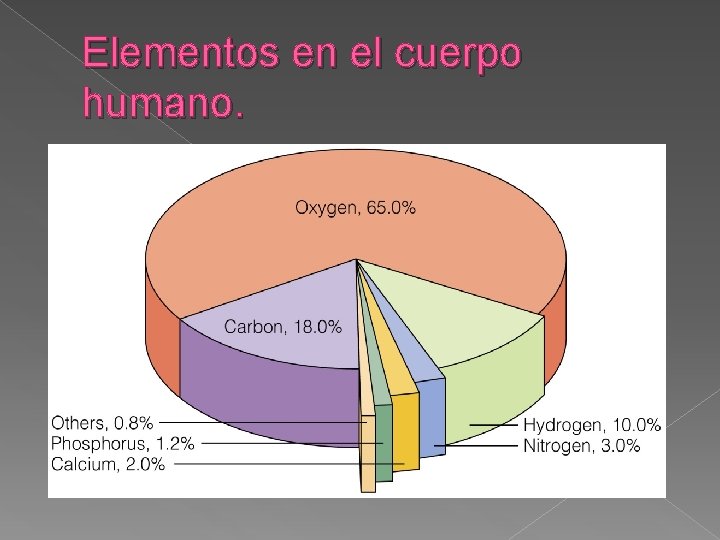
Elementos en el cuerpo humano.

CONFIGURACIÓN ELECTRONICA Camino que recorren los electrones en los átomos. En un átomo, cada electrón tiene una energía específica conocida como NIVEL DE ENERGIA. A éstos se les asignan valores llamados numeros cuànticos principales (n). En los àtomos de elementos conocidos existen 4. Al aumentar el número cuantico principal aumenta la energía de los electrones. 1<2<3<4 A la conf. electrónica se deben muchas de las propiedades de los elementos. Electrones por nivel = 2 n 2
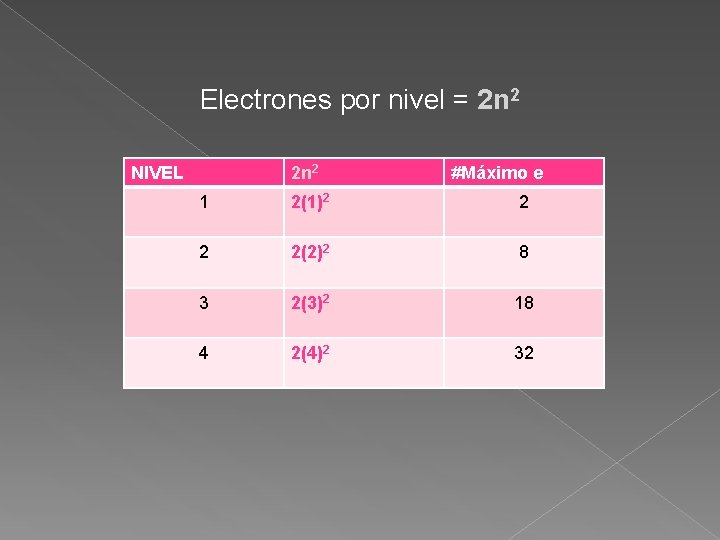
Electrones por nivel = 2 n 2 NIVEL 2 n 2 #Máximo e 1 2(1)2 2 2 2(2)2 8 3 2(3)2 18 4 2(4)2 32
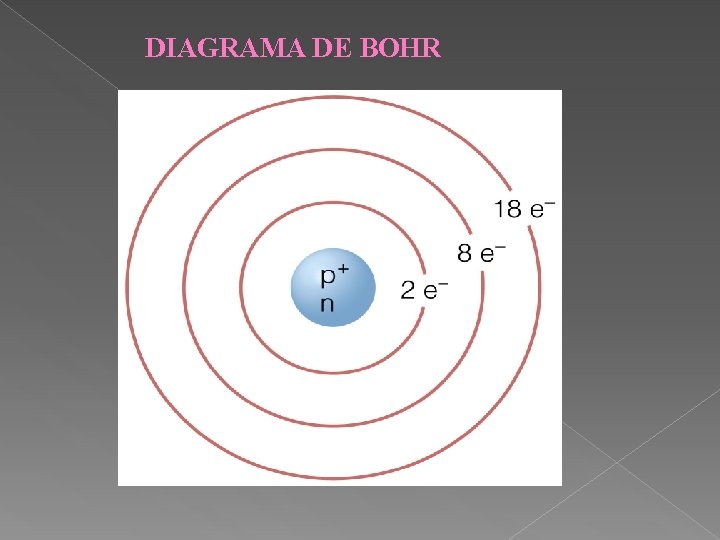
DIAGRAMA DE BOHR
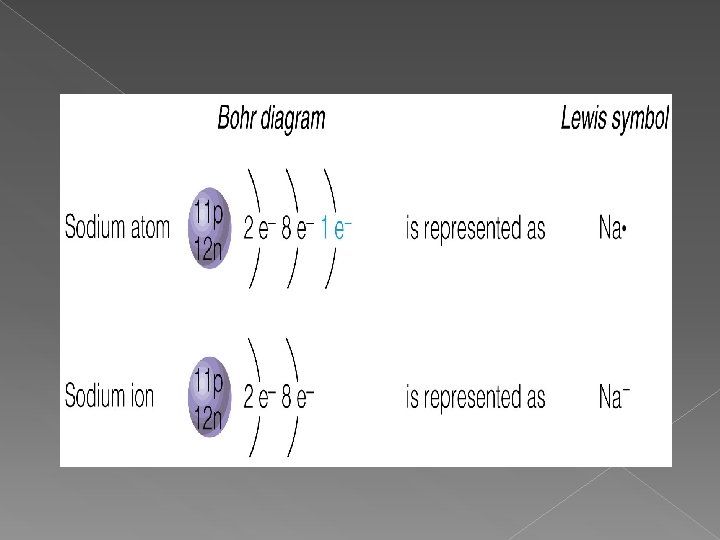


Electrones de Valencia Son los electrones que están en el nivel externo de energía (son los que intervienen en las reacciones químicas). En los elementos representativos equivalen al No. de columna. Cada nivel de Energía está constituido por uno o más subniveles y cada uno de ellos tiene uno o más orbitales en forma tridimensional.
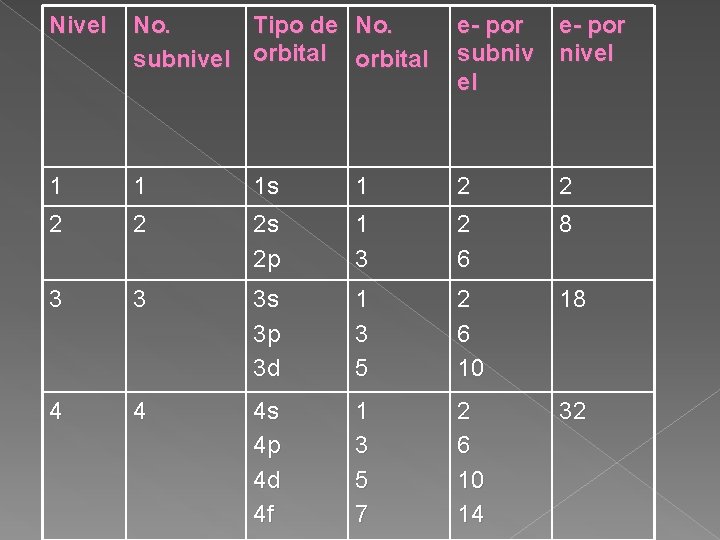
Nivel No. Tipo de No. subnivel orbital e- por subniv nivel el 1 1 1 s 1 2 2 2 s 2 p 1 3 2 6 8 3 3 3 s 3 p 3 d 1 3 5 2 6 10 18 4 4 4 s 4 p 4 d 4 f 1 3 5 7 2 6 10 14 32
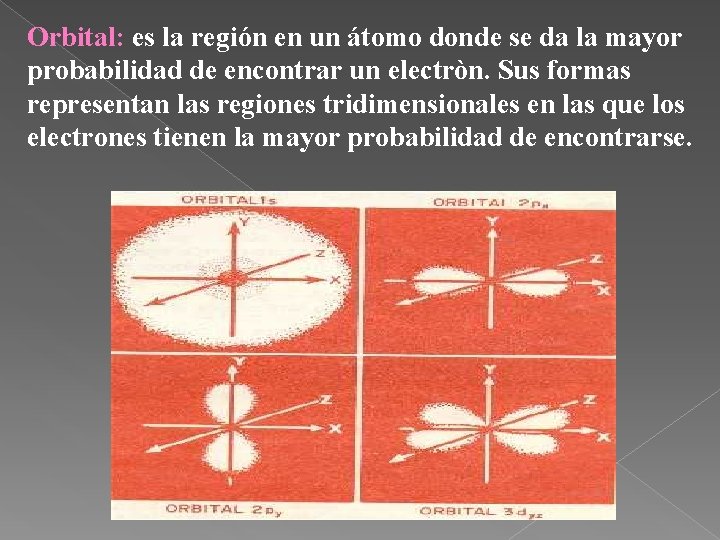
Orbital: es la región en un átomo donde se da la mayor probabilidad de encontrar un electròn. Sus formas representan las regiones tridimensionales en las que los electrones tienen la mayor probabilidad de encontrarse.
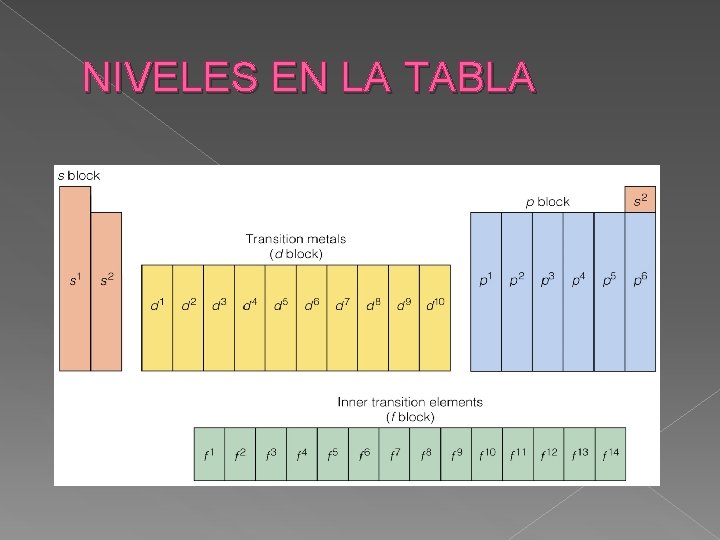
NIVELES EN LA TABLA

La localización de los elementos en la tabla periódica va de acuerdo con las disposición de los electrones de valencia en los subniveles. La configuración electrónica para un átomo en su estado basal se puede representar:
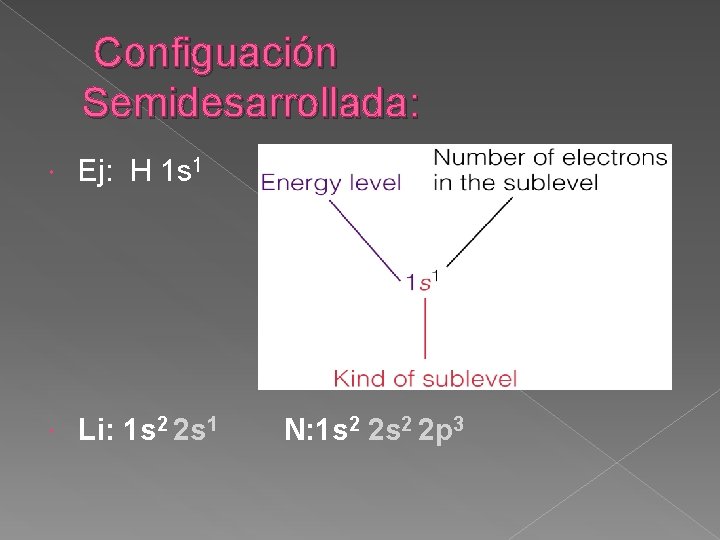
Configuación Semidesarrollada: Ej: H 1 s 1 Li: 1 s 2 2 s 1 N: 1 s 2 2 p 3
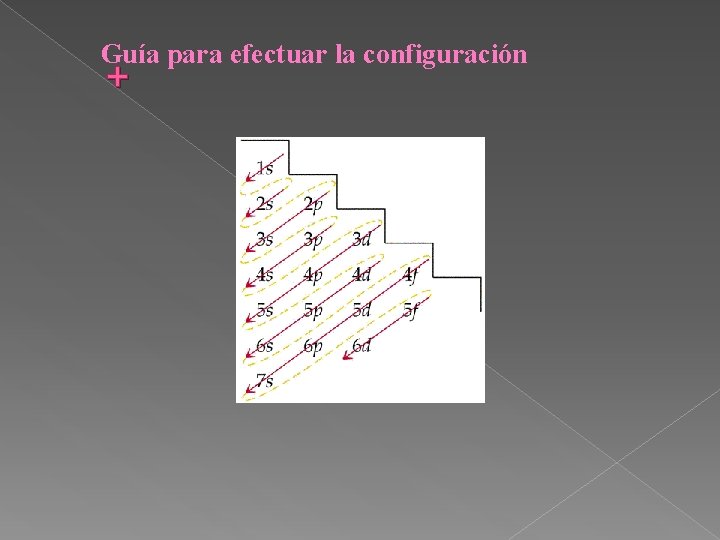
Guía para efectuar la configuración +

Configuración Abreviada Se escribe entre corchetes el símbolo del gas noble que antecede al elemento y luego, la configuración de los electrones de valencia. Ej. Na: [Ne] 3 s 1

Configuración de Iones Ion: Partícula cargada que se produce cuando un átomo gana o pierde electrones. Cationes: átomos de metales que perdieron electrones de valencia. Aniones: átomos no metálicos que ganaron electrones. Tienden a formar un octeto de electrones.
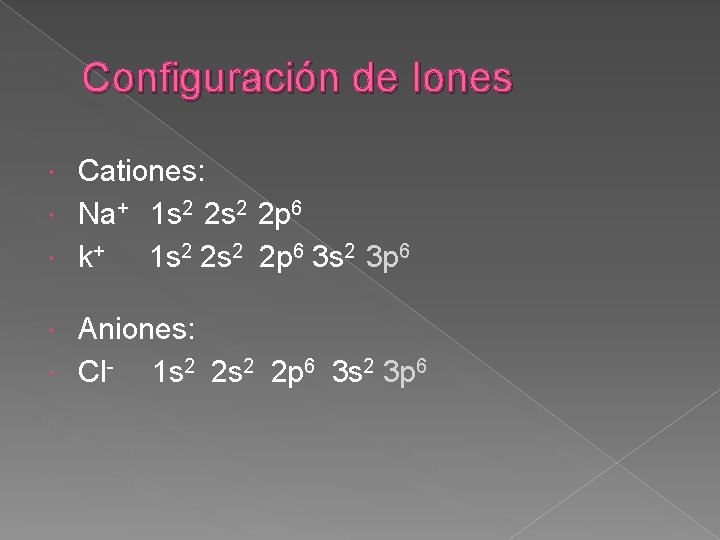
Configuración de Iones Cationes: Na+ 1 s 2 2 p 6 k+ 1 s 2 2 p 6 3 s 2 3 p 6 Aniones: Cl 1 s 2 2 p 6 3 s 2 3 p 6

ELECTRONEGATIVIDAD Es una medida de la tendencia que muestra un átomo en un enlace para atraer electrones compartidos. La electronegatividad aumenta de izquierda a derecha, es decir conforme aumenta el No. Atómico. Dentro de un grupo la electronegatividad disminuye a medida que el No. Atómico aumenta.
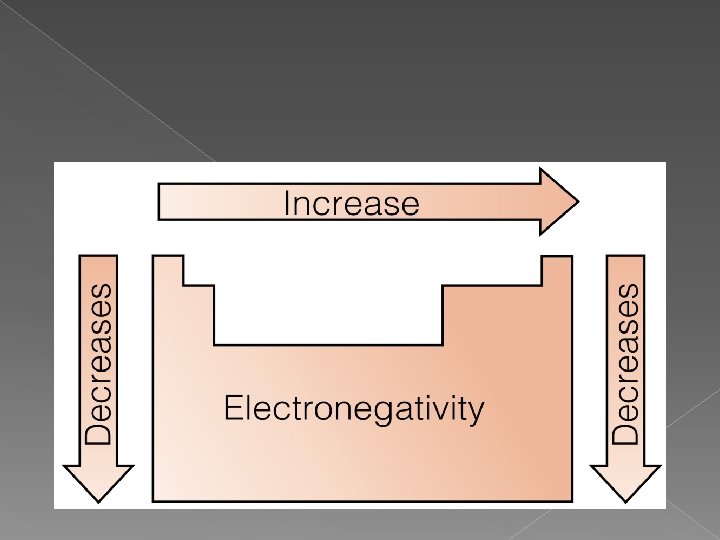

ELECTRONEGATIVIDAD

FIN
- Slides: 45