2 HAtom Grundlagen 2 1 SchrdingerGleichung mit RadialPotenzial


























- Slides: 33

2. H-Atom Grundlagen 2. 1 Schrödinger-Gleichung mit Radial-Potenzial 2. 2 Die Radial-Abhängigkeit der Wellenfunktion 2. 3 Die Winkel-Abhängigkeit der Wellenfunktion 2. 4 Drehimpuls 24 2 8 17 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 1

2. 1 Schrödingergleichung mit Radial-Potenzial Äquipotenzial-Flächen des Coulomb-Potenzials: 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 2

Polar-Koordinaten 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 3

Separation der Variablen 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 4

Magnet-Quantenzahl m = 0, ± 1, ± 2, … m = 3: 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 5

Denselben Trick nochmal 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 6

Drei Differential-Gleichungen 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 7

2. 2 Die Radial-Abhängigkeit der Wellenfunktion ℓ=2 ℓ=1 ℓ=0 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 8

Radial-Wellenfkt. für kleine und grosse Abstände 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 9

Haupt- und Bahndrehimpuls-Quantenzahlen n, l 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 10

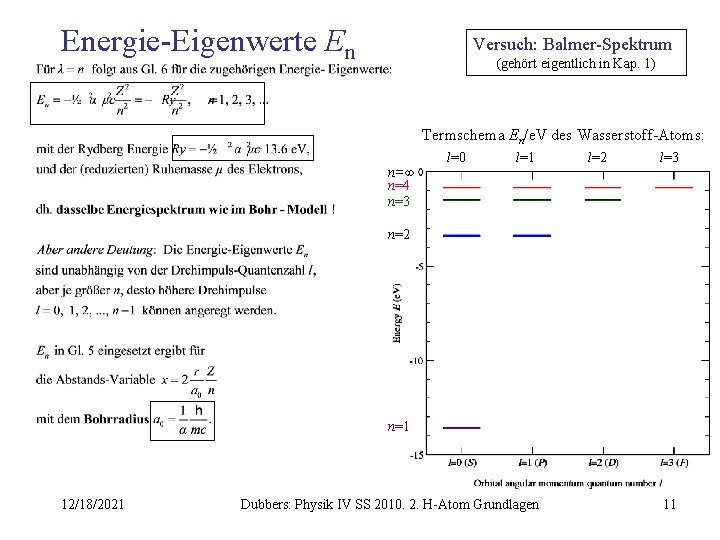
Energie-Eigenwerte En Versuch: Balmer-Spektrum (gehört eigentlich in Kap. 1) Termschema En/e. V des Wasserstoff-Atoms: n=∞ n=4 n=3 l=0 l=1 l=2 l=3 n=2 n=1 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 11

Radial-Wellenfunktionen Rnl(r) 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 12

Grundzustand n=1 des Wasserstoff-Atoms |Rnl|2 d. V 4πr 2|Rnl|2 dr Rnl(r) n = 1: r 2|Rnl|2(r) l = 0: 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 13

Erster angeregter Zustand n=2 des H-Atoms Rnl(r) n = 2: r 2|Rnl|2(r) l = 0: l = 1: 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 14

Zweiter angeregter Zustand n=3 des H-Atoms Rnl(r) n = 3: r 2|Rnl|2(r) l = 0: l = 1: l = 2: 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 15

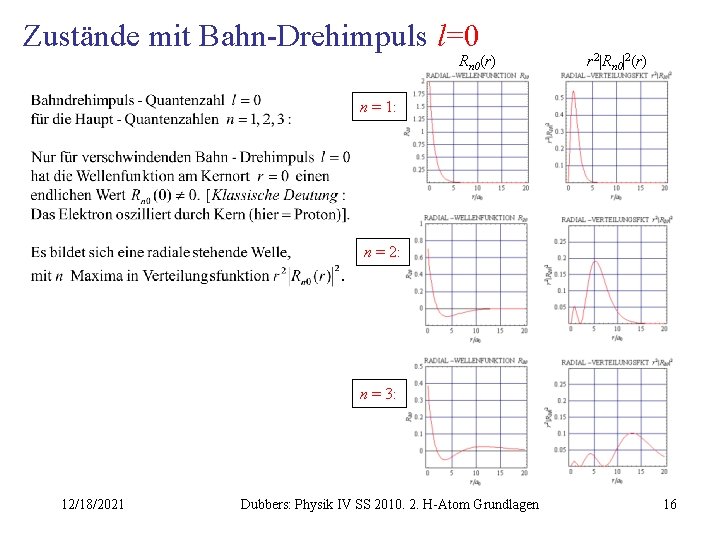
Zustände mit Bahn-Drehimpuls l=0 Rn 0(r) r 2|Rn 0|2(r) n = 1: n = 2: n = 3: 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 16

2. 3 Die Winkelabhängigkeit der Wellenfunktion P 10 = cos θ: z P 11 = sin θ: z θ sinθ θ + ←Thaleskreis 1 θ cosθ − 1 alles rotations-symmetrisch um z 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 17

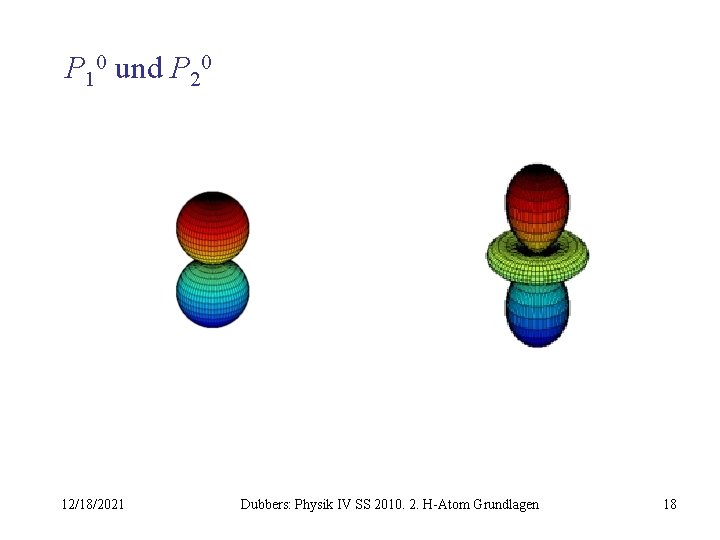
P 10 und P 20 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 18

Kugelflächen-Funktionen Ylm(θ, φ) 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 19

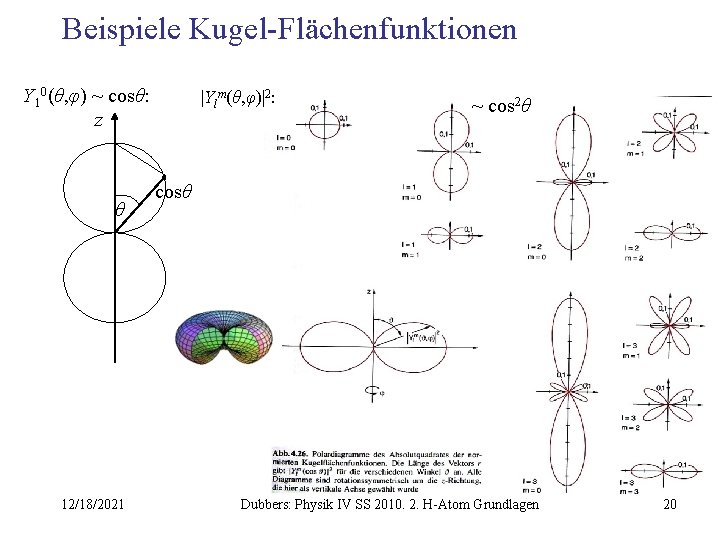
Beispiele Kugel-Flächenfunktionen Y 10(θ, φ) ~ cosθ: z θ 12/18/2021 |Ylm(θ, φ)|2: ~ cos 2θ cosθ Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 20

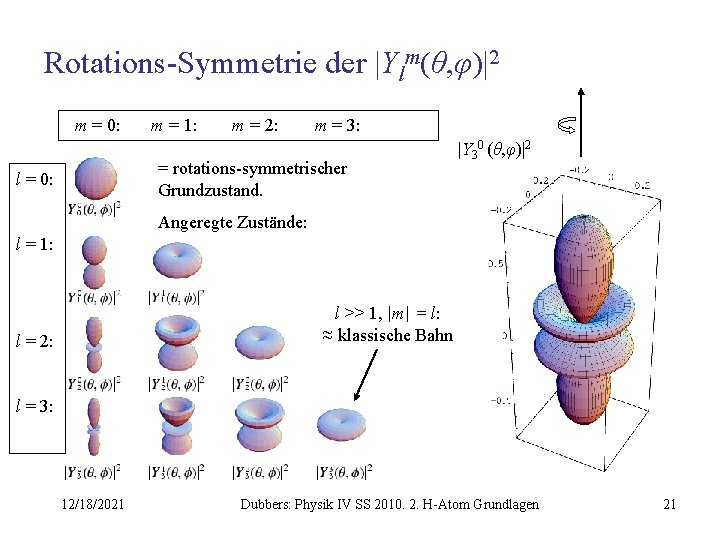
Rotations-Symmetrie der |Ylm(θ, φ)|2 m = 0: m = 1: m = 2: m = 3: = rotations-symmetrischer Grundzustand. l = 0: |Y 30 (θ, φ)|2 Angeregte Zustände: l = 1: l >> 1, |m| = l: ≈ klassische Bahn l = 2: l = 3: 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 21

Beispiel: n=7, 8 Orbitale 7 g 7 s andere Darstellungsweise: 7 f 7 p 7 d 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 22

Gesamt-Wellenfunktionen des H-Atoms ψ(r, θ, φ) = Rnl(r) Ylm(θ, φ): Grundzustand (E 1 = − 13. 6 e. V) 1. angeregter Zustand (E 2 = − 3. 4 e. V) 2. angeregter Zustand (E 3 = − 1. 5 e. V) 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 23

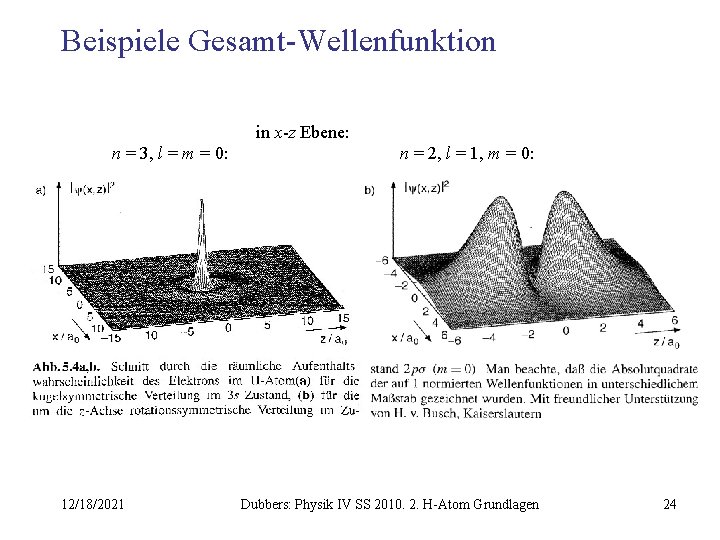
Beispiele Gesamt-Wellenfunktion in x-z Ebene: n = 3, l = m = 0: 12/18/2021 n = 2, l = 1, m = 0: Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 24

2. 4 Drehimpuls 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 25

Drehimpuls in Polar-Koordinaten 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 26

Messgrössen der Quantenmechanik 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 27

Richtungs-Quantelung des Drehimpulses 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 28

Elektronen-Spin 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 29

Gesamt-Drehimpuls j = 1/2: j = 3/2: s s j l l j = 0: s l 12/18/2021 j = 1: l j Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen s j j j = 2: s l j 30

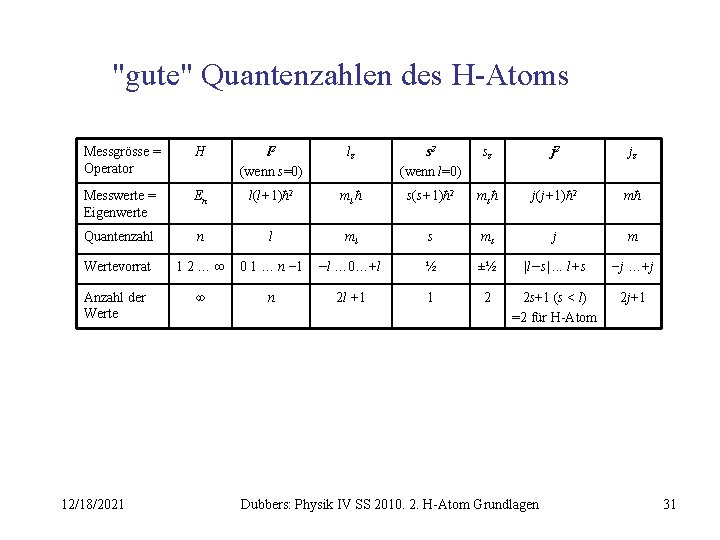
"gute" Quantenzahlen des H-Atoms Messgrösse = Operator H l 2 (wenn s=0) lz s 2 (wenn l=0) sz j 2 jz Messwerte = Eigenwerte En l(l+1)ħ 2 ml ħ s(s+1)ħ 2 ms ħ j(j+1)ħ 2 mħ Quantenzahl n l ml s ms j m Wertevorrat 12…∞ 0 1 … n − 1 −l … 0…+l ½ ±½ |l−s|. . . l+s −j …+j Anzahl der Werte ∞ n 2 l +1 1 2 2 s+1 (s < l) =2 für H-Atom 2 j+1 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 31

Nomenklatur Termschema En/e. V des Wasserstoff-Atoms: l=0 l=1 l=2 l=3 n=∞ 4 2 S 1/2 4 2 P 1/2, 3/2 4 2 D 3/2, 5/2 4 2 F 5/2, 7/2 n=4 n=3 3 2 S 1/2 3 2 P 1/2, 3/2 3 2 D 3/2, 5/2 n=2 2 2 S 1/2 2 2 P 1/2, 3/2 n=1 12/18/2021 1 2 S 1/2 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 32

Entartung der Energie-Niveaus 12/18/2021 Dubbers: Physik IV SS 2010. 2. H-Atom Grundlagen 33