2 EL NCLEO ATMICO TAMAO ATOMO 10 10

















- Slides: 46

2 EL NÚCLEO ATÓMICO

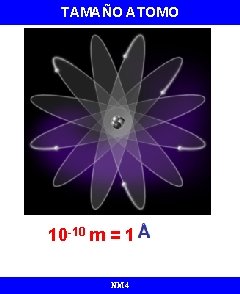
TAMAÑO ATOMO 10 -10 m = 1 NM 4

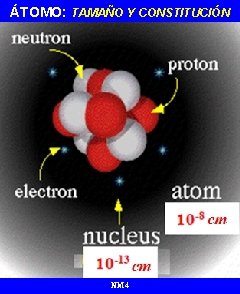
ÁTOMO: TAMAÑO Y CONSTITUCIÓN NM 4

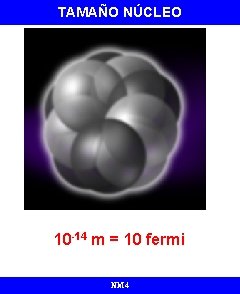
TAMAÑO NÚCLEO 10 -14 m = 10 fermi NM 4

TAMAÑO NUCLEÓN 10 -15 m = 1 fermi NM 4

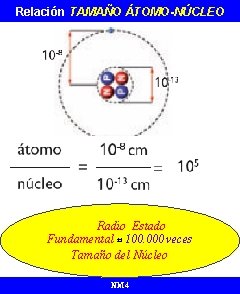
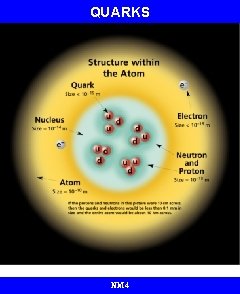
Relación TAMAÑO ÁTOMO-NÚCLEO Radio Estado Fundamental = 100. 000 veces Tamaño del Núcleo NM 4

DIMENSIONES ATÓMICAS

MASA PROTÓN / MASA ELECTRÓN LA MASA DEL PROTÓN ES 1836 VECES LA MASA DEL ELECTRÓN mp = 1836 me NM 4

NÚCLEO ATÓMICO CONSTITUIDO POR NUCLEONES: PROTONES (p+) Y NEUTRONES (n) Nº ATÓMICO (Z): Número de protones del Núcleo Nº MÁSICO (A): Nº de Protones + Nº de Neutrones 99, 97% DE LA MASA DEL ÁTOMO NM 4

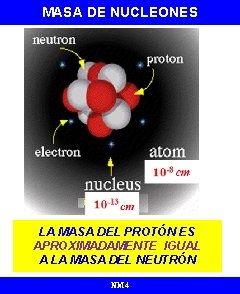
MASA DE NUCLEONES LA MASA DEL PROTÓN ES APROXIMADAMENTE IGUAL A LA MASA DEL NEUTRÓN NM 4

UNIDAD DE MASA ATÓMICA µ (uma) µ equivale a la doceava (1/12) parte de la masa de un átomo neutro de C-12 1 µ = 1. 660559 · 10− 27 kg Masa del Protón en reposo: Mp= 1, 0073 (µ) Masa del Neutrón: Mp= 1, 0087 (µ) Expresar la masa del Protón y del Neutrón en (kg). NM 4

NÚCLEO ATÓMICO: ISÓTOPOS Átomos con igual número Z pero diferente número A Los Elementos Químicos son una mezcla de diversos Isótopos en diferentes proporciones NM 4

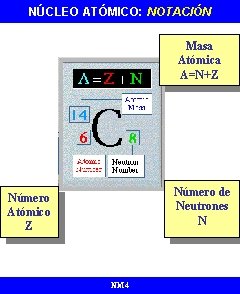
NÚCLEO ATÓMICO: NOTACIÓN Masa Atómica A=N+Z Número de Neutrones N Número Atómico Z NM 4

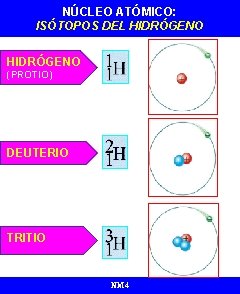
NÚCLEO ATÓMICO: ISÓTOPOS DEL HIDRÓGENO (PROTIO) DEUTERIO TRITIO NM 4

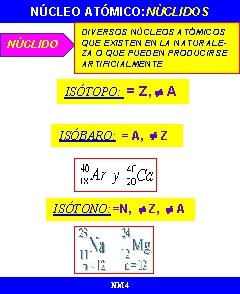
NÚCLEO ATÓMICO: NÙCLIDOS NÚCLIDO DIVERSOS NÚCLEOS ATÓMICOS QUE EXISTEN EN LA NATURALEZA O QUE PUEDEN PRODUCIRSE ARTIFICIALMENTE ISÓTOPO: = Z, A ISÓBARO: = A, Z ISÓTONO: =N, Z, A NM 4

TAMAÑO NÚCLEO ATÓMICO DEPENDE DEL NÚMERO DE NUCLEONES QUE LO CONSTITUYEN SU RADIO R SE PUEDE DETERMINAR POR LA EXPRESIÓN: EJEMPLO: RADIO NÚCLEO DEL CARBONO-14: R = 1, 2 x 10 -15 x (14)1/3 m = ? ? R = 1, 2 x 10 -15 x 2, 41 m = 2, 9 X 10 -15 m NM 4

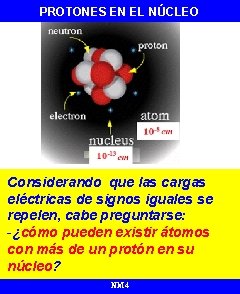
PROTONES EN EL NÚCLEO Considerando que las cargas eléctricas de signos iguales se repelen, cabe preguntarse: -¿cómo pueden existir átomos con más de un protón en su núcleo? NM 4

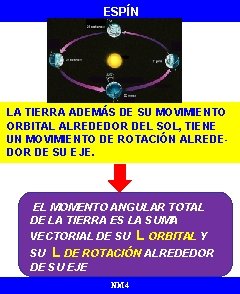
ESPÍN LA TIERRA ADEMÁS DE SU MOVIMIENTO ORBITAL ALREDEDOR DEL SOL, TIENE UN MOVIMIENTO DE ROTACIÓN ALREDEDOR DE SU EJE. EL MOMENTO ANGULAR TOTAL DE LA TIERRA ES LA SUMA VECTORIAL DE SU L ORBITAL Y SU L DE ROTACIÓN ALREDEDOR DE SU EJE NM 4

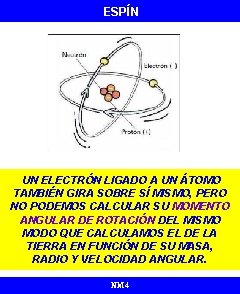
ESPÍN UN ELECTRÓN LIGADO A UN ÁTOMO TAMBIÉN GIRA SOBRE SÍ MISMO, PERO NO PODEMOS CALCULAR SU MOMENTO ANGULAR DE ROTACIÓN DEL MISMO MODO QUE CALCULAMOS EL DE LA TIERRA EN FUNCIÓN DE SU MASA, RADIO Y VELOCIDAD ANGULAR. NM 4

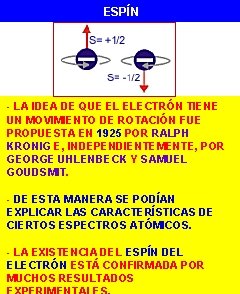
ESPÍN - LA IDEA DE QUE EL ELECTRÓN TIENE UN MOVIMIENTO DE ROTACIÓN FUE PROPUESTA EN 1925 POR RALPH KRONIG E, INDEPENDIENTEMENTE, POR GEORGE UHLENBECK Y SAMUEL GOUDSMIT. - DE ESTA MANERA SE PODÍAN EXPLICAR LAS CARACTERÍSTICAS DE CIERTOS ESPECTROS ATÓMICOS. - LA EXISTENCIA DEL ESPÍN DEL ELECTRÓN ESTÁ CONFIRMADA POR MUCHOS RESULTADOS NM 4

ESPÍN PROPIEDAD FÍSICA DE LA MATERIA, POR LA CUAL TODA PARTÍCULA ELEMENTAL TIENE UN MOMENTO ANGULAR INTRÍNSECO DE VALOR FIJO. -LA PARTÍCULA AL GIRAR SOBRE SU PROPIO EJE GENERA UN CAMPO MAGNÉTICO (ESPIN). -ES UN FENÓMENO EXCLUSIVAMENTE NM 4 CUÁNTICO

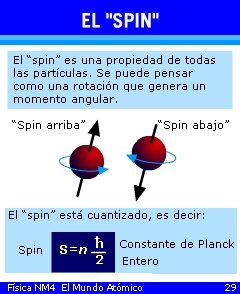
ESPÍN: CUALIDADES DIFERENCIAS CON EL L CLÁSICO: 1ª) EL VALOR DE ESPÍN ESTÁ CUANTIZADO: MÚLTIPLO ENTERO DE h/2 . 2ª) CUANDO SE REALIZA UNA MEDICIÓN DEL ESPÍN EN DIFERENTES DIRECCIONES, SÓLO EXISTEN DOS POSIBLES VALORES IGUALES Y DE SIGNO CONTRARIO, QUE SON SUS POSIBLES PROYECCIONES SOBRE UNA DIRECCIÓN PREDETERMINADA: +1/2 (h/2 ) O -1/2 (h/2 ) NM 4

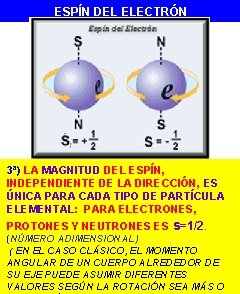
ESPÍN DEL ELECTRÓN 3ª) LA MAGNITUD DEL ESPÍN, INDEPENDIENTE DE LA DIRECCIÓN, ES ÚNICA PARA CADA TIPO DE PARTÍCULA ELEMENTAL: PARA ELECTRONES, PROTONES Y NEUTRONES ES s=1/2. (NÚMERO ADIMENSIONAL) ( EN EL CASO CLÁSICO, EL MOMENTO ANGULAR DE UN CUERPO ALREDEDOR DE SU EJE PUEDE ASUMIR DIFERENTES VALORES SEGÚN LA NM 4 ROTACIÓN SEA MÁS O


ESPÍN NUCLEAR SU VALOR DEPENDE DE A (Nº MÁSICO) DEL NÚCLEO: Ø SI A ES PAR: S = 0, 1, 2, 3, …. Ø SI A ES IMPAR: S = 1/2, 3/2, 5/2, …. ESTÁ ÍNTIMAMENTE RELACIONADO CON LA FORMA DE LOS NÚCLEOS: Ø SI S = 0 ó 1/2: NÚCLEO ESFÉRICO Ø SI S > 1/2: NÚCLEO DE FORMA ESFEROIDE NM 4

ESPÍN DE PARTÍCULAS ELEMENTALES CLASIFICACIÓN SEGÚN EL VALOR DEL ESPIN: DOS GRANDES GRUPOS: 1) FERMIONES: VALOR FRACCIONARIO (1/2; 3/2…) 2) BOSONES: VALOR ENTERO (0, 1, …) EL ESPÍN DE LAS PARTÍCULAS ESTÁ RELACIONADO CON EL CAMPO MAGNÉTICO: - PARTÍCULA CON ESPÍN s=0, NO POSEE CAMPO MAGNÉTICO. -PARTÍCULAS QUE NO POSEEN CARGA PUEDEN POSEER UN ESPÍN s 0 (EJ. EL NEUTRON) NM 4

PRINCIPIO CONSERVACIÓN DEL ESPÍN EN TODO PROCESO FÍSICO EL ESPÍN TOTAL DEL SISTEMA DEBE PERMANECER CONSTANTE - SI DOS PARTÍCULAS QUE ROTAN EN SENTIDOS OPUESTOS SE COMBINAN, LA PARTÍCULA RESULTANTE NO PUEDE ROTAR. - SI UNA PARTÍCULA QUE ROTA EN UN SENTIDO DADO SE DESCOMPONE EN OTRAS TRES, LA SUMA DE LOS ESPINES DE LAS TRES PARTÍCULAS RESULTANTES DEBEN DAR EL MISMO VALOR QUE AL PRINCIPIO. NM 4

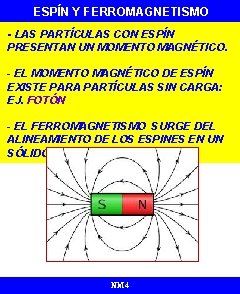
ESPÍN Y FERROMAGNETISMO - LAS PARTÍCULAS CON ESPÍN PRESENTAN UN MOMENTO MAGNÉTICO. - EL MOMENTO MAGNÉTICO DE ESPÍN EXISTE PARA PARTÍCULAS SIN CARGA: EJ. FOTÓN - EL FERROMAGNETISMO SURGE DEL ALINEAMIENTO DE LOS ESPINES EN UN SÓLIDO. NM 4

ESPÍN Y FERROMAGNETISMO EL FERROMAGNETISMO SURGE DEL ALINEAMIENTO DE LOS ESPINES EN UN SÓLIDO.

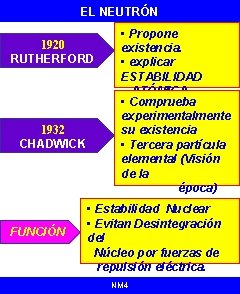
EL NEUTRÓN 1920 RUTHERFORD 1932 CHADWICK FUNCIÓN • Propone existencia. • explicar ESTABILIDAD ATÓMICA • Comprueba experimentalmente su existencia • Tercera partícula elemental (Visión de la época) • Estabilidad Nuclear • Evitan Desintegración del Núcleo por fuerzas de repulsión eléctrica. NM 4

EL NEUTRÓN: PROPIEDADES • RESIDE EN NÚCLEO ATÓMICO • MASA Y TAMAÑO SIMILAR AL PROTÓN • FUERA DEL NÚCLEO: INESTABLES • VIDA MEDIA: 15 MINUTOS • s= +1/2 y s = -1/2 DESINTEGRACIÓN NM 4 • 1 Protón + 1 Electrón + 1 Neutrino

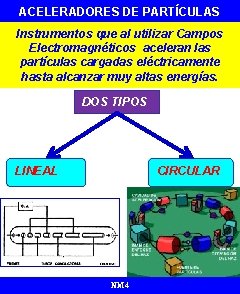
ACELERADORES DE PARTÍCULAS Instrumentos que al utilizar Campos Electromagnéticos aceleran las partículas cargadas eléctricamente hasta alcanzar muy altas energías. DOS TIPOS LINEAL CIRCULAR NM 4

ACELERADORES DE PARTÍCULAS Cuando las partículas han logrado gran energía cinética se les hace colisionar para que se fragmenten. DESCUBRIMIENTO DE NUEVAS PARTÍCULAS ELEMENTALES QUARKS NM 4

LOS QUARKS §DESCUBIERTOS EN 1963, POR MURRAY GELL-MANN Y GEORGE ZWEIG §SON CONSTITUYENTES FUNDAMENTALES DE LOS NUCLEONES. §VARIAS ESPECIES DE QUARKS SE COMBINAN DE MANERA ESPECÍFICA PARA FORMAR PROTONES Y NEUTRONES. NM 4

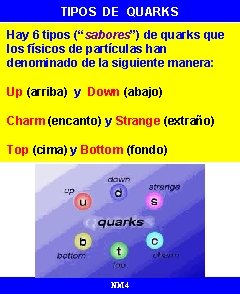
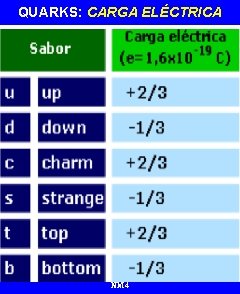
TIPOS DE QUARKS Hay 6 tipos (“sabores”) de quarks que los físicos de partículas han denominado de la siguiente manera: Up (arriba) y Down (abajo) Charm (encanto) y Strange (extraño) Top (cima) y Bottom (fondo) NM 4

QUARKS: PROPIEDADES - POSEEN CARGA ELÉCTRICA FRACCIONARIA: +2/3 ó -1/3 - EN LA NATURALEZA NO SE ENCUENTRAN AISLADOS: SIEMPRE AGRUPADOS EN HADRONES: -Mesones: grupo de 2 quarks -Bariones: grupo de 3 quarks. SON LAS ÚNICAS PARTÍCULAS ELEMENTALES QUE INTERACTÚAN CON LAS 4 FUERZAS FUNDAMENTALES NM 4

QUARKS: PROPIEDADES • ADEMÁS DEL “SABOR”, SE LES CLASIFICA SEGÚN EL “COLOR”, PROPIEDAD ENTENDIDA COMO OTRO NÚMERO CUÁNTICO: ROJO, VERDE y AZUL. • LA FUERZA DE ATRACCIÓN ENTRE ELLOS NO DISMINUYE CON LA DISTANCIA. • SI SE QUIEREN SEPARAR 2 QUARKS, SE INVIERTE CADA VEZ MÁS ENERGÍA, HASTA QUE SE FORMA UNA NUEVA PAREJA DE QUARKS. NM 4

QUARKS: CARGA ELÉCTRICA NM 4

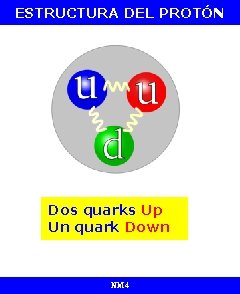
ESTRUCTURA DEL PROTÓN Dos quarks Up Un quark Down NM 4

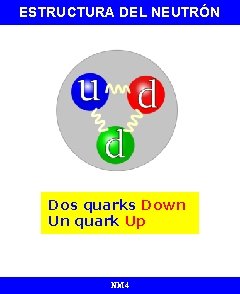
ESTRUCTURA DEL NEUTRÓN Dos quarks Down Un quark Up NM 4

QUARKS NM 4

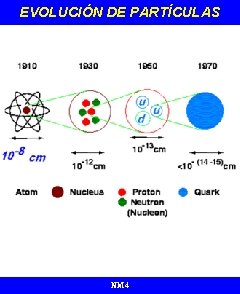
EVOLUCIÓN DE PARTÍCULAS NM 4

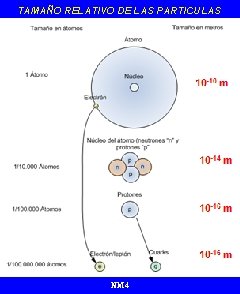
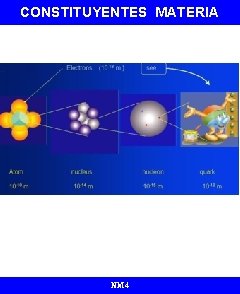
TAMAÑO RELATIVO DE LAS PARTICULAS NM 4

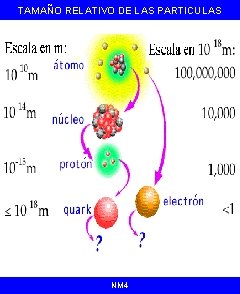
TAMAÑO RELATIVO DE LAS PARTICULAS NM 4

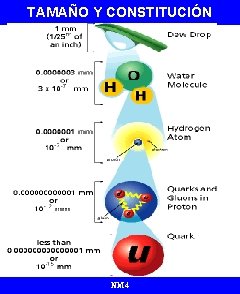
TAMAÑO Y CONSTITUCIÓN NM 4

CONSTITUYENTES MATERIA NM 4