2 Aufbau der Materie Erde Luft Feuer Wasser

2. Aufbau der Materie Erde … Luft… Feuer Wasser… Kapitel 2 Aufbau der Materie

Richard P. Feynman 1918 – 1988 1965 Nobelpreis “Alle Körper sind aus Atomen aufgebaut, aus kleinen, sich ständig bewegenden Teilchen. Wenn Atome einander zu nahe kommen, wirken zwischen ihnen abstoßende Kräfte. Entfernen sie sich etwas voneinander, so treten anziehende Kräfte auf. ” Kapitel 2 Aufbau der Materie

Demokrit aus Abdera um 460 – um 370 v. Chr. “Nichts existiert als die Atome und der leere Raum. ” Kapitel 2 Aufbau der Materie

• Historisch: Streit: Kontinuum Kleinste Teilchen. • Demokrit, 5. Jh. v. Chr. : Es gibt Atome (atomos=unteilbar) Er hatte ein mechanistisches Modell. Atome müssen ausgedehnt und unteilbar sein. • Aristoteles sah darin einen Widerspruch. • Zu Beginn des 19. Jh. waren die chem. Untersuchungsmethoden soweit gediehen, dass sich quantitative Messungen durchführen ließen. Kapitel 2 Aufbau der Materie
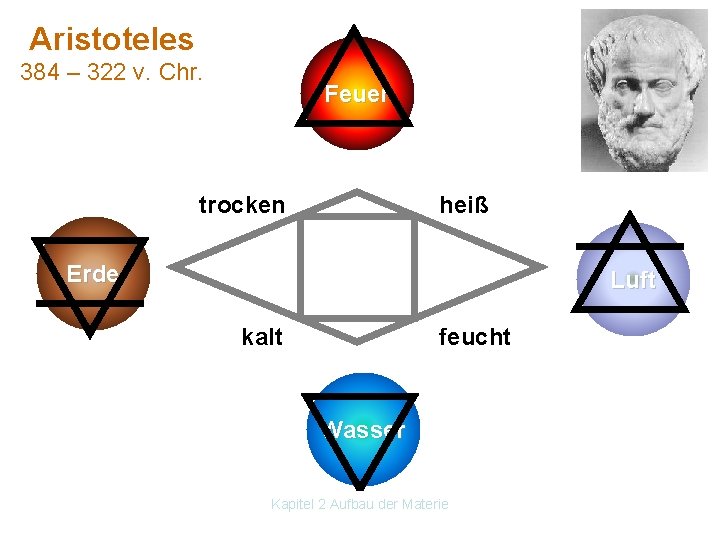
Aristoteles 384 – 322 v. Chr. Feuer trocken heiß Erde Luft kalt feucht Wasser Kapitel 2 Aufbau der Materie

John Dalton 1766 – 1844 Gesetz von der Erhaltung der Masse: Bei chemischen Reaktionen bleibt die Gesamtmasse der Reaktionsteilnehmer unverändert. Gesetz der konstanten Proportionen: In einer chemischen Verbindung sind die einzelnen Bestandteile stets in einem bestimmten, charakteristischen Massenverhältnis enthalten. Gesetz der multiplen Proportionen: Können zwei Bestandteile mehrere chemische Verbindungen bilden, so stehen die Mengen des einen Bestandteils, welche sich mit ein und derselben Menge des anderen Bestandteils verbinden können, im Verhältnis ganzer Zahlen. Kapitel 2 Aufbau der Materie

Zum Gesetz der konstanten Proportionen z. B. 2 g H 2 + 16 g ½O 2 → 18 g H 2 O Zum Gesetz der multiplen Proportionen: z. B. 63, 54 g. Cu + 16 g. O → 79, 54 g Cu. O (Kupfer II – Oxid) 127, 08 g. Cu + 16 g O → 143, 08 g Cu 2 O (Kupfer I – Oxid) John Dalton (1766 1844) sah in diesen Gesetzen den Beweis für den atomaren Aufbau der Materie. Atome verbinden sich zu Gruppen mit einheitlicher Struktur. → Verbindungen. Kapitel 2 Aufbau der Materie
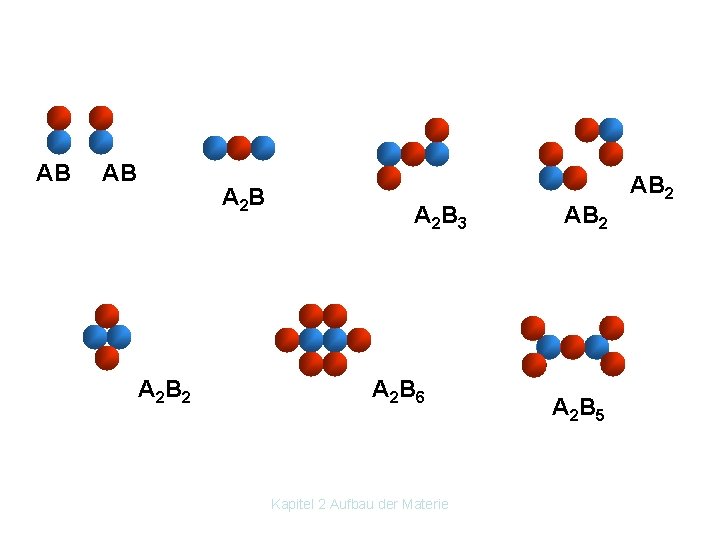
AB AB A 2 B 2 A 2 B 3 A 2 B 6 Kapitel 2 Aufbau der Materie AB 2 A 2 B 5 AB 2

Joseph John Thomson 1856 – 1940 „verschmierte“ positive Ladung enthält Elektronen „Rosinenkuchenmodell“ Rutherford: Beschuss mit Teilchen Erwartung: „leichte“ Ablenkung durch die Elektronen Kapitel 2 Aufbau der Materie
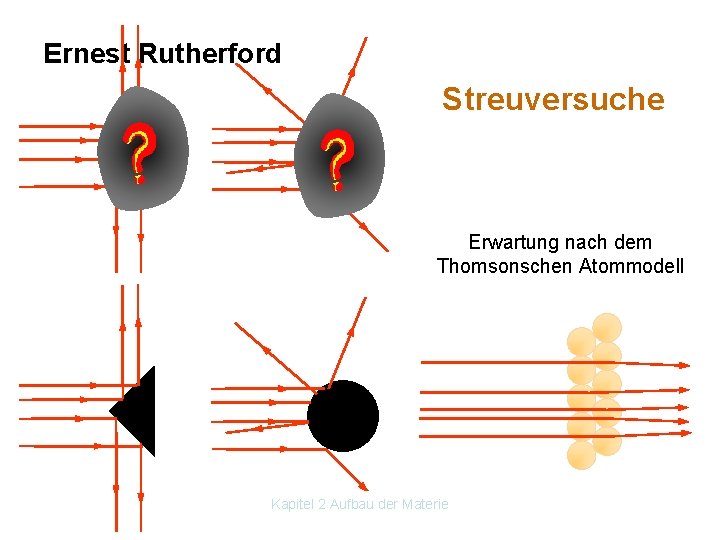
Ernest Rutherford Streuversuche Erwartung nach dem Thomsonschen Atommodell Kapitel 2 Aufbau der Materie
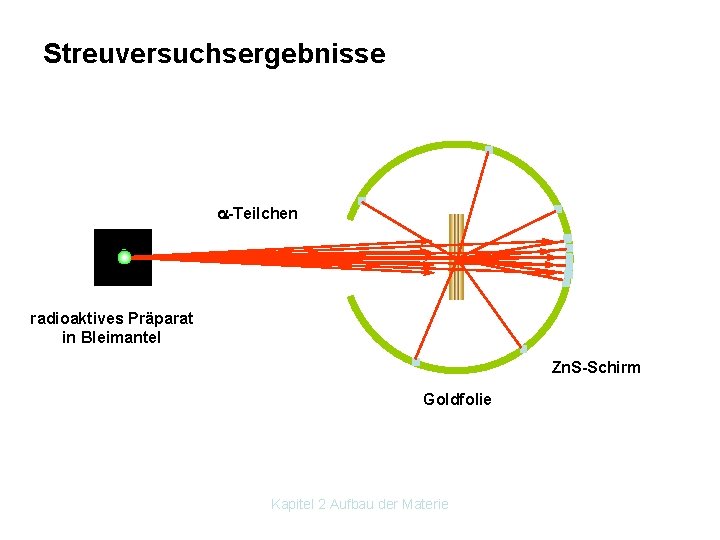
Streuversuchsergebnisse -Teilchen radioaktives Präparat in Bleimantel Zn. S-Schirm Goldfolie Kapitel 2 Aufbau der Materie

Rutherford - Atommodell Ernest Rutherford 1911 Kapitel 2 Aufbau der Materie
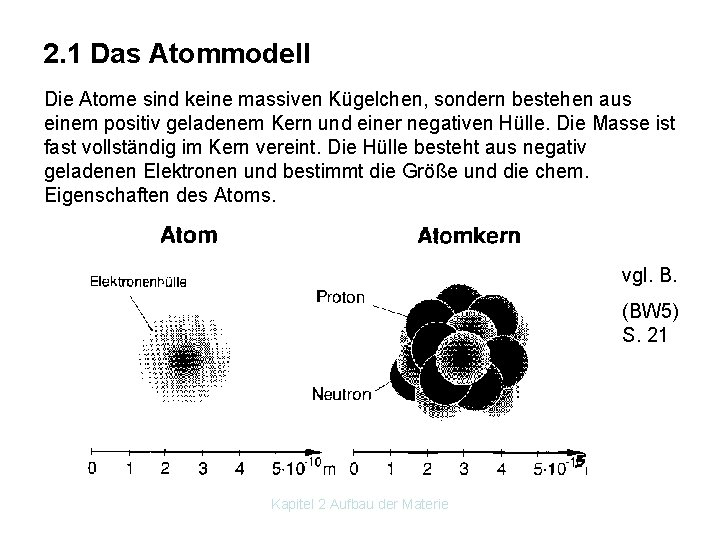
2. 1 Das Atommodell Die Atome sind keine massiven Kügelchen, sondern bestehen aus einem positiv geladenem Kern und einer negativen Hülle. Die Masse ist fast vollständig im Kern vereint. Die Hülle besteht aus negativ geladenen Elektronen und bestimmt die Größe und die chem. Eigenschaften des Atoms. vgl. B. (BW 5) S. 21 Kapitel 2 Aufbau der Materie

Protonen (p+) und Neutronen (n) nennen wir Nukleonen Z. . . Ordnungszahl = Anzahl der p Die Atome sind meist neutral. Daher Anzahl p+ = Anzahl der e Hat ein Atom ein oder mehrere e zuwenig oder zuviel. → ION. Kapitel 2 Aufbau der Materie

2. 2 Begriffe: Relative Molekularmasse ist Summe der relativen Atommassen, diese Verbindung aufbauen. Beispiel: 1 + 16 = 18 Atomare Masseneinheit: 1 u = 1 u mp mn 1 u = 1, 6605402(10) · 10 27 kg Kapitel 2 Aufbau der Materie Atoms

Größe der Atome: Größe des Kerns: d 10 10 bis 5. 10 10 m d 10 15 bis 5. 10 15 m Massenzahl = Protonenzahl + Neutronenzahl A = Z + N ( Nukleonenzahl) Kapitel 2 Aufbau der Materie
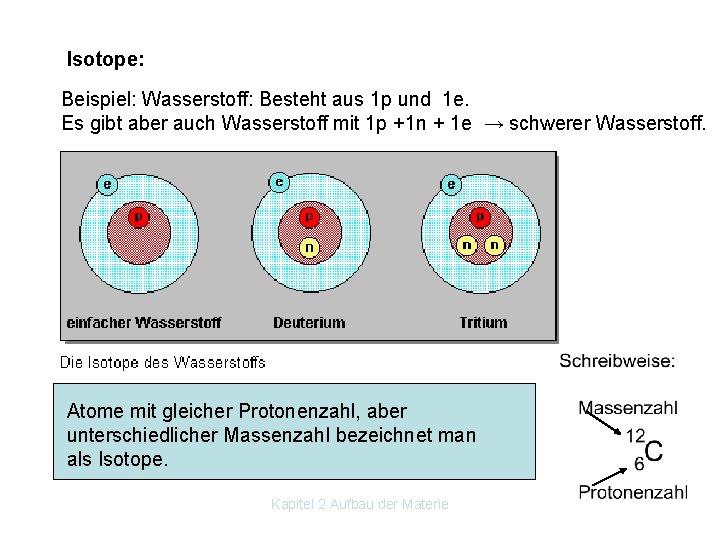
Isotope: Beispiel: Wasserstoff: Besteht aus 1 p und 1 e. Es gibt aber auch Wasserstoff mit 1 p +1 n + 1 e → schwerer Wasserstoff. Atome mit gleicher Protonenzahl, aber unterschiedlicher Massenzahl bezeichnet man als Isotope. Kapitel 2 Aufbau der Materie

Vgl. B. (BW 5) Seite 25 Die Isotope sind in sogenannten Isotopentafeln aufgeschrieben. Kapitel 2 Aufbau der Materie

Mol – Einheit der Stoffmenge n 1 Mol ist gleich der Stoffmenge, eines Systems, das aus ebenso vielen Teilchen besteht, wie Atome in 12 g des Nuklids C 12 enthalten sind. 1 Mol enthält stets NA = 6, 0221367(36). 1023 mol 1 Teilchen NA … Avogadro Konstante oder Lohschmidtsche Zahl Kapitel 2 Aufbau der Materie

Übungen: B. S. 27 , Aufgaben 1, 2, 5, 6 Kapitel 2 Aufbau der Materie

2. 3 Das Periodensystem der Elemente Ordnungszahl als Ordnungsprinzip Perioden: Anzahl der Schalen (Zeilen) Hauptgruppen: Anzahl der e in der äußersten Schale. (Spalten) vgl. B. (BW 5) S. 104 Kapitel 2 Aufbau der Materie

Aufbau der Atome Kapitel 2 Aufbau der Materie

Ernest Rutherford Atomkern Atomhülle Niels Bohr bestimmte Kapitel 2 Aufbau der Materie Bahnen Erwin Schrödinger
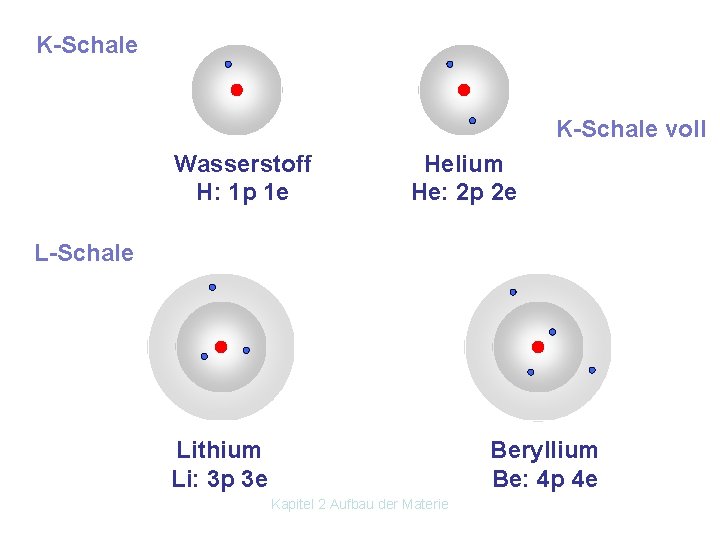
K-Schale voll Wasserstoff H: 1 p 1 e Helium He: 2 p 2 e L-Schale Lithium Li: 3 p 3 e Beryllium Be: 4 p 4 e Kapitel 2 Aufbau der Materie
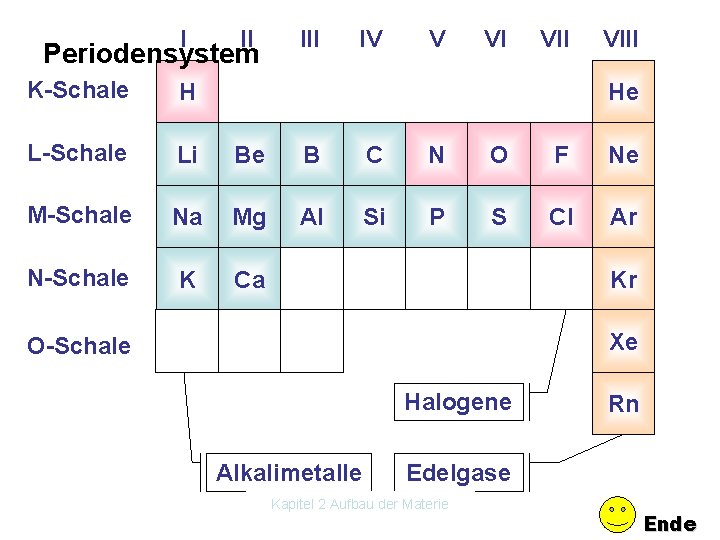
I III IV V VI VIII Periodensystem K-Schale H L-Schale Li Be B C N O F Ne M-Schale Na Mg Al Si P S Cl Ar N-Schale K Ca He Kr Xe O-Schale Halogene Alkalimetalle Rn Edelgase Kapitel 2 Aufbau der Materie Ende

Kapitel 2 Aufbau der Materie
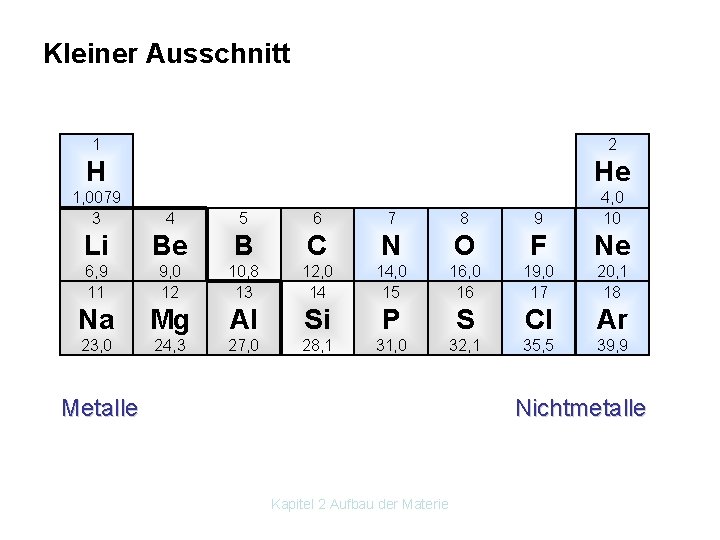
Kleiner Ausschnitt 1 2 H He 1, 0079 3 4 5 6 7 8 9 4, 0 10 Li Be B C N O F Ne 6, 9 11 9, 0 12 10, 8 13 12, 0 14 14, 0 15 16, 0 16 19, 0 17 20, 1 18 Na Mg Al Si P S Cl Ar 23, 0 24, 3 27, 0 28, 1 31, 0 32, 1 35, 5 39, 9 Metalle Nichtmetalle Kapitel 2 Aufbau der Materie
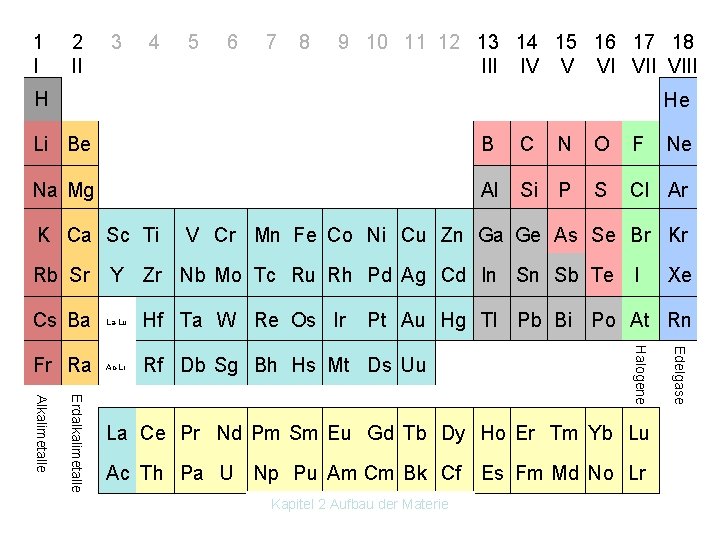
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 I II III IV V VII VIII H He Li Be Na Mg K Ca Sc Ti B C N O F Ne Al Si P S Cl Ar V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Cs Ba La Lu Hf Ta W Re Os Ir Fr Ra Ac Lr Rf Db Sg Bh Hs Mt Ds Uu Pt Au Hg Tl Pb Bi Po At Rn U Np Pu Am Cm Bk Cf Es Fm Md No Lr Ac Th Pa U Kapitel 2 Aufbau der Materie Edelgase Halogene Erdalkalimetalle Alkalimetalle La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu Xe
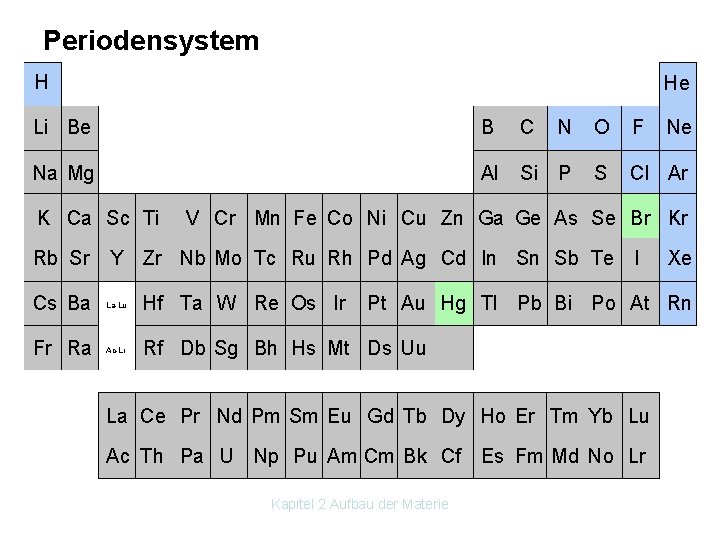
Periodensystem H He Li Be Na Mg K Ca Sc Ti B C N O F Ne Al Si P S Cl Ar V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Cs Ba La Lu Hf Ta W Re Os Ir Fr Ra Ac Lr Rf Db Sg Bh Hs Mt Ds Uu Pt Au Hg Tl Pb Bi Po At Rn La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu U Np Pu Am Cm Bk Cf Es Fm Md No Lr Ac Th Pa U Kapitel 2 Aufbau der Materie Xe

Unter Alltagsbedingungen sind Li Be 11 Elemente gasförmig (H, N, O, F, Cl und die Edelgase He, Ne, Ar, Kr, Xe, Rn), B C N O F Ne Na Mg 2 Elemente flüssig (Br, Hg). Al Si H K Ca Sc Ti He P S Cl Ar V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Cs Ba La Lu Hf Ta W Re Os Ir Fr Ra Ac Lr Rf Db Sg Bh Hs Mt Ds Uu Pt Au Hg Tl Pb Bi Po At Rn La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu U Np Pu Am Cm Bk Cf Es Fm Md No Lr Ac Th Pa U Kapitel 2 Aufbau der Materie Periodensystem der Elemente Xe

2. 4 Bindungsarten Erarbeite aus dem Buch S. 24 die 3 Bindungsarten! Metallbindung Ionenbindung Atombindung Aufgaben 2 und 3 B (BW 5) S. 24 Lösungen: A 2: Metallbindung: gute el. und Wärmeleitfähigkeit, Verformbarkeit Ionenbindung: schlechte Leitfähigkeit, spröde, in Wasser löslich dann leitfähig Atombindung: schlechte Leiter, sehr häufig in Form von Kristallen meist hart A 3: NH 3. . . Atombindung Na 2 O. . . Ionenbindung Kapitel 2 Aufbau der Materie
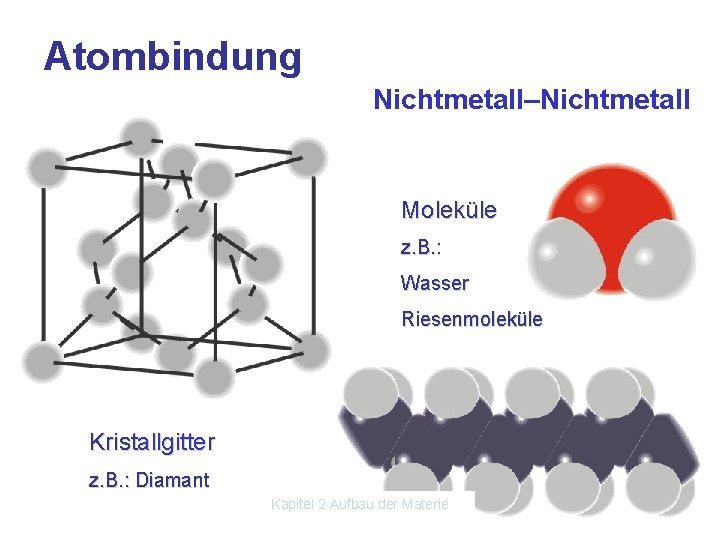
Atombindung Nichtmetall–Nichtmetall Moleküle z. B. : Wasser Riesenmoleküle Kristallgitter z. B. : Diamant Kapitel 2 Aufbau der Materie
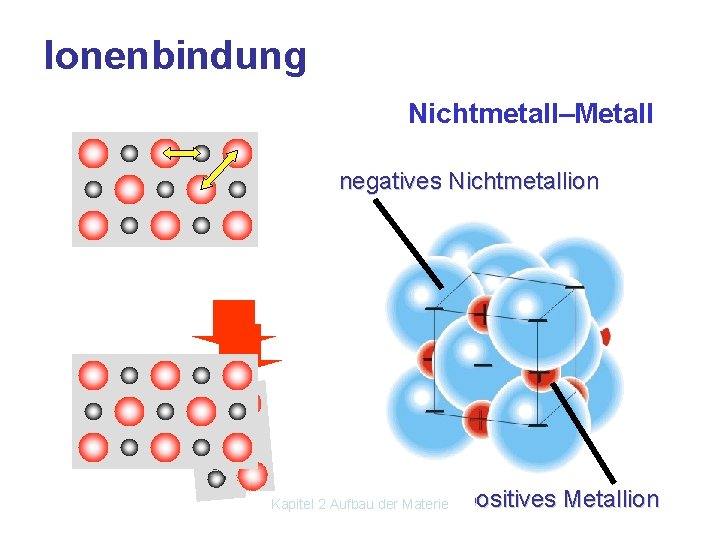
Ionenbindung Nichtmetall–Metall negatives Nichtmetallion Kapitel 2 Aufbau der Materie positives Metallion
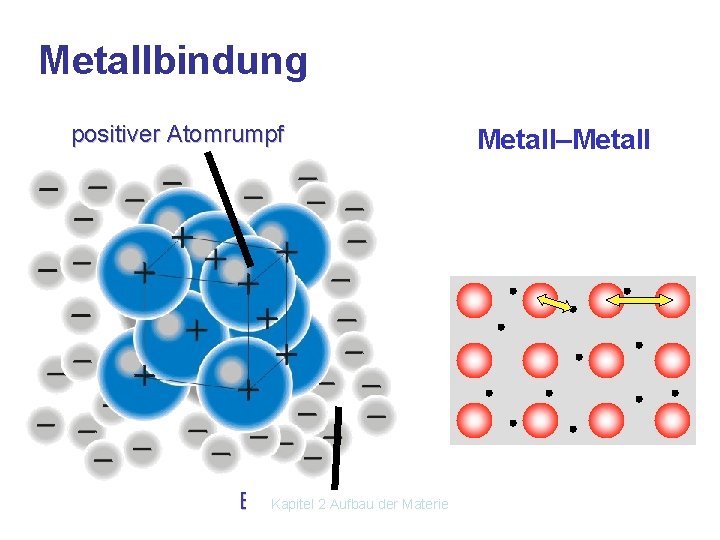
Metallbindung positiver Atomrumpf Kapitel 2 Aufbau der Materie Elektronengas Metall–Metall
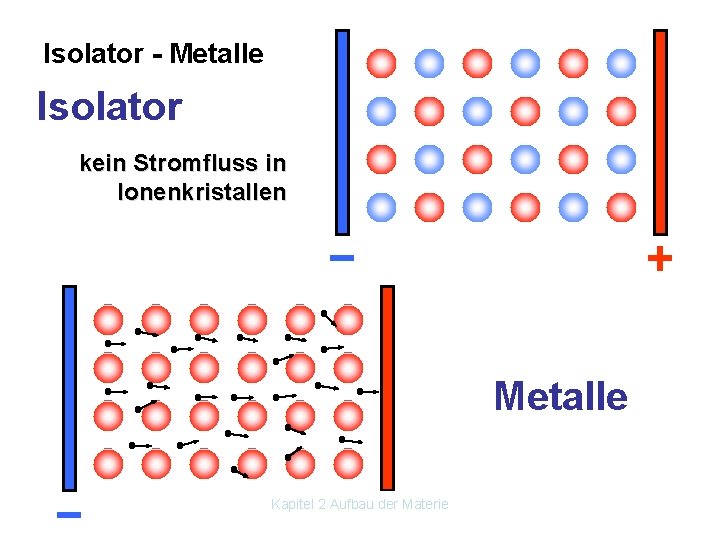
Isolator - Metalle Isolator kein Stromfluss in Ionenkristallen Metalle Kapitel 2 Aufbau der Materie
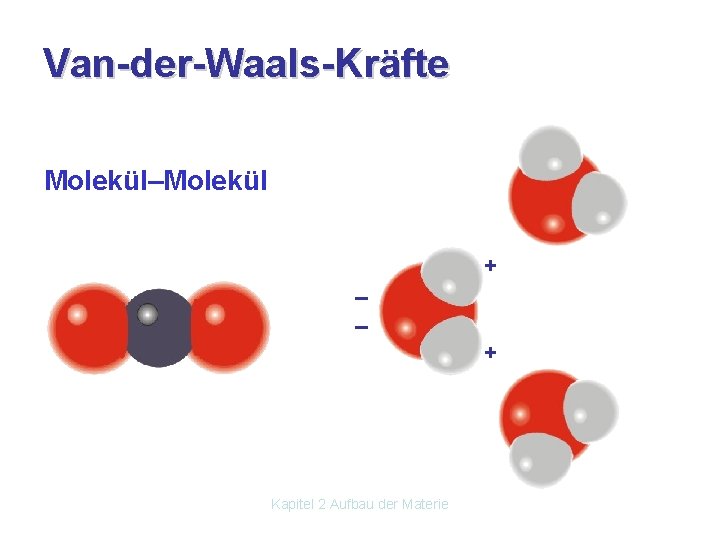
Van-der-Waals-Kräfte Molekül–Molekül + – – Kapitel 2 Aufbau der Materie +

Schneekristalle Kapitel 2 Aufbau der Materie

Kapitel 2 Aufbau der Materie

2. 5 Stabile und instabile Kerne - Radioaktivität • Die Bindung von e an den Atomkern kann durch das Wirken der elektrischen Kräfte erklärt werden. el. WW • Zwischen den Nukleonen wirken die Kernkräfte (Starke WW). Diese haben nur eine geringe Reichweite (10 15 m) (Kräfte zwischen den Quarks). • verschiedene Atome können ohne äußere Einwirkung Teilchen aussenden. Radioaktivität. • Sie wurde 1896 von Henri Becquerel zufällig entdeckt. Ein Urankristall in der Nähe einer Fotoplatte schwärzte diese. Becquerel erhielt zusammen mit M. Curie und Pierre Curie 1903 den Nobelpreis für Physik. • Madame Curie wies 1898 nach, dass es sich dabei um und in der Uranerzblende handelte. • Die Aktivität eines radioaktiven Stoffes wird in Becquerel angegeben. Kapitel 2 Aufbau der Materie
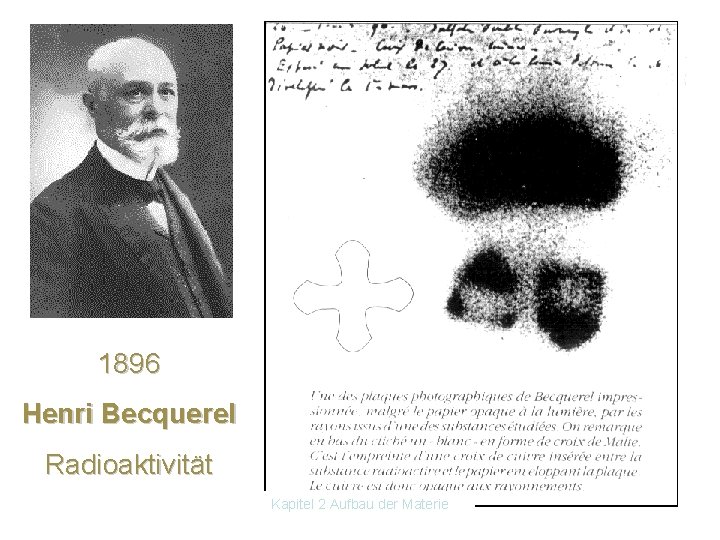
1896 Henri Becquerel Radioaktivität Kapitel 2 Aufbau der Materie

1898 Marie und Pierre Curie Polonium 84 Po Radium 88 Ra Kapitel 2 Aufbau der Materie

Viktor Franz Hess (1883 – 1964) Kapitel 2 Aufbau der Materie

Einheit für den radioaktiven Zerfall • 1 Becquerel = 1 Zerfall pro Sekunde (1 Bq = 1 s 1 ) • alte Einheit: 1 Curie = 3, 7∙ 1010 Bq (1 Ci) • 1 Ci entspricht der Aktivität von 1 g Radium Führe Aufgabe A 1 auf Seite 29 aus! Kapitel 2 Aufbau der Materie
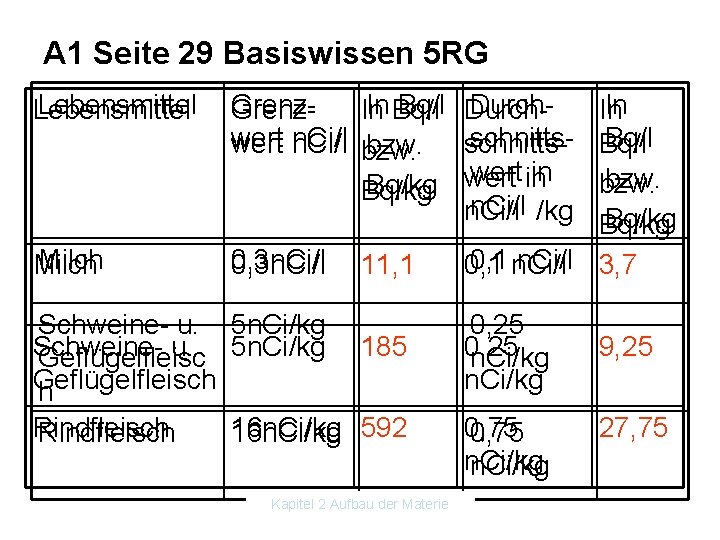
A 1 Seite 29 Basiswissen 5 RG Lebensmittel Grenz wert n. Ci/l In Bq/l bzw. Bq/kg Milch 0, 3 n. Ci/l 11, 1 Schweine u. Geflügelfleisch h Rindfleisch 5 n. Ci/kg 185 16 n. Ci/kg 592 Kapitel 2 Aufbau der Materie Durch schnitts wert in n. Ci/l /kg In In Bq/l bzw. Bq/kg 0, 1 n. Ci/l 3, 7 0, 1 n. Ci/l 0, 25 n. Ci/kg 0, 75 n. Ci/kg 9, 25 27, 75
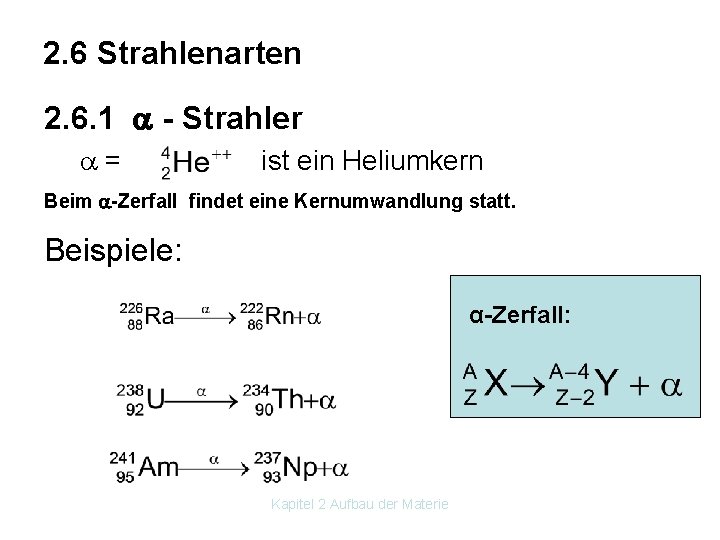
2. 6 Strahlenarten 2. 6. 1 - Strahler = ist ein Heliumkern Beim -Zerfall findet eine Kernumwandlung statt. Beispiele: α-Zerfall: Kapitel 2 Aufbau der Materie
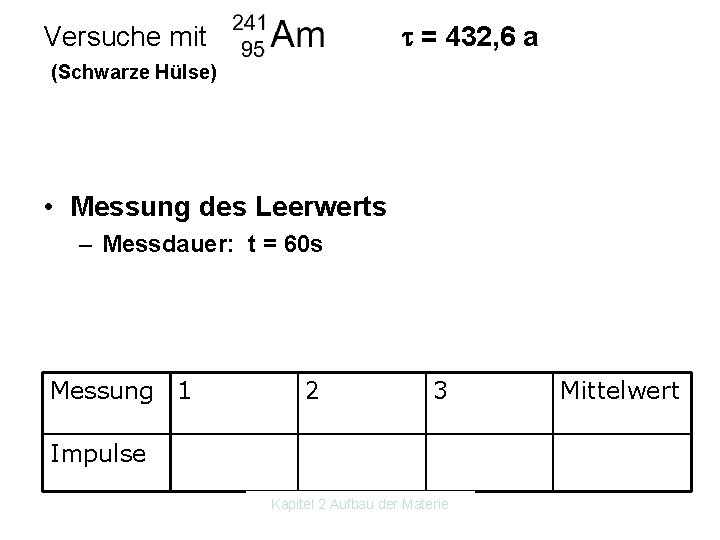
Versuche mit = 432, 6 a (Schwarze Hülse) • Messung des Leerwerts – Messdauer: t = 60 s Messung 1 2 3 Impulse Kapitel 2 Aufbau der Materie Mittelwert
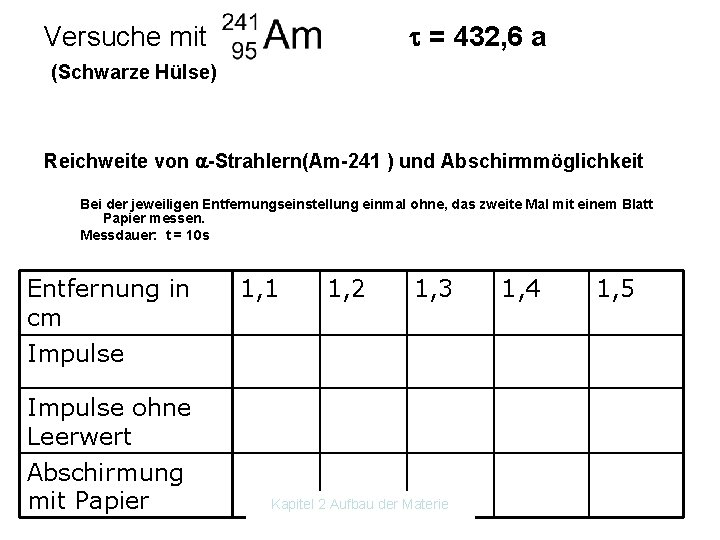
Versuche mit = 432, 6 a (Schwarze Hülse) Reichweite von -Strahlern(Am-241 ) und Abschirmmöglichkeit Bei der jeweiligen Entfernungseinstellung einmal ohne, das zweite Mal mit einem Blatt Papier messen. Messdauer: t = 10 s Entfernung in cm 1, 1 1, 2 1, 3 Impulse ohne Leerwert Abschirmung mit Papier Kapitel 2 Aufbau der Materie 1, 4 1, 5

Versuche mit = 432, 6 a (Schwarze Hülse) Ergebnis: • Die Reichweite ist sehr gering. In Luft einige cm. - Strahlen können bereits mit einem Blatt Papier abgeschirmt werden. • Sie sind trotzdem sehr gefährlich, weil sie stark ionisierend wirken. • Bemerkung: Die noch auftretende Reststrahlung rührt von der Strahlung her. Kapitel 2 Aufbau der Materie

2. 6. 2 ß--Strahler (grüne Hülse) HWZ: 10, 76 a /(4, 48 h). . . . Antineutrino, entsteht infolge der schwachen Wechselwirkung. Reichweite von ß--Strahlern: Messdauer: t = 10 s Entfernung in cm 5 10 20 Impulse ohne Leerwert Kapitel 2 Aufbau der Materie 30 50

Reichweite von ß Strahlern: Ergebnis: Noch in 50 cm haben wir erhöhte Strahlung, die Reichweite der ß- - Strahler beträgt etwa 2 m - 3 m. Kapitel 2 Aufbau der Materie
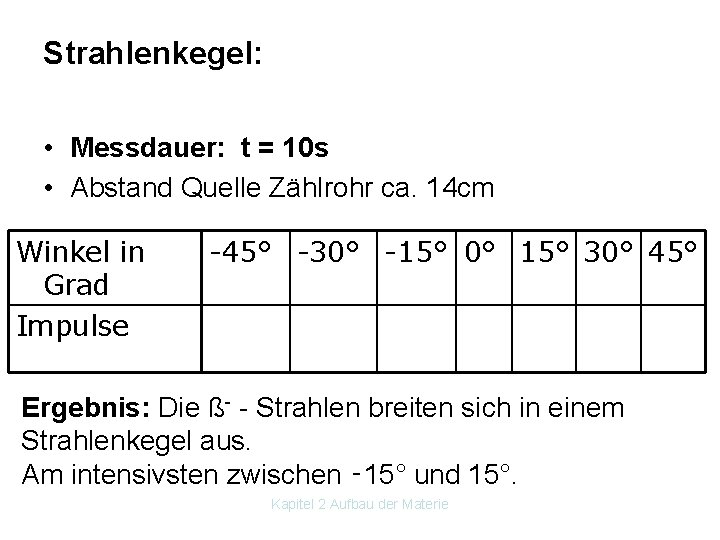
Strahlenkegel: • Messdauer: t = 10 s • Abstand Quelle Zählrohr ca. 14 cm Winkel in Grad Impulse -45° -30° -15° 0° 15° 30° 45° Ergebnis: Die ß Strahlen breiten sich in einem Strahlenkegel aus. Am intensivsten zwischen ‑ 15° und 15°. Kapitel 2 Aufbau der Materie
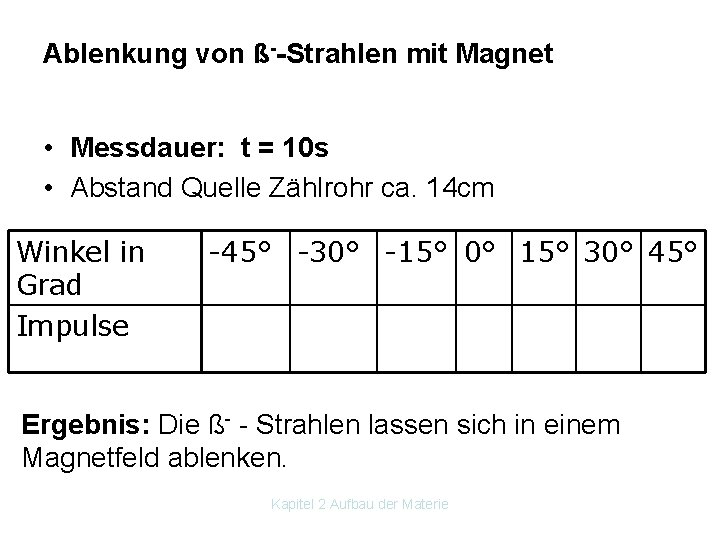
Ablenkung von ß--Strahlen mit Magnet • Messdauer: t = 10 s • Abstand Quelle Zählrohr ca. 14 cm Winkel in Grad Impulse -45° -30° -15° 0° 15° 30° 45° Ergebnis: Die ß Strahlen lassen sich in einem Magnetfeld ablenken. Kapitel 2 Aufbau der Materie
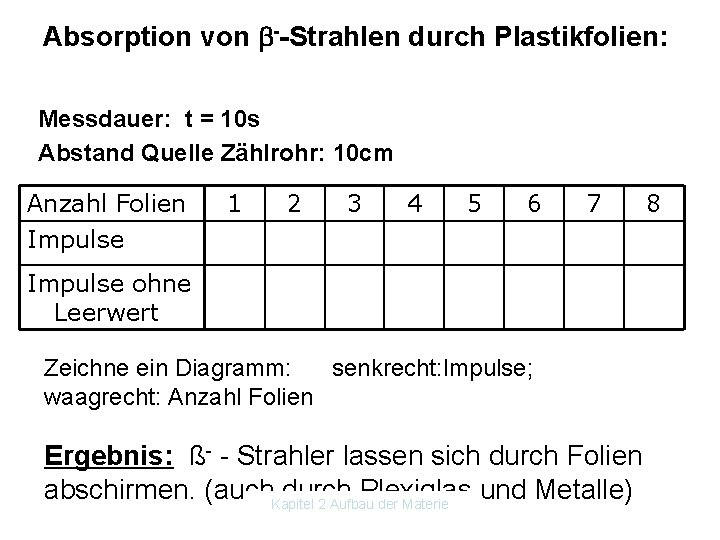
Absorption von --Strahlen durch Plastikfolien: Messdauer: t = 10 s Abstand Quelle Zählrohr: 10 cm Anzahl Folien Impulse 1 2 3 4 5 6 7 8 Impulse ohne Leerwert Zeichne ein Diagramm: senkrecht: Impulse; waagrecht: Anzahl Folien Ergebnis: ß Strahler lassen sich durch Folien abschirmen. (auch durch Plexiglas und Metalle) Kapitel 2 Aufbau der Materie

2. 6. 3 -Strahlen • Ihre Strahlung ist ähnlich dem Licht , aber nicht sichtbar und viel durchdringender. • Ihre Aussendung erfolgt in Form von "Energieportionen" "Quanten". • Beispiele: Kapitel 2 Aufbau der Materie

Absorption von -Strahlen durch Bleiplatten: • Messdauer: t = 10 s • Abstand Quelle Zählrohr: 5 cm Schichtdicke Pb [mm] 0 2 4 6 8 10 12 14 16 18 20 Impulse Diagramm: senkrecht: Impulse; waagrecht: Schichtdicke von Blei Ermittle die Halbwertsdicke: (Dicke, bei der die Strahlung auf die Hälfte des Wertes abgesunken ist. ) Kapitel 2 Aufbau der Materie

Absorption von -Strahlen durch Bleiplatten: • Messdauer: t = 10 s • Abstand Quelle Zählrohr: 5 cm Schichtdicke Pb [mm] 0 2 4 6 8 10 12 14 16 18 20 Impulse 99 92 75 68 64 52 49 42 41 32 32 Diagramm: senkrecht: Impulse; waagrecht: Schichtdicke von Blei Ermittle die Halbwertsdicke: (Dicke, bei der die Strahlung auf die Hälfte des Wertes abgesunken ist. ) Kapitel 2 Aufbau der Materie
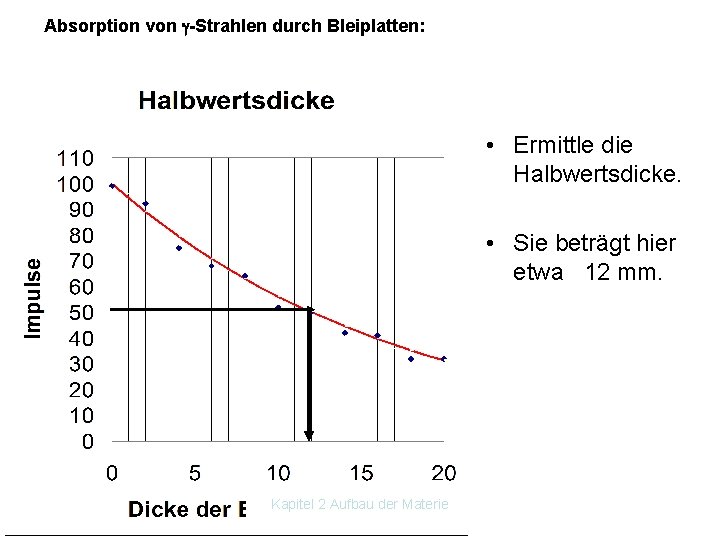
Absorption von -Strahlen durch Bleiplatten: • Ermittle die Halbwertsdicke. • Sie beträgt hier etwa 12 mm. Kapitel 2 Aufbau der Materie

Absorption von -Strahlen durch Bleiplatten: Ergebnis: Die Halbwertsdicke bei Co 60 beträgt ca. …. . mm. Folgerung: Die Strahlen sind aufgrund ihrer großen Durchdringungsfähigkeit und ihrer großen Reichweite sehr gefährlich, da sie auch schwer abschirmbar sind. Die Intensität der Strahlung (Dosisleistung), sinkt mit dem Quadrat der Entfernung von der Quelle. Kapitel 2 Aufbau der Materie

Der radioaktive Ballon Versuch: Ein Ballon (nicht aufgeblasen) wird unter einen Geigerzähler gelegt. Ergebnis 1: Die Impulsanzahl entspricht etwa früheren Messungen des Leerwerts. Der Luftballon wird aufgeblasen und durch Reiben an Schafwolle oder fettfreiem Kopfhaar elektrisch ge laden. Anschließend wird er so aufgehängt, dass er sich nicht durch Kontakt mit leitenden Objekten entladen kann. Ergebnis 2: Nach einiger Zeit (10 Minuten bis 2 Stunden) wird der Ballon ausgelassen. Mit dem Geigerzähler lässt sich jetzt eine wesentlich über der Leerrate liegende Aktivität auf der Ballonhaut nachweisen. Das elektrische Feld ließ Ionen der Tochterprodukte des Radon zum Ballon wandern. Kapitel 2 Aufbau der Materie
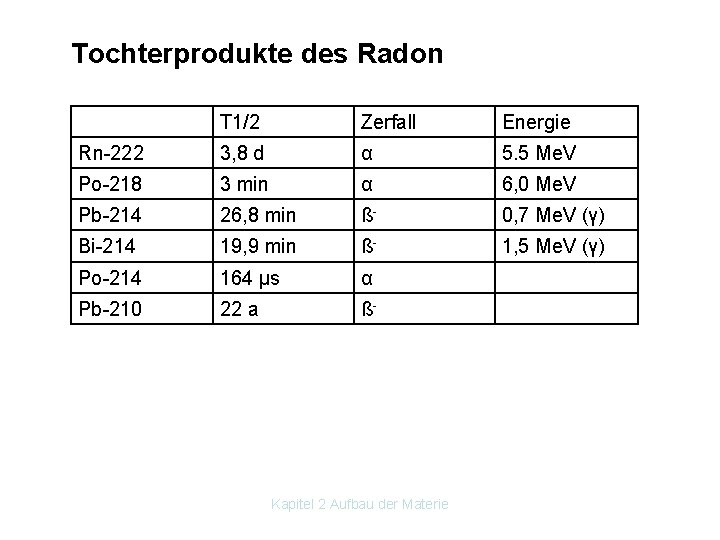
Tochterprodukte des Radon T 1/2 Zerfall Energie Rn 222 3, 8 d α 5. 5 Me. V Po 218 3 min α 6, 0 Me. V Pb 214 26, 8 min ß 0, 7 Me. V (γ) Bi 214 19, 9 min ß 1, 5 Me. V (γ) Po 214 164 µs α Pb 210 22 a ß Kapitel 2 Aufbau der Materie

2. 7 Bilden von Arbeitsgruppen • Kosmische Strahlung (S. 31, A 1) (Folie B 2. 11) • Halbwertszeit ( S. 32 + (Folie B 2. 12/1+2 ) (A 2 u. A 3) • Radiocarbonmethode und radiometrische Altersbestimmung (S. 33) (A 1, A 2 S 33) • Strahlenquellen und Strahlenschutz (S. 34) (Folie B 2. 13) A 2 u. A 3 • Isotopentafel erklären • Fundamentale Wechselwirkungen B. S. 35 Kapitel 2 Aufbau der Materie
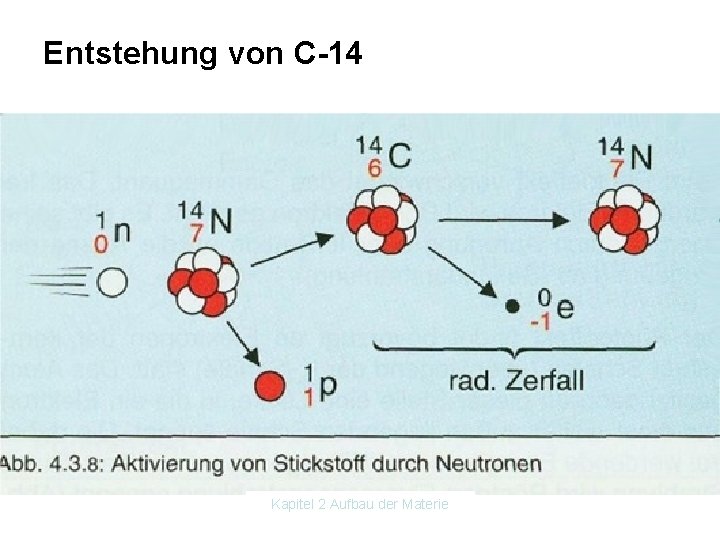
Entstehung von C-14 Kapitel 2 Aufbau der Materie

Glühstrümpfe Zunächst benutzte Carl Auer von Welsbach Magnesium Oxide, Zirconiumdioxid, dann Lanthan, Yttrium und Praseodym Verbindungen. Sie alle weisen ein mäßiges Absorptionsvermögen im sichtbaren Bereich auf und produzieren nur ein braunweißes Leuchten. Der Durchbruch gelang ihm mit Ceroxid, zusammen mit Thoriumdioxid zur Stabilitätsverbesserung. Die Zusammensetzung von 1 Prozent Ce. O 2 und 99 Prozent Th. O 2 wurde erst vor wenigen Jahrzehnten durch eine Mischung aus Yttriumoxid und Ceroxid abgelöst, um auf das leicht radioaktive Th. O 2 verzichten zu können. Th 232 ist ein Strahler 1, 4∙ 1010 a Ce (Ordnungszahl 58) hat mehrere stabile Isotope Kapitel 2 Aufbau der Materie
![Radiotoxizität [Bearbeiten] Das Thoriumisotop 232 Th ist mit seiner Halbwertszeit von 14, 05 Mrd. Radiotoxizität [Bearbeiten] Das Thoriumisotop 232 Th ist mit seiner Halbwertszeit von 14, 05 Mrd.](http://slidetodoc.com/presentation_image_h/a5caff65af5a73ff3134665656ba0713/image-64.jpg)
Radiotoxizität [Bearbeiten] Das Thoriumisotop 232 Th ist mit seiner Halbwertszeit von 14, 05 Mrd. Jahren noch wesentlich schwächer radioaktiv (geringere Dosisleistung) als Uran, da durch die längere Halbwertszeit weniger Zerfälle pro Sekunde stattfinden und auch die Konzentration der kurzlebigen Zerfallsprodukte geringer bleibt. Thorium ist ein α Strahler und aufgrund dieser Strahlungsart gefährlich bei Inhalation und Ingestion. Metall Stäube und vor allem Oxide sind aufgrund ihrer Lungengängigkeit radiotoxisch besonders gefährlich und können Krebs verursachen. Beim Lagern und Umgang von bzw. mit Thorium und seinen Verbindungen ist auch die stetige Anwesenheit der Elemente aus der Zerfallsreihe zu beachten. Besonders gefährlich sind starke Beta- und die mit einem hohen 2, 6 Me. V Anteil sehr energiereichen und durchdringungsfähigen Gammastrahler. Kapitel 2 Aufbau der Materie

Die Zerfallsprodukte des natürlich vorkommenden Thoriums 232 sind in folgender Reihenfolge: Radium 228 Ra (Halbwertszeit 5, 75 a), Actinium 228 Ac (6, 15 h), Thorium 228 Th (1, 9116 a), Radium 224 Ra (3, 66 d), Radon 220 Rn (55, 6 s), Polonium 216 Po (0, 145 s), Blei 212 Pb (10, 6 h), Bismut 212 Bi (60, 55 min), daraus zu 64 % Polonium 212 Po (3· 10− 7 s) und zu 36 % Thallium 208 Tl (3, 053 min), aus beiden stabiles Blei 208 Pb. Kapitel 2 Aufbau der Materie
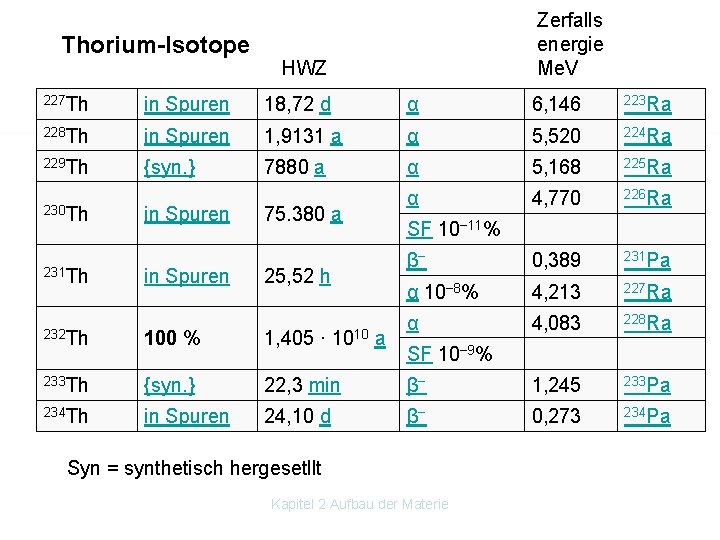
Thorium-Isotope Zerfalls energie Me. V HWZ 227 Th in Spuren 18, 72 d α 6, 146 223 Ra 228 Th in Spuren 1, 9131 a α 5, 520 224 Ra 229 Th {syn. } 7880 a α 5, 168 225 Ra α 4, 770 226 Ra β− 0, 389 231 Pa α 10− 8% 4, 213 227 Ra α 4, 083 228 Ra 230 Th 231 Th in Spuren 75. 380 a 25, 52 h SF 10− 11% 232 Th 100 % 1, 405 · 1010 a 233 Th {syn. } 22, 3 min β− 1, 245 233 Pa 234 Th in Spuren 24, 10 d β− 0, 273 234 Pa SF 10− 9% Syn = synthetisch hergesetllt Kapitel 2 Aufbau der Materie

Titel: Strahlenschutz Kapitel 2 Aufbau der Materie

Aktivität, Ionendosis Aktivität einer Strahlungsquelle = Anzahl der Zerfälle pro Sekunde Einheit: 1 Becquerel=1 Bq=1 s– 1 Ionendosis = Betrag der elektrischen Ladungen gleichen Vorzeichens, die pro Kilogramm des bestrahlten Körpers erzeugt werden. Einheit: 1 C/kg Kapitel 2 Aufbau der Materie
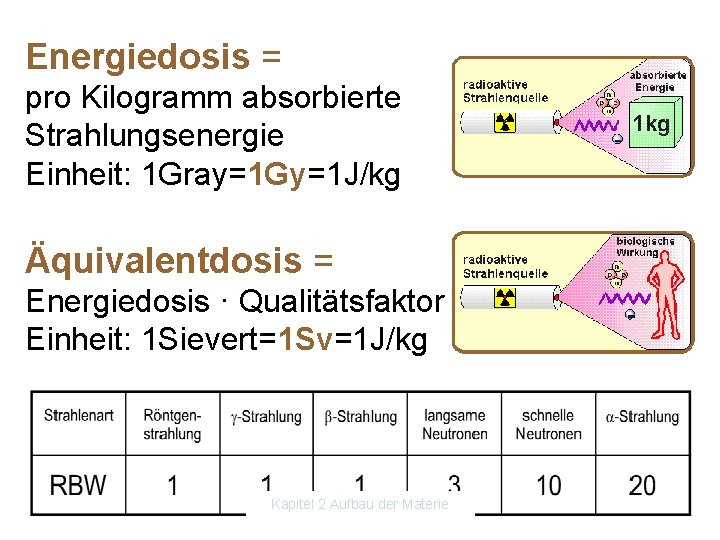
Energiedosis = pro Kilogramm absorbierte Strahlungsenergie Einheit: 1 Gray=1 Gy=1 J/kg Äquivalentdosis = Energiedosis · Qualitätsfaktor Einheit: 1 Sievert=1 Sv=1 J/kg Kapitel 2 Aufbau der Materie

effektive Dosis in Sv 0 bis 0, 5 bis 1 1 bis 2 ab 4 ab 6 über 7 über 100 Strahlenwirkungen Ohne größeren diagnostischen Aufwand keine unmittelbar nachteiligen Wirkungen feststellbar, aber Schwächung des Immunsystems, Veränderungen des Blutbilds, Hautrötungen, vereinzelt Übelkeit, Erbrechen, sehr selten Todesfälle, nachteilige Wirkungen auf das Knochenmark, Erbrechen, Übelkeit, schlechtes Allgemeinbefinden, etwa 20% Sterblichkeit, schwere Einschränkungen des Allgemeinbefindens sowie schwere Störungen der Blutbildung, die Infektionsbereitschaft ist stark erhöht, 50%ige Sterblichkeit, neben den genannten schweren Störungen treten gastrointestinale Symptome auf, die Überlebensrate ist nur noch sehr gering, nahezu 100 %ige Sterblichkeit, zusätzlich Schädigung des ZNS, bis hin zu Lähmungen, schneller Tod durch Ausfall des ZNS (Sekundentod). Symptome bei einem Menschen, der einer kurzzeitigen Ganzkörperbestrahlung ausgesetzt war. Kapitel 2 Aufbau der Materie
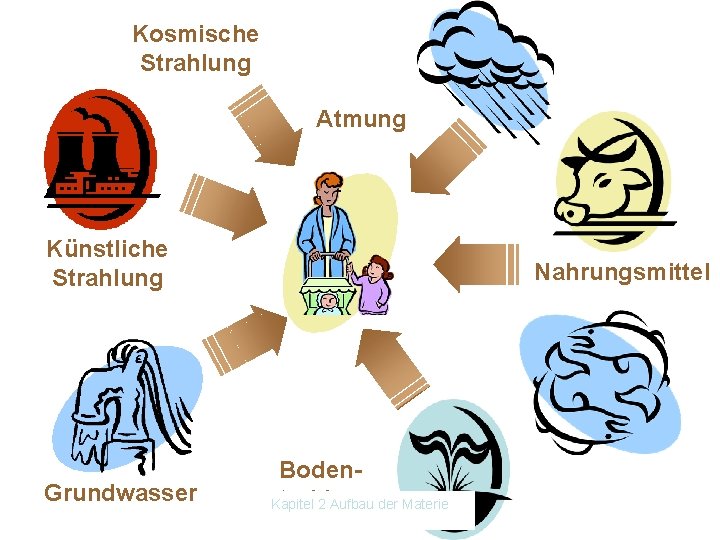
Kosmische Strahlung Atmung Künstliche Strahlung Grundwasser Nahrungsmittel Bodenstrahlung Kapitel 2 Aufbau der Materie
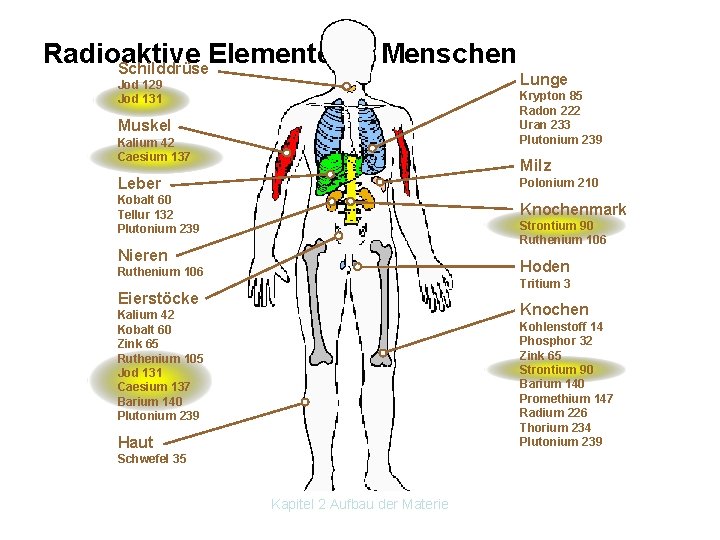
Radioaktive Elemente im Menschen Schilddrüse Jod 129 Jod 131 Lunge Krypton 85 Radon 222 Uran 233 Plutonium 239 Muskel Kalium 42 Caesium 137 Milz Leber Polonium 210 Kobalt 60 Tellur 132 Plutonium 239 Knochenmark Strontium 90 Ruthenium 106 Nieren Hoden Ruthenium 106 Tritium 3 Eierstöcke Knochen Kalium 42 Kobalt 60 Zink 65 Ruthenium 105 Jod 131 Caesium 137 Barium 140 Plutonium 239 Kohlenstoff 14 Phosphor 32 Zink 65 Strontium 90 Barium 140 Promethium 147 Radium 226 Thorium 234 Plutonium 239 Haut Schwefel 35 Kapitel 2 Aufbau der Materie
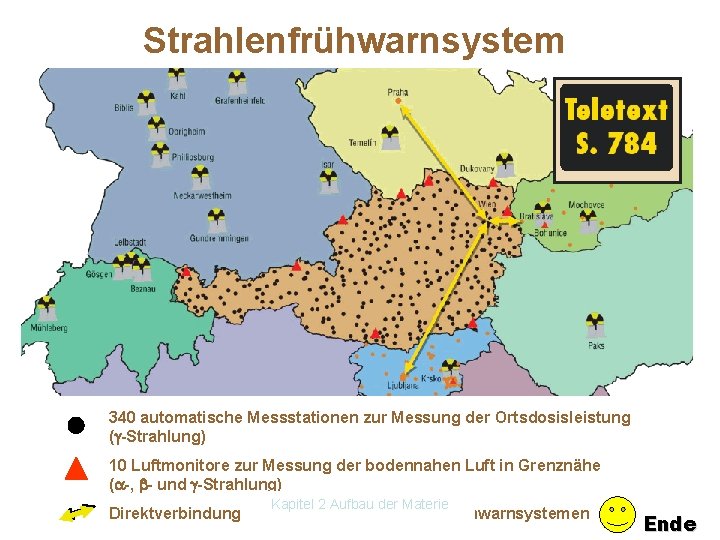
Strahlenfrühwarnsystem 340 automatische Messstationen zur Messung der Ortsdosisleistung ( -Strahlung) 10 Luftmonitore zur Messung der bodennahen Luft in Grenznähe ( -, - und -Strahlung) Kapitel 2 Aufbau der Materie Direktverbindung zu ausländischen Strahlenfrühwarnsystemen Ende

Übersicht Gravitation (Massenanziehung, Schwerkraft) Elektromagnetische Wechselwirkung Starke WW Kapitel 2 Aufbau der Materie Schwache WW

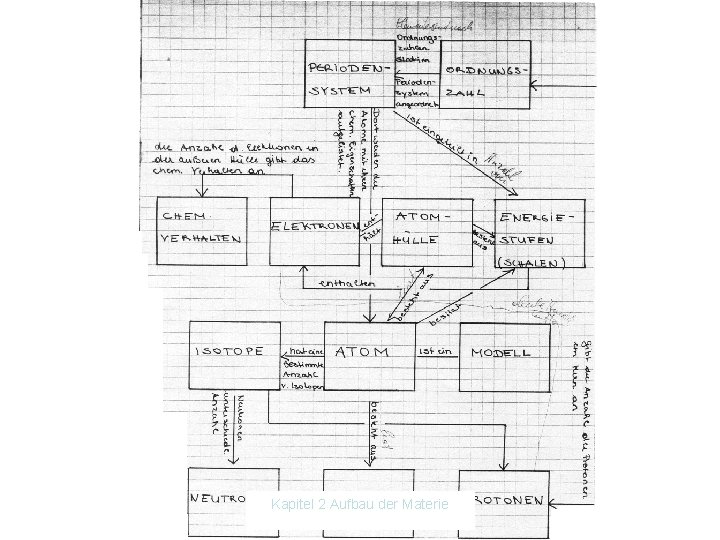
Konstruieren von Begriffsnetzen mit Concept Mapping Den Schülerinnen und Schülern werden Begriffe zu einem Themengebiet vorgegeben. In Gruppenarbeit (ca. 4 Schüler/innen) sollen sie diese Begriffe in ein Begriffsnetz bringen. Die Schüler schreiben jeden dieser Begriffe auf einen Zettel eines Haftnotizblocks. Diese Zettel kleben sie auf ein Packpapier und versuchen nun Beziehungen zwischen den Begriffen herzustellen. Dies deuten sie durch Pfeile, die von einem zum anderen Begriff führen, an. Zusätzlich schreiben sie die Art der Beziehung zu diesem Pfeil. Es sollten möglichst viele Verbindungen hergestellt werden, dabei sollten sich nicht zu viele Pfeile kreuzen. Eventuell müssen die Begriffe umgeordnet werden. Die Pfeile und die Beschriftung sollte man vorerst mit Bleistift durchführen, damit sich Korrekturen leichter durchführen lassen. Kapitel 2 Aufbau der Materie

Wenn das Concept Map „fertig“ ist (nach Diskussion mit dem Lehrer oder Korrektur), ist es günstig, dieses nochmals auf ein DIN a 4 Blatt zu zeichnen, damit man es kopieren kann und alle Gruppenteilnehmer das Ergebnis zum Lernen mitnehmen können. Ordne folgende Begriffe einander zu! Elektronen Energiestufen (Schalen) Atomhülle chem. Verhalten Neutronen Nukleonen Isotope Atom Ordnungszahl Protonen Massenzahl Periodensystem Modell Atomkern Kapitel 2 Aufbau der Materie
Kapitel 2 Aufbau der Materie
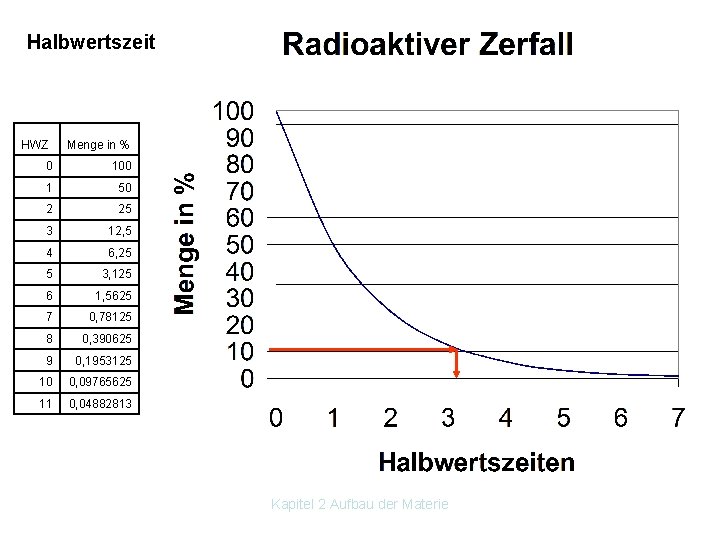
Halbwertszeit HWZ Menge in % 0 100 1 50 2 25 3 12, 5 4 6, 25 5 3, 125 6 1, 5625 7 0, 78125 8 0, 390625 9 0, 1953125 10 0, 09765625 11 0, 04882813 Kapitel 2 Aufbau der Materie
- Slides: 78