1me ANNEE DE MEDECINE DENTAIRE BIOCHIMIE STRUCTURE DES

1éme ANNEE DE MEDECINE DENTAIRE BIOCHIMIE STRUCTURE DES LIPIDES Dr BOUAZDI Pr CHICOUCHE

LES LIPIDES I - INTRODUCTION : II- CLASSIFICATION III – STRUCTURE DES LIPIDES: 1 - LES ACIDES GRAS : 1 -1 - Définition : 1 -2 - Acides gras saturés 1 -3 - Acides gras insaturés 1 -4 - Propriétés des acides gras. 2 - LES LIPIDES SIMPLES : 2 -1 - LES GLYCERIDES : 2 -2 - LES CERIDES : 2 -3 - LES STERIDES : 3 - LES LIPIDES COMPLEXES : 3 -1 - LES GLYCEROPHOSPHOLIPIDES : 3 -2 - LES SPHINGOLIPIDES : IV- Les composés à caractère lipidique STRUCTURE 1

I - INTRODUCTION : Chez les êtres vivants: Les lipides : forme de réserve énergétique (+++) graisses: animaux huiles: végétaux. Double origine : - Exogène: Alimentation: apporte 100 à 150 g de graisses/j (graisses exogènes) 95 à 97% = graisses neutres (triglycérides ) 3 à 5 % = phospholipides sphingolipides cholestérol. - Endogène: Synthétisée par l’organisme (graisses endogènes).

Les lipides sont caractérisés par une propriété physique : la solubilité Définition : Substances très hétérogènes Avec un Critère commun : insolubles dans l’eau Solubles dans les solvants organiques apolaires (tel que le benzène ou le chloroforme, etc. )

Termes d’huile, beurres, graisses, cires = Désignent leur état physique liquide ou solide à la température ambiante. Ce sont des molécules qui peuvent être : - complètement apolaire (lipides neutres) - ou bipolaires ou amphiphile (ou amphipathique).

Rôles : Nombreux. 1) Réserves intracellulaires d’énergie (triglycérides) 2) Matériaux de structure - Couches de protection de cellules - Composants des membranes biologiques ( phospholipides et cholestérol) 3) Molécules actives: En concentration faible Précurseurs d’hormones stéroïdes Médiateurs extracellulaire Messagers intracellulaires Vitamines liposolubles.
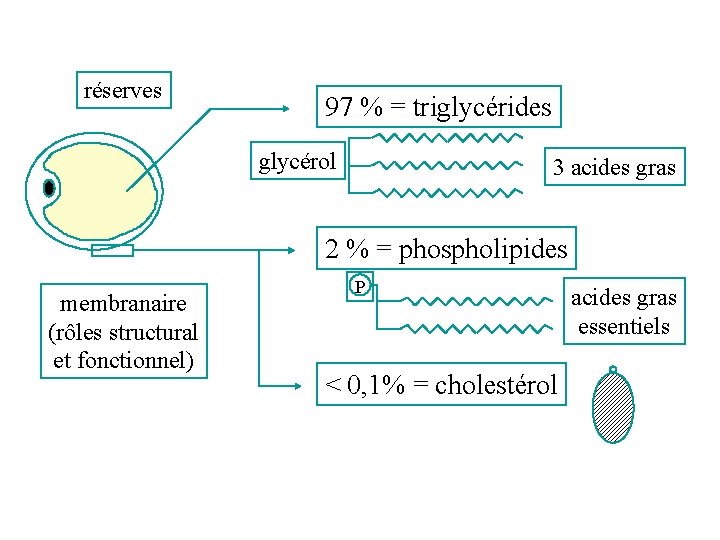
réserves 97 % = triglycérides glycérol 3 acides gras 2 % = phospholipides membranaire (rôles structural et fonctionnel) P < 0, 1% = cholestérol acides gras essentiels
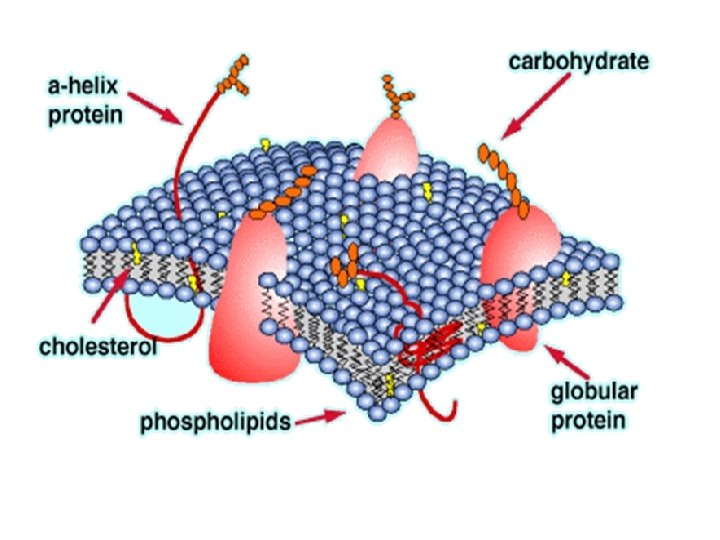

Transport : Les lipides sont insolubles Transporter dans le sang sous forme d’une association moléculaire lipidoprotéique soluble appelée lipoprotéines ( triglycérides, cholesterol, phospholipides. Noter: Acides gras libres transportés par l’albumine.

II - CLASSIFICATION DES LIPIDES : Classification utilisée : A- Les lipides vrais : 1 - Les lipides simples : 2 - Les lipides complexes : B- Les composés à caractères lipidiques (lipoïdes)

A-Les lipides vrais : . 1 - Les lipides simples : Contiennent dans leurs structures du carbone, de l’hydrogène et de l’oxygène (C, H, O), Résultent de l’estérification d’alcool par des acides gras et regroupent : - les glycérides ( l’alcool = le glycérol) - Les cérides( l’alcool = alcool à longue chaîne aliphatique) - Les stérides ( l’alcool = le stérol). 2 - Les lipides complexes : Renferment du C , O , H et de l’azote, du phosphore et du soufre (N, P, S. ou des oses, Regroupent : - Les glycérophospholipides - Les sphingolipides
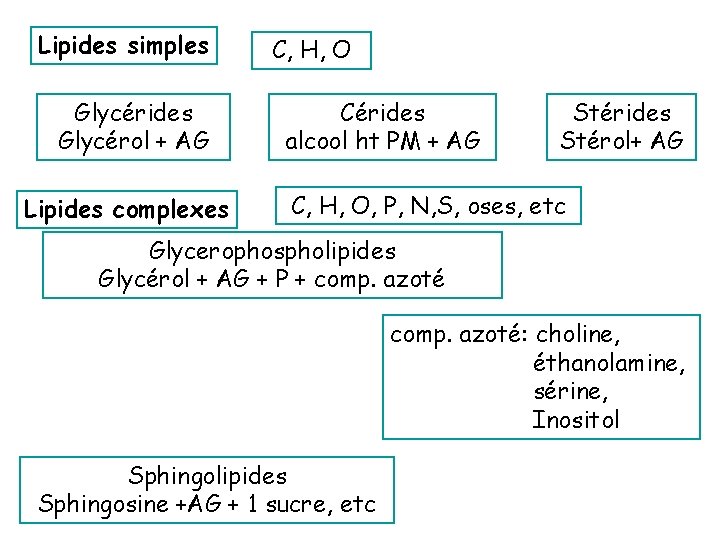
Lipides simples Glycérides Glycérol + AG Lipides complexes C, H, O Cérides alcool ht PM + AG Stérides Stérol+ AG C, H, O, P, N, S, oses, etc Glycerophospholipides Glycérol + AG + P + comp. azoté: choline, éthanolamine, sérine, Inositol Sphingolipides Sphingosine +AG + 1 sucre, etc
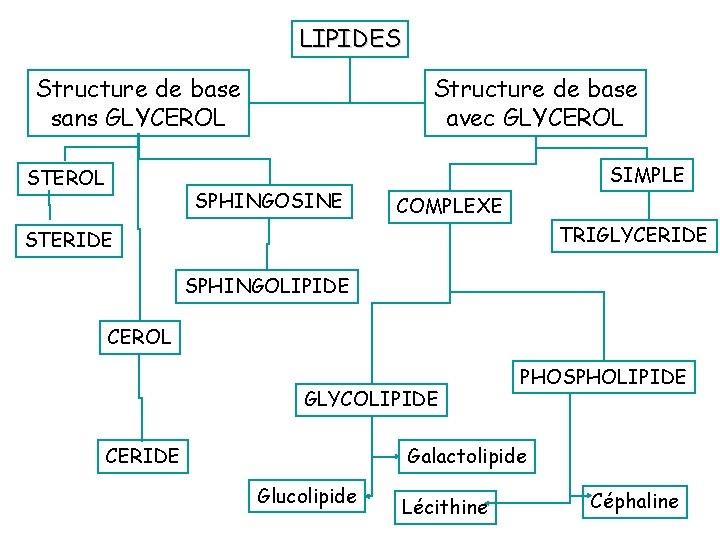
LIPIDES Structure de base sans GLYCEROL STEROL Structure de base avec GLYCEROL SPHINGOSINE SIMPLE COMPLEXE TRIGLYCERIDE STERIDE SPHINGOLIPIDE CEROL GLYCOLIPIDE CERIDE PHOSPHOLIPIDE Galactolipide Glucolipide Lécithine Céphaline
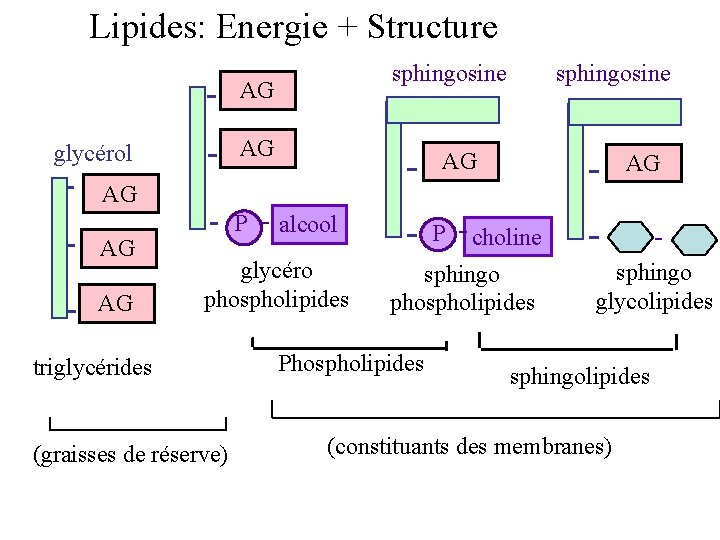
Lipides: Energie + Structure sphingosine AG AG glycérol sphingosine AG AG AG P alcool glycéro phospholipides triglycérides (graisses de réserve) P choline sphingo phospholipides Phospholipides sphingo glycolipides sphingolipides (constituants des membranes)

B- Les composés à caractères lipidiques (lipoïdes) - Isoprénoides, dérivés d’unités isoprène (à 5 C): Exemple: les dérivés du stérol et les vitamines liposolubles A D E K. - Icosanoides qui sont des médiateurs dérivés d’acides gras : Exemple: Les prostaglandines, etc.

Remarque : En se basant sur leur comportement dans les milieux aqueux (solubilité dans l’eau), on peut subdivise les lipides en : - lipides apolaires ou non polaires - lipides polaires 1 - Lipides non polaires ou apolaire: les lipides insolubles dans l’eau et regroupent : - triglycérides. - esters de cholestérol. 2 - Lipides polaires : renferment dans leur structure un pôle hydrophile et un pôle hydrophobe qui leur donnent un caractère amphipathique. et regroupent : - les phospholipides - le cholestérol libre.
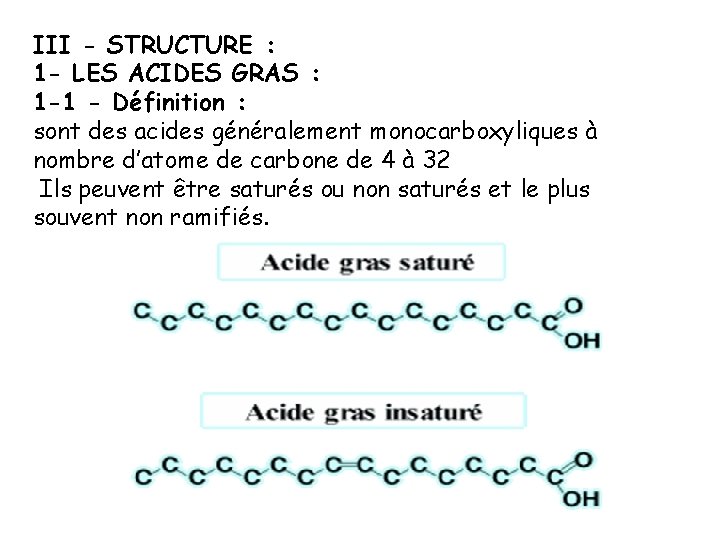
III - STRUCTURE : 1 - LES ACIDES GRAS : 1 -1 - Définition : sont des acides généralement monocarboxyliques à nombre d’atome de carbone de 4 à 32 Ils peuvent être saturés ou non saturés et le plus souvent non ramifiés.

Dans leur grande majorité les acides gras ont un nombre pair d’atome de carbone. On parle de: - chaîne courte (‹ à C 10) - chaîne moyenne (C 12 et C 16) - chaîne longue (› C 16) Saturés ou Insaturés

Nomenclature des acides gras : Nomenclature systématique : Pour désigner un acide gras : . Il faut indiquer le nombre de carbone de l’acide gras (en grec), . Suivi du suffixe Anoique pour les acides gras saturés, Ou -enoique, pour les monoinsaturés Ou -dienoique pour les di-insaturés Ou -trienoique pour les tri-insaturés. . Ensuite indiquer pour les insaturés: Le nombre des double liaisons (Δ), La positions des double liaisons (Δ), et La configurations des double liaisons (Δ), (cis ou trans)

Mais noter: . Les noms communs des acides gras restent très largement utilisés. . Et on utilise une nomenclature en série : La série est de la forme ωn oŭ n est la position de la première double liaison notée par rapport à la position ω, du dernier carbone de la chaîne aliphatique.

1 -2 - Acides gras saturés : . Sont les plus répandus dans la nature, . Leur formule brute est : Cn H 2 n. O 2 ou Cn (Hn. O)2 Ou CH 3 -(CH 2)(n-2)- COOH Partie hydrophobe CH 3 -(CH 2)n-2 - COOH Molécule amphiphile Partie hydrophile
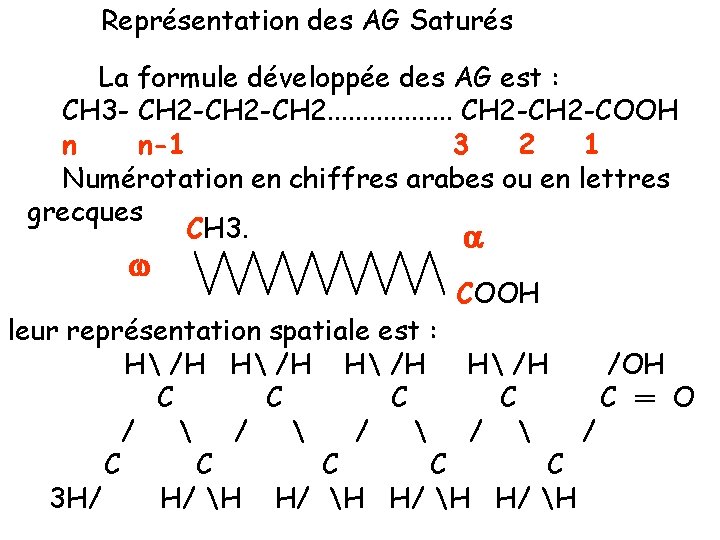
Représentation des AG Saturés La formule développée des AG est : CH 3 - CH 2 -CH 2. . . . CH 2 -COOH n n-1 3 2 1 Numérotation en chiffres arabes ou en lettres grecques CH 3. w COOH leur représentation spatiale est : H /H /OH C C C ═ O / / / C C C 3 H/ H/ H
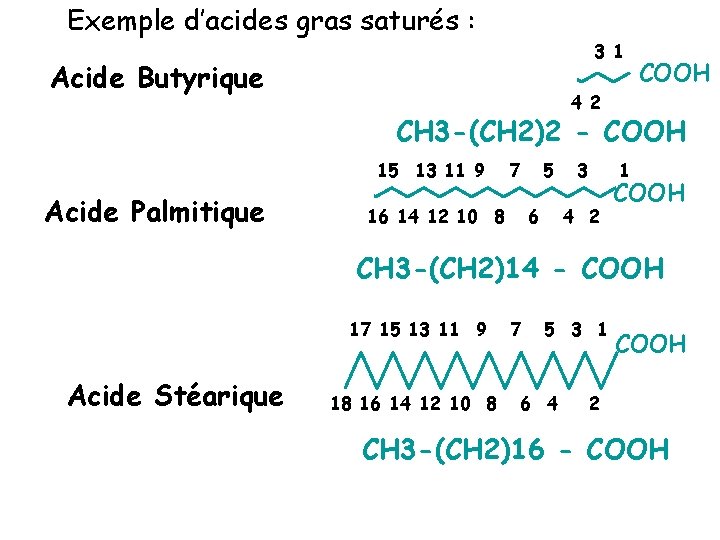
Exemple d’acides gras saturés : 3 1 Acide Butyrique COOH 4 2 CH 3 -(CH 2)2 - COOH 15 13 11 9 Acide Palmitique 7 5 16 14 12 10 8 6 3 1 4 2 COOH CH 3 -(CH 2)14 - COOH 17 15 13 11 9 Acide Stéarique 18 16 14 12 10 8 7 5 3 1 6 4 COOH 2 CH 3 -(CH 2)16 - COOH
![Nomenclature des acides gras saturés : Le nom systématique s’écrit : n- [n C] Nomenclature des acides gras saturés : Le nom systématique s’écrit : n- [n C]](http://slidetodoc.com/presentation_image_h2/59af01de23812927962e54ea4f2e21ed/image-24.jpg)
Nomenclature des acides gras saturés : Le nom systématique s’écrit : n- [n C] an oique n : indique l’acide gras est normal (chaîne non branchée) [n. C] : nombre de carbones (en grec) an : indique la chaîne est saturée oique : pour acide le symbole est Cn: 0 (0 indique la chaîne est saturée) Le nom courant rappelle son origine. Les acides gras saturés sont :
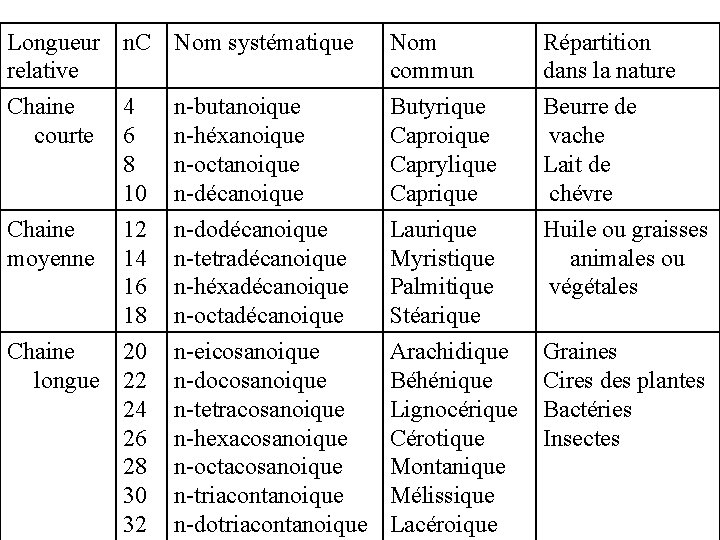
Longueur n. C Nom systématique relative Nom commun Répartition dans la nature Chaine courte n-butanoique n-héxanoique n-octanoique n-décanoique Butyrique Caproique Caprylique Caprique Beurre de vache Lait de chévre n-dodécanoique n-tetradécanoique n-héxadécanoique n-octadécanoique n-eicosanoique n-docosanoique n-tetracosanoique n-hexacosanoique n-octacosanoique n-triacontanoique n-dotriacontanoique Laurique Myristique Palmitique Stéarique Arachidique Béhénique Lignocérique Cérotique Montanique Mélissique Lacéroique Huile ou graisses animales ou végétales Chaine moyenne 4 6 8 10 12 14 16 18 Chaine 20 longue 22 24 26 28 30 32 Graines Cires des plantes Bactéries Insectes

Les acides gras peuvent également se présenter sous forme ramifiée. La plupart de ces acides ne possède qu’une seule ramification dont les plus importants sont ceux présents dans des bactéries du bacille de Koch (BK). - Acide tuberculostéarique ou acide 10 -methylstéarique : CH 3 -(CH 2)7 -CH-(CH 2)8 -COOH │ CH 3 - Acide mycocérosique ou acide 2, 4, 6, 8 - tetraméthyloctacosanoique. CH 3 -(CH 2)19 -CH-CH 2 -CH-CH 2 -CH-COOH │ │ CH 3
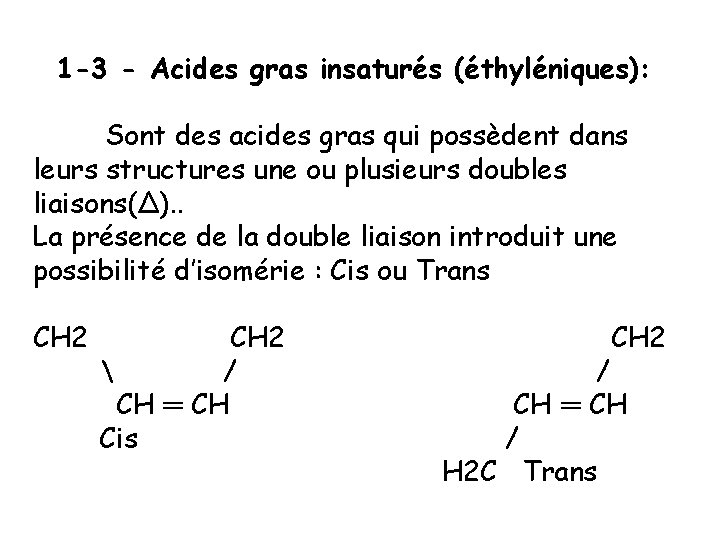
1 -3 - Acides gras insaturés (éthyléniques): Sont des acides gras qui possèdent dans leurs structures une ou plusieurs doubles liaisons(Δ). . La présence de la double liaison introduit une possibilité d’isomérie : Cis ou Trans CH 2 / CH ═ CH Cis CH 2 / CH ═ CH / H 2 C Trans

- Acides gras monoéthyléniques ou monoinsaturés (Cn : 1) : ils renferment dans leurs structures une double liaison. Exemples : -acide palmitoleique ou acide 9, 10 - hexadecenoique (C 16 9). CH 3 - (CH 2)5 - CH = CH - (CH 2)7 - COOH -acide oleique ou acide 9, 10 -octadecenoique (C 18 9). CH 3 - (CH 2)7 - CH = CH - (CH 2)7 – COOH +++ Ces acides gras sont très répandus dans la nature et présents dans toutes les graisses animales et les huiles végétales.
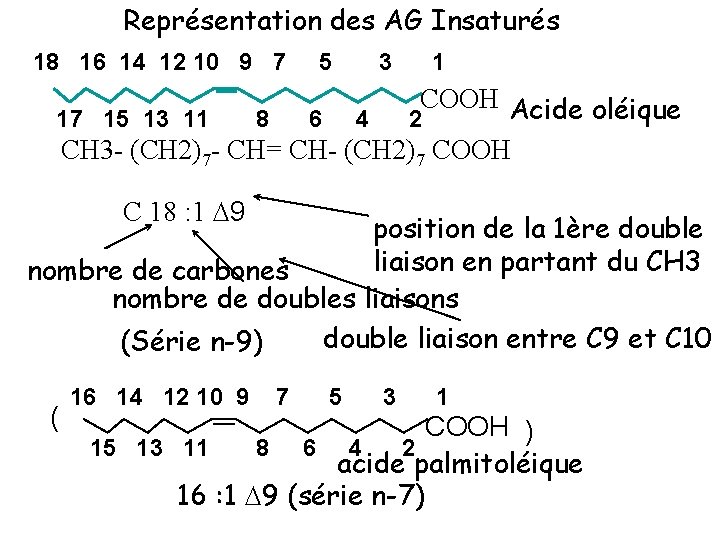
Représentation des AG Insaturés 18 16 14 12 10 9 7 5 3 1 COOH Acide oléique 17 15 13 11 8 6 4 2 CH 3 - (CH 2)7 - CH= CH- (CH 2)7 COOH C 18 : 1 9 position de la 1ère double liaison en partant du CH 3 nombre de carbones nombre de doubles liaisons double liaison entre C 9 et C 10 (Série n-9) 7 5 3 1 COOH 15 13 11 8 6 4 2 acide palmitoléique 16 : 1 9 (série n-7) ( ( 16 14 12 10 9

. - Acides gras di- tri- et polyethyleniques ou polyinsaturés : sont les acides gras qui renferment dans leurs structures 2, 3 ou plusieurs doubles liaisons. Exemples : - acide linoléique ou acide 9 -10, 12 -13 – octadécadienoique (C 18 : 2 9 , 12). CH 3 - (CH 2)4 - CH = CH - CH 2 - CH = CH - (CH 2)7 - COOH. -acide linolénique ou acide 9 -10, 12 -13, 15 -, , 16 octadécatrienoique (C 18: 3 9, 12, 15). CH 3 -(CH 2)-CH=CH-CH 2 -CH=CH-CH 2)7 -COOH.
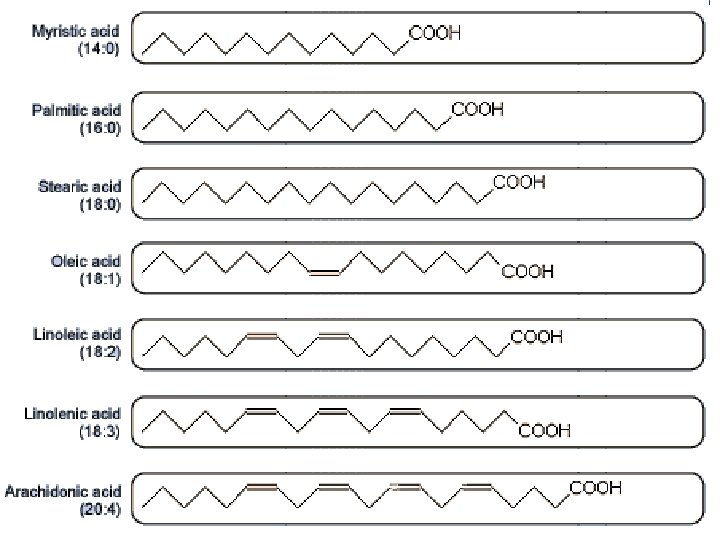

Régles : La première ou la seule double liaison est établie entre les C 9 et les C 10, les doubles liaisons sont en configuration CIS et sont séparées par un groupe méthylène en position malonique ─C═C─C─C═

Ces doubles liaisons peuvent être dans certains AG rares. - Soit en position succinique ( acide clupadonique ou acide 4 -5, 8 -9, 12 -13, 16 -17, 20 -21 -docosenoique CH 3─CH═CH─(CH 2)2─CH═CH─(CH)2─CH ═ CH─(CH 2)2─COOH - Soit en position conjuguée (acide éleostéarique ou acide 9 -10, 11 -12, 13 -14 -octadécatrienoique) CH 3─(CH 2)3─ CH ═ CH─(CH 2)7─COOH

Remarque : Du point de vue nutritionnel, certains acides gras polyinsaturés sont dits indispensables, car il ne peuvent être synthétisés par l’organisme et doivent, par conséquent, être apportés par l’alimentation ; ils sont au nombre de 3 : - acide linoléique C 18 : 2 9 , 12 - acide linolénique C 18 : 3 9 , 12, 15 - acide arachidonique C 20 : 4 5, 8, 11, 14. A partir de l’acide linoléique, l’organisme peut synthétiser les deux autres.
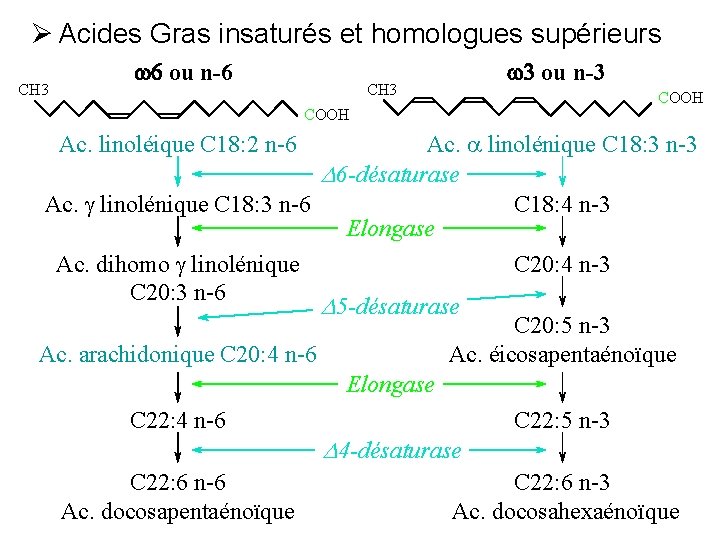
Ø Acides Gras insaturés et homologues supérieurs CH 3 w 6 ou n-6 CH 3 COOH w 3 ou n-3 COOH Ac. a linolénique C 18: 3 n-3 D 6 -désaturase Ac. g linolénique C 18: 3 n-6 C 18: 4 n-3 Elongase Ac. dihomo g linolénique C 20: 4 n-3 C 20: 3 n-6 D 5 -désaturase C 20: 5 n-3 Ac. arachidonique C 20: 4 n-6 Ac. éicosapentaénoïque Elongase C 22: 4 n-6 C 22: 5 n-3 D 4 -désaturase C 22: 6 n-6 C 22: 6 n-3 Ac. docosapentaénoïque Ac. docosahexaénoïque Ac. linoléique C 18: 2 n-6

Sources alimentaires d'AGE Acide Linoléique Linolénique Arachidonique % des AG tot(18: 2 n-6) (18: 3 n-3) (20: 4 n-6) Huile maïs 50 2 olive 11 1 arachide 29 1 colza 16 -23 10 -11 soja 52 7 tournesol 52 traces Viande (muscle) bœuf maigre 26 1 13 agneau 18 4 7 poulet 18 1 6
![Nomenclature des acides gras insaturés : Le nom systématique s’écrit : conf-p- [n. C] Nomenclature des acides gras insaturés : Le nom systématique s’écrit : conf-p- [n. C]](http://slidetodoc.com/presentation_image_h2/59af01de23812927962e54ea4f2e21ed/image-37.jpg)
Nomenclature des acides gras insaturés : Le nom systématique s’écrit : conf-p- [n. C] x én oique conf-p : configuration et position des doubles liaisons. [n. C] : nombre de carbones én : indique la chaîne est insaturée et le symbole est Cn: mΔ(p, p’. . ) Cn: nombre de carbones mΔ : nombre de doubles liaisons (p, p’. . ) : positions des doubles liaisons en numérotation normale Le nom courant rappelle son origine.

Noter: les acides gras sont classés aussi par série ; Il existe 4 séries principales : ω 3, ω 6, ω 7, ω 9. Dans la série ω 3, 3 est la position de la premier double liaison notée par rapport à la position ω, dernier carbone de la chaîne aliphatique
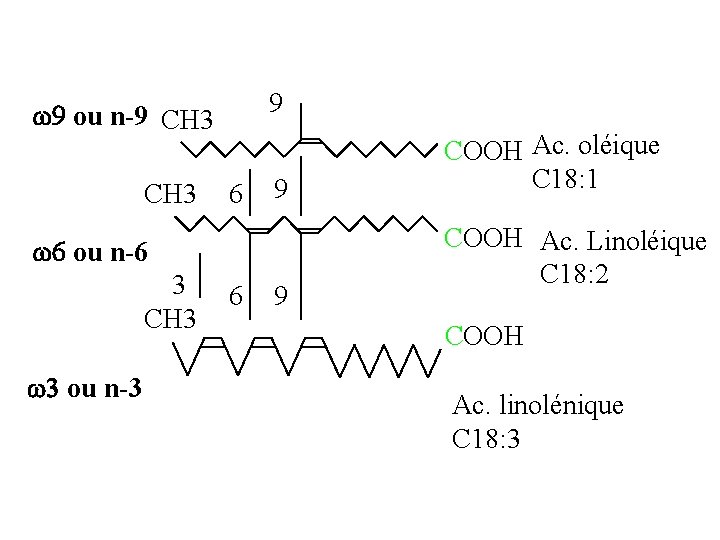
9 w 9 ou n-9 CH 3 6 9 w 6 ou n-6 3 CH 3 w 3 ou n-3 6 9 COOH Ac. oléique C 18: 1 COOH Ac. Linoléique C 18: 2 COOH Ac. linolénique C 18: 3

La notation symbolique: qui mélange la notation systématique et la notion de série est quelquefois rencontrée, Par exemple : Acide arachidonique , ou encore C 20 : 4 5, 8, 11, 14 ou C 20 : 4 ω 6
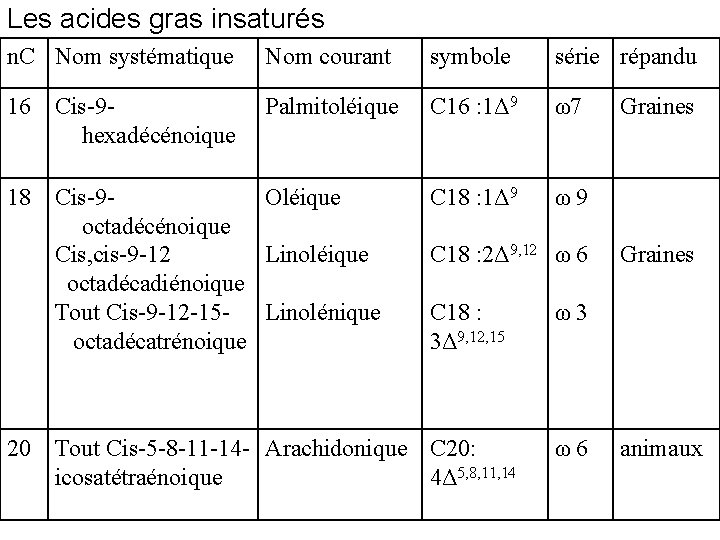
Les acides gras insaturés n. C Nom systématique Nom courant symbole série répandu 16 Cis-9 hexadécénoique Palmitoléique C 16 : 1Δ 9 ω7 C 18 : 1Δ 9 ω9 18 Cis-9 Oléique octadécénoique Cis, cis-9 -12 Linoléique octadécadiénoique Tout Cis-9 -12 -15 - Linolénique octadécatrénoique C 18 : 2Δ 9, 12 ω 6 C 18 : 3Δ 9, 12, 15 20 Tout Cis-5 -8 -11 -14 - Arachidonique C 20: icosatétraénoique 4Δ 5, 8, 11, 14 Graines ω3 ω6 animaux

Acides gras atypiques : Acides gras avec trans : très rare, on les trouve dans certaines bactéries. Acides gras avec des doubles liaison en position anormales : l’acide érucique du colza en C 22 : 1 13. Un acide, à nombre impair de carbones, du cheveu porte une double liaison terminale C 11 : 1 10 : c’est un antifongique contre les teignes, abondant dans la graisse des cheveux de l’adulte et presque absent chez l’enfant. Des doubles liaisons conjuguées existent dans des acides gras de plantes C 18 : 3 9, 11, 13

Certains acides gras contiennent des cycles dans leur structure telles que l’acide cyclopenténique contenue dans l’huile de graines de chaulmoogra (arbre tropical d’inde). HC ─ CH-(CH 2)12 -COOH ║ │ HC CH 2 / CH 2 Les prostaglandines, médiateurs biologiques, sont des acides gras cyclopenténiques de la famille des icosanoides(C 20).

1 -4 - Propriétés des acides gras. 1 -4 -1 - Propriétés physiques : a) Point de fusion C’est la température de passage entre l’état liquide et l’état solide. - Les acides gras à courte chaîne sont solubles dans l’eau alors que les acides gras à chaîne longue sont insolubles. - Les acides gras ayant une chaîne de moins de 10 carbones sont à l’état liquide à température ordinaire, mais ils sont à l’état solide si le nombre de carbone est supérieur à 10. - La présence de la double liaison abaisse le point de fusion d’un acide gras, c’est à dire que pour une même chaîne celui qui a une double liaison aura le point de fusion le plus bas.

Point fusion (°C) Acides gras saturés C 4 butyrique C 6 caproïque C 8 C 10 C 12 laurique C 14 myristique C 16 palmitique C 18 stéarique C 20 arachidique C 22 C 24 lignocérique -8 -3 +17 +31 +44 +54 +63 +70 +75 +80 +84 Acides gras insaturés C 18 : 1 oléique + 13. 4 C 18 : 2 linoléique -9 C 18 : 3 linolénique -17 C 20 : 4 arachidonique - 49. 5

b) Point d’ébullition plus le nombre de C augmente plus le point d’ébullition augmente. c) La solubilité des acides gras composés amphotères avec deux pôles : hydrophile et hydrophobe, CH 3 -(CH 2)n----------------COOH : pole non réactif ou hydrophobe pole réactif ou hydrophile en dessus de C 4 et C 5, les acides gras sont insolubles et s’organisent : - Soit en film moléculaire (mono ou bicouche, ou multicouche) à l’interface eau-air. - Soit en micelles (émulsion).
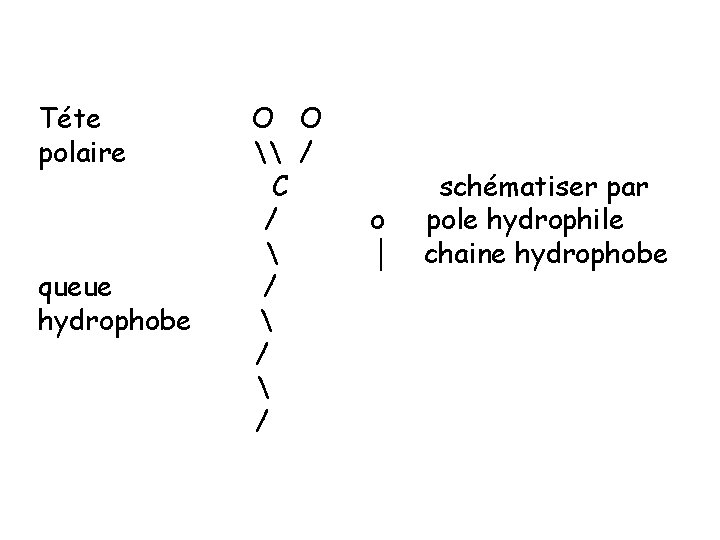
Téte polaire queue hydrophobe O O \ / C / / / o │ schématiser par pole hydrophile chaine hydrophobe
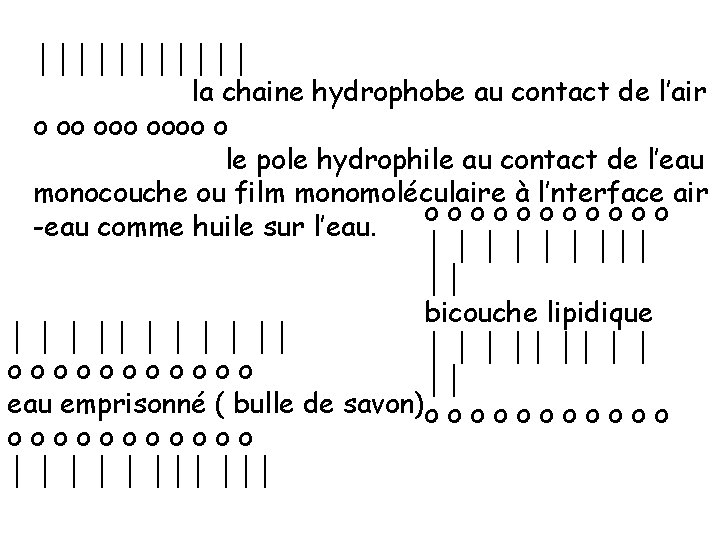
││││││ la chaine hydrophobe au contact de l’air o oo oooo o le pole hydrophile au contact de l’eau monocouche ou film monomoléculaire à l’nterface air oooooo -eau comme huile sur l’eau. │ │ │ │││ ││ bicouche lipidique │ │ │ ││ ││ │ │ oooooo ││ eau emprisonné ( bulle de savon)o o o oooooo │ │ │││ │││

d) Propriétés spectrales Les acides gras sont incolores, mais si présence de doubles liaisons conjuguées, ils auront un spectre à l’U. V. Remarque : Si des positions sont en position malonique, on peut les rendre en position conjuguée pour avoir un spectre à l’U. V. , pour cela on fait un chauffage à 180° pendant une heure en présence de potasse alcoolique ; c’est une propriété qui permet le dosage des acides gras.

1 -4 -2 - Propriétés chimiques : 1 -4 -2 -1 - Propriétés dues au groupement carboxylique : - Formation de sels : Le traitement d’un acide gras par un hydroxyle métallique (Na. OH, KOH) aboutit à un sel alcalin : savons.

En milieu aqueux, les savons peuvent se dissocier en anions R-COO- , Les anions de type R-COO- abaissent la tension superficielle aux interfaces : ils sont tensioactifs. De cet ensemble de caractéristiques, résultent les propriétés mouillantes, moussantes et émulsionnantes des acides gras, ceci leur donne le pouvoir de solubiliser les graisses.
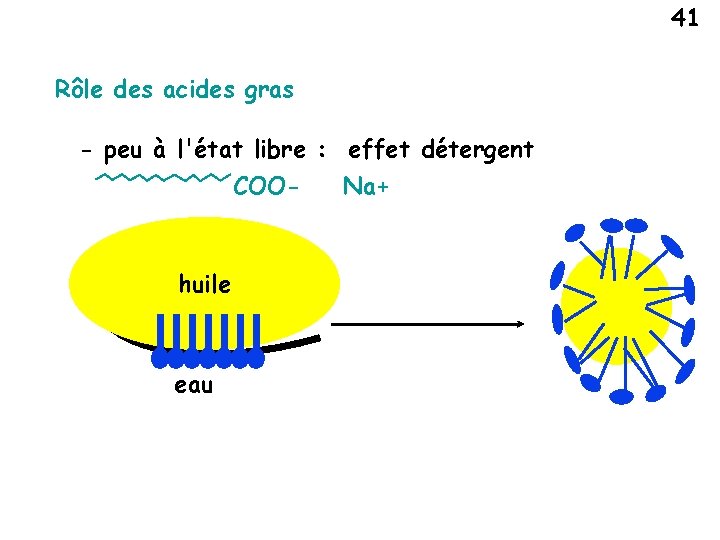
41 Rôle des acides gras - peu à l'état libre : effet détergent COO- huile eau Na+

- Formation d’esters : cette réaction est à la base de le formation de toute les classes de lipides que nous avons vues avec une variété d’alcool (glycérol, alcools aliphatiques, cholestérol). Avec le méthanol, on a des esters d’acides gras volatils ; cette propriété est utilisée pour la séparation et l’identification des acides gras par Chromatographie en phase gazeuse.

1 -4 -2 -2 - Propriétés dues à la présence de double liaisons : - Réactions d’halogénation : ou réaction d’addition; quand un acide gras monoinsaturé est traité par un halogène (Br, I 2) ; on obtient un dérivé dihalogène au niveau des doubles liaisons. Une des applications de cette propriété est la détermination de l’indice d’iode. CH 3 -(CH 2)x-CH=CH-(CH 2)y-COOH + I 2 ↓ CH 3 -(CH 2)x-CHI-(CH 2)y-COOH Indice d’iode Ii = Quantité d’iode en g fixée par 100 g de lipides. La valeur de l’indice d’iode est d’autant plus élevée que le nombre de double liaisons est plus grand.

- Réactions d’hydrogénation : Mécanisme enzymatique ou industriel qui consiste à fixer de l’hydrogène sur une liaison insaturée et conduit aux acides gras saturés correspondants. C’est le durcissement des huiles. CH 3 -(CH 2)x-CH=CH-(CH 2)y-COOH + H 2 ↓ CH 3 -(CH 2)x-CH 2 -(CH 2)y-COOH L’application industrielle de cette opération permet de transformer les huiles végétales en margarine solide à la température ordinaire. Elle fait appel à un catalyseur (nickel) ; l’opération se fait à chaud (100 - 200° C), l’hydrogène étant introduit sous pression.

- Isomérie CIS; TRANS Cette isomérisation est possible par voie chimique en présence de catalyseurs. Acide oléique qui est en Cis donne l’acide Elaidique en Trans Cet acide Elaidique n’est pas un acide gras naturel, il se forme en quantité appréciable au cours de l’hydrogénation catalytique des huiles végétales liquides (fabrication des graisses de cuisson solide comme la margarine). - Migration des doubles liaisons C’est une étape nécessaire pour le dosage spectrophotométrique des AG insaturés, à double liaison malonique.
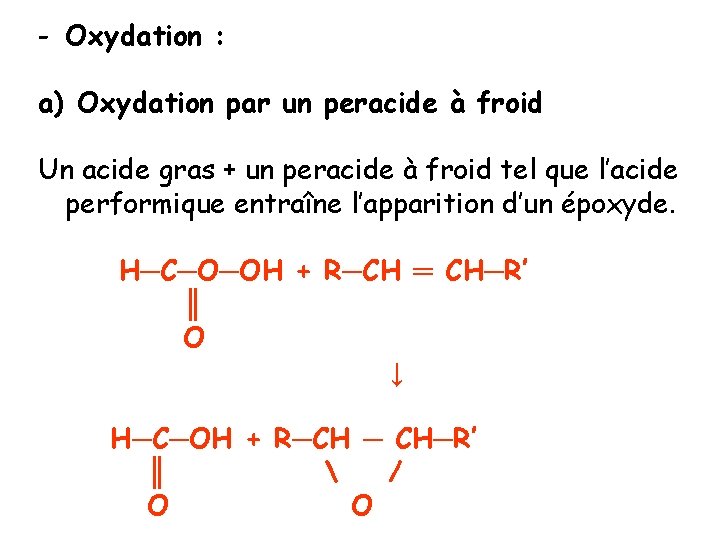
- Oxydation : a) Oxydation par un peracide à froid Un acide gras + un peracide à froid tel que l’acide performique entraîne l’apparition d’un époxyde. H─C─O─OH + R─CH ═ CH─R’ ║ O ↓ H─C─OH + R─CH ─ CH─R’ ║ / O O
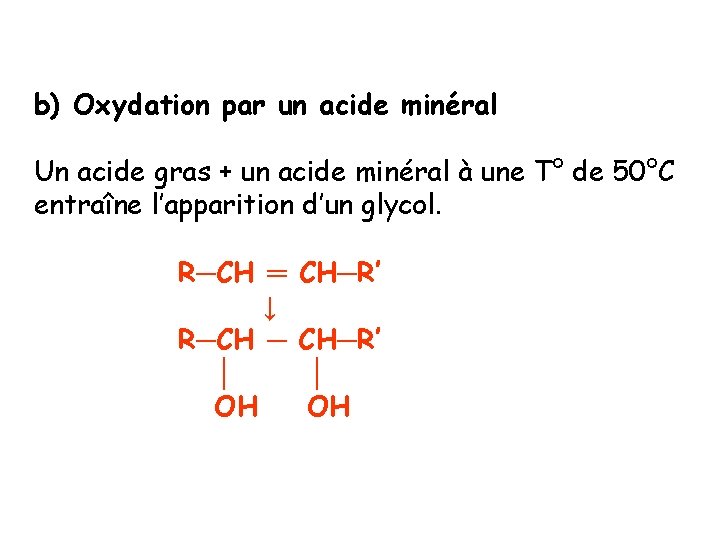
b) Oxydation par un acide minéral Un acide gras + un acide minéral à une T° de 50°C entraîne l’apparition d’un glycol. R─CH ═ ↓ R─CH ─ │ OH CH─R’ │ OH

c) Oxydation par un oxydant puissant Un acide gras insaturé traité par un oxydant puissant tel que: une solution concentrée de KMn. O 4 fait apparaître 2 acides par coupure au niveau de la double liaison. CH 3─(CH 2)5─CH═CH─(CH 2)7─COOH ↓ CH 3─(CH 2)5─COOH + HOOC─(CH 2)7─COOH Monoacide Diacide

d) Auto oxydation des acides gras : - le rancissement, processus qui se déroule normalement à l’air et produit des peroxydes puis, par rupture de la chaine, des aldéhydes responsables de l’odeur rance des graisses, et des acides (tous toxiques). Les doubles liaisons sont facilement oxydables ; si l’oxydation est très énergique, la chaîne carbonée peut être rompue au niveau de la double liaison avec formation de 2 fragments acides : R-CH=CH-(CH 2)n-COOH + 2 O 2 ↓ R-COOH + HOOC-(CH 2)n-COOH Plus le nombre de liaison de l’AG insaturé est élevé, plus l’autooxydation est rapide.

- La siccativité : Par fixation du dioxygéne, les huiles polyinsaturées comme l’huile de lin, Se polymérisent en vernis et solides imperméables.

e) Oxydation biologique - les lipides insaturés des membranes subissent une dégradation lors d’agression oxydation (irradiation ultra-violette, espèces réactives de l’oxygène comme les peroxydes ou les radicaux libres). La vitamine E, composé terpénique, a un effet protecteur contre cette dégradation. - Les oxygénations enzymatiques, par différentes oxygénases, du précurseur acide arachidonique conduisent aux prostaglandines, etc.

2 - LES LIPIDES SIMPLES : Qui sont encore appelés homolipides, sont des corps ternaires (C, H, O). Ils sont des esters d’acides gras que l’on classe en fonction de l’alcool : - Les glycérides ( l’alcool = le glycérol) - Les cérides( l’alcool = alcool à longue chaîne aliphatique) - Les stérides ( l’alcool = le stérol).

2 -1 - LES GLYCERIDES : ou acylglycérols, appelés également graisses neutres, ils constituent la classe de lipides naturels la plus importante. Les glycérides sont des esters d’acides gras et de glycérol. Le glycérol : est un trialcool qui présente 3 possibilités d’estérification. CH 2 OH │ CHOH │ ’ CH 2 OH

Nomenclature des glycérides : Elle est basée sur l’utilisation de 2 critères : - Nombre d’estérifications : on parle d’un monoglycéride lorsqu’une seule fonction OH estérifiée et de diglycéride et triglycéride si 2 et 3 fonctions le sont. selon 2 critères : - Nature des acides gras : un glycérides est dit homogène lorsque les A. G. sont identiques, il est dit hétérogène lorsqu’ils sont différents.
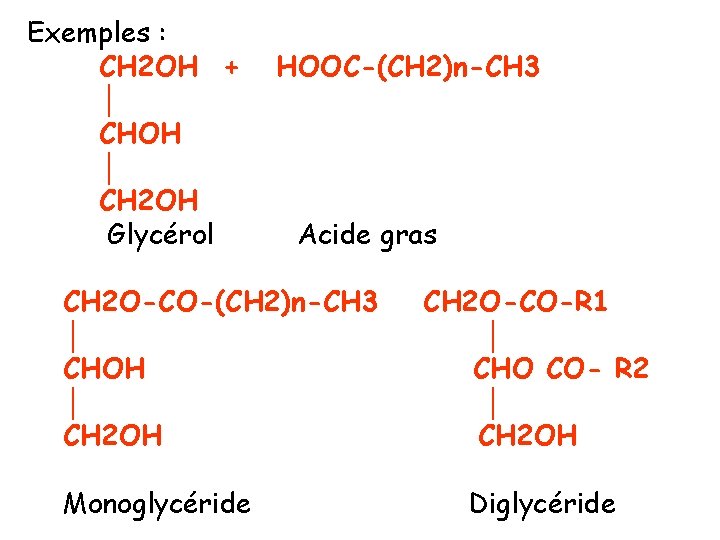
Exemples : CH 2 OH + │ CHOH │ CH 2 OH Glycérol HOOC-(CH 2)n-CH 3 Acide gras CH 2 O-CO-(CH 2)n-CH 3 │ CHOH │ CH 2 OH Monoglycéride CH 2 O-CO-R 1 │ CHO CO- R 2 │ CH 2 OH Diglycéride
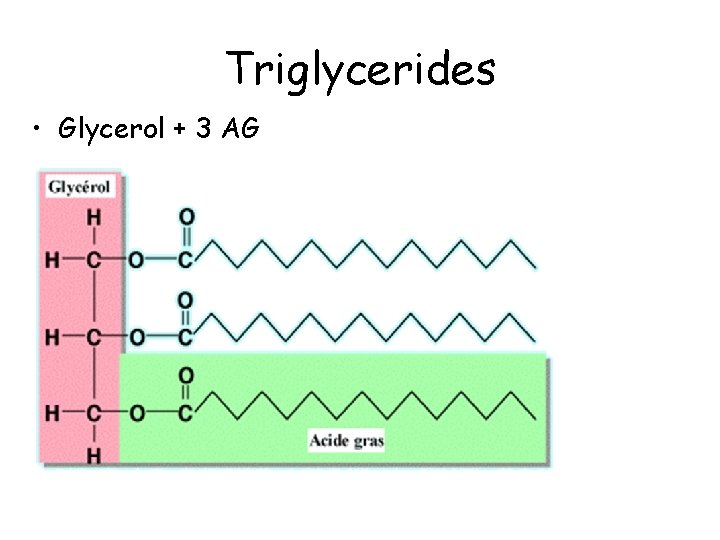
Triglycerides • Glycerol + 3 AG
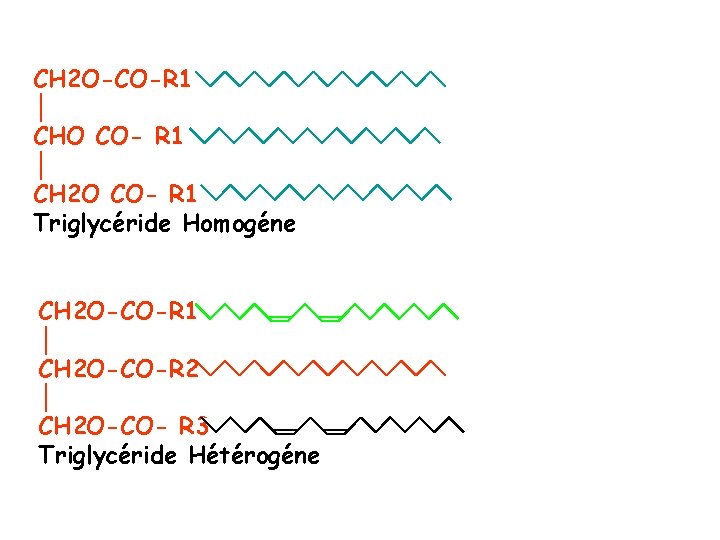
CH 2 O-CO-R 1 │ CHO CO- R 1 │ CH 2 O CO- R 1 Triglycéride Homogéne CH 2 O-CO-R 1 │ CH 2 O-CO-R 2 │ CH 2 O-CO- R 3 Triglycéride Hétérogéne
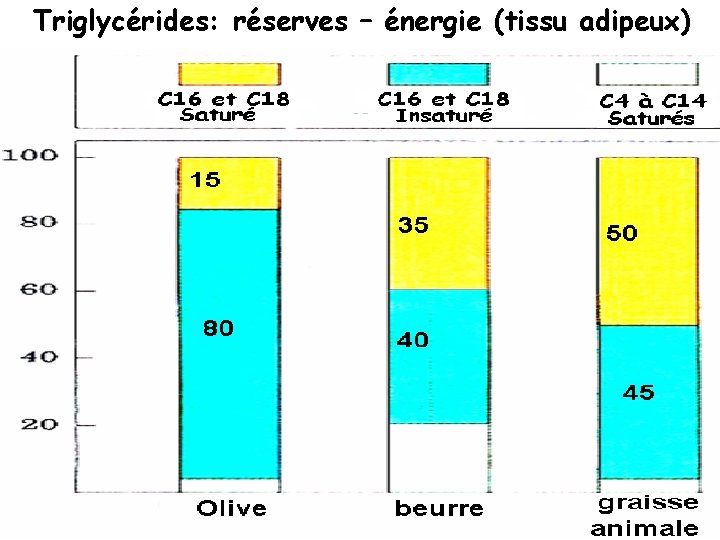
Triglycérides: réserves – énergie (tissu adipeux)

Les triacylglycérols forment la réserve énergétique la plus importante pour l’organisme (graisses de réserve ) et représentent 95% des graisses neutres (apolaires, très hydrophobes ). Ils sont présents: - sous forme de gouttelettes huileuses dans le cytoplasme des cellules spécialisées appelées adipocytes. - graines des plantes Dans l'alimentation : on les trouve dans les huiles végétales, produits laitiers, graisses animales
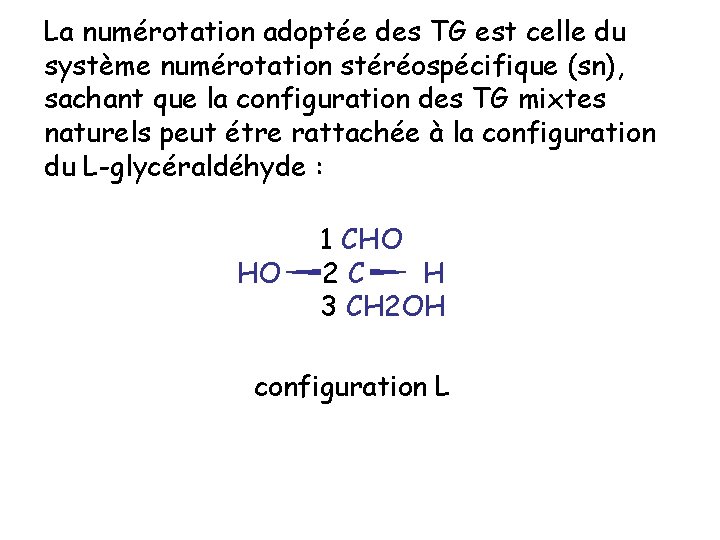
La numérotation adoptée des TG est celle du système numérotation stéréospécifique (sn), sachant que la configuration des TG mixtes naturels peut étre rattachée à la configuration du L-glycéraldéhyde : HO 1 CHO 2 C H 3 CH 2 OH configuration L

1) On considère le glycérol comme dérivant du Lglycéraldéhyde 2) La formule du TG est écrite en sachant que l’OH secondaire est à gauche en projection de Fisher 3) On numérote le squelette du glycérol de haut en bas 4) On décline les groupements acyle précédés du numéro du carbone du squelette du glycérol sur lequel a lieu la liaison ester, suivi de snglycérol 1 CH 2 OH HO -2 C -H 3 CH 2 OH
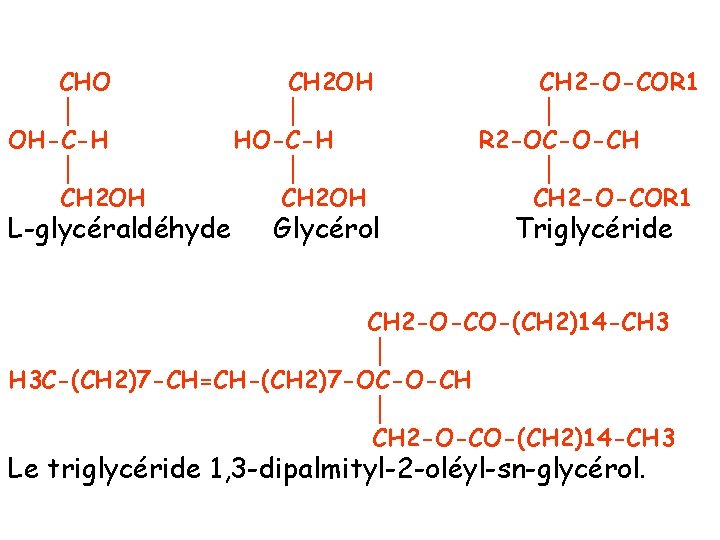
CHO │ OH-C-H │ CH 2 OH L-glycéraldéhyde CH 2 OH │ HO-C-H │ CH 2 OH Glycérol CH 2 -O-COR 1 │ R 2 -OC-O-CH │ CH 2 -O-COR 1 Triglycéride CH 2 -O-CO-(CH 2)14 -CH 3 │ H 3 C-(CH 2)7 -CH=CH-(CH 2)7 -OC-O-CH │ CH 2 -O-CO-(CH 2)14 -CH 3 Le triglycéride 1, 3 -dipalmityl-2 -oléyl-sn-glycérol.

Propriétés des glycérides a) Propriétés physiques Les groupes polaires (hydroxyles ou carboxyle) disparaissent dans les liaisons esters, donc la propriété physique dominante est le caractère complètement apolaire des acylglycérols naturels, essentiellement des TG. - Ils sont insolubles dans l’eau et très solubles dans les solvants apolaires comme l’acétone, - Agités dans l’eau, ils forment des émulsions très instables qui se transforment en système biphasique. Les agents tensioactifs, comme les savons, les dispersent et stabilisent ces émulsions où les TG se mettent en suspension sous forme de micelles

b) Proppriétés chimiques Elles sont celles des chaînes d’acides gras et celles des esters : L’hydrolyse chimique Le traitement acide libère les constituants : les acides gras et du glycérol mais en général de façon incompléte. En milieu acide par l’acide sulfurique H 2 SO 4 à 5% CH 2 O-CO-R CH 2 OH │ │ CHO-CO-R + KOH → CHOH + 3 R-COOH │ │ CH 2 O-CO-R CH 2 OH

L’hydrolyse enzymatique Des lipases hydrolysent les TG avec différentes spécificités.

La saponification: Les triglycérides traités par des bases en solution alcoolique (hydroxyle de sodium ou de potassium (la potasse = KOH)) et à chaud coupent les liaisons esters des glycérides en libérant les acides gras sous formes de sels de sodium (savons durs) ou de potassium (savons mous): CH 2 O-CO-R CH 2 OH │ │ CHO-CO-R + KOH → CHOH + 3 R-COOK │ │ CH 2 O-CO-R CH 2 OH savon

Cette réaction a reçu une application industrielle très large et permet de caractériser les graisses selon leur indice de saponification. L’indice de saponification (Is) : est la quantité de KOH (en mg) nécessaire pour saponifier 1 g de graisse. Plus le poids moléculaire des glycérides est faible (acides gras à courte chaîne), plus le nombre de molécules sera grand et, par conséquent le nombre de molécules de KOH nécessaires à sa saponification sera également élevé.

2 -2 - LES CERIDES : Ils doivent leur nom au fait qu’ils sont les principaux constituants des cires animales, végétales et bactériennes. Les cérides sont des monoesters d’acides gras et d’alcools aliphatiques à longue chaine qui sont en général des alcools primaires, à nombre pair de carbones, saturés et non ramifiés. La longueur des chaines carbonées varie de 14 à 30 carbones pour l’acide gras et de 16 à 36 carbones pour l’alcool gras
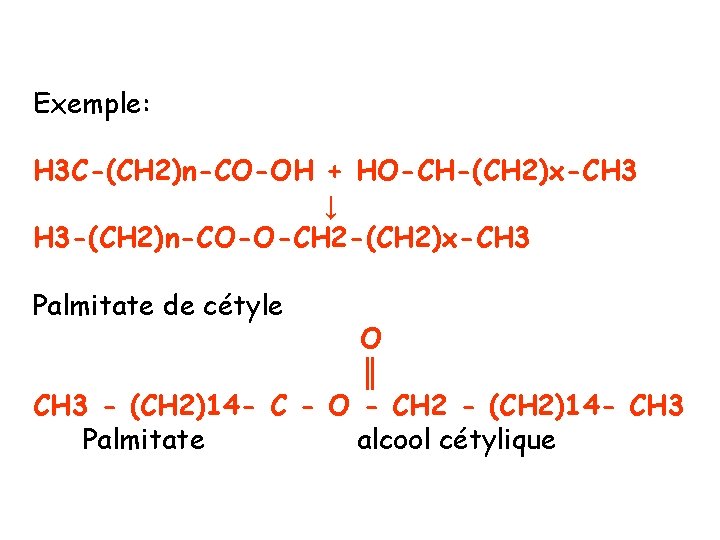
Exemple: H 3 C-(CH 2)n-CO-OH + HO-CH-(CH 2)x-CH 3 ↓ H 3 -(CH 2)n-CO-O-CH 2 -(CH 2)x-CH 3 Palmitate de cétyle O ║ CH 3 - (CH 2)14 - C - O - CH 2 - (CH 2)14 - CH 3 Palmitate alcool cétylique

Propriétés: Les cérides sont des composés à température de fusion élevée (60 à 100°C) et solides à température ordinaire. Ils sont insolubles dans l’eau et seulement solubles à chaud dans les solvants organiques.

Rôles biologiques Ce sont des molécules essentielles des revêtements de protection des organismes vivants, comme enduits imperméabilisant les plumes d’oiseaux aquatiques. On les trouve aussi au niveau de la peau des animaux marins et des fourrures. - Cuticule des feuilles brillantes - Pellicule de fruits qui a un rôle de prévention contre l’évaporation, le développement de moisissures et l’infection par les parasites. - Paroi résistante de bacilles

Remarque: Les animaux supérieurs et l’homme ne métabolisent pas les cires, seuls les insectes en sont capables. Noter bien : De la cire d’abeille à l’huile de Jojoba, ces cérides sont utilisés comme bases des lotions, onguents, pommades, crèmes, fards et aussi dans les enduits et encaustiques.

2 -3 - LES STERIDES : Sont des esters d’acides gras et d’alcools, les stérols. Les stérols constituent une large famille de composés à fonction biochimique et hormonale variée. Le noyau fondamental des stérols (dont le noyau de base est le noyau cyclopentanoperhydrophantréne) Qui est formé de 4 cycles dont un pentagonal, désignés par les lettres A, B, C et D et, d’une chaîne latérale portant des ramifications.
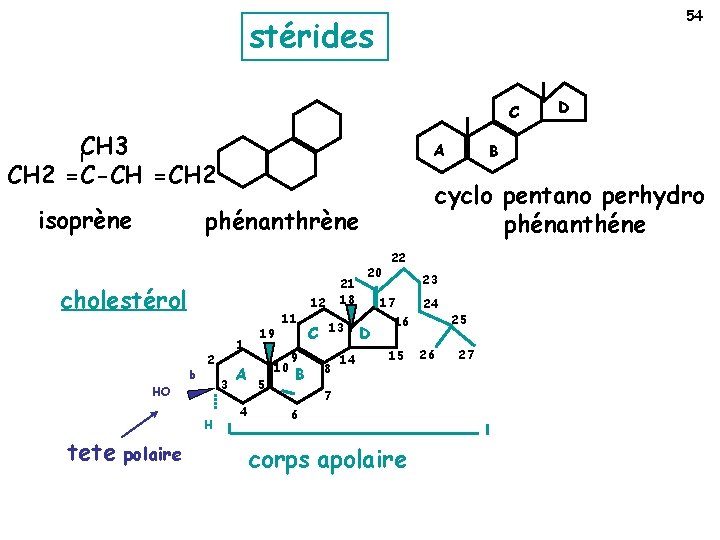
54 stérides C CH 3 CH 2 =C-CH =CH 2 isoprène A cholestérol b 2 3 HO H tete polaire 1 A 4 19 11 10 5 9 B 12 C 13 8 14 B cyclo pentano perhydro phénanthéne phénanthrène 21 18 D 20 22 23 17 D 24 16 15 7 6 corps apolaire 26 25 27
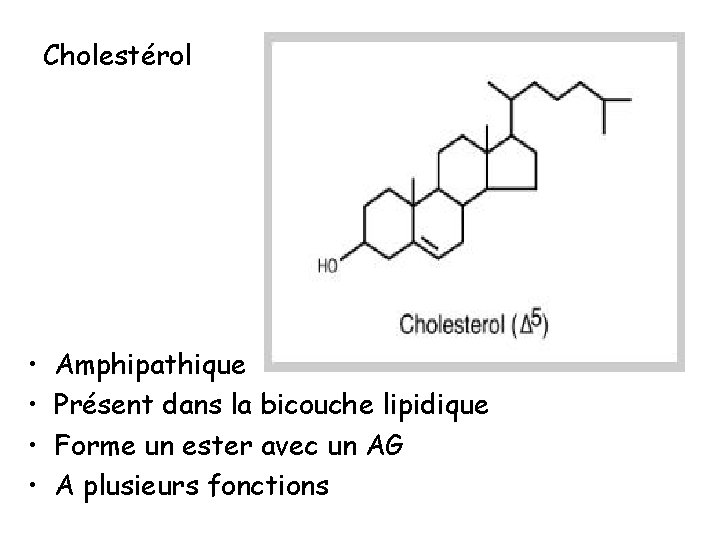
Cholestérol • • Amphipathique Présent dans la bicouche lipidique Forme un ester avec un AG A plusieurs fonctions

Noter Bien: Le cholestérol est le représentant le plus important des stérols chez les animaux supérieurs tant quantitativement qu’en raison des dérivés auxquels il donne naissance (hormones stéroïdes, acides biliaires et les vitamines). Il existe d’autre stérols dans la nature tel que l’ergostérol chez les végétaux. Le cholestérol existe à l’état naturel sous forme libre ou estérifiée dans le sang et dans la plupart des tissus. Il peut former des dépôts pathologiques à l’intérieur des parois des artères (athérosclérose) ou à l’intérieur du canal cholédoque (calculs biliaires).
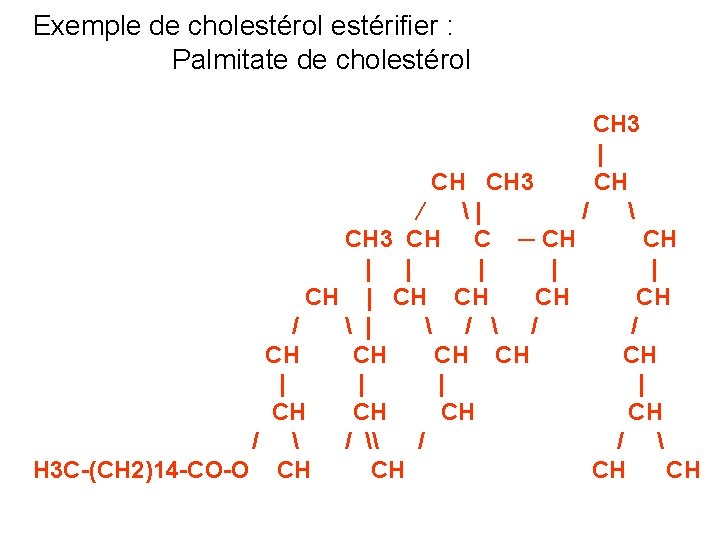
Exemple de cholestérol estérifier : Palmitate de cholestérol CH 3 | CH / CH CH 3 ∕ | CH 3 CH C ─ CH CH | | | CH CH / | / / CH CH CH | | CH CH / \ / / H 3 C-(CH 2)14 -CO-O CH CH
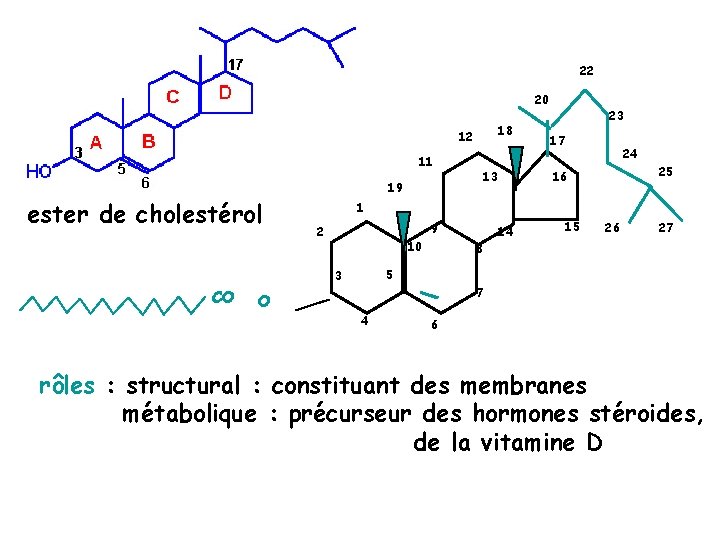
22 20 18 12 11 ester de cholestérol 19 O 17 24 25 16 13 1 9 2 10 14 15 26 27 8 5 3 CO 23 7 4 6 rôles : structural : constituant des membranes métabolique : précurseur des hormones stéroides, de la vitamine D
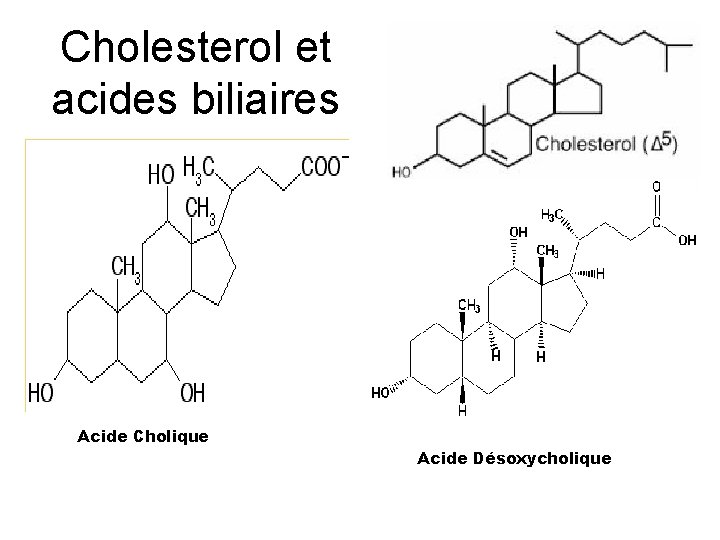
Cholesterol et acides biliaires Acide Cholique Acide Désoxycholique
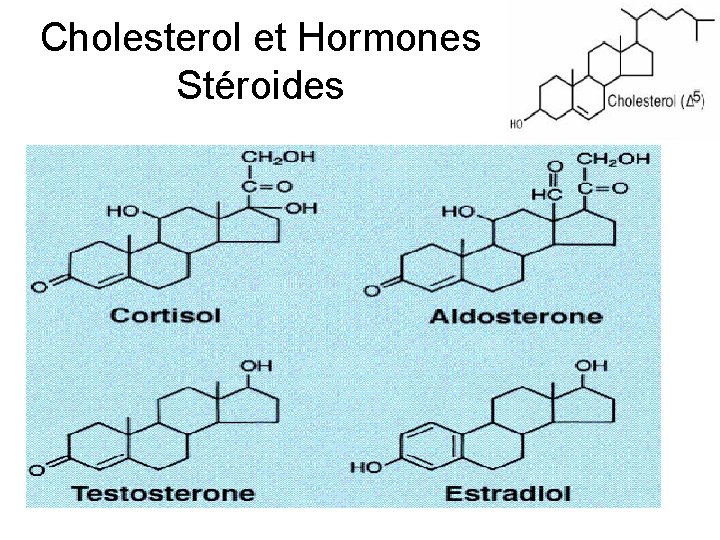
Cholesterol et Hormones Stéroides
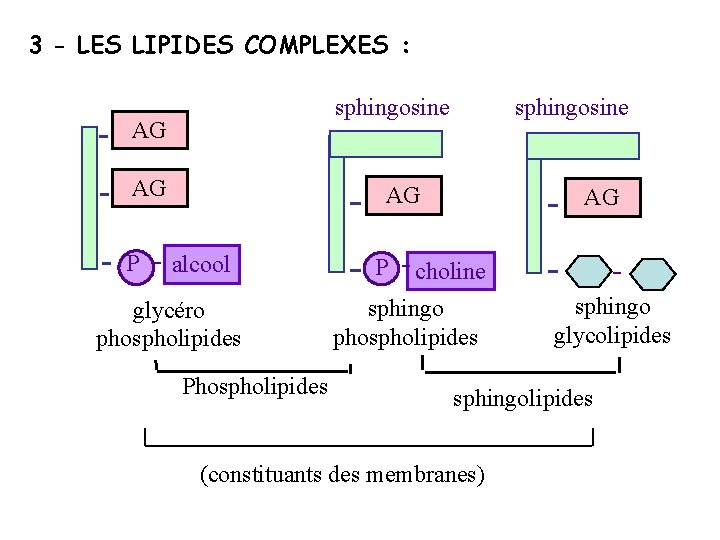
3 - LES LIPIDES COMPLEXES : sphingosine AG AG P sphingosine AG alcool glycéro phospholipides P AG choline sphingo phospholipides sphingo glycolipides sphingolipides (constituants des membranes)
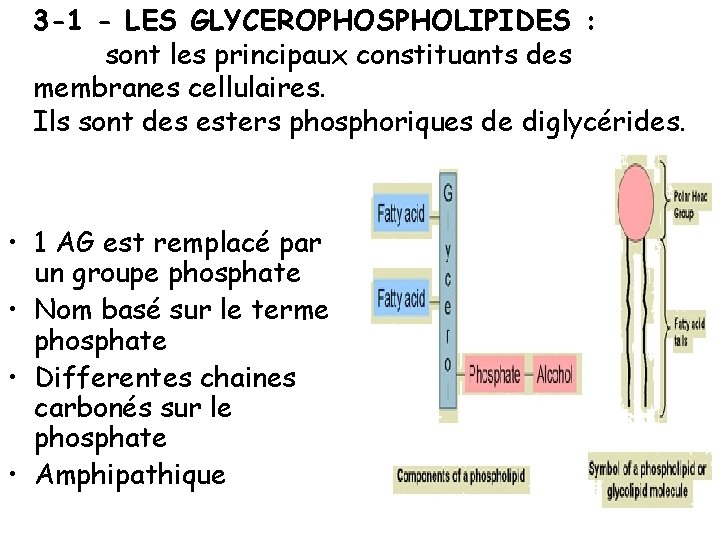
3 -1 - LES GLYCEROPHOSPHOLIPIDES : sont les principaux constituants des membranes cellulaires. Ils sont des esters phosphoriques de diglycérides. • 1 AG est remplacé par un groupe phosphate • Nom basé sur le terme phosphate • Differentes chaines carbonés sur le phosphate • Amphipathique

La molécule de base est l’acide phosphatidique qui est de l’acide glycérophosphorique ou du snglycérol 3 phosphate estérifié par 2 AG au niveau des C 1 et 2. CH 2 O-CO-(CH 2)x-CH 3 │ CHO- CO-(CH 2)y-CH 3 │ CH 2 O-P-OH // O OH l’acide phosphatidique ou AP

Un glycérophospholipide est de l’acide phosphatidique dont l’acide phosphorique estérifié par un alcool aminé ou un polyalcool sans azote XOH CH 2 O-CO-(CH 2)x-CH 3 │ CHO- CO-(CH 2)y-CH 3 │ CH 2 O-P-O-X // O OH Phosphoglycérolipide ou AP-X

- les alcools aminés peuvent étre, la sérine , son produit de décarboxylation, l’éthanolamine, le dérivé N-triméthyle de cette derniere, la choline. - les polyols non azotés comme l’inositol et le glycérol.
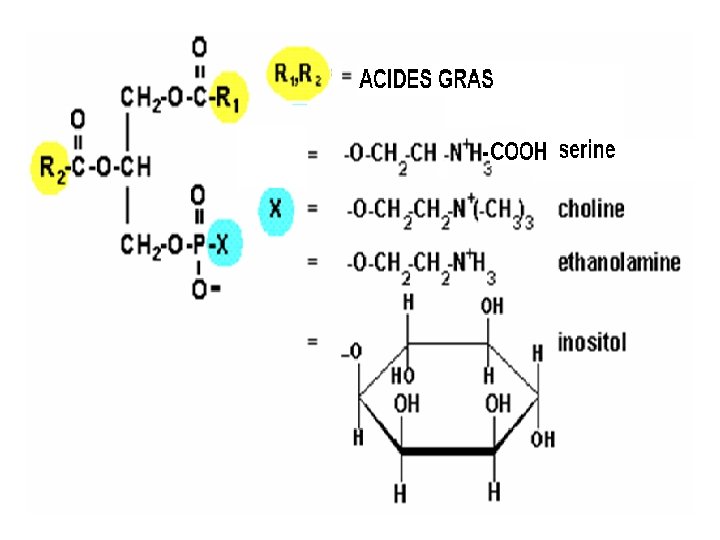
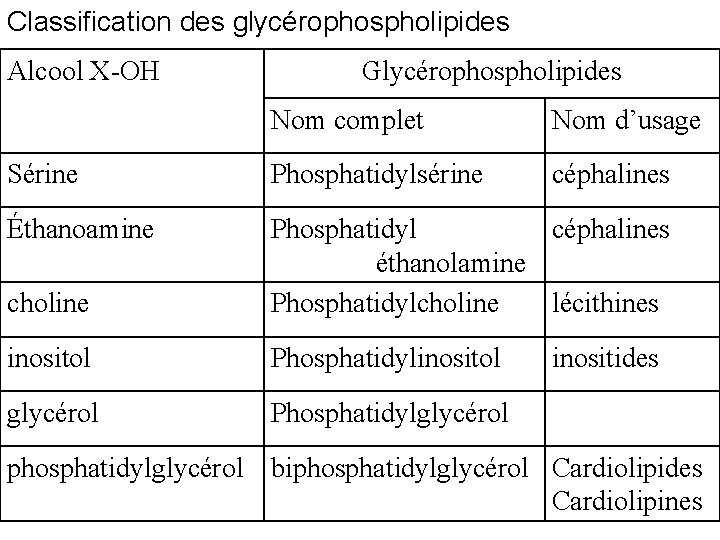
Classification des glycérophospholipides Alcool X-OH Glycérophospholipides Nom complet Nom d’usage Sérine Phosphatidylsérine céphalines Éthanoamine choline Phosphatidyl céphalines éthanolamine Phosphatidylcholine lécithines inositol Phosphatidylinositol glycérol Phosphatidylglycérol inositides phosphatidylglycérol biphosphatidylglycérol Cardiolipides Cardiolipines
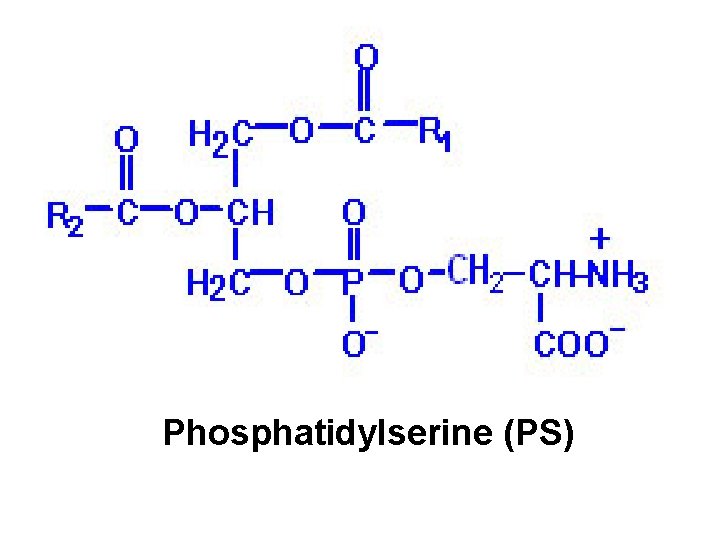
Phosphatidylserine (PS)
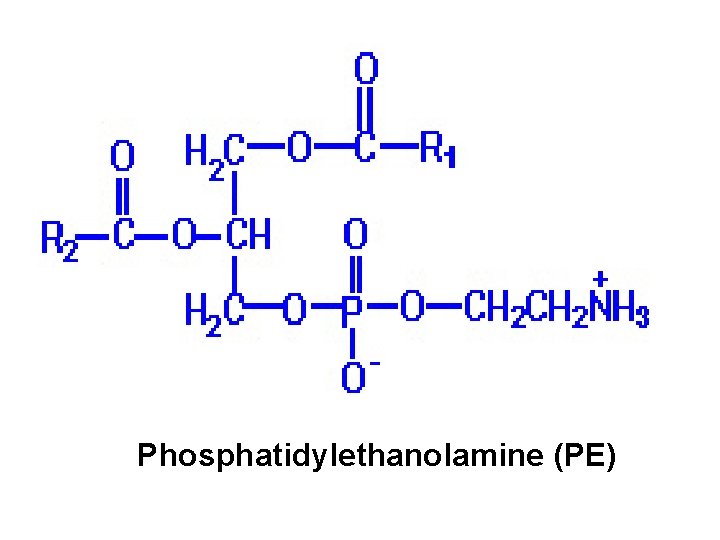
Phosphatidylethanolamine (PE)
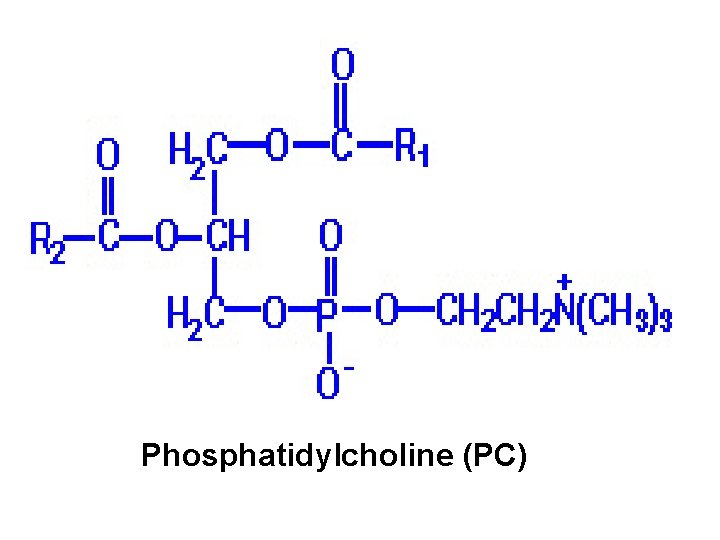
Phosphatidylcholine (PC)
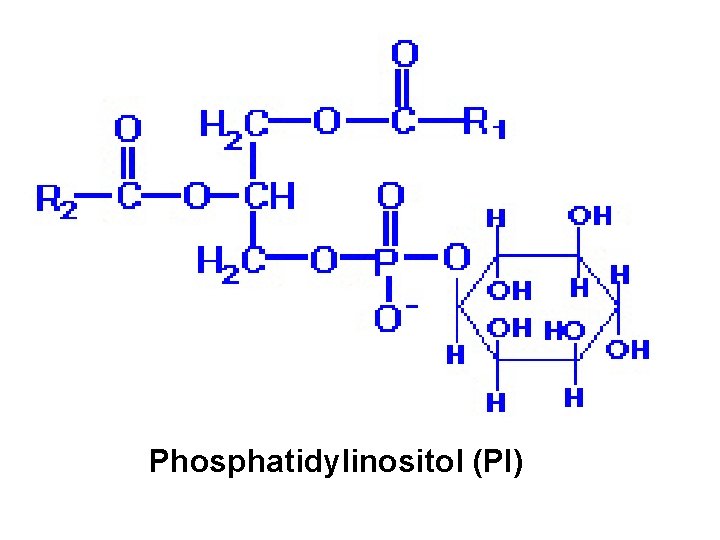
Phosphatidylinositol (PI)
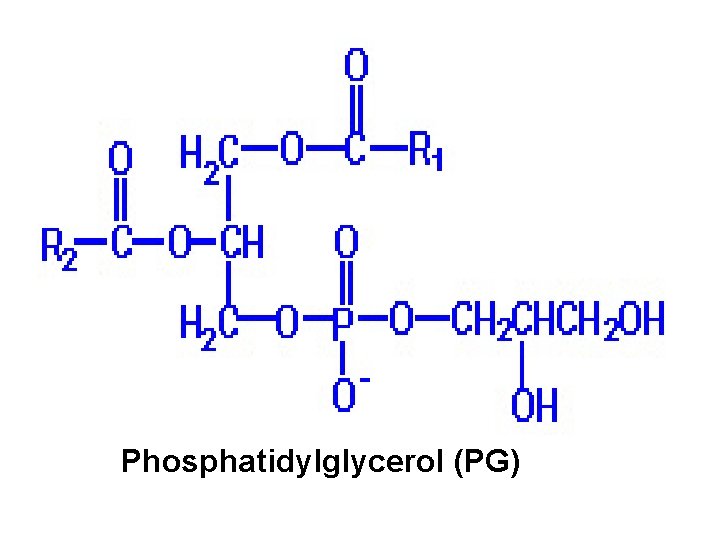
Phosphatidylglycerol (PG)
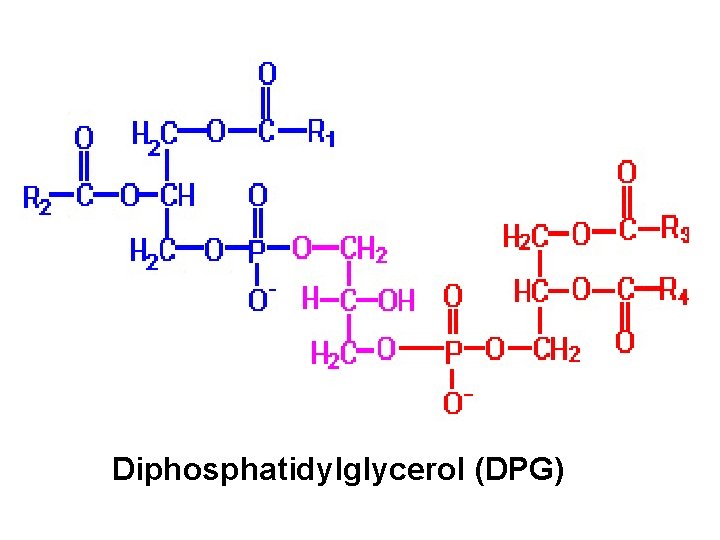
Diphosphatidylglycerol (DPG)
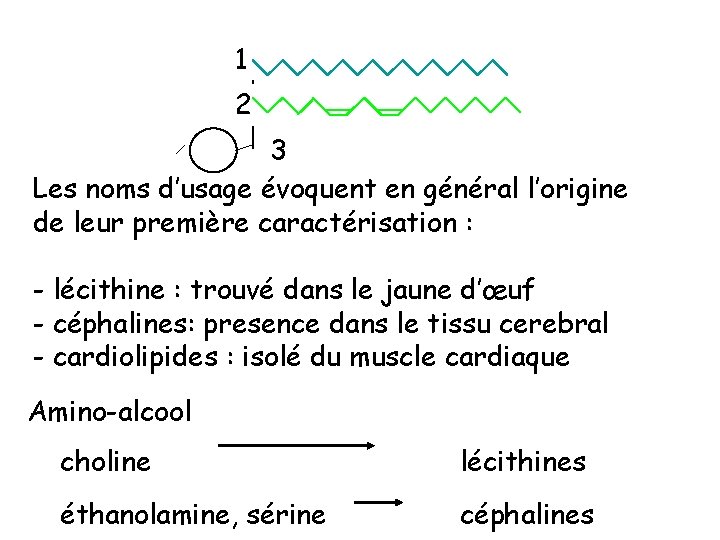
1 2 P 3 Les noms d’usage évoquent en général l’origine de leur première caractérisation : - lécithine : trouvé dans le jaune d’œuf - céphalines: presence dans le tissu cerebral - cardiolipides : isolé du muscle cardiaque Amino-alcool choline lécithines éthanolamine, sérine céphalines
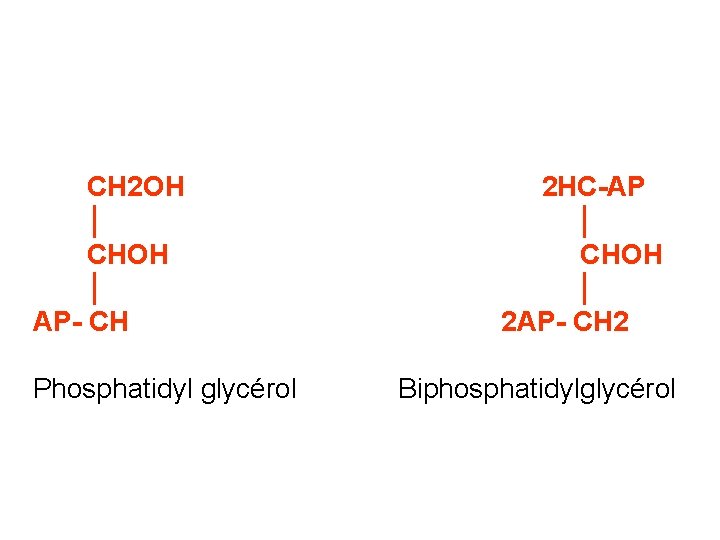
CH 2 OH │ CHOH │ AP- CH Phosphatidyl glycérol 2 HC-AP │ CHOH │ 2 AP- CH 2 Biphosphatidylglycérol

NOTER BIEN : Les lysoglycérophospholipides sont obtenus après l’action d’une phospholipase sur un glycérophospholipide, ( hydrolyse de la liaison ester du C 2 et libération d’un AG)

Propriétés physiques des glycérophopholipides Les glycérophospholipides sont des corps amphiphiles : Une tête polaire et ionisée : le phosphoglycérol substitué Une partie apolaire : les deux queues constituées par les chaînes hydrocarbonées des acides gras. Ils auront une affinité pour les milieux hydrophobes par l’extrémité apolaire et une affinité pour les milieux hydrophiles par l’autre extrémité polaire.
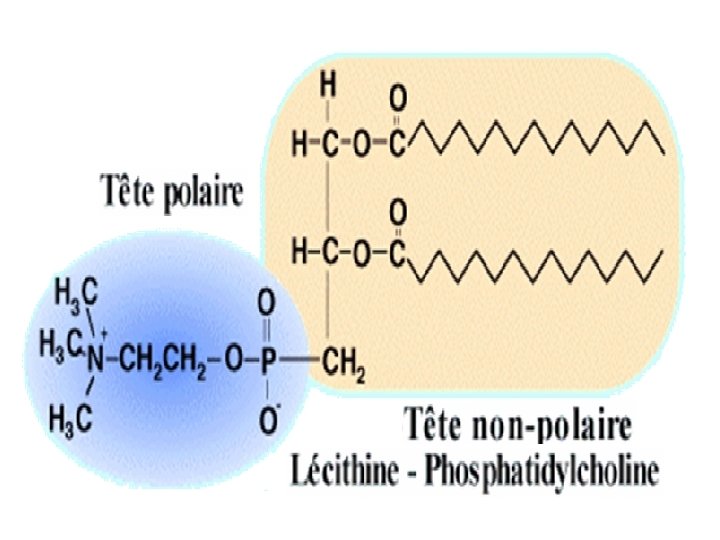

Leur solubilité dans l’eau est très limitée, ils s’organisent en micelles ou en couches (bicouche lipidique sphérique) dont la face externe est hydrophile ainsi que la face interne. En milieu acqueux, les glycérophospholipides ont tendance à s’agréger de manière à dissimuler leur parties hydrophobes et à exposer leur parties hydrophiles ; ils se disposent spontanément en doubles couches dans lesquelles chaînes hydrophobes sont prises en sandwich entre les têtes polaires hydrophiles.
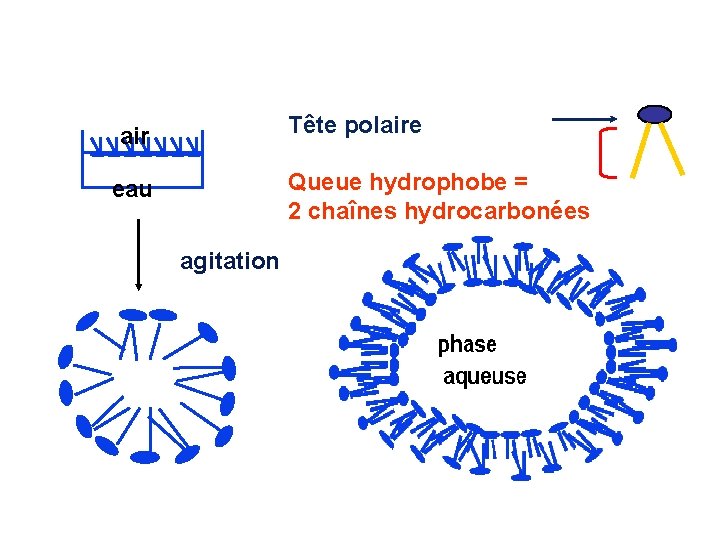
Tête polaire air Queue hydrophobe = 2 chaînes hydrocarbonées eau agitation
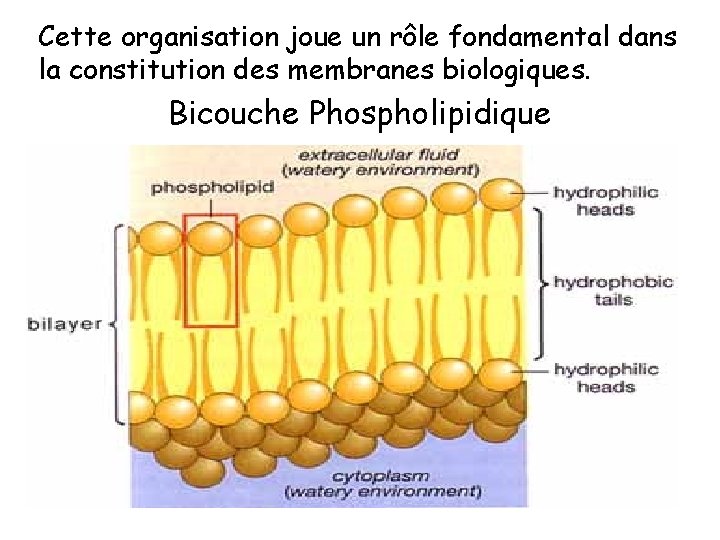
Cette organisation joue un rôle fondamental dans la constitution des membranes biologiques. Bicouche Phospholipidique

" Mer de lipides dans laquelle nagent des protéines"

Ce sont des molécules tensioactives : cette propriété est cruciale au niveau pulmonaire à la surface des alvéoles, dans les échanges gazeux, empêchant les cellules de ces dernières de collapser.

Propriétés des phosphoglycérides Hydrolyse chimique Alcaline douce Libération des AG sous forme de savons + squelette glycérol - acide – alcool Alcaline forte Libération des AG sous forme de savons + Alcool +squelette glycérol-acide. Acide Séparation du glycérol et de l’acide phosphorique qui donne un diglycéride + alcool (X) phosphorylé
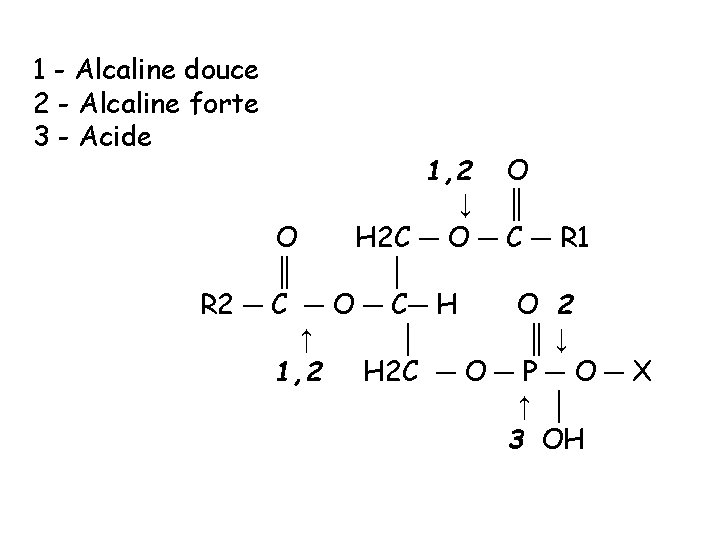
1 - Alcaline douce 2 - Alcaline forte 3 - Acide 1, 2 O ↓ ║ O H 2 C ─ O ─ C ─ R 1 ║ │ R 2 ─ C ─ O ─ C─ H O 2 ↑ │ ║↓ 1, 2 H 2 C ─ O ─ P ─ O ─ X ↑ │ 3 OH

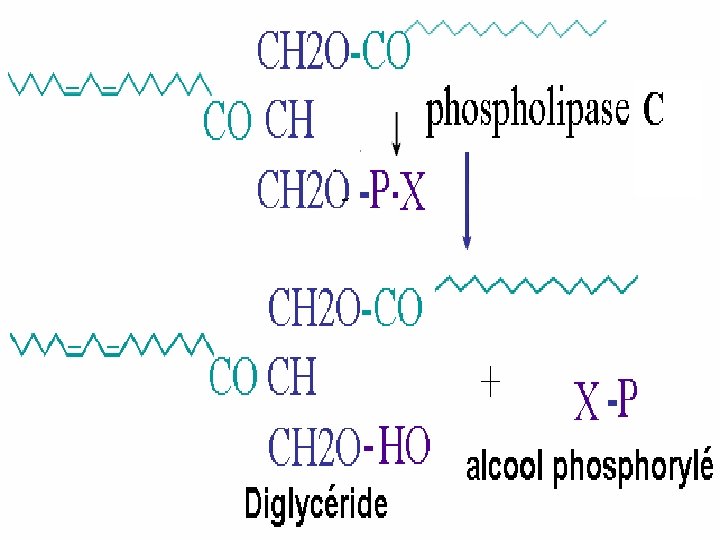
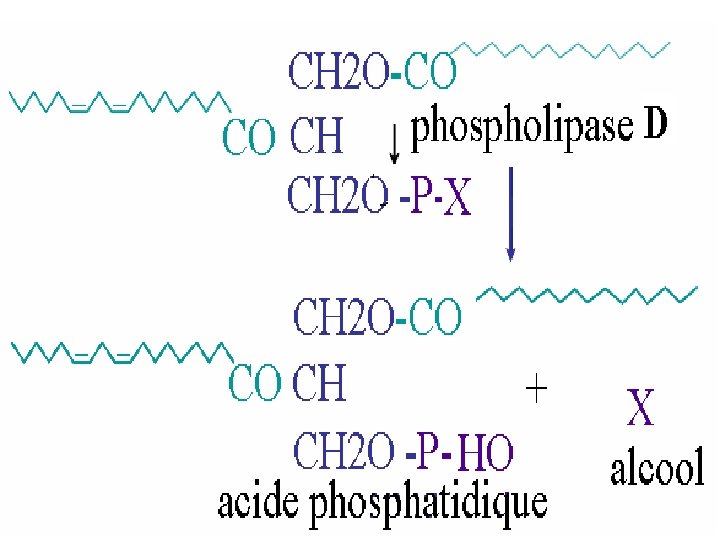
Hydrolyse enzymatique Phospholipase A 1 : extrait du cerveau Phospholipase A 2 : extrait du pancréas ou venin de serpent = lysophospholipide + AG Phospholipase C : extrait des toxines bactériennes = DG 1, 2 + base phosphorylée (phosphorylcholine) Phospholipase D : extrait des plantes = base azotée (choline) + acide phosphatidique Phospholipase B ou lysophospholipase: extrait du pancréas ou de tissus = AG + glycerophosphorylcholine (éthanolamine)
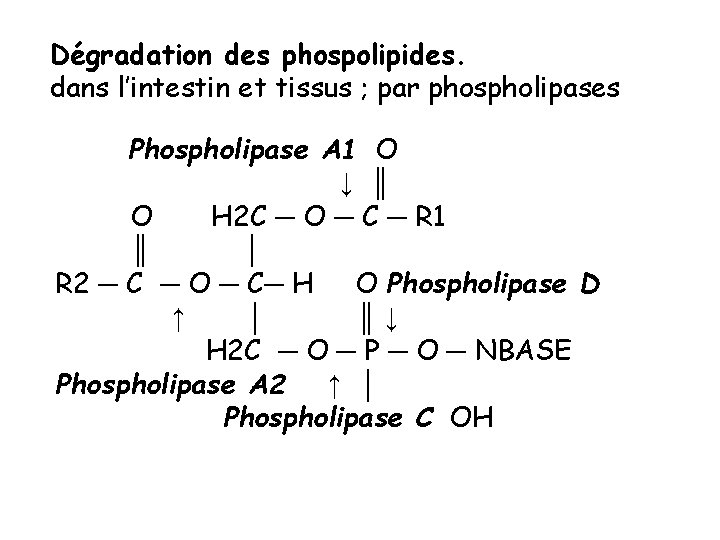
Dégradation des phospolipides. dans l’intestin et tissus ; par phospholipases Phospholipase A 1 O ↓ ║ O H 2 C ─ O ─ C ─ R 1 ║ │ R 2 ─ C ─ O ─ C─ H O Phospholipase D ↑ │ ║↓ H 2 C ─ O ─ P ─ O ─ NBASE Phospholipase A 2 ↑ │ Phospholipase C OH
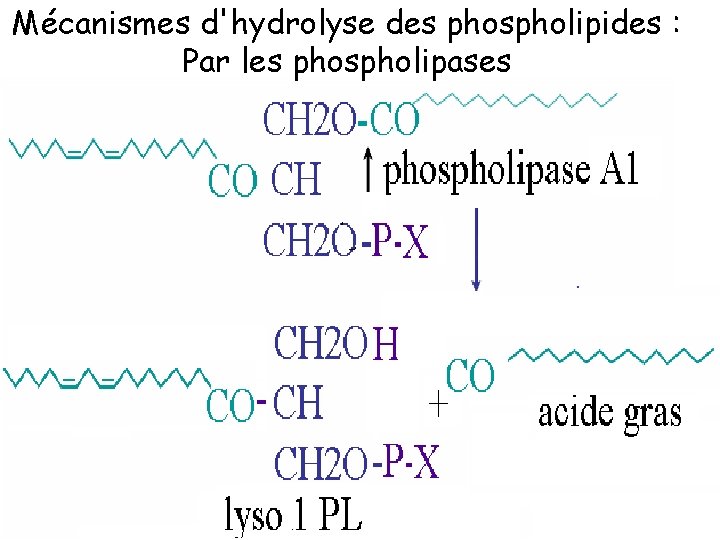
Mécanismes d'hydrolyse des phospholipides : Par les phospholipases
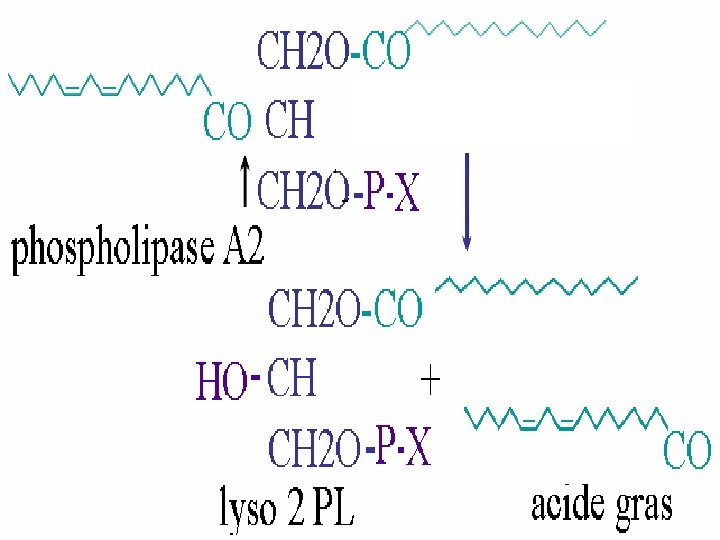

3 -2 - LES SPHINGOLIPIDES : Dans les sphingolipides on trouve un alcool aminé à longue chaîne = la sphingosine : H 3 C-(CH 2)12 -CH═CH-CH-CH-CH 2 -OH │ │ OH NH 2 La fixation d’un AG sur le groupe amine par une liaison amide donne une céramide (=Acide gras + sphingosine) qui est la molécule de base ou précurseur de tous les sphingolipides.
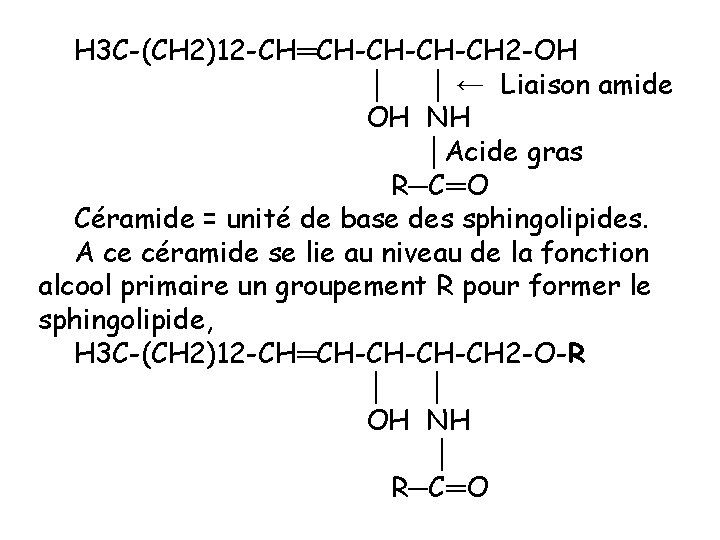
H 3 C-(CH 2)12 -CH═CH-CH-CH-CH 2 -OH │ │ ← Liaison amide OH NH │Acide gras R─C═O Céramide = unité de base des sphingolipides. A ce céramide se lie au niveau de la fonction alcool primaire un groupement R pour former le sphingolipide, H 3 C-(CH 2)12 -CH═CH-CH-CH-CH 2 -O-R │ │ OH NH │ R─C═O
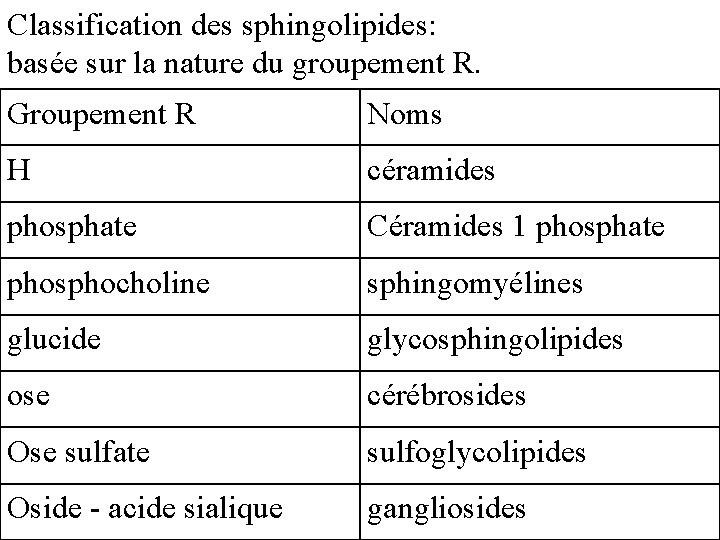
Classification des sphingolipides: basée sur la nature du groupement R. Groupement R Noms H céramides phosphate Céramides 1 phosphate phosphocholine sphingomyélines glucide glycosphingolipides ose cérébrosides Ose sulfate sulfoglycolipides Oside - acide sialique gangliosides
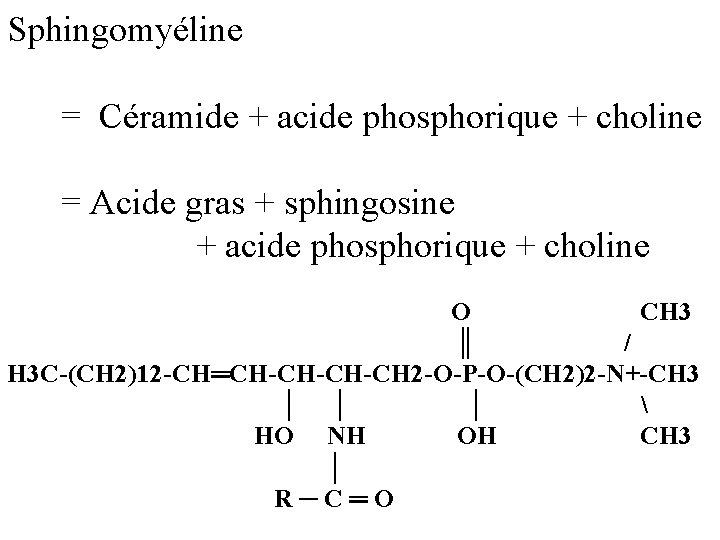
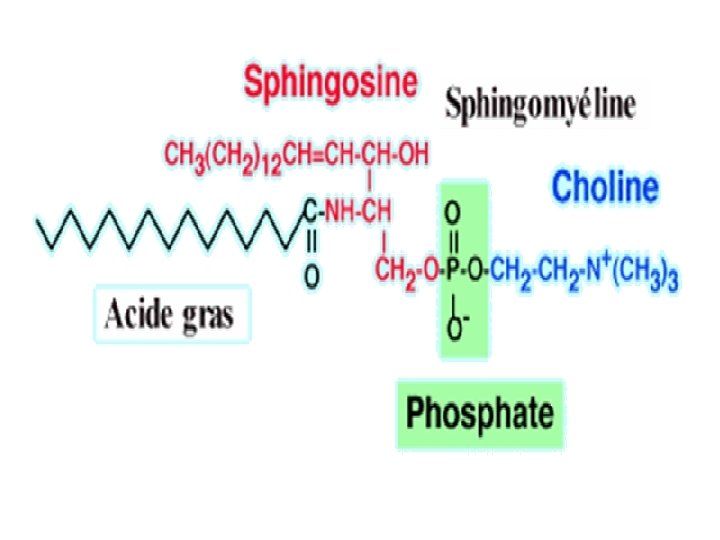
Sphingomyéline = Céramide + acide phosphorique + choline = Acide gras + sphingosine + acide phosphorique + choline O CH 3 ║ / H 3 C-(CH 2)12 -CH═CH-CH-CH-CH 2 -O-P-O-(CH 2)2 -N+-CH 3 │ │ │ HO NH OH CH 3 │ R─C═O

Les composés à caractère lipidique : Ce sont des composés naturels dépourvus d’acides gras, mais qui leur sont apparentés par leurs propriétés physiques et en particulier leur solubilité ; Ce sont surtout les prostaglandines qui sont des dérivés de l’acide polyinsaturé : arachidonique. Ces prostaglandines sont des médiateurs à action extracellulaire : facteurs d’adhérence, d’agrégation plaquettaire, de perméabilité vasculaire ou encore intermédiaire de réaction inflammatoire ou allergie. Leur nom dérivent de leur localisation (prostaglandines ou PG = sécrétion de la prostate).
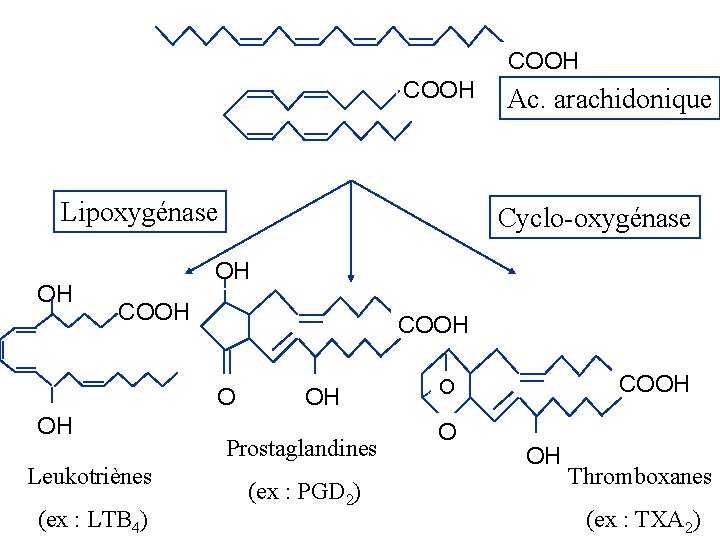
COOH Lipoxygénase OH Ac. arachidonique Cyclo-oxygénase OH COOH O OH Leukotriènes (ex : LTB 4) OH Prostaglandines (ex : PGD 2) COOH O O OH Thromboxanes (ex : TXA 2)
- Slides: 129