1913 Bohr Modelo atmico fundamentado na teoria dos


1913 - Bohr • Modelo atômico fundamentado na teoria dos quanta e sustentado experimentalmente com base na espectroscopia. • Distribuição eletrônica em níveis de energia.

A teoria de Bohr fundamenta-se nos seguintes postulados: • Os elétrons descrevem órbitas circulares estacionárias ao redor do núcleo, sem emitirem nem absorverem energia.
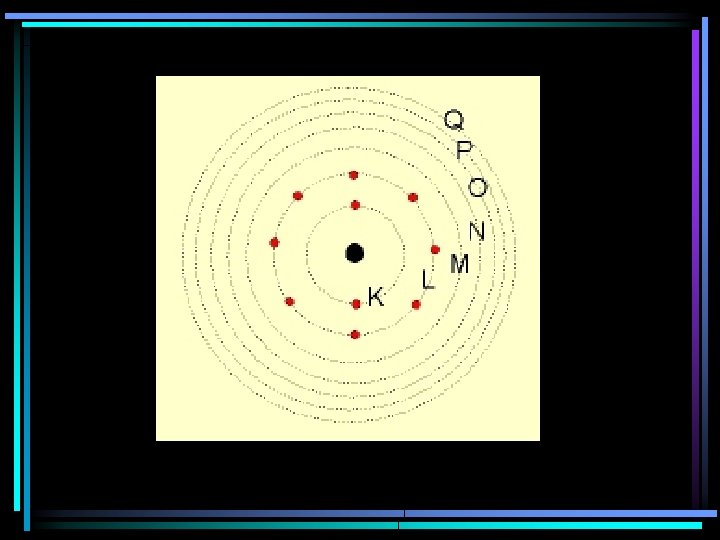

• Fornecendo energia (elétrica, térmica, . . ) a um átomo, um ou mais elétrons a absorvem e saltam para níveis mais afastados do núcleo. Ao voltarem as suas órbitas originais, devolvem a energia recebida em forma de luz (fenômeno observado, tomando como exemplo, uma barra de ferro aquecida ao rubro).
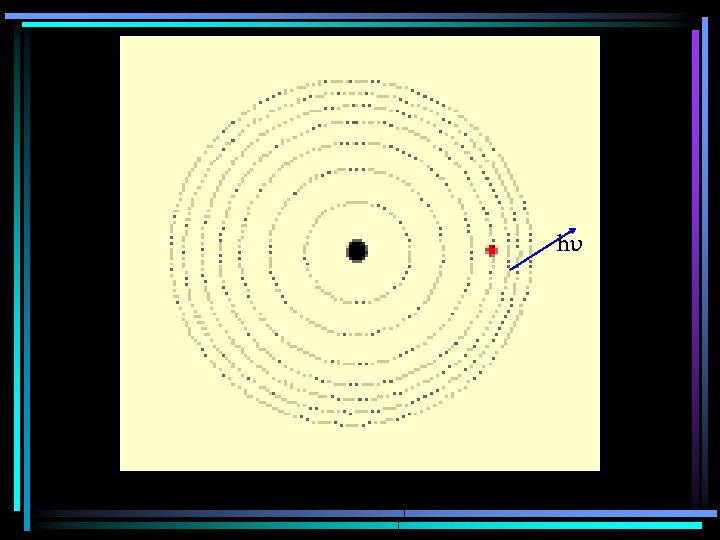


De acordo com Max Planck (1900), quando uma partícula passa de uma situação de maior para outra de menor energia ou vice -versa, a energia é perdida ou recebida em "pacotes" que recebe o nome de quanta (quantum é o singular de quanta).

O quantum é o pacote fundamental de energia e é indivisível. Cada tipo de energia tem o seu quantum. A Teoria Quântica permitiu a identificação dos elétrons de um determinado átomo, surgindo assim os "números quânticos".

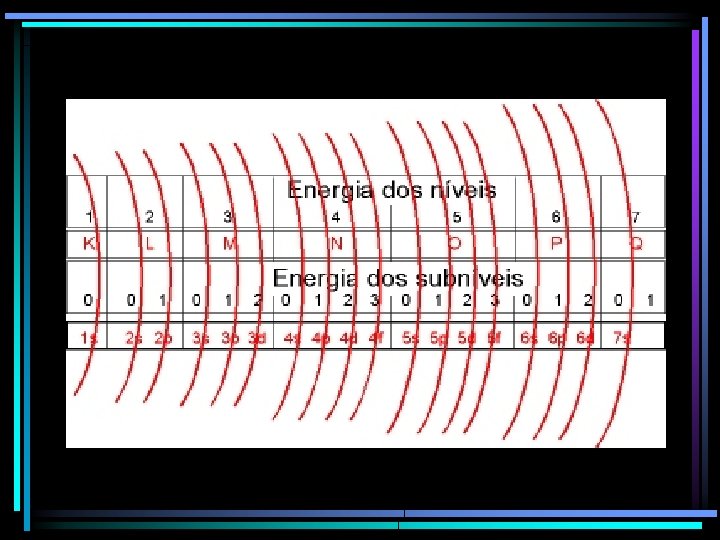
Modelo Atômico de Sommerfeld (1916) Ao pesquisar o átomo, Sommerfeld concluiu que os elétrons de um mesmo nível, ocupam órbitas de trajetórias diferentes (circulares e elípticas) a que denominou de subníveis, que podem ser de quatro tipos: s , p , d , f.

O elétron é uma partícula ou onda?

De acordo com Einstein: E = m c 2 De acordo com Max Planck: E=hν=hc/λ

Juntando as duas expressões: hc / λ = mc 2 Que pode ser reescrita por: h / λ = mc Ou λ = h / mc.

• Princípio da Dualidade de De Broglie • Principio da Incerteza de Heisenberg

Teoria da Mecânica Ondulatória Em 1926, 1926 Erwin Shrödinger teoria chamada de "Teoria Ondulatória" que determinou "orbital" formulou uma da Mecânica o conceito de.

Orbital é a região do espaço ao redor do núcleo onde existe a máxima probabilidade de se encontrar o elétron.
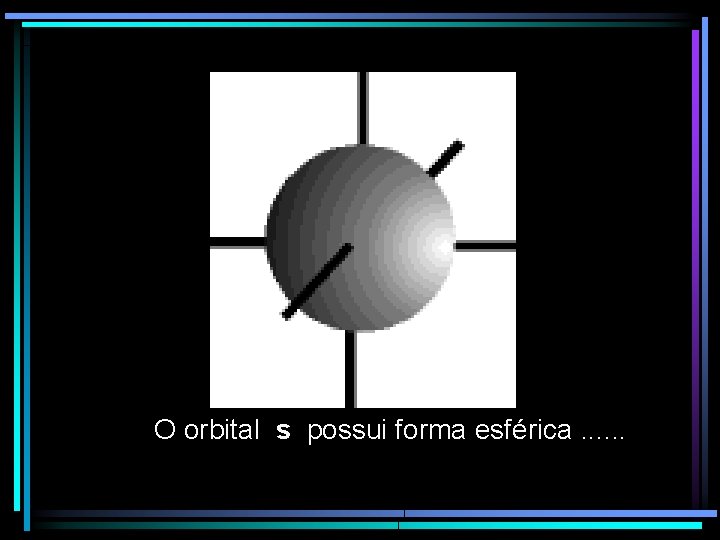
O orbital s possui forma esférica. . .
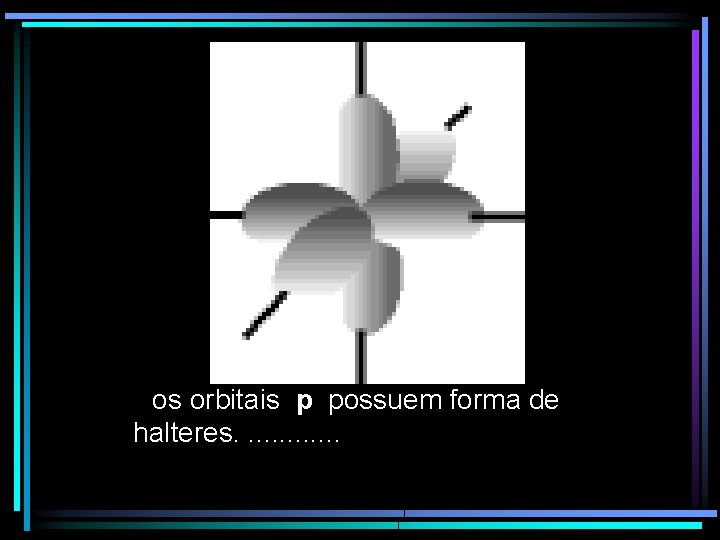
os orbitais p possuem forma de halteres. . . e

Principio da Exclusão de Pauli Em um orbital podemos encontrar, até no máximo, dois elétrons com spins contrários.

Logo: • Subnível s: 1 orbital com 2 elétrons. • Subnível p: 3 orbitais, resultando em 6 elétrons. • Subnível d: 5 orbitais, resultando em 10 elétrons. • Subnível f: 7 orbitais, resultando em 14 elétrons.

Então: Camada Camada K (nível 1) – subnível s L (nível 2) – subníveis s e p M (nível 3) – subníveis s, p e d N (nível 4) – subníveis s, p, d e f O (nível 5) – subníveis s, p, d e f P (nível 6) – subníveis s, p e d Q (nível 7) – subníveis s e p

Diagrama de Pauling 1 s 2 s 3 s 4 s 5 s 6 s 7 s 2 p 3 p 4 p 5 p 6 p 7 p 3 d 4 d 4 f 5 d 5 f 6 d 1 s 2 = 2 elétrons no 1º nível, subnível s

VAMOS EXERCITAR?
- Slides: 24