18 Oktober 2018 UNIVERSITAS MUHAMMADIYAH PALANGKA RAYA METODE

18 Oktober 2018 UNIVERSITAS MUHAMMADIYAH PALANGKA RAYA METODE PERHITUNGAN ISOTONIS OLEH RABIATUL ADAWIYAH (MUHAMMAD PRIYADI) PROGRAM STUDI D 3 FARMASI FAKULTAS ILMU KESEHATAN

METODE PERHITUNGAN ISOTONIS 1. Metode ekivalensi Na. Cl (E) 2. Penurunan titik beku (ΔTf) 3. Metode Liso

METODE EKIVALENSI NACL (E) Suatu faktor yang dikonversikan terhadap sejumlah tertentu zat terlarut terhadap jumlah Na. Cl yang memberikan efek osmotik yang sama (isoosmotik) atau ekivalensi Na. Cl memberikan jumlah Na. Cl (g) yang menghasilkan tekanan osmotik sama seperti 1 g bahan obat dengan syarat bahwa baik natrium klorida maupun bahan obat berada dalam larutan bervolume sama. Misalnya ekivalensi obat X terhadap Na. Cl adalah 0, 5 yang berarti 1 g obat X di dalam larutan memberikan jumlah partikel yang sama dengan 0, 5 g Na. Cl. Nilai E pada literatur dapat bervariasi, tergantung pada konsentrasi bahan, pemilihan E didasarkan pada konsentrasi yang paling mendekati konsentrasi bahan yang digunakan dalam formula. Nilai E dapat dilihat pada FI IV hal. 1236
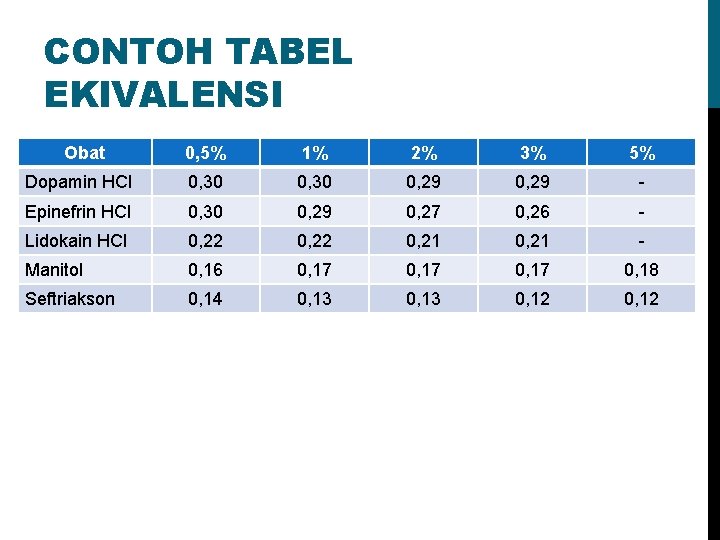
CONTOH TABEL EKIVALENSI Obat 0, 5% 1% 2% 3% 5% Dopamin HCl 0, 30 0, 29 - Epinefrin HCl 0, 30 0, 29 0, 27 0, 26 - Lidokain HCl 0, 22 0, 21 - Manitol 0, 16 0, 17 0, 18 Seftriakson 0, 14 0, 13 0, 12

CONTOH SOAL 1. Suatu industri ingin membuat sediaan Manitol 3% berapakah jumlah Na. Cl yang perlu ditambahkan agar isotonis ? (nilai E manitol = 0, 17) Jawab : Nilai ekivalensi manitol = 3% x 0, 17 = 0, 51% Kebutuhan Na. Cl = 0, 9%- 0, 51% = 0, 39% (0, 39 g/100 m. L)

Dibuat Dopamin 0, 5% berapa diperlukan (E dopamin = 0, 30) : Na. Cl yang Jawab : Ekivalensi dopamin = 0, 5 x 0, 30 = 0, 15 % Kebutuhan Na. Cl = 0, 9% - 0, 15% = 0, 75% ( 0, 75 g/100 m. L) atau 7, 5 mg/m. L

PENURUNAN TITIK BEKU (ΔTF) Titik beku darah dan airmata = - 0, 52 OC karena dalam darah ada komponen bahan terlarut maupun bahan lain. Larutan yang mempunyai Titik Beku = - 0, 52 OC disebut mempunyai tekanan osmosis yang sama dengan darah atau airmata (isoosmotik) Suatu sediaan dikatakan isotonis jika mengakibatkan penurunan titik beku (ΔTf) sebanyak 0, 52 dari titik beku pelarut murni yang digunakan. ΔTf = 0, 52 ini adalah penurunan titik beku yang diakibatkan oleh 0, 9% Na. Cl atau 5, 5% Dekstrosa dalam air. Nilai ΔTf dapat dilihat pada FI IV hal. 1236 0, 52 - A W = -------B W = Berat zat pengisotoni (g) dalam 100 ml larutan A = Penurunan titik beku air oleh zat terlarut yang belum isotoni B = Penurunan titik beku 1% b/v larutan zat pengisotoni
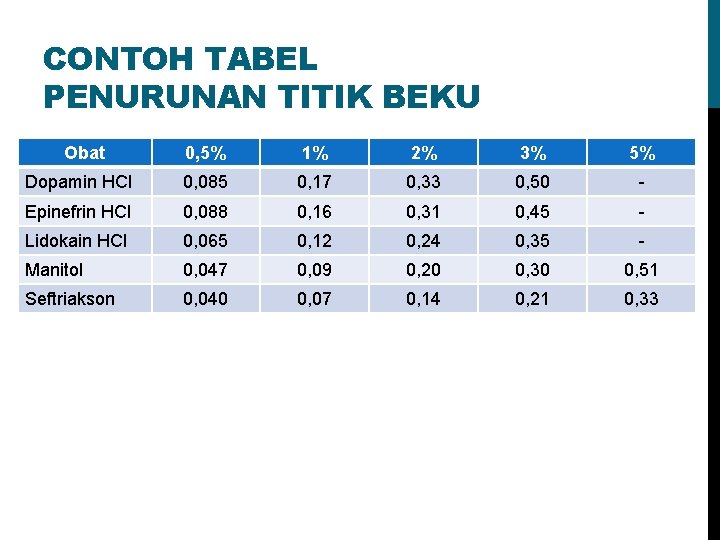
CONTOH TABEL PENURUNAN TITIK BEKU Obat 0, 5% 1% 2% 3% 5% Dopamin HCl 0, 085 0, 17 0, 33 0, 50 - Epinefrin HCl 0, 088 0, 16 0, 31 0, 45 - Lidokain HCl 0, 065 0, 12 0, 24 0, 35 - Manitol 0, 047 0, 09 0, 20 0, 30 0, 51 Seftriakson 0, 040 0, 07 0, 14 0, 21 0, 33

CONTOH SOAL 1. Suatu industri ingin membuat sediaan seftriakson 0, 5 % berapakah jumlah Na. Cl yang perlu ditambahkan agar isotonis ? (nilai ΔTf seftriakson = 0, 040) Jawab : Nilai penurunan titik beku seftriakson = 0, 5% x 0, 040 = 0, 02 W = (0, 52 - A)/B W = (0, 52 - 0, 02)/ 0, 52 = 0, 9615 x 0, 9% Na. Cl = 0, 86535 %

METODE LISO Metode ini dipakai jika data E dan ΔTf tidak diketahui. Dengan menggunakan Liso dapat dicari harga E atau ΔTf zat lalu perhitungan tonisitas dapat dilanjutkan seperti cara di atas.
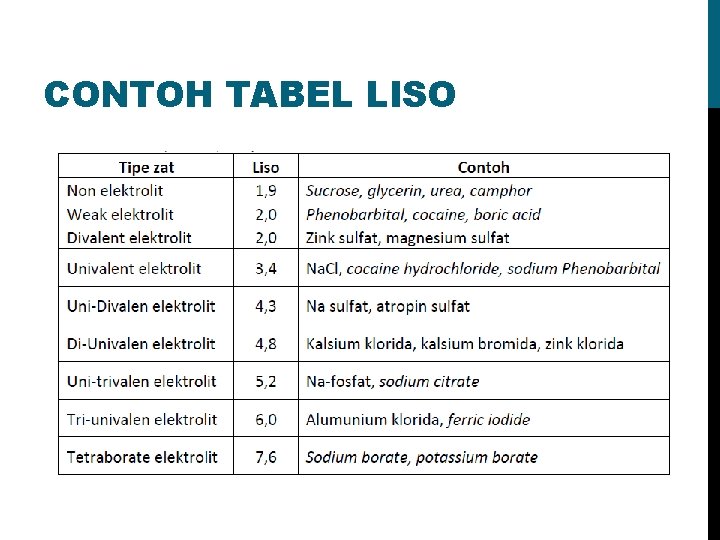
CONTOH TABEL LISO

CONTOH SOAL Suatu industri ingin membuat sediaan Manitol 5% berapakah jumlah Na. Cl yang perlu ditambahkan agar isotonis ? (BM Manitol =182, 17) Jawab : E = 17 (Liso/M) E = 17 X ( 1, 9/182, 17) = 0, 1773 *Nilai ekivalensi manitol = 5% x 0, 1773 = 0, 8865 % *Kebutuhan Na. Cl = 0, 9 % - 0, 8865 % = 0, 0135 % (0, 0135 g/100 m. L)

PUSTAKA 1. DEPKES. 1994. Farmakope Indonesia IV. Jakarta. 2. Allen, Popovich, Ansel. 2011. Ansel’s Pharmaceutical Dosage Forms and Drug Delivery Systems. Edisi ke 9. 3. Kemenkes. 2016. Praktikum Teknologi Sediaan Steril. Jakarta.

TERIMA KASIH “Berpikir positif dan optimis“
- Slides: 14