15 Minutos Sobre Terapia Adyuvante en Cncer del

15 Minutos Sobre Terapia Adyuvante en Cáncer del Pulmón de Células No Pequeñas Mauricio Lema, MD Oncología Clínica / Hematología Director Médico Clínica de Oncología Astorga Medellín, Colombia Oncología Clínica / Hematología Clínica SOMA Medellín, Colombia

Conflictos de Interés: Mauricio Lema Ninguno para esta conferencia

Terapia adyuvante Terapia sistémica que se administra después de cirugía (o radioterapia) potencialmente curativa Incrementa supervivencia erradicando micrometástasis no reseca(das/bles) Cuando se administra ANTES de la terapia locorregional potencialmente curativa se denomina NEOADYUVANTE

Tratamiento Adyuvante en Cáncer del Pulmón de Células No Pequeñas - NSCLC -
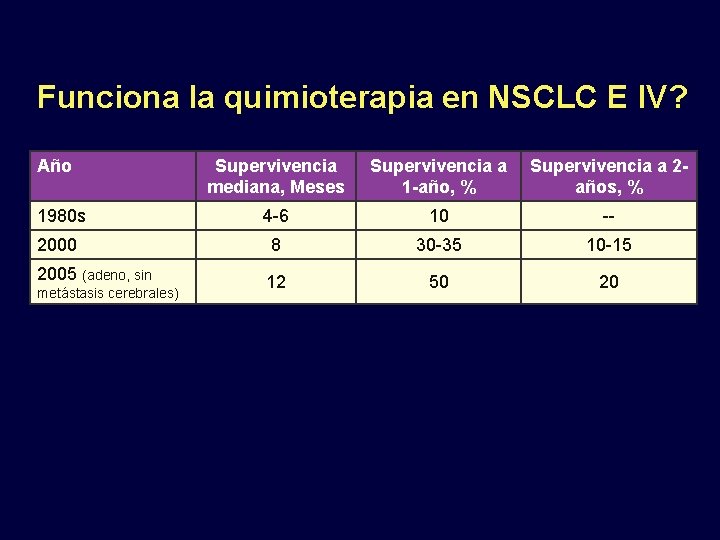
Funciona la quimioterapia en NSCLC E IV? Año Supervivencia mediana, Meses Supervivencia a 1 -año, % Supervivencia a 2 años, % 1980 s 4 -6 10 -- 2000 8 30 -35 10 -15 2005 (adeno, sin 12 50 20 metástasis cerebrales)

Meta-análisis de quimioterapia con Cisplatino en NSCLC 8 estudios clínicos basados en cisplatino (n = 1394) – Pacientes aleatorizados a Cirugía sóla o Cirugía + Quimioterapia Reducción del 13% en el riesgo de muerte en el grupo de pacientes tratados con cirugía + quimioterapia adyuvante vs cirugía sóla (P =. 08) Non-Small Cell Lung Cancer Collaborative Group. BMJ. 1995; 311: 889 -890.
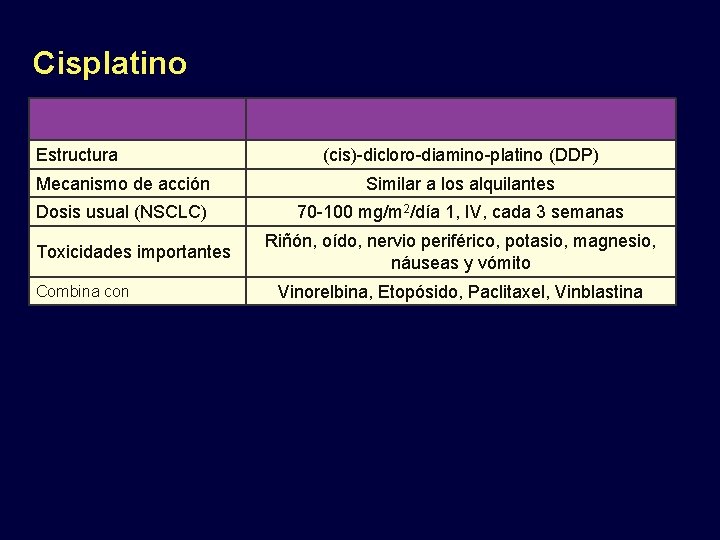
Cisplatino Estructura (cis)-dicloro-diamino-platino (DDP) Mecanismo de acción Similar a los alquilantes Dosis usual (NSCLC) 70 -100 mg/m 2/día 1, IV, cada 3 semanas Toxicidades importantes Combina con Riñón, oído, nervio periférico, potasio, magnesio, náuseas y vómito Vinorelbina, Etopósido, Paclitaxel, Vinblastina

IALT: Terapia basada en Cisplatino luego de resección en NSCLC Pacientes con NSCLC estadío I-III de 18 -75 años de edad, sin historia de cáncer, después de una resección quirúrgica completa* Quimioterapia basada en Cisplatino† (n = 932) No quimioterapia (n = 935) (N = 1867) *Radioterapia postoperatoria permitida. †Regímenes de quimioterapia: etoposido: 56. 5%; vinorelbina: 26. 8%; vinblastina: 11. 0%; vindesina: 5. 8%. Arriagada R, et al. N Engl J Med. 2004; 350: 351 -360.
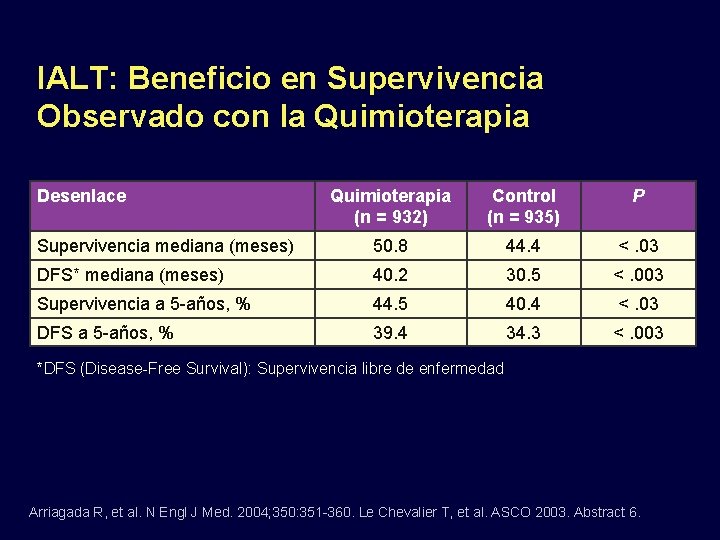
IALT: Beneficio en Supervivencia Observado con la Quimioterapia Desenlace Quimioterapia (n = 932) Control (n = 935) P Supervivencia mediana (meses) 50. 8 44. 4 <. 03 DFS* mediana (meses) 40. 2 30. 5 <. 003 Supervivencia a 5 -años, % 44. 5 40. 4 <. 03 DFS a 5 -años, % 39. 4 34. 3 <. 003 *DFS (Disease-Free Survival): Supervivencia libre de enfermedad Arriagada R, et al. N Engl J Med. 2004; 350: 351 -360. Le Chevalier T, et al. ASCO 2003. Abstract 6.

ANITA: Vinorelbina + Cisplatino Adyuvante vs Observación Abierto, Multicéntrico Delta esperada en la supervivencia global a 2 años: 10% Muertes esperadas: 466 eventos Estratificado por Centro, Estadío, e Histología Pacientes con NSCLC estadío IB-IIIA de 18 -75 años de edad, sin malignidad previa, después de una resección completa* Vinorelbina 30 mg/m 2 IV cada semana x 16 + Cisplatino 100 mg/m 2 IV on Días 1, 29, 57, 85 (n = 407) (N = 840) Observación (n = 433) *Radioterapia postoperatoria permitida. Douillard JY, et al. Lancet Oncol. 2006; 7: 719 -727.
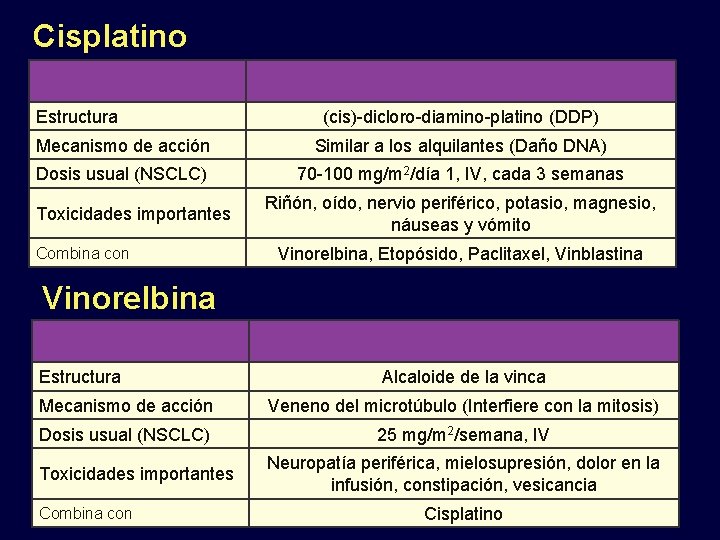
Cisplatino Estructura (cis)-dicloro-diamino-platino (DDP) Mecanismo de acción Similar a los alquilantes (Daño DNA) Dosis usual (NSCLC) 70 -100 mg/m 2/día 1, IV, cada 3 semanas Toxicidades importantes Combina con Riñón, oído, nervio periférico, potasio, magnesio, náuseas y vómito Vinorelbina, Etopósido, Paclitaxel, Vinblastina Vinorelbina Estructura Alcaloide de la vinca Mecanismo de acción Veneno del microtúbulo (Interfiere con la mitosis) Dosis usual (NSCLC) 25 mg/m 2/semana, IV Toxicidades importantes Combina con Neuropatía periférica, mielosupresión, dolor en la infusión, constipación, vesicancia Cisplatino
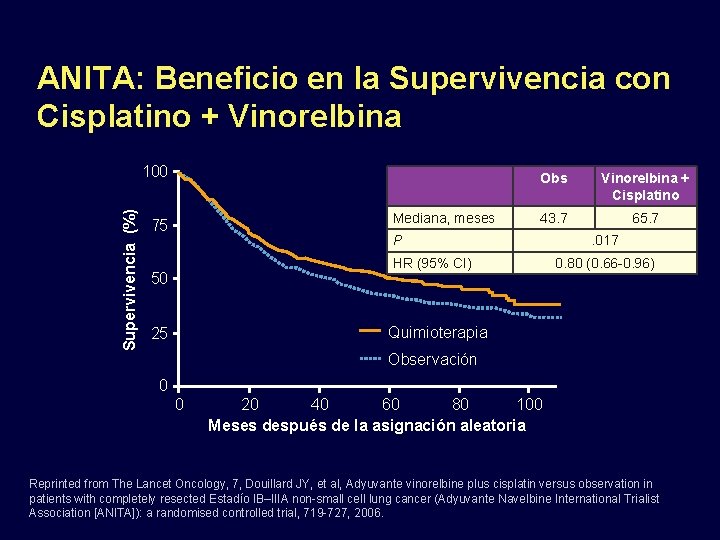
ANITA: Beneficio en la Supervivencia con Cisplatino + Vinorelbina Supervivencia (%) 100 Mediana, meses 75 Obs Vinorelbina + Cisplatino 43. 7 65. 7 P HR (95% CI) 50 . 017 0. 80 (0. 66 -0. 96) Quimioterapia 25 Observación 0 0 20 40 60 80 100 Meses después de la asignación aleatoria Reprinted from The Lancet Oncology, 7, Douillard JY, et al, Adyuvante vinorelbine plus cisplatin versus observation in patients with completely resected Estadío IB–IIIA non-small cell lung cancer (Adyuvante Navelbine International Trialist Association [ANITA]): a randomised controlled trial, 719 -727, 2006.
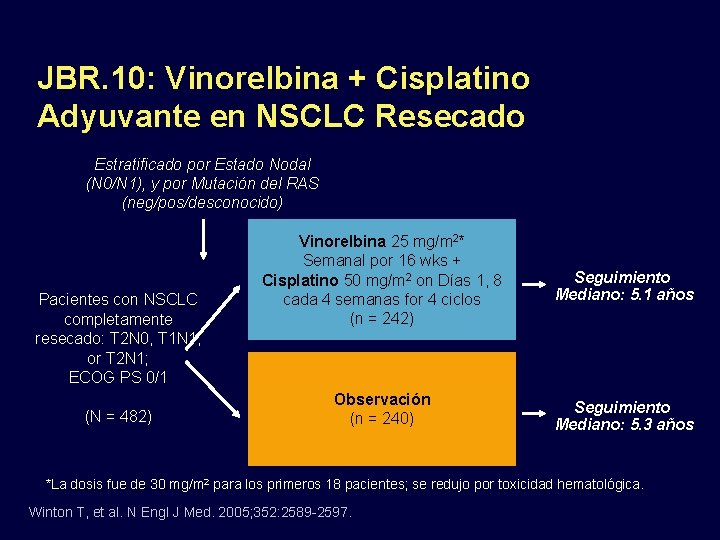
JBR. 10: Vinorelbina + Cisplatino Adyuvante en NSCLC Resecado Estratificado por Estado Nodal (N 0/N 1), y por Mutación del RAS (neg/pos/desconocido) Pacientes con NSCLC completamente resecado: T 2 N 0, T 1 N 1, or T 2 N 1; ECOG PS 0/1 (N = 482) Vinorelbina 25 mg/m 2* Semanal por 16 wks + Cisplatino 50 mg/m 2 on Días 1, 8 cada 4 semanas for 4 ciclos (n = 242) Seguimiento Mediano: 5. 1 años Observación (n = 240) Seguimiento Mediano: 5. 3 años *La dosis fue de 30 mg/m 2 para los primeros 18 pacientes; se redujo por toxicidad hematológica. Winton T, et al. N Engl J Med. 2005; 352: 2589 -2597.
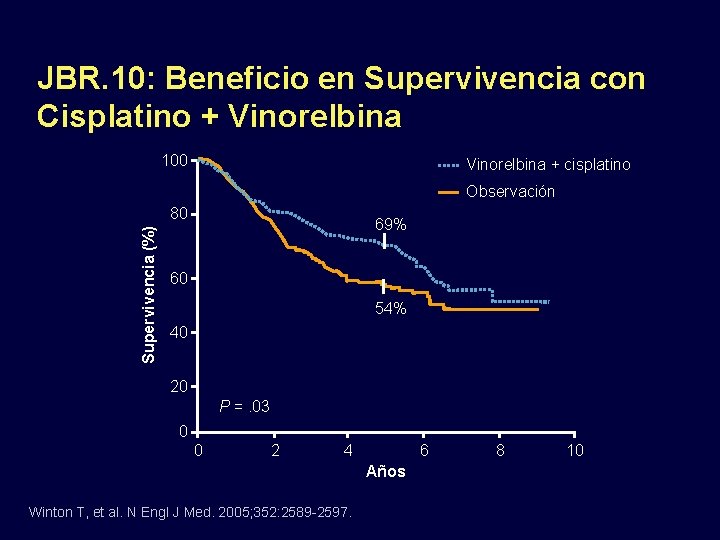
JBR. 10: Beneficio en Supervivencia con Cisplatino + Vinorelbina 100 Vinorelbina + cisplatino Observación Supervivencia (%) 80 69% 60 54% 40 20 P =. 03 0 0 2 4 6 Años Winton T, et al. N Engl J Med. 2005; 352: 2589 -2597. 8 10

CALGB 9633: Quimioterapia adyuvante en NSCLC Estadíos IB Estratificado por Escamocelular vs Otros; Pobremente diferenciado vs Otros; Mediastinoscopia: Si/No Pacientes con NSCLC completamente resecados T 2 N 0 M 0 Estadío IB Quimioterapia adyuvante Paclitaxel 200 mg/m 2 IV + Carboplatinoo AUC 6 4 ciclos en 12 wks (n = 173) (N = 344) Strauss GM, et al. J Clin Oncol. 2008; 26: 5043 -5051. Observación (n = 171)
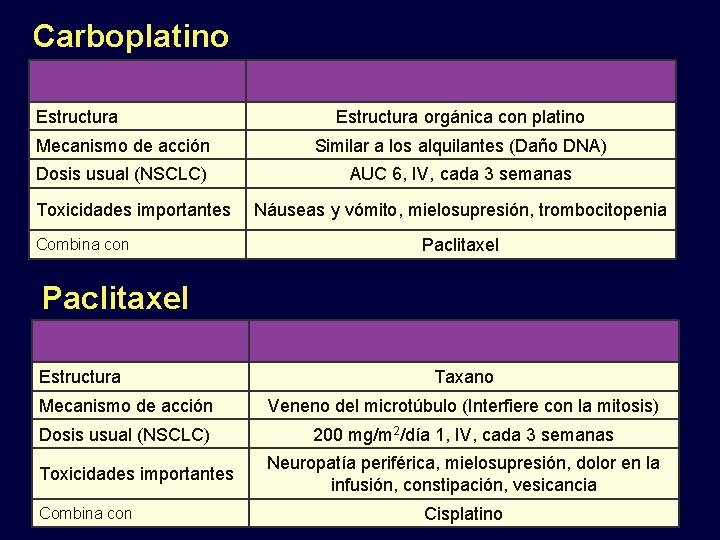
Carboplatino Estructura orgánica con platino Mecanismo de acción Similar a los alquilantes (Daño DNA) Dosis usual (NSCLC) AUC 6, IV, cada 3 semanas Toxicidades importantes Combina con Náuseas y vómito, mielosupresión, trombocitopenia Paclitaxel Estructura Taxano Mecanismo de acción Veneno del microtúbulo (Interfiere con la mitosis) Dosis usual (NSCLC) 200 mg/m 2/día 1, IV, cada 3 semanas Toxicidades importantes Combina con Neuropatía periférica, mielosupresión, dolor en la infusión, constipación, vesicancia Cisplatino
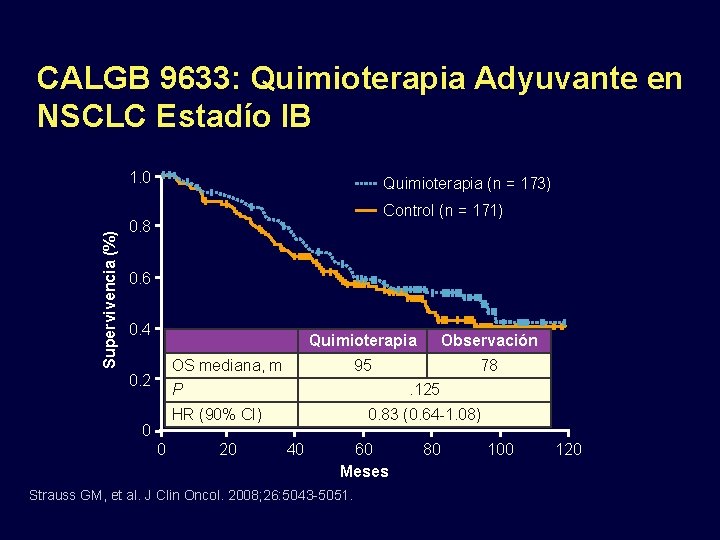
CALGB 9633: Quimioterapia Adyuvante en NSCLC Estadío IB Supervivencia (%) 1. 0 Quimioterapia (n = 173) Control (n = 171) 0. 8 0. 6 0. 4 Quimioterapia Observación 95 78 OS mediana, m 0. 2 P . 125 HR (90% CI) 0 0 20 0. 83 (0. 64 -1. 08) 40 60 Meses Strauss GM, et al. J Clin Oncol. 2008; 26: 5043 -5051. 80 100 120

CALGB 1 B Estudio Adyuvante: Único
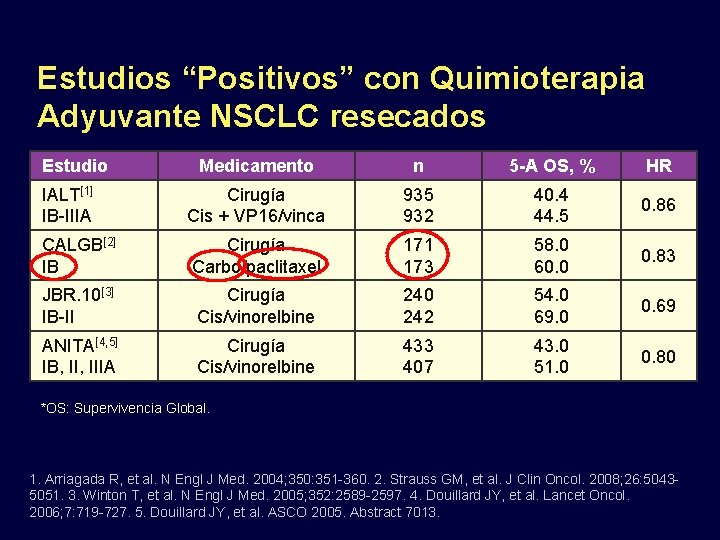
Estudios “Positivos” con Quimioterapia Adyuvante NSCLC resecados Estudio Medicamento n 5 -A OS, % HR IALT[1] IB-IIIA Cirugía Cis + VP 16/vinca 935 932 40. 4 44. 5 0. 86 CALGB[2] IB Cirugía Carbo/paclitaxel 171 173 58. 0 60. 0 0. 83 JBR. 10[3] IB-II Cirugía Cis/vinorelbine 240 242 54. 0 69. 0 0. 69 ANITA[4, 5] IB, IIIA Cirugía Cis/vinorelbine 433 407 43. 0 51. 0 0. 80 *OS: Supervivencia Global. 1. Arriagada R, et al. N Engl J Med. 2004; 350: 351 -360. 2. Strauss GM, et al. J Clin Oncol. 2008; 26: 50435051. 3. Winton T, et al. N Engl J Med. 2005; 352: 2589 -2597. 4. Douillard JY, et al. Lancet Oncol. 2006; 7: 719 -727. 5. Douillard JY, et al. ASCO 2005. Abstract 7013.

Adyuvante Quimioterapia Use and Survival for NSCLC Pts With Surgical Resection Uptake of Adyuvante Quimioterapia examined in patients in Ontario diagnosed from 2001 -2006 who underwent surgical resection (N = 6304) Proportion of patients receiving Adyuvante Quimioterapia increased from 7% in 2001 -2003 time period to 31% in 20042006 time period (P <. 001) – Uptakes coincided with data presented at annual ASCO conferences Rate of hospitalization did not increase with uptake of Adyuvante therapy Significant improvement in 4 -yr OS with uptake of Adyuvante Quimioterapia from 52. 5% to 56. 1% (P =. 001) Booth CM, et al. J Clin Oncol. 2010; 28: 3472 -3478.

Quimioterapia adyuvante: Para todos? Estadío Quimioterapia Dura el efecto?
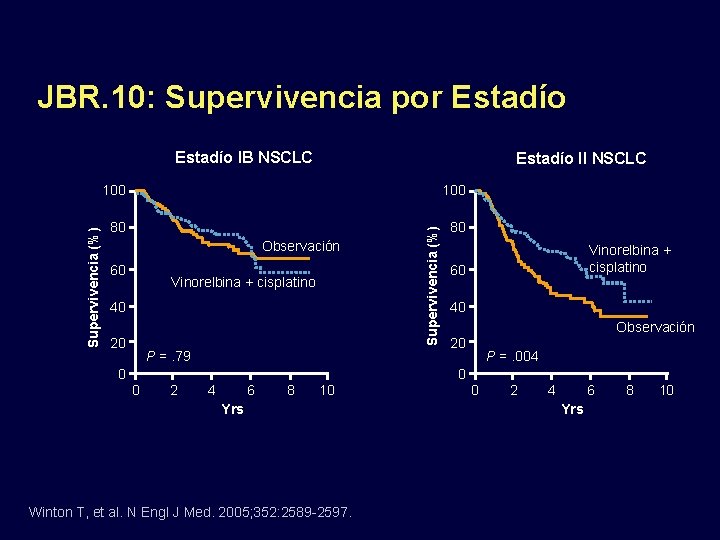
JBR. 10: Supervivencia por Estadío II NSCLC 100 80 80 Observación 60 Vinorelbina + cisplatino 40 20 0 P =. 79 0 2 4 6 8 10 Yrs Winton T, et al. N Engl J Med. 2005; 352: 2589 -2597. Supervivencia (%) Estadío IB NSCLC Vinorelbina + cisplatino 60 40 Observación 20 0 P =. 004 0 2 4 6 Yrs 8 10
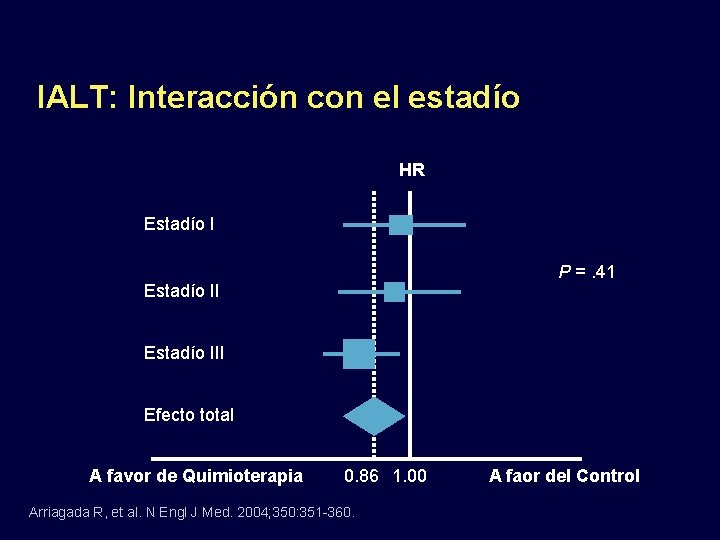
IALT: Interacción con el estadío HR Estadío I P =. 41 Estadío III Efecto total A favor de Quimioterapia 0. 86 1. 00 Arriagada R, et al. N Engl J Med. 2004; 350: 351 -360. A faor del Control
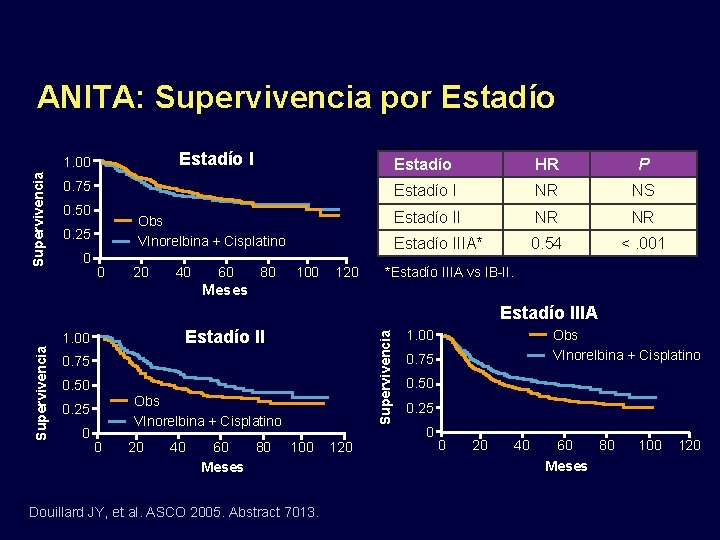
ANITA: Supervivencia por Estadío I Supervivencia 1. 00 0. 75 0. 50 Obs VInorelbina + Cisplatino 0. 25 0 0 20 40 60 80 100 120 Estadío HR P Estadío I NR NS Estadío II NR NR Estadío IIIA* 0. 54 <. 001 *Estadío IIIA vs IB-II. Meses Estadío IIIA Supervivencia Estadío II 1. 00 0. 75 0. 50 Observation VInorelbina + Cisplatino 0. 25 0 0 20 Quimioterapia 40 60 80 100 Meses Douillard JY, et al. ASCO 2005. Abstract 7013. 120 Obs VInorelbina + Cisplatino 1. 00 0. 75 0. 50 0. 25 0 0 20 40 60 80 Meses 100 120
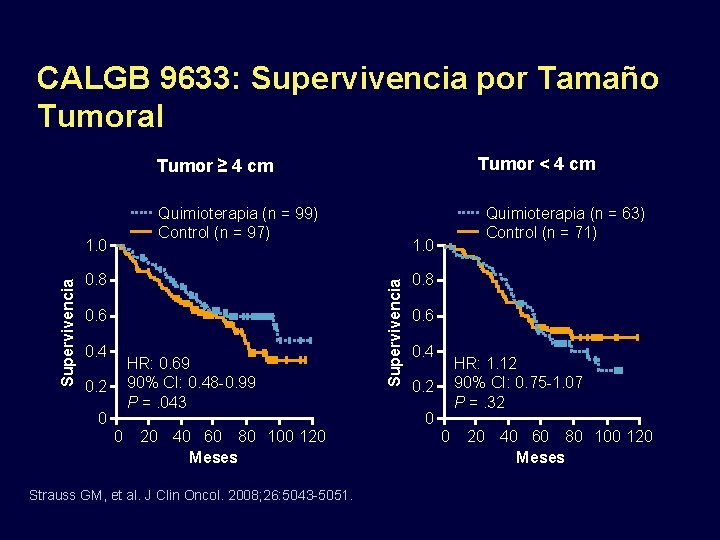
CALGB 9633: Supervivencia por Tamaño Tumoral Tumor < 4 cm Tumor ≥ 4 cm Quimioterapia (n = 99) Control (n = 97) 0. 8 0. 6 0. 4 HR: 0. 69 90% CI: 0. 48 -0. 99 P =. 043 0. 2 0 0 20 40 60 80 100 120 Meses Strauss GM, et al. J Clin Oncol. 2008; 26: 5043 -5051. 1. 0 Supervivencia 1. 0 Quimioterapia (n = 63) Control (n = 71) 0. 8 0. 6 0. 4 HR: 1. 12 90% CI: 0. 75 -1. 07 P =. 32 0. 2 0 0 20 40 60 80 100 120 Meses
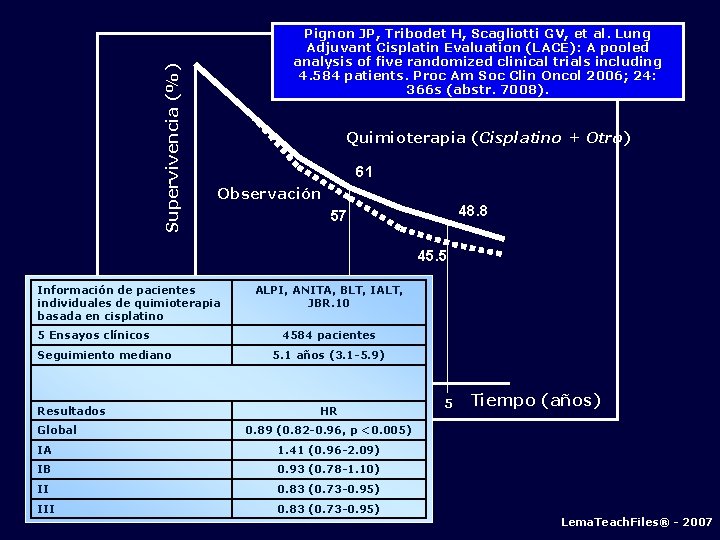
Supervivencia (%) Pignon JP, Tribodet H, Scagliotti GV, et al. Lung Adjuvant Cisplatin Evaluation (LACE): A pooled analysis of five randomized clinical trials including 4. 584 patients. Proc Am Soc Clin Oncol 2006; 24: 366 s (abstr. 7008). Quimioterapia (Cisplatino + Otro) 61 Observación 48. 8 57 45. 5 Información de pacientes individuales de quimioterapia basada en cisplatino 5 Ensayos clínicos Seguimiento mediano Resultados Global ALPI, ANITA, BLT, IALT, JBR. 10 4584 pacientes 5. 1 años (3. 1 -5. 9) HR 5 Tiempo (años) 0. 89 (0. 82 -0. 96, p <0. 005) IA 1. 41 (0. 96 -2. 09) IB 0. 93 (0. 78 -1. 10) II 0. 83 (0. 73 -0. 95) III 0. 83 (0. 73 -0. 95) Lema. Teach. Files® - 2007
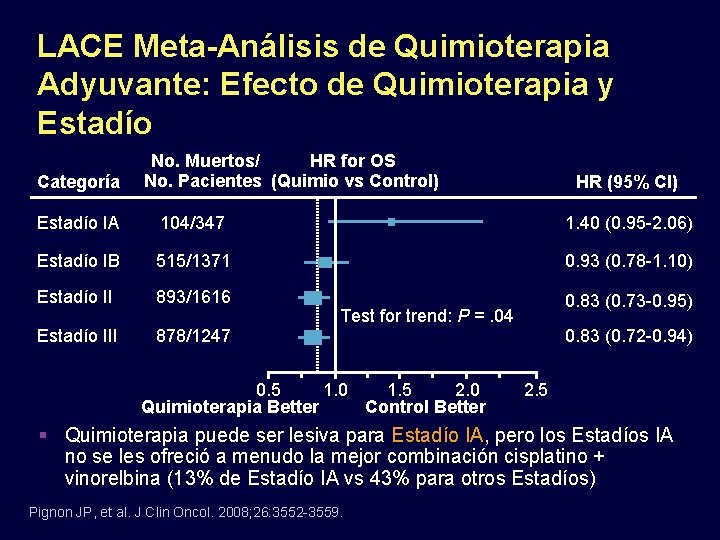
LACE Meta-Análisis de Quimioterapia Adyuvante: Efecto de Quimioterapia y Estadío Categoría No. Muertos/ HR for OS No. Pacientes (Quimio vs Control) HR (95% CI) Estadío IA 104/347 1. 40 (0. 95 -2. 06) Estadío IB 515/1371 0. 93 (0. 78 -1. 10) Estadío II 893/1616 0. 83 (0. 73 -0. 95) Estadío III 878/1247 Test for trend: P =. 04 0. 5 1. 0 1. 5 2. 0 Quimioterapia Better Control Better 0. 83 (0. 72 -0. 94) 2. 5 Quimioterapia puede ser lesiva para Estadío IA, pero los Estadíos IA no se les ofreció a menudo la mejor combinación cisplatino + vinorelbina (13% de Estadío IA vs 43% para otros Estadíos) Pignon JP, et al. J Clin Oncol. 2008; 26: 3552 -3559.
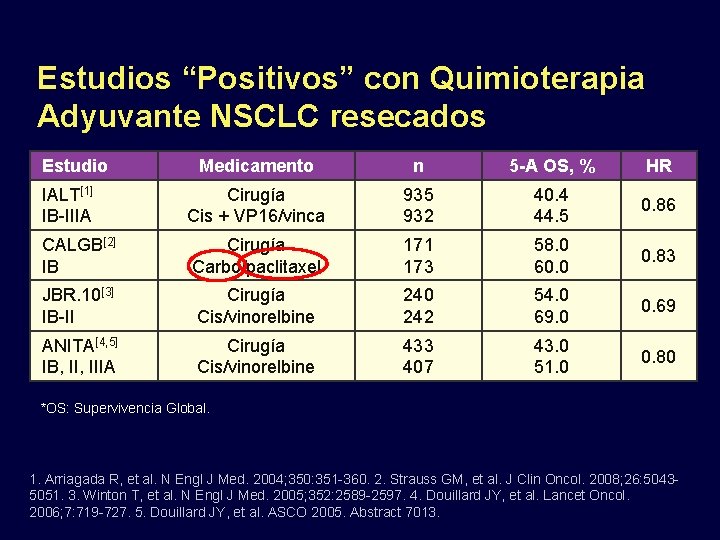
Estudios “Positivos” con Quimioterapia Adyuvante NSCLC resecados Estudio Medicamento n 5 -A OS, % HR IALT[1] IB-IIIA Cirugía Cis + VP 16/vinca 935 932 40. 4 44. 5 0. 86 CALGB[2] IB Cirugía Carbo/paclitaxel 171 173 58. 0 60. 0 0. 83 JBR. 10[3] IB-II Cirugía Cis/vinorelbine 240 242 54. 0 69. 0 0. 69 ANITA[4, 5] IB, IIIA Cirugía Cis/vinorelbine 433 407 43. 0 51. 0 0. 80 *OS: Supervivencia Global. 1. Arriagada R, et al. N Engl J Med. 2004; 350: 351 -360. 2. Strauss GM, et al. J Clin Oncol. 2008; 26: 50435051. 3. Winton T, et al. N Engl J Med. 2005; 352: 2589 -2597. 4. Douillard JY, et al. Lancet Oncol. 2006; 7: 719 -727. 5. Douillard JY, et al. ASCO 2005. Abstract 7013.
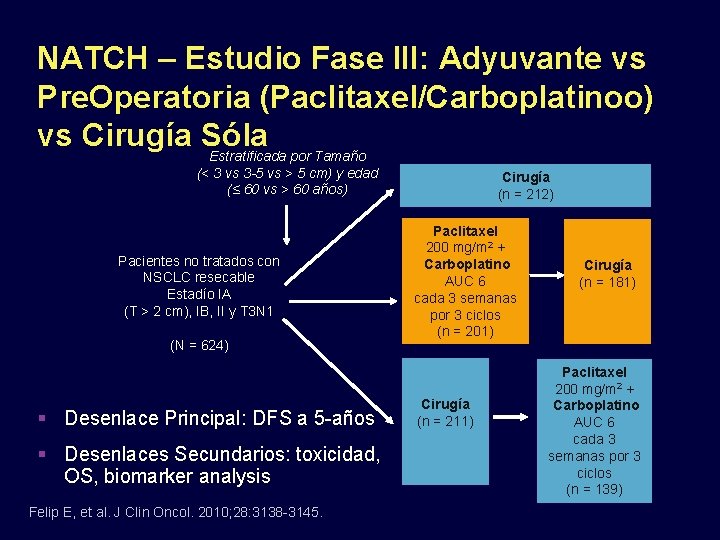
NATCH – Estudio Fase III: Adyuvante vs Pre. Operatoria (Paclitaxel/Carboplatinoo) vs Cirugía Sóla Estratificada por Tamaño (< 3 vs 3 -5 vs > 5 cm) y edad (≤ 60 vs > 60 años) Pacientes no tratados con NSCLC resecable Estadío IA (T > 2 cm), IB, II y T 3 N 1 (N = 624) Desenlace Principal: DFS a 5 -años Desenlaces Secundarios: toxicidad, OS, biomarker analysis Felip E, et al. J Clin Oncol. 2010; 28: 3138 -3145. Cirugía (n = 212) Paclitaxel 200 mg/m 2 + Carboplatino AUC 6 cada 3 semanas por 3 ciclos (n = 201) Cirugía (n = 211) Cirugía (n = 181) Paclitaxel 200 mg/m 2 + Carboplatino AUC 6 cada 3 semanas por 3 ciclos (n = 139)
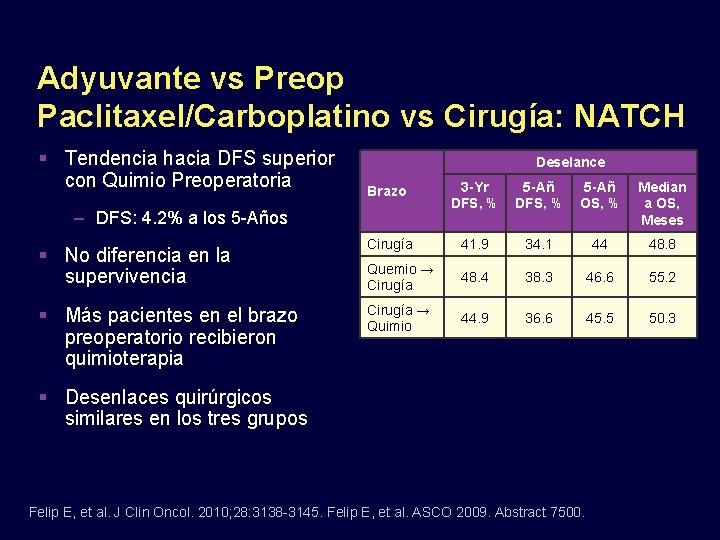
Adyuvante vs Preop Paclitaxel/Carboplatino vs Cirugía: NATCH Tendencia hacia DFS superior con Quimio Preoperatoria Deselance Brazo 3 -Yr DFS, % 5 -Añ OS, % Median a OS, Meses No diferencia en la supervivencia Cirugía 41. 9 34. 1 44 48. 8 Quemio → Cirugía 48. 4 38. 3 46. 6 55. 2 Más pacientes en el brazo preoperatorio recibieron quimioterapia Cirugía → Quimio 44. 9 36. 6 45. 5 50. 3 – DFS: 4. 2% a los 5 -Años Desenlaces quirúrgicos similares en los tres grupos Felip E, et al. J Clin Oncol. 2010; 28: 3138 -3145. Felip E, et al. ASCO 2009. Abstract 7500.
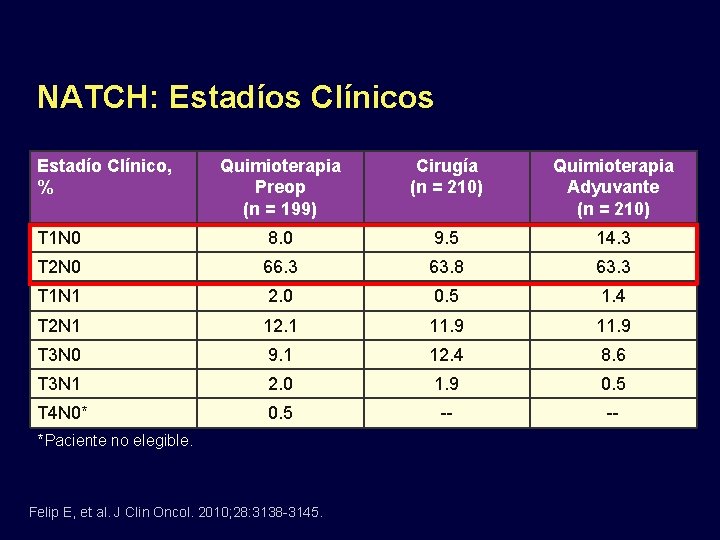
NATCH: Estadíos Clínicos Estadío Clínico, % Quimioterapia Preop (n = 199) Cirugía (n = 210) Quimioterapia Adyuvante (n = 210) T 1 N 0 8. 0 9. 5 14. 3 T 2 N 0 66. 3 63. 8 63. 3 T 1 N 1 2. 0 0. 5 1. 4 T 2 N 1 12. 1 11. 9 T 3 N 0 9. 1 12. 4 8. 6 T 3 N 1 2. 0 1. 9 0. 5 T 4 N 0* 0. 5 -- -- *Paciente no elegible. Felip E, et al. J Clin Oncol. 2010; 28: 3138 -3145.
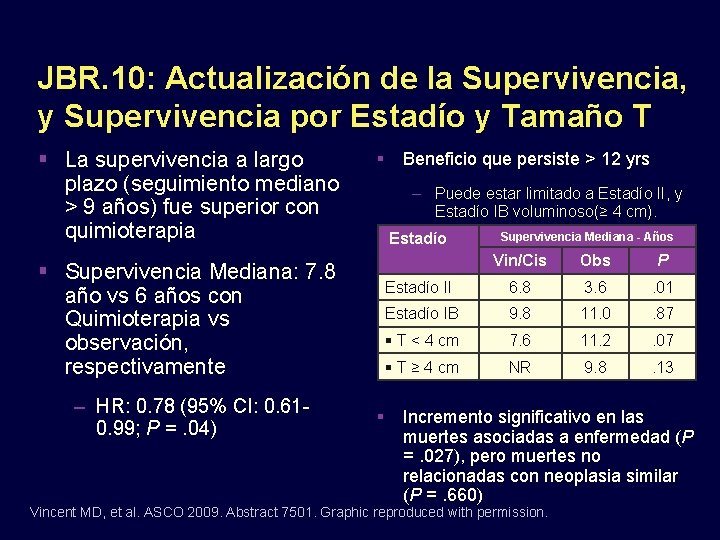
JBR. 10: Actualización de la Supervivencia, y Supervivencia por Estadío y Tamaño T La supervivencia a largo plazo (seguimiento mediano > 9 años) fue superior con quimioterapia – Puede estar limitado a Estadío II, y Estadío IB voluminoso(≥ 4 cm). Estadío Supervivencia Mediana: 7. 8 año vs 6 años con Quimioterapia vs observación, respectivamente – HR: 0. 78 (95% CI: 0. 610. 99; P =. 04) Beneficio que persiste > 12 yrs Supervivencia Mediana - Años Vin/Cis Obs P Estadío II 6. 8 3. 6 . 01 Estadío IB 9. 8 11. 0 . 87 T < 4 cm 7. 6 11. 2 . 07 T ≥ 4 cm NR 9. 8 . 13 Incremento significativo en las muertes asociadas a enfermedad (P =. 027), pero muertes no relacionadas con neoplasia similar (P =. 660) Vincent MD, et al. ASCO 2009. Abstract 7501. Graphic reproduced with permission.

Quimioterapia adyuvante: Lecciones aprendidas Agentes – El Platino seleccionado es importante – Probablemente Cisplatino – No hay un estudio con potencia suficiente con Carboplatino – La Vinorelbina es eficaz – No hay información suficiente con otros medicamentos junto con cisplatino Estadío – II-IIIA – IB continúa siendo controvertido

Cáncer de Páncreas: Viven más de 3 meses Mauricio Lema, MD Oncología Clínica / Hematología Director Médico Clínica de Oncología Astorga Medellín, Colombia Oncología Clínica / Hematología Clínica SOMA Medellín, Colombia

Conflictos de Interés: Mauricio Lema Ninguno para esta conferencia
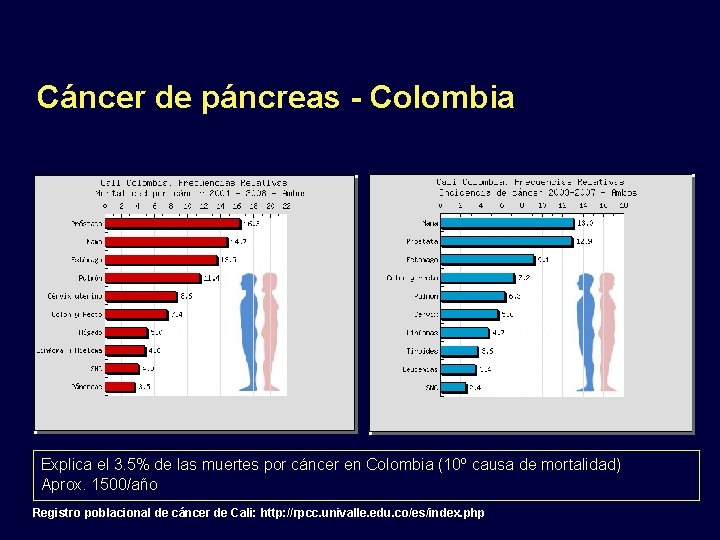
Cáncer de páncreas - Colombia Explica el 3. 5% de las muertes por cáncer en Colombia (10º causa de mortalidad) Aprox. 1500/año Registro poblacional de cáncer de Cali: http: //rpcc. univalle. edu. co/es/index. php
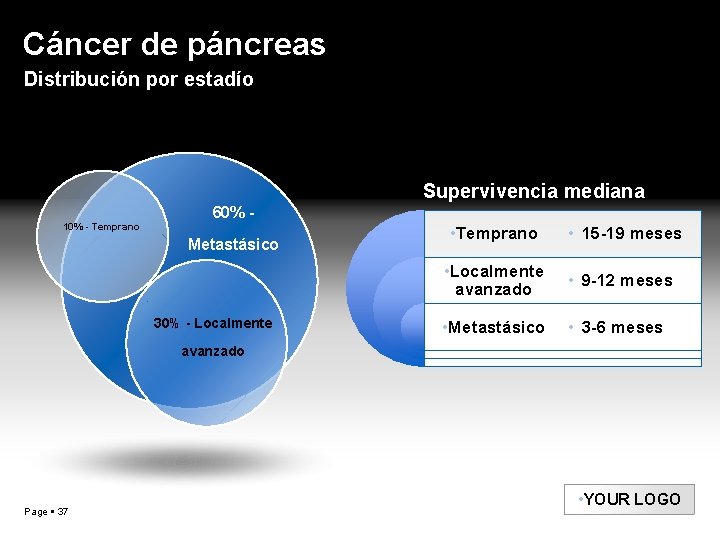
Cáncer de páncreas Distribución por estadío Supervivencia mediana 10% - Temprano 60% Metastásico 30% - Localmente • Temprano • 15 -19 meses • Localmente avanzado • 9 -12 meses • Metastásico • 3 -6 meses avanzado Page 37 • YOUR LOGO
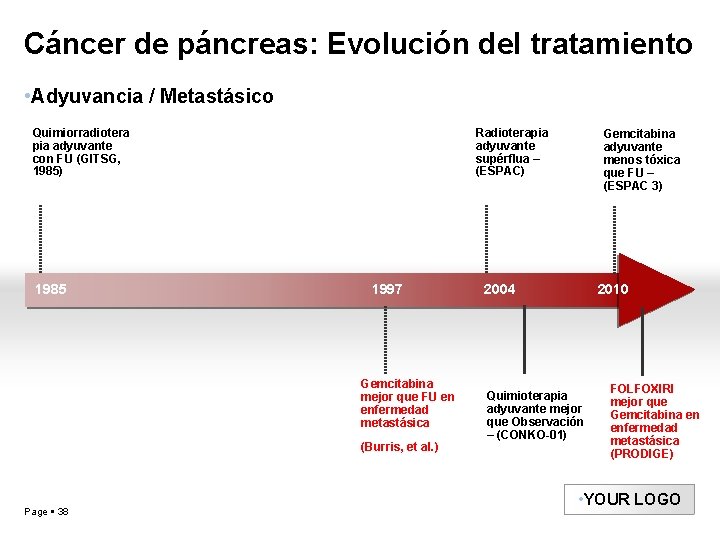
Cáncer de páncreas: Evolución del tratamiento • Adyuvancia / Metastásico Quimiorradiotera pia adyuvante con FU (GITSG, 1985) 1985 Radioterapia adyuvante supérflua – (ESPAC) 1997 Gemcitabina mejor que FU en enfermedad metastásica (Burris, et al. ) Page 38 Gemcitabina adyuvante menos tóxica que FU – (ESPAC 3) 2004 2010 Quimioterapia adyuvante mejor que Observación – (CONKO-01) FOLFOXIRI mejor que Gemcitabina en enfermedad metastásica (PRODIGE) • YOUR LOGO

Cáncer de Páncreas Metastásico - Quimioterapia con intención paliativa -
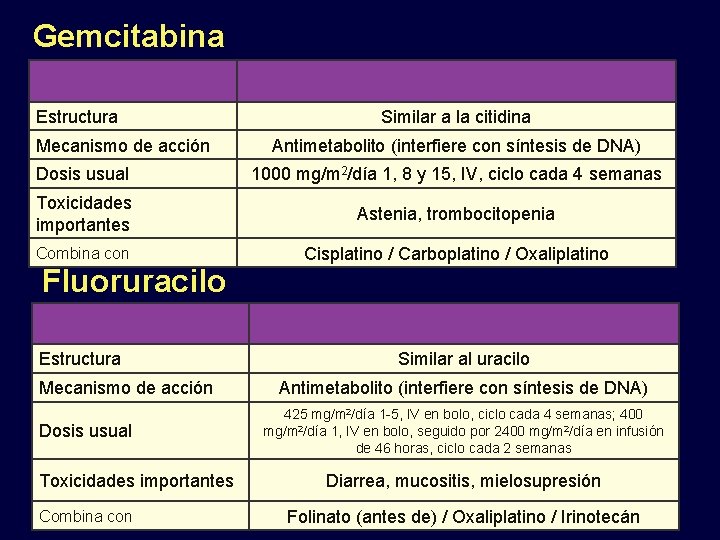
Gemcitabina Estructura Mecanismo de acción Similar a la citidina Antimetabolito (interfiere con síntesis de DNA) Dosis usual 1000 mg/m 2/día 1, 8 y 15, IV, ciclo cada 4 semanas Toxicidades importantes Astenia, trombocitopenia Combina con Cisplatino / Carboplatino / Oxaliplatino Fluoruracilo Estructura Mecanismo de acción Dosis usual Toxicidades importantes Combina con Similar al uracilo Antimetabolito (interfiere con síntesis de DNA) 425 mg/m 2/día 1 -5, IV en bolo, ciclo cada 4 semanas; 400 mg/m 2/día 1, IV en bolo, seguido por 2400 mg/m 2/día en infusión de 46 horas, ciclo cada 2 semanas Diarrea, mucositis, mielosupresión Folinato (antes de) / Oxaliplatino / Irinotecán
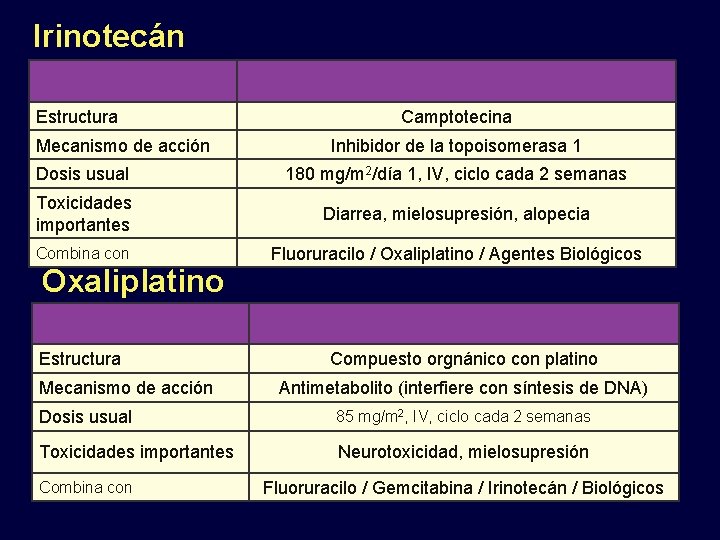
Irinotecán Estructura Mecanismo de acción Camptotecina Inhibidor de la topoisomerasa 1 Dosis usual 180 mg/m 2/día 1, IV, ciclo cada 2 semanas Toxicidades importantes Diarrea, mielosupresión, alopecia Combina con Fluoruracilo / Oxaliplatino / Agentes Biológicos Oxaliplatino Estructura Mecanismo de acción Compuesto orgnánico con platino Antimetabolito (interfiere con síntesis de DNA) Dosis usual 85 mg/m 2, IV, ciclo cada 2 semanas Toxicidades importantes Neurotoxicidad, mielosupresión Combina con Fluoruracilo / Gemcitabina / Irinotecán / Biológicos

Burris: Gemcitabina vs FU en Cáncer de Páncreas Metastásico Cáncer de páncreas avanzado, sintomático (n = 126) Gemcitabina* FULV* *Gemcitabina: 1000 mg/m 2 IV cada semana x 7, seguido por 1 semana de descanso. Seguido por Gemcitabina semanal x 3, de cada 4 semanas FULV: Folinato de calcio 20 mg/m 2/día seguido por FU (Fluoruracilo) 425 mg/m 2/día en bolo x 5 días, cada 4 semanas, hasta progresión Desenlace principal: Beneficio Clínico (índice compuesto por control del dolor, desempeño y peso). Se requiere de la mejoría de 1 parámetro por más de 1 mes, sin el deterioro de otros. – Gemcitabina: 22% vs FU: 4% (p=0. 002) – Supervivencia mediana: 5. 6 vs 4. 1 meses, a favor de Gemcitabina (p=0. 002) – Supervivencia al año: 18% vs 2%, a favor de la Gemcitabina Referencia: Burris HA, et al. JCO 15; 2403, 1997

Irinotecan Plus Gemcitabine Results in No Survival Advantage Compared With Gemcitabine Monotherapy in Patients With Locally Advanced or Metastatic Pancreatic Cancer Despite Increased Tumor Response Rate Estratificado por Desempeño, Extensión de la enfermedad, Radioterapia previa Pacientes con cáncer de páncreas localmente avanzado o metastásico (N = 360) Pacientes seguidos cada mes por 1 año, y cada 3 meses en adelante Gemcitabina + Irinotecan (n = 173) Gemcitabina (n = 169) Se continúa tratamiento hasta progresión de la enfermedad, toxicidad, pérdida de adherencia o retiro del consentimiento. IV = intravenous Gemcitabine + Irinotecan: 1000 mg/m 2 gemcitabina en 30 -min IV seguido por 100 mg/m 2 irinotecan IV en 90 mins, en Días 1 y 8 de cada ciclo de 3 semanas. Gemcitabina: 1000 mg/m 2 cada semana por 7 weeks durante el ciclo de inducción de 8 semanas, seguido por cada semana x 3 en ciclo de cada 4 semanas Rocha Lima CM, Green MR, Rotche R, et al. J Clin Oncol. 2004; 22: 3776 -3783.
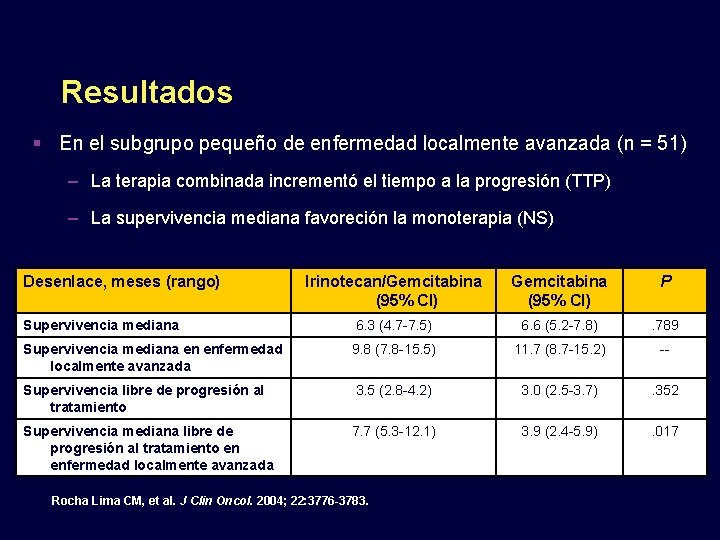
Resultados En el subgrupo pequeño de enfermedad localmente avanzada (n = 51) – La terapia combinada incrementó el tiempo a la progresión (TTP) – La supervivencia mediana favoreción la monoterapia (NS) Desenlace, meses (rango) Irinotecan/Gemcitabina (95% CI) P Supervivencia mediana 6. 3 (4. 7 -7. 5) 6. 6 (5. 2 -7. 8) . 789 Supervivencia mediana en enfermedad localmente avanzada 9. 8 (7. 8 -15. 5) 11. 7 (8. 7 -15. 2) -- Supervivencia libre de progresión al tratamiento 3. 5 (2. 8 -4. 2) 3. 0 (2. 5 -3. 7) . 352 Supervivencia mediana libre de progresión al tratamiento en enfermedad localmente avanzada 7. 7 (5. 3 -12. 1) 3. 9 (2. 4 -5. 9) . 017 Rocha Lima CM, et al. J Clin Oncol. 2004; 22: 3776 -3783.

PRODIGE: Gemcitabina vs FOLFIRINOX en Cáncer de Páncreas Metastásico Cáncer de páncreas avanzado, sintomático, PS 0/1, (n = 342) Gemcitabina* FOLFIRINOX* *Gemcitabina: 1000 mg/m 2 IV cada semana x 7, seguido por 1 semana de descanso. Seguido por Gemcitabina semanal x 3, de cada 4 semanas FOLFIRINOX: Oxaliplatino 85 mg/m 2/día 1, Irinotecán 180 mg/m 2/día 1, seguido por Folinato de calcio 400 mg/m 2/día 1 seguido por FU (Fluoruracilo) 400 mg/m 2/día en bolo, seguido por Fluoruracilo 2400 mg/m 2 en infusión de 46 horas, cada 2 semanas, hasta progresión Supervivencia Global (mediana) – FOLFIRINOX: 11 meses vs Gemcitabina: 6. 8 meses (p=0. 001, HR: 0. 57) Supervivencia libre de progresión – FOLFIRINOX: 6. 4 meses vs Gemcitabina: 3. 3 meses (p=0. 001, HR: 0. 47) Respuesta objetiva – FOLFIRINOX 31. 6% vs 9. 4% (p=0. 001) Toxicidad mayor con FOLFIRINOX (Neutropenia febril 5. 4%) Referencia: Conroy T, et al. NEJM, 2011; 364: 1817 -25

Cáncer de Páncreas Resecable - Quimiorradioterapia adyuvante -

GITSG: Quimiorradioterapia, seguida por fluoruracilo vs Observación – (1985) Pacientes con cáncer de páncreas resecable Radioterapia* + Fluoruracilo, seguido Por Fluoruracilo x 2 años (N = 43) Observación *Radioterapia: En curso dividido – dosis total de 40 Gy Supervivencia Mediana – 20 meses vs 11 meses, a favor de quimiorradioterapia Supervivencia a 2 años – 43% vs 18%, a favor de quimiorradioterapia Referencia:
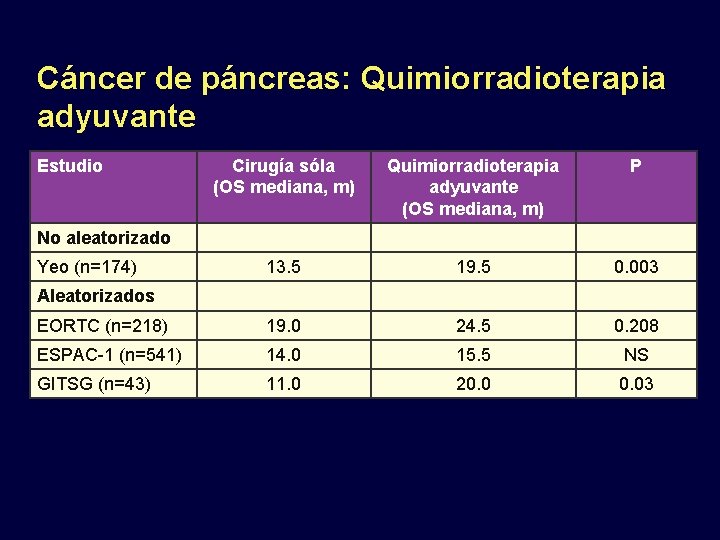
Cáncer de páncreas: Quimiorradioterapia adyuvante Estudio Cirugía sóla (OS mediana, m) Quimiorradioterapia adyuvante (OS mediana, m) P 13. 5 19. 5 0. 003 EORTC (n=218) 19. 0 24. 5 0. 208 ESPAC-1 (n=541) 14. 0 15. 5 NS GITSG (n=43) 11. 0 20. 03 No aleatorizado Yeo (n=174) Aleatorizados

EORTC: Quimiorradioterapia vs Observación – (1999) Pacientes con cáncer de páncreas resecable (incluyeron tumores ampulares) (N = 218) Quimiorradioterapia* con fluoruracilo Observación *Radioterapia: En curso dividido – dosis total de 40 Gy Supervivencia Mediana – 24. 5 meses vs 19 meses, (p=0. 21) Supervivencia a 2 años – 41% vs 51%, (p=0. 21) Superioridad en tumores de la cabeza del páncreas – Supervivencia a 2 años: 34% vs 26% (p=009) – Supervivencia mediana 17. 1 meses vs 12. 6 meses Referencia:

A randomized trial of chemoradiotherapy and chemotherapy after resection of pancreatic cancer Neoptolemos JP, Stocken DD, Friess H, et al. N Engl J Med. 2004; 350: 1200 -1210.

Consideraciones El cáncer de páncreas tiene un mal pronóstico – Supervivencia a 5 años del 4%, o menos La resección quirúrgica mejora la supervivencia pero el pronóstico sigue siendo malo Los estudios aleatorizados muestran beneficios con quimioterapia y radioquimioterapia adyuvante – Pero los resultados no son uniformes • Neoptolemos, et al. N Engl J Med. 2004; 350: 1200 -1210.
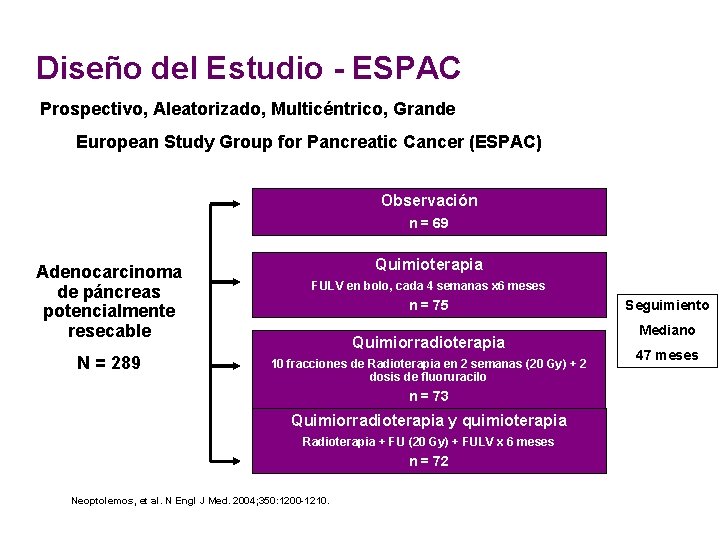
Diseño del Estudio - ESPAC Prospectivo, Aleatorizado, Multicéntrico, Grande European Study Group for Pancreatic Cancer (ESPAC) Observación n = 69 Adenocarcinoma de páncreas potencialmente resecable N = 289 Quimioterapia FULV en bolo, cada 4 semanas x 6 meses n = 75 Quimiorradioterapia 10 fracciones de Radioterapia en 2 semanas (20 Gy) + 2 dosis de fluoruracilo n = 73 Quimiorradioterapia y quimioterapia Radioterapia + FU (20 Gy) + FULV x 6 meses n = 72 Neoptolemos, et al. N Engl J Med. 2004; 350: 1200 -1210. Seguimiento Mediano 47 meses
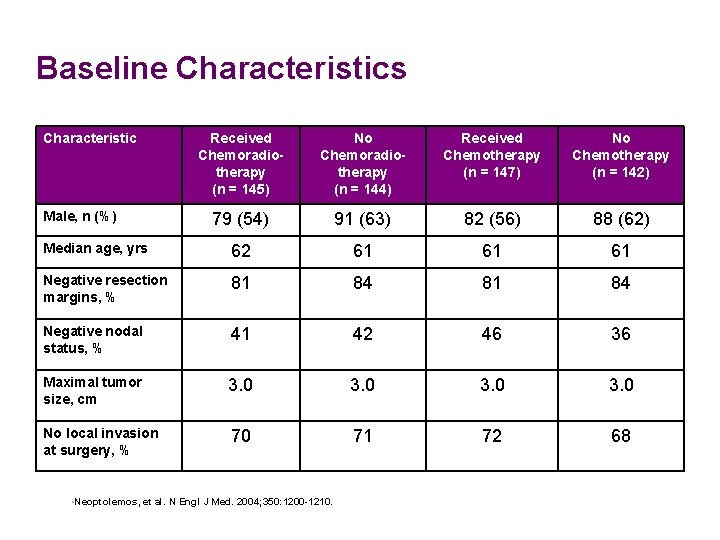
Baseline Characteristics Characteristic Received Chemoradiotherapy (n = 145) No Chemoradiotherapy (n = 144) Received Chemotherapy (n = 147) No Chemotherapy (n = 142) 79 (54) 91 (63) 82 (56) 88 (62) Median age, yrs 62 61 61 61 Negative resection margins, % 81 84 Negative nodal status, % 41 42 46 36 Maximal tumor size, cm 3. 0 No local invasion at surgery, % 70 71 72 68 Male, n (%) • Neoptolemos, et al. N Engl J Med. 2004; 350: 1200 -1210.

Quimioterapia vs No quimioterapia Quimioterapia se asocia a una mejor supervivencia – Supervivencia mediana – 20. 1 meses con quimioterapia – 15. 1 meses sin quimioterapia Recurrencia de la enfermedad – Menos común, menos rápida con quimioterapia – 72% con una mediana de 15. 3 meses con quimioterapia – 81% con una media de 9. 4 meses sin quimioterapia • Neoptolemos, et al. N Engl J Med. 2004; 350: 1200 -1210.

Quimiorradioterapia vs No quimiorradioterapia Quimiorradioterapia asociada a menor supervivencia – Supervivencia mediana – 15. 9 meses con quimiorradioterapia – 17. 9 meses sin quimiorradioterapia Recurrencia de la enfermedad – Más frecuente, más rápica con quimiorradioterapia – 82% con una median de 10. 7 meses con quimiorradioterapia – 70% con una mediana de 15. 2 meses sin quimiorradioterapia • Neoptolemos, et al. N Engl J Med. 2004; 350: 1200 -1210.

Conclusiones La quimioterapia de mantenimiento incrementa la supervivencia en pacientes con cáncer de páncreas resecado Sin embargo, la combinación de quimioterapia con radioterapia puede disminuir la supervivencia El estándar de tratamiento en pacientes con cáncer de páncreas resecable debe incluir quimioterapia adyuvante • Neoptolemos, et al. N Engl J Med. 2004; 350: 1200 -1210.

RTOG 9704: Quimiorradioterapia con FU + (Gemcitabina vs FU adyuvante) Pacientes con cáncer de páncreas T 1 -T 4 N 0 -N 1 MO) (N = 442) FU x 1 mes, seguido por XRT+FU, seguido por FU x 3 meses* Gemcitabina x 1 mes, seguido por XRT+FU, seguido por Gemcitabina x 3 meses *Gemcitabina: 1000 mg/m 2 IV cada semana x 3 (antes de RT), y por 12 semanas (después de RT) FU (Fluoruracilo) 250 mg/m 2/día en infusión continua por 3 semanas (antes de RT) y por 3 meses (después de RT) XRT: 50. 4 Gy + FU 250 mg/m 2/día en infusión continua durante la radioterapia No diferencia en la supervivencia al analizar todos los grupos – Sin embargo, los pacientes con tumores de la cabeza de páncreas mostraron incremento de la supervivencia a favor de gemcitabina – Supervivencia mediana: 36. 9 meses vs 20. 6 meses (p=0. 047, HR: 0. 79) – Supervivencia a 3 años: 32% vs 21% Referencia: -, 2006

Cáncer de Páncreas Resecable - Quimioterapia adyuvante -

CONKO-001: Quimioterapia vs Observación Pacientes con cáncer de páncreas resecable (R 0 o R 1) (N = 368) Gemcitabina* Observación *Gemcitabina: 1000 mg/m 2 IV cada semana x 3. Se repite ciclo cada 4 semanas, x 6 Supervivencia libre de enfermedad (DFS) Mediana – 13. 4 meses vs 6. 9 meses, a favor de quimioterapia (p=0. 001) – R 0: 13. 1 meses vs 7. 3 meses – R 1: 15. 8 meses vs 5. 5 meses Supervivencia mediana – 22. 1 meses vs 20. 2 meses, (p=0. 06) – Recaídas en 83% de los pacientes Referencia: Oettle et al. JAMA, 2007

ESPAC 3: Gemcitabina vs FU adyuvante Pacientes con cáncer de páncreas resecado (n = 1088) Gemcitabina x 6 meses* FULV x 6 meses* *Gemcitabina: 1000 mg/m 2 IV cada semana x 3, se repite ciclo cada 4 semanas, por 6 ciclos. FULV: Folinato de calcio 20 mg/m 2/día seguido por FU (Fluoruracilo) 425 mg/m 2/día en bolo x 5 días, cada 4 semanas, por 6 ciclos No diferencia en la supervivencia al analizar todos los grupos – Supervivencia mediana: 23 meses en ambos grupos Gemcitabina con menores eventos adversos serios (7. 5% vs 14%), p=0. 01 Referencia: Neoptolemos JP, et al. JAMA 310(10); 1073, 2010
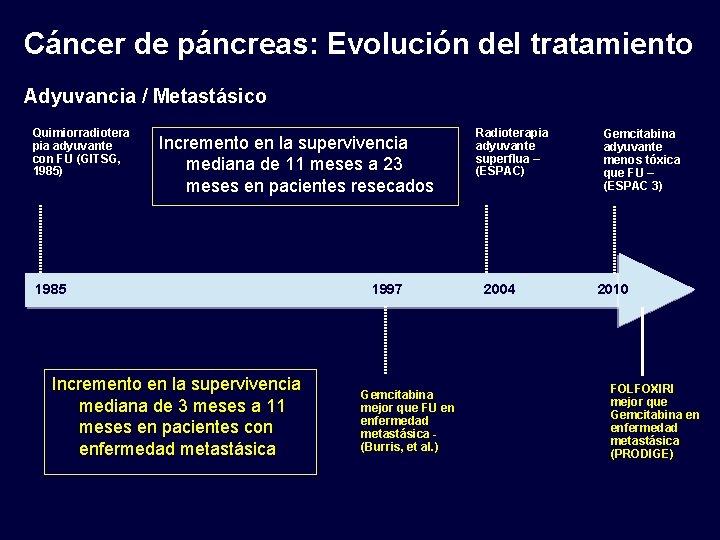
Cáncer de páncreas: Evolución del tratamiento Adyuvancia / Metastásico Quimiorradiotera pia adyuvante con FU (GITSG, 1985) Incremento en la supervivencia mediana de 11 meses a 23 meses en pacientes resecados 1985 Incremento en la supervivencia mediana de 3 meses a 11 meses en pacientes con enfermedad metastásica 1997 Gemcitabina mejor que FU en enfermedad metastásica (Burris, et al. ) Radioterapia adyuvante superflua – (ESPAC) 2004 Gemcitabina adyuvante menos tóxica que FU – (ESPAC 3) 2010 FOLFOXIRI mejor que Gemcitabina en enfermedad metastásica (PRODIGE)
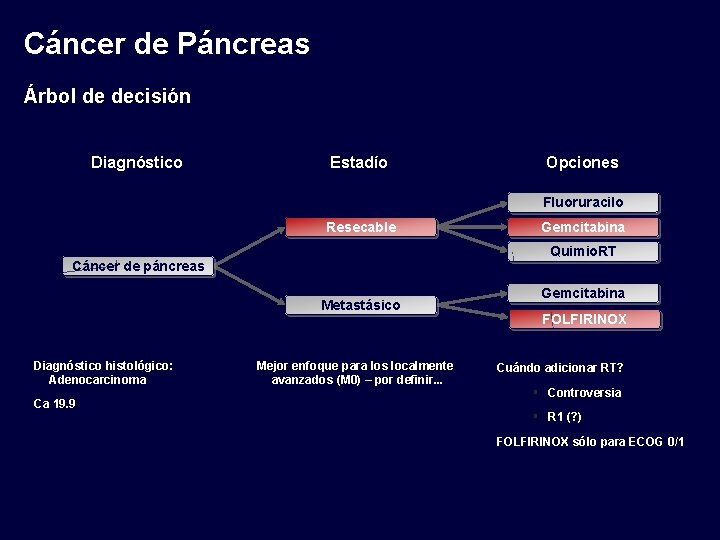
Cáncer de Páncreas Árbol de decisión Diagnóstico Estadío Opciones Fluoruracilo Resecable Quimio. RT Cáncer de páncreas Metastásico Diagnóstico histológico: Adenocarcinoma Ca 19. 9 Gemcitabina Mejor enfoque para los localmente avanzados (M 0) – por definir. . . Gemcitabina FOLFIRINOX Cuándo adicionar RT? Controversia R 1 (? ) FOLFIRINOX sólo para ECOG 0/1

Cáncer de mama triple negativo Mauricio Lema, MD Oncología Clínica / Hematología Director Médico Clínica de Oncología Astorga Medellín, Colombia Oncología Clínica / Hematología Clínica SOMA Medellín, Colombia

Conflictos de Interés: Mauricio Lema Asesor y Speaker de Bristol-Myers Squibb que manufacturan Ixabepilona y Paclitaxel Asesor y Speaker de Roche que manufacturan Capecitabina y Bevacizumab
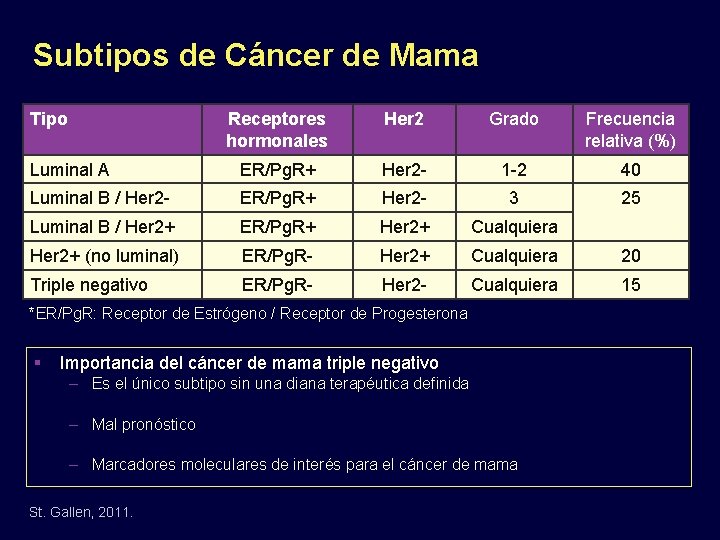
Subtipos de Cáncer de Mama Tipo Receptores hormonales Her 2 Grado Frecuencia relativa (%) Luminal A ER/Pg. R+ Her 2 - 1 -2 40 Luminal B / Her 2 - ER/Pg. R+ Her 2 - 3 25 Luminal B / Her 2+ ER/Pg. R+ Her 2+ Cualquiera Her 2+ (no luminal) ER/Pg. R- Her 2+ Cualquiera 20 Triple negativo ER/Pg. R- Her 2 - Cualquiera 15 *ER/Pg. R: Receptor de Estrógeno / Receptor de Progesterona Importancia del cáncer de mama triple negativo – Es el único subtipo sin una diana terapéutica definida – Mal pronóstico – Marcadores moleculares de interés para el cáncer de mama St. Gallen, 2011.
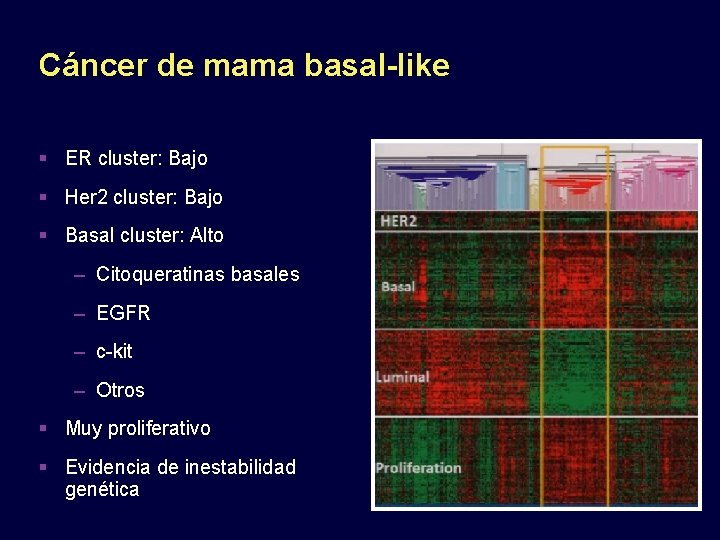
Cáncer de mama basal-like ER cluster: Bajo Her 2 cluster: Bajo Basal cluster: Alto – Citoqueratinas basales – EGFR – c-kit – Otros Muy proliferativo Evidencia de inestabilidad genética
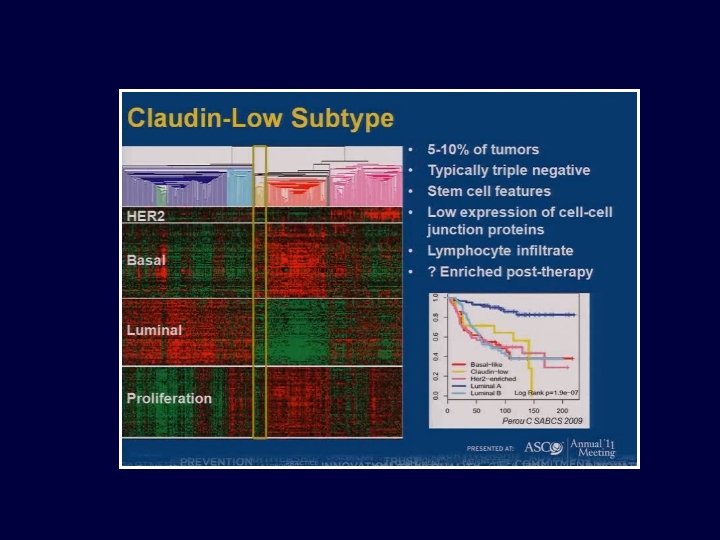
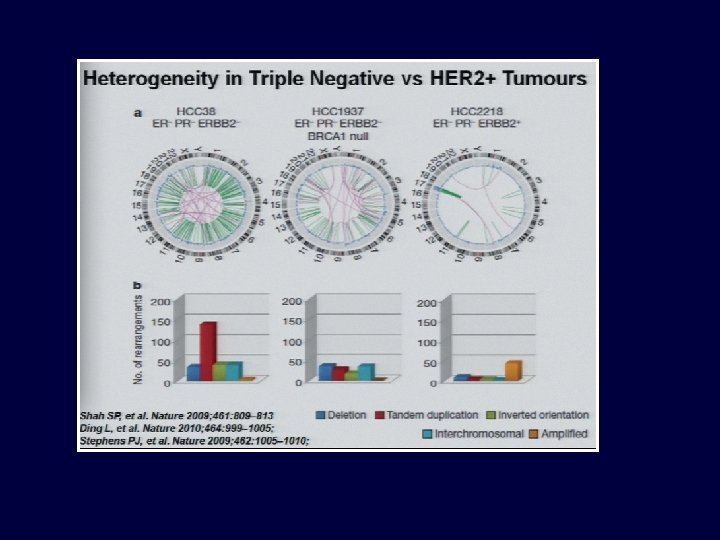
Fenotipo triple negativo y subtipos moléculares Triple negativo 25% TN sin BL Baja claudina Concordancia: 75% Basal-like 25% BL sin TN Usualmente Her 2+ Page 69 • YOUR LOGO
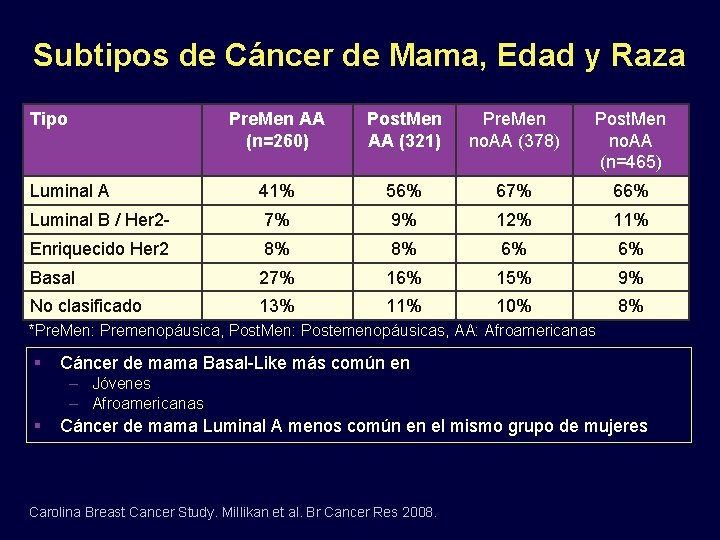
Subtipos de Cáncer de Mama, Edad y Raza Tipo Pre. Men AA (n=260) Post. Men AA (321) Pre. Men no. AA (378) Post. Men no. AA (n=465) Luminal A 41% 56% 67% 66% Luminal B / Her 2 - 7% 9% 12% 11% Enriquecido Her 2 8% 8% 6% 6% Basal 27% 16% 15% 9% No clasificado 13% 11% 10% 8% *Pre. Men: Premenopáusica, Post. Men: Postemenopáusicas, AA: Afroamericanas Cáncer de mama Basal-Like más común en – Jóvenes – Afroamericanas Cáncer de mama Luminal A menos común en el mismo grupo de mujeres Carolina Breast Cancer Study. Millikan et al. Br Cancer Res 2008.
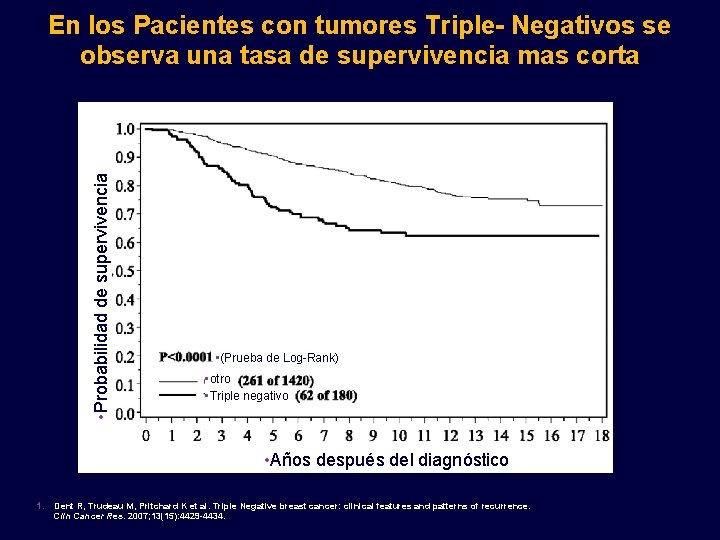
• Probabilidad de supervivencia En los Pacientes con tumores Triple- Negativos se observa una tasa de supervivencia mas corta • (Prueba de Log-Rank) • otro • Triple negativo • Años después del diagnóstico 1. Dent R, Trudeau M, Pritchard K et al. Triple Negative breast cancer: clinical features and patterns of recurrence. Clin Cancer Res. 2007; 13(15): 4429 -4434.
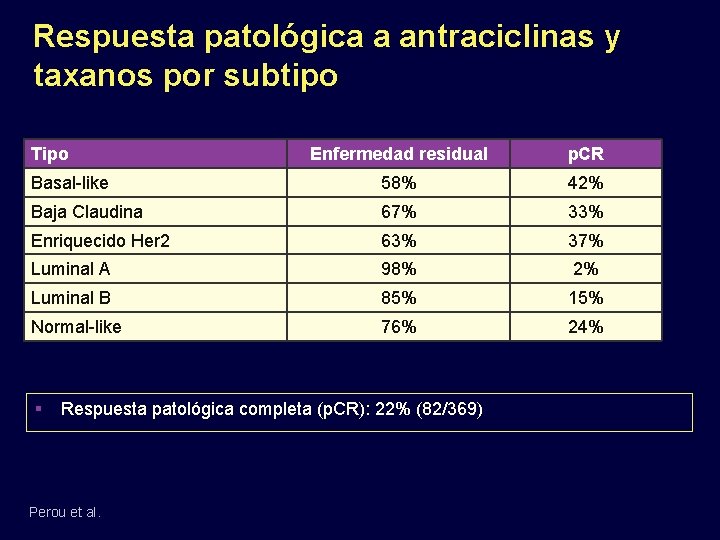
Respuesta patológica a antraciclinas y taxanos por subtipo Tipo Enfermedad residual p. CR Basal-like 58% 42% Baja Claudina 67% 33% Enriquecido Her 2 63% 37% Luminal A 98% 2% Luminal B 85% 15% Normal-like 76% 24% Respuesta patológica completa (p. CR): 22% (82/369) Perou et al.
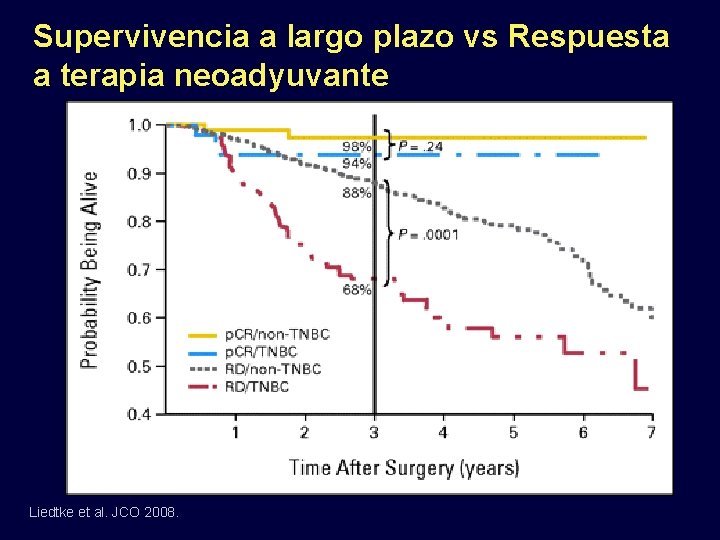
Supervivencia a largo plazo vs Respuesta a terapia neoadyuvante Liedtke et al. JCO 2008.
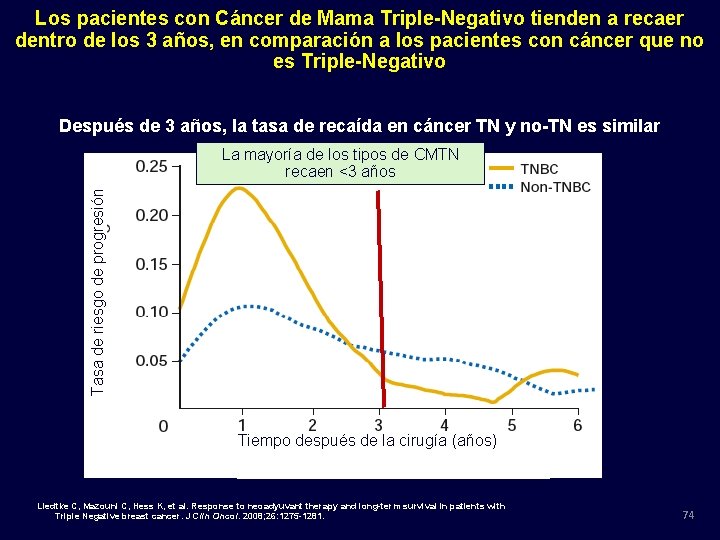
Los pacientes con Cáncer de Mama Triple-Negativo tienden a recaer dentro de los 3 años, en comparación a los pacientes con cáncer que no es Triple-Negativo Después de 3 años, la tasa de recaída en cáncer TN y no-TN es similar Tasa de riesgo de progresión La mayoría de los tipos de CMTN recaen <3 años Tiempo después de la cirugía (años) Liedtke C, Mazouni C, Hess K, et al. Response to neoadyuvant therapy and long-term survival in patients with Triple Negative breast cancer. J Clin Oncol. 2008; 26: 1275 -1281. 74

CALGB 9344: AC +/- Paclitaxel adyuvante Pacientes con cáncer de mama temprano de alto riesgo operable, con ganglios linfáticos comprometidos (N = 3121) AC x 4 seguido por Observación AC x 4 seguiro por Paclitaxel x 4* *AC (había diferentes dosis de Doxorrubicina en el AC), Paclitaxel 175 mg/m 2/día 1, cada 3 semanas x 4 Supervivencia libre de enfermedad (DFS) a 5 años – Superior para paclitaxel sobre antraciclinas: 65% vs 70% Superioridad en supervivencia global a 5 años a favor de paclitaxel – 80% vs 77% Paclitaxel luego de AC estándar es superior con un HR de 0. 72 Referencia: Henderson, IC. et al. J Clin Oncol 21: 976– 983, 2003
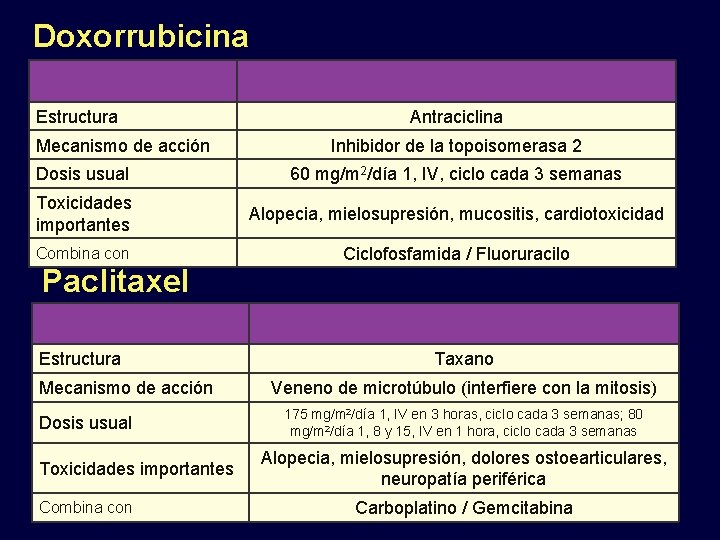
Doxorrubicina Estructura Mecanismo de acción Antraciclina Inhibidor de la topoisomerasa 2 Dosis usual 60 mg/m 2/día 1, IV, ciclo cada 3 semanas Toxicidades importantes Alopecia, mielosupresión, mucositis, cardiotoxicidad Combina con Ciclofosfamida / Fluoruracilo Paclitaxel Estructura Mecanismo de acción Dosis usual Toxicidades importantes Combina con Taxano Veneno de microtúbulo (interfiere con la mitosis) 175 mg/m 2/día 1, IV en 3 horas, ciclo cada 3 semanas; 80 mg/m 2/día 1, 8 y 15, IV en 1 hora, ciclo cada 3 semanas Alopecia, mielosupresión, dolores ostoearticulares, neuropatía periférica Carboplatino / Gemcitabina
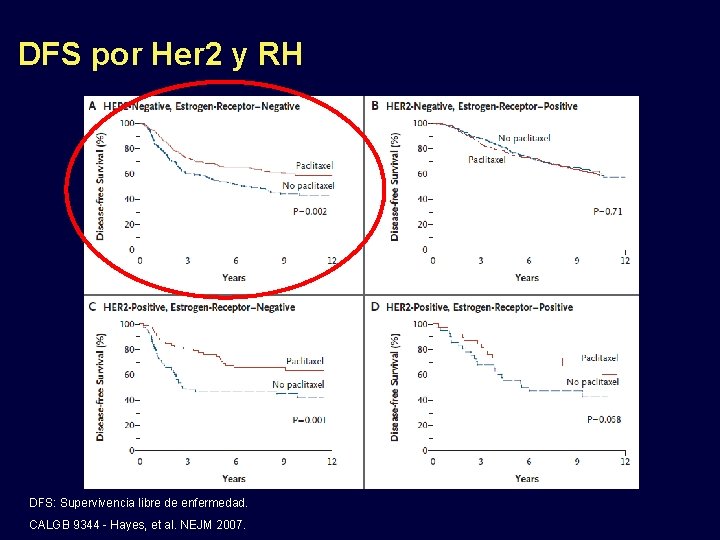
DFS por Her 2 y RH DFS: Supervivencia libre de enfermedad. CALGB 9344 - Hayes, et al. NEJM 2007.
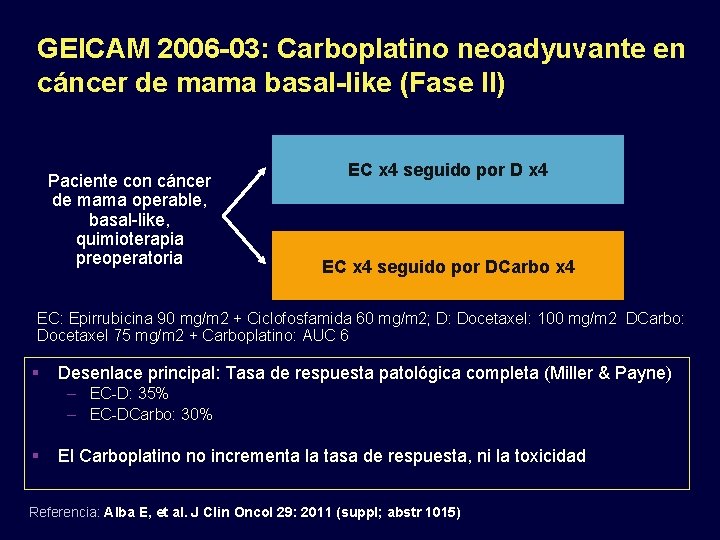
GEICAM 2006 -03: Carboplatino neoadyuvante en cáncer de mama basal-like (Fase II) Paciente con cáncer de mama operable, basal-like, quimioterapia preoperatoria EC x 4 seguido por D x 4 EC x 4 seguido por DCarbo x 4 EC: Epirrubicina 90 mg/m 2 + Ciclofosfamida 60 mg/m 2; D: Docetaxel: 100 mg/m 2 DCarbo: Docetaxel 75 mg/m 2 + Carboplatino: AUC 6 Desenlace principal: Tasa de respuesta patológica completa (Miller & Payne) – EC-D: 35% – EC-DCarbo: 30% El Carboplatino no incrementa la tasa de respuesta, ni la toxicidad Referencia: Alba E, et al. J Clin Oncol 29: 2011 (suppl; abstr 1015)

RIBBON-2: QT +/-Bevacizumab en 2 nda línea Cáncer de mama metastásico, Her 2 -, que ya recibieron una 1 a línea (N = 642) Quimioterapia + Placebo* 2: 1 Bevacizumab vs Placebo Quimioterapia + Bevacizumab *Quimioterapia podía ser: capecitabina, taxano, vinorelbina o gemcitabina Supervivencia libre de progresión (PFS) mediana – Superior para Bevacizumab sobre placebo: 7. 2 meses vs 5. 1 meses – HR: 0. 78 No superioridad en supervivencia global Referencia: Brufsky AM, et al. J Clin Oncol , 2011
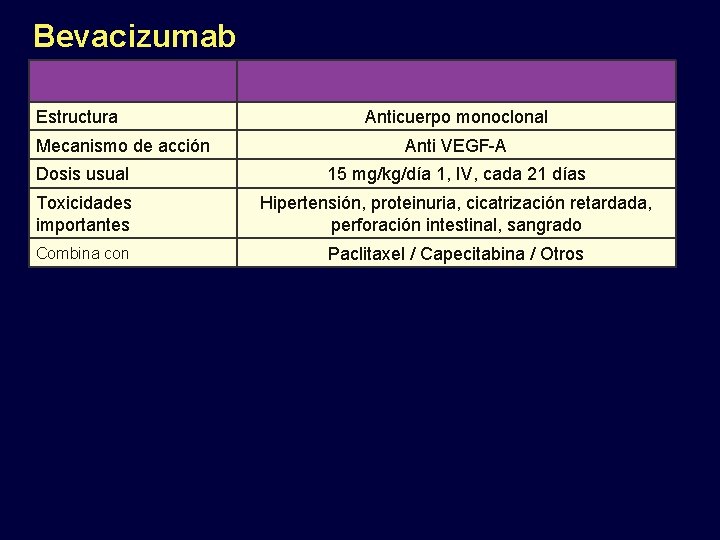
Bevacizumab Estructura Mecanismo de acción Anticuerpo monoclonal Anti VEGF-A Dosis usual 15 mg/kg/día 1, IV, cada 21 días Toxicidades importantes Hipertensión, proteinuria, cicatrización retardada, perforación intestinal, sangrado Combina con Paclitaxel / Capecitabina / Otros
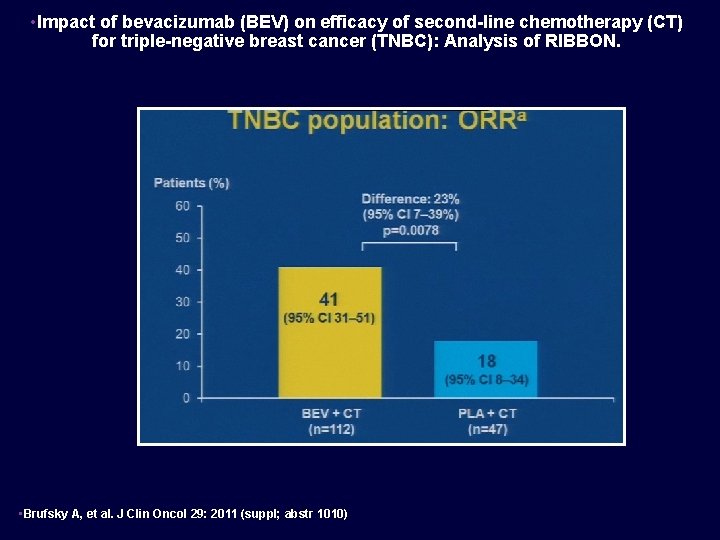
• Impact of bevacizumab (BEV) on efficacy of second-line chemotherapy (CT) for triple-negative breast cancer (TNBC): Analysis of RIBBON. • Brufsky A, et al. J Clin Oncol 29: 2011 (suppl; abstr 1010)
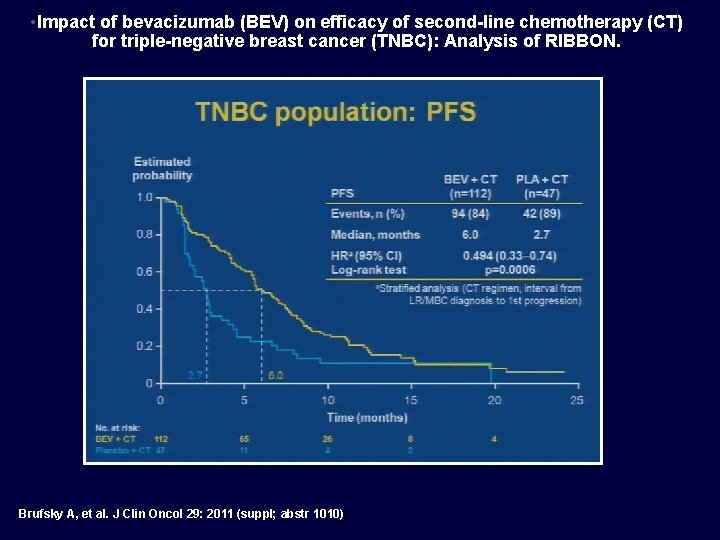
• Impact of bevacizumab (BEV) on efficacy of second-line chemotherapy (CT) for triple-negative breast cancer (TNBC): Analysis of RIBBON. Brufsky A, et al. J Clin Oncol 29: 2011 (suppl; abstr 1010)
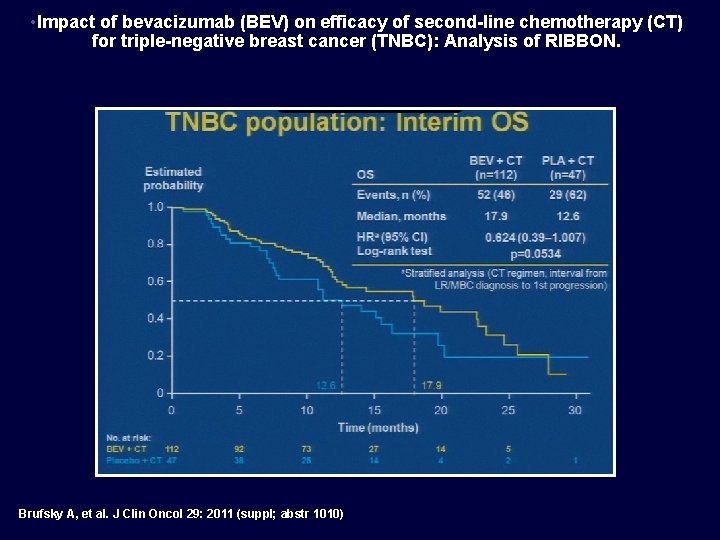
• Impact of bevacizumab (BEV) on efficacy of second-line chemotherapy (CT) for triple-negative breast cancer (TNBC): Analysis of RIBBON. Brufsky A, et al. J Clin Oncol 29: 2011 (suppl; abstr 1010)

Estudios Ixabepilona en Cáncer de Mama Fase II: Agente único ixabepilona en cáncer de mama triplemente refractario Estudio 081 N=126 Previo Tx con Antraciclina, taxano y capecitabina en CMM Ixabepilona Objetivo primario: Respuesta global Dos Estudios de Fase III: Ixabepilona más capecitabina Estudio 046 N=752 Resistentes a A/T < 3 líneas Ixabepilona + Capecitabina Estudio 048 N=1221 Pre- tratados con A/T < 2 líneas Ixabepilona + Capecitabina Objetivo primario: Supervivencia libre de progresión (SLP) Objetivo primario: Supervivencia global (OS) Capecitabina 1. Perez E, Lerzo G, Pivot X, et al. Efficacy y Safety of Ixabepilone (BMS-247550) in a Phase II study of patients With Advanced breast cancer resistant to an Anthracycline, a Taxane, and Capecitabine. J Clin Oncol. 2007; 25(23): 3407 -3414. 2. Thomas E, Gomez H, Li R, et al. Ixabepilone plus Capecitabine for Metastatic breast cancer Progressing After Anthracycline and Taxane Treatment. J Clin Oncol. 2007; 25(33): 5210 -5217. 3. Hortobagyi GN, Perez E, Vrdoljak C, et al. Analysis of Overall Survival (OS) among patients (pts) with metastatic breast cancer (MBC) receiving either ixabepilone (I) plus capecitabine (C) o (C) alone: Results from two randomized phase II Studies. American Society of Clinical Oncology (ASCO) Breast Cancer Symposium. May 2008. Chicago, Illinois. Abstract 186. 84
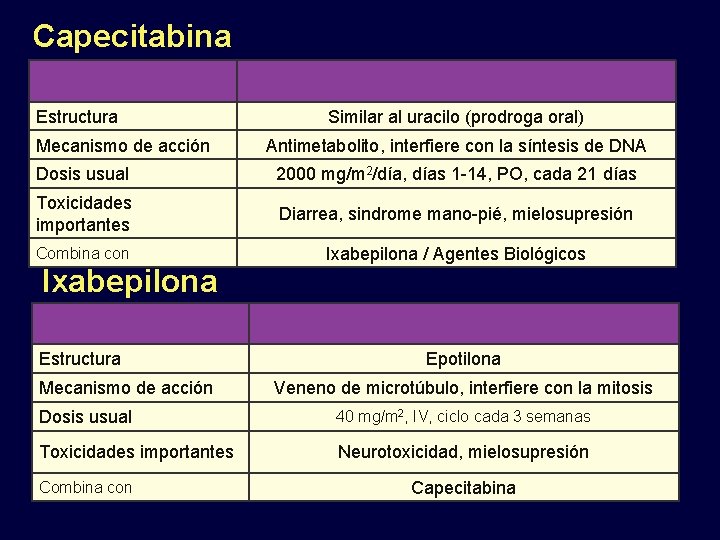
Capecitabina Estructura Mecanismo de acción Similar al uracilo (prodroga oral) Antimetabolito, interfiere con la síntesis de DNA Dosis usual 2000 mg/m 2/día, días 1 -14, PO, cada 21 días Toxicidades importantes Diarrea, sindrome mano-pié, mielosupresión Combina con Ixabepilona / Agentes Biológicos Ixabepilona Estructura Mecanismo de acción Epotilona Veneno de microtúbulo, interfiere con la mitosis Dosis usual 40 mg/m 2, IV, ciclo cada 3 semanas Toxicidades importantes Neurotoxicidad, mielosupresión Combina con Capecitabina
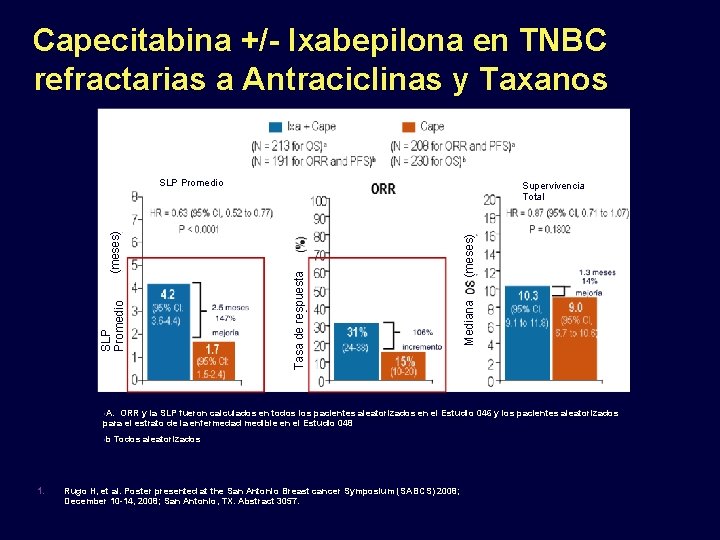
Capecitabina +/- Ixabepilona en TNBC refractarias a Antraciclinas y Taxanos • A. Mediana (meses) Supervivencia Total Tasa de respuesta SLP Promedio (meses) SLP Promedio ORR y la SLP fueron calculados en todos los pacientes aleatorizados en el Estudio 046 y los pacientes aleatorizados para el estrato de la enfermedad medible en el Estudio 048 • b 1. Todos aleatorizados Rugo H, et al. Poster presented at the San Antonio Breast cancer Symposium (SABCS) 2008; December 10 -14, 2008; San Antonio, TX. Abstract 3057.

Estudios negativos en Cáncer de Mama Triple Negativo CMF vs CMF + Epirrubicina (Cáncer de mama temprano)1 – CMF es insuficiente, se requiere de la antraciclina Carboplatino (Neoadyuvante, Cáncer de mama temprano)2 – No incrementa la tasa de respuesta patológica Inhibidor de la PARP-1 (Iniparib)3 – No incrementa la supervivencia global en pacientes con cáncer de mama metastásico triple negativo Inhibidor de tirosina kinasa antiangiogénico + (Sorafenib)4 – No incrementa la supervivencia libre de progresión 1. Rocca A, et al. J Clin Oncol 29: 2011 (suppl; abstr 1031) 2. Alba E, et al. J Clin Oncol 29: 2011 (suppl; abstr 1015) 3. O’Shaughnessy J, et al. ASCO 2011 (suppl; abstr 1007). 4. Hudis C et al. J Clin Oncol 29: 2011 (suppl; abstr 1009)
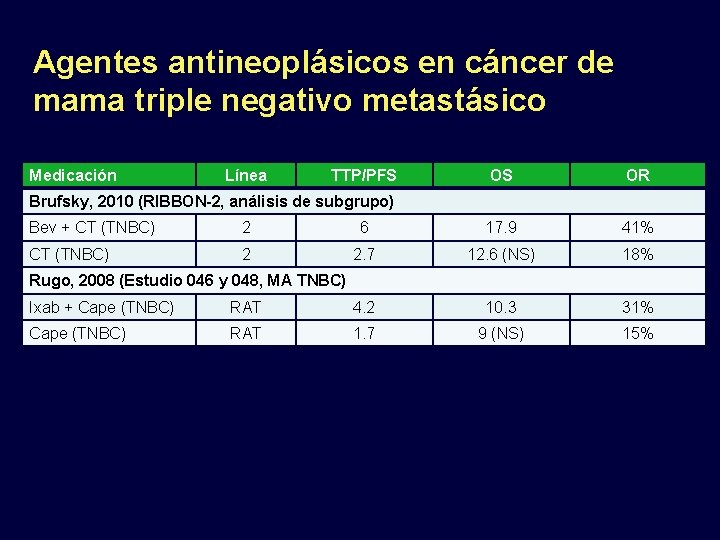
Agentes antineoplásicos en cáncer de mama triple negativo metastásico Medicación Línea TTP/PFS OS OR Brufsky, 2010 (RIBBON-2, análisis de subgrupo) Bev + CT (TNBC) 2 6 17. 9 41% CT (TNBC) 2 2. 7 12. 6 (NS) 18% Rugo, 2008 (Estudio 046 y 048, MA TNBC) Ixab + Cape (TNBC) RAT 4. 2 10. 3 31% Cape (TNBC) RAT 1. 7 9 (NS) 15%

Conclusiones El cáncer de mama triple negativo: – Es definido como lo que NO es. . . Que en nada ilustra lo que es – Heterogéneo desde el punto de vista molecular (Basal, Claudina, otros) – 15% de las pacientes con cáncer de mama – Epidemiología distinta, más agresivo, recaídas tempranas La quimioterapia es la única estrategia de terapia sistémica – Antraciclinas y Taxanos necesarios para una respuesta óptima – Sin respuesta patológica completa (neoadyuvante), mal pronóstico – Opciones limitadas en enfermedad metastásica – Bevacizumab + Quimioterapia – Ixabepilina con capecitabina Sólo las raras pacientes con mutación del BRCA tienen un mecanismo entendido potencialmente explotable – Letalidad sintética

Cáncer de colon y recto metastásico potencialmente resecable: perspectiva del oncólogo Mauricio Lema, MD Oncología Clínica / Hematología Director Médico Clínica de Oncología Astorga Medellín, Colombia Oncología Clínica / Hematología Clínica SOMA Medellín, Colombia

Conflictos de Interés: Mauricio Lema No conflictos de interés para esta conferencia
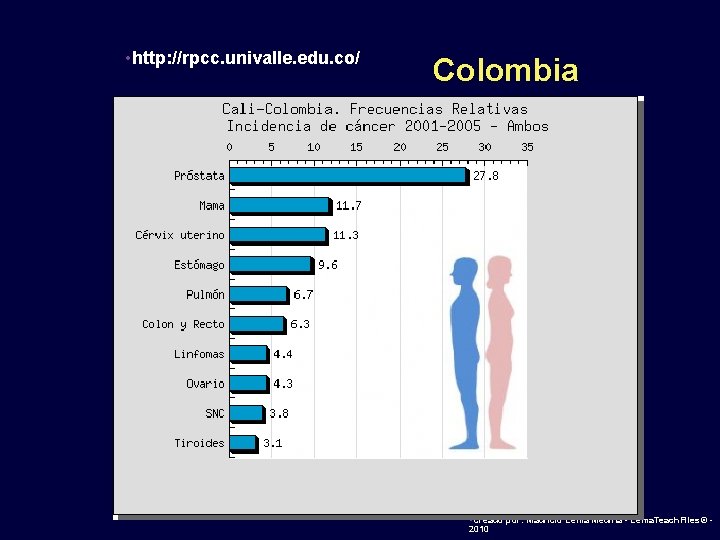
• http: //rpcc. univalle. edu. co/ Colombia • • Creado por: Mauricio Lema Medina - Lema. Teach. Files© 2010

• http: //rpcc. univalle. edu. co/ Colombia • • Creado por: Mauricio Lema Medina - Lema. Teach. Files© 2010

Cáncer de colon y recto en Colombia 12 5 Casos nuevos por día en Colombia Muertes diarias
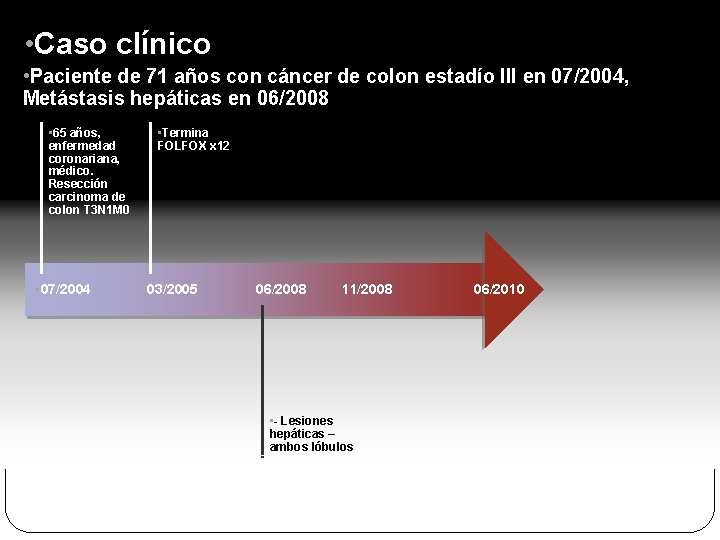
• Caso clínico • Paciente de 71 años con cáncer de colon estadío III en 07/2004, Metástasis hepáticas en 06/2008 • 65 años, enfermedad coronariana, médico. Resección carcinoma de colon T 3 N 1 M 0 • 07/2004 • Termina FOLFOX x 12 03/2005 06/2008 11/2008 • - Lesiones hepáticas – ambos lóbulos 06/2010
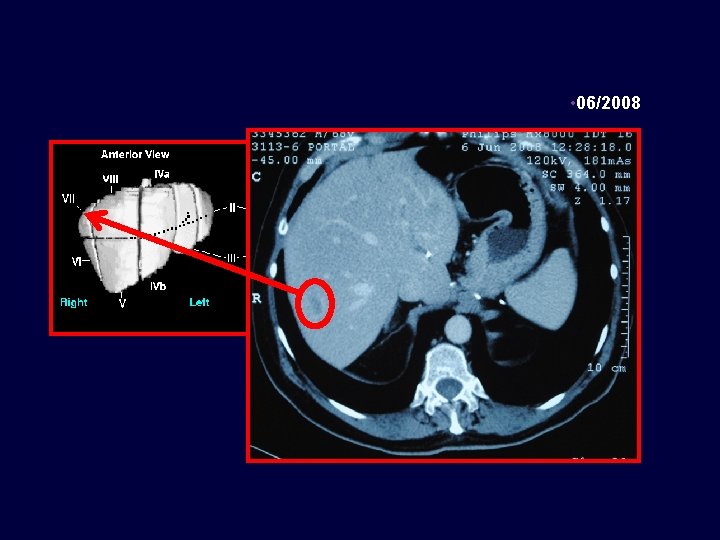
• 06/2008
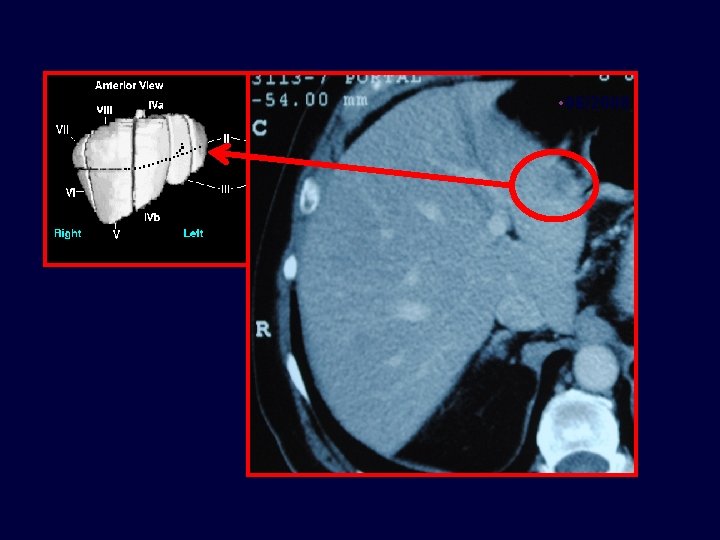
• 06/2008
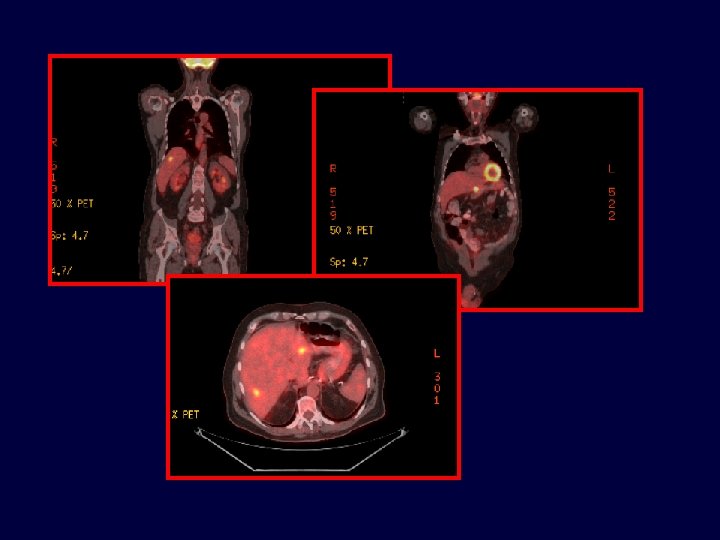

Metástasis hepáticas 15– 20% resecables 80– 85% no resecables Quimioterapia Resección 10– 20% se vuelven resecables Total resecables 30%

Criterios de resecabilidad Resección completa (+/-ablación) del tumor Márgen libre de neoplasia Preservar al menos 1 de las 3 venas hepáticas Preservación del pedículo portal homolateral Preservación de ≥ 25% del parénquima hepático La resecabilidad NO depende del número de metástasis

Quimioterapia postoperatoria luego de resección de metástasis hepáticas

Supervivencia después de resección por enfermedad metastásica hepática de cáncer colorrectal: Tendencias en los desenlaces para 1, 600 pacientes durante dos décadas en una institución única N+ en el tumor primario Intervalo libre de enfermedad > 12 meses > 1 Metástasis hepáticas > 5 cm (en cualquier lesión) CEA antes de la cirugía > 200 ng/m. L – Bajo riesgo – CRS 0, 1 or 2 – Alto riesgo – CRS 3, 4 or 5 House MG, et al. J Am Coll Surg 2010; 210: 744 -54. Fong Y et al. Ann Surg 1999.
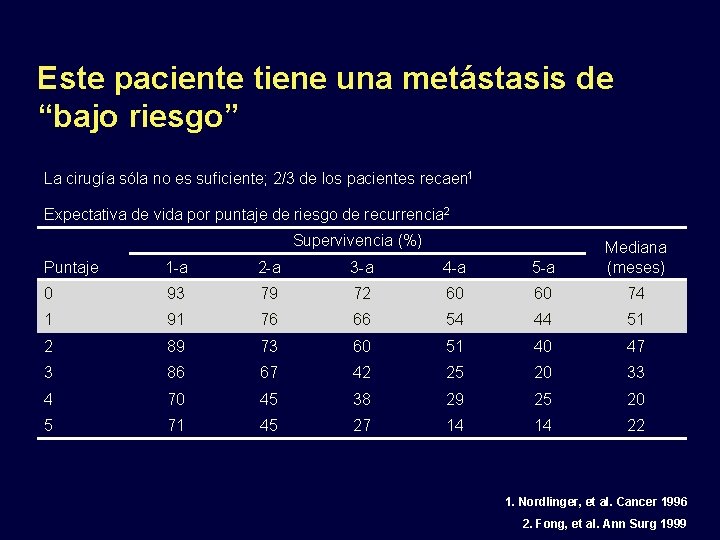
Este paciente tiene una metástasis de “bajo riesgo” La cirugía sóla no es suficiente; 2/3 de los pacientes recaen 1 Expectativa de vida por puntaje de riesgo de recurrencia 2 Supervivencia (%) Puntaje 1 -a 2 -a 3 -a 4 -a 5 -a Mediana (meses) 0 93 79 72 60 60 74 1 91 76 66 54 44 51 2 89 73 60 51 40 47 3 86 67 42 25 20 33 4 70 45 38 29 25 20 5 71 45 27 14 14 22 1. Nordlinger, et al. Cancer 1996 2. Fong, et al. Ann Surg 1999
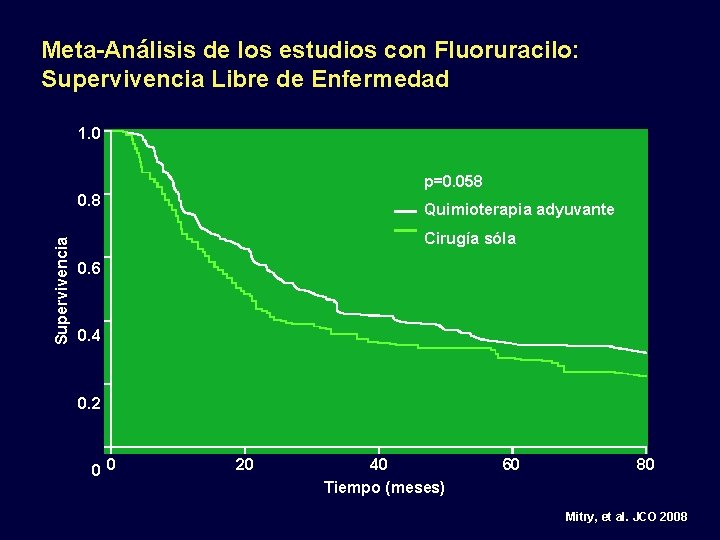
Meta-Análisis de los estudios con Fluoruracilo: Supervivencia Libre de Enfermedad 1. 0 p=0. 058 Supervivencia 0. 8 Quimioterapia adyuvante Cirugía sóla 0. 6 0. 4 0. 2 0 0 20 40 Tiempo (meses) 60 80 Mitry, et al. JCO 2008
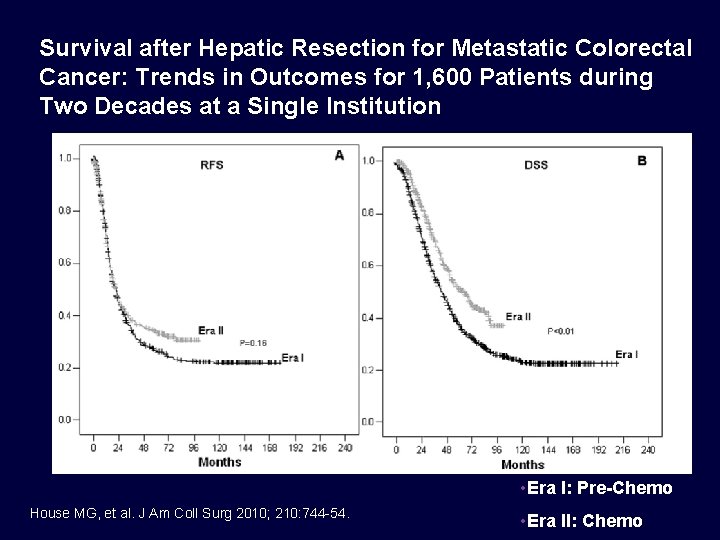
Survival after Hepatic Resection for Metastatic Colorectal Cancer: Trends in Outcomes for 1, 600 Patients during Two Decades at a Single Institution • Era I: Pre-Chemo House MG, et al. J Am Coll Surg 2010; 210: 744 -54. • Era II: Chemo

Quimioterapia perioperatoria (antes y después)
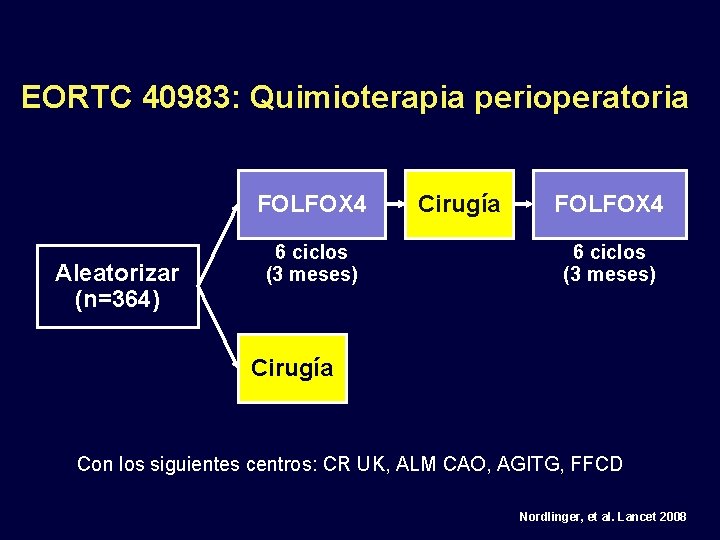
EORTC 40983: Quimioterapia perioperatoria FOLFOX 4 Aleatorizar (n=364) 6 ciclos (3 meses) Cirugía FOLFOX 4 6 ciclos (3 meses) Cirugía Con los siguientes centros: CR UK, ALM CAO, AGITG, FFCD Nordlinger, et al. Lancet 2008
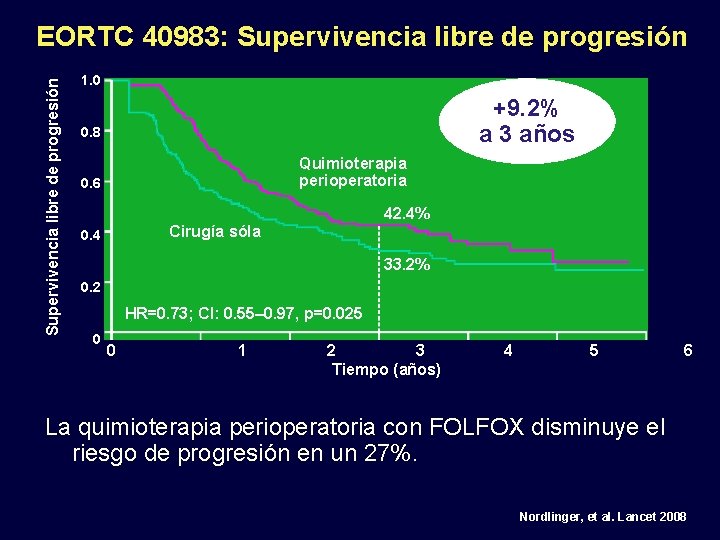
Supervivencia libre de progresión EORTC 40983: Supervivencia libre de progresión 1. 0 +9. 2% a 3 años 0. 8 Quimioterapia perioperatoria 0. 6 42. 4% Cirugía sóla 0. 4 33. 2% 0. 2 HR=0. 73; CI: 0. 55– 0. 97, p=0. 025 0 0 1 2 3 Tiempo (años) 4 5 6 La quimioterapia perioperatoria con FOLFOX disminuye el riesgo de progresión en un 27%. Nordlinger, et al. Lancet 2008

FOLFOX-4 FOLFOX 4: ciclo de 14 -días iv 2 h d 1 5 -FU 600 mg/m 2 iv 22 h LV 200 mg/m 2 iv 2 h d 2 5 -FU 400 mg/m 2 iv bolus iv 2 h LV 200 mg/m 2 5 -FU 400 mg/m 2 iv bolus OX 85 mg/m 2 5 -FU 600 mg/m 2 iv 22 h d 3 5 -FU = 5 -fluorouracilo; LV = leucovorin (Folinato de calcio); OX = oxaliplatino
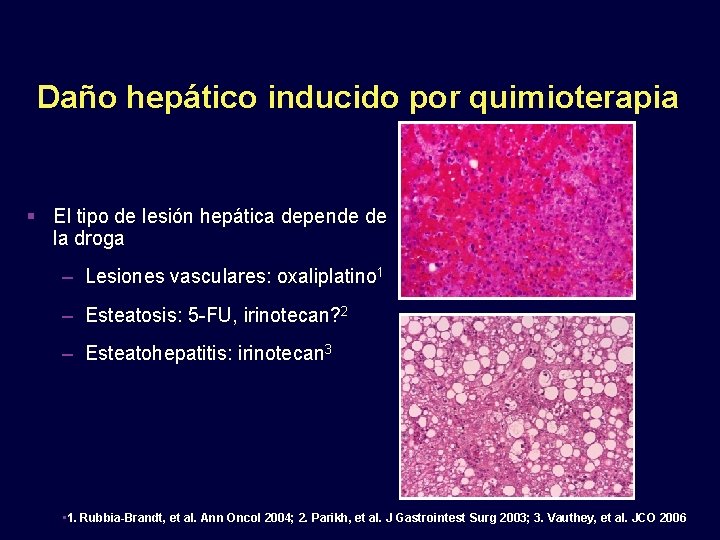
Daño hepático inducido por quimioterapia El tipo de lesión hepática depende de la droga – Lesiones vasculares: oxaliplatino 1 – Esteatosis: 5 -FU, irinotecan? 2 – Esteatohepatitis: irinotecan 3 • 1. Rubbia-Brandt, et al. Ann Oncol 2004; 2. Parikh, et al. J Gastrointest Surg 2003; 3. Vauthey, et al. JCO 2006

Cáncer de colon metastásico resecable Sospecha
Cáncer de colon metastásico resecable Sospecha TAC de TAP PET-CT
Cáncer de colon metastásico resecable Sospecha TAC de TAP PET-CT Cirugía hepática
Cáncer de colon metastásico resecable Sospecha TAC de TAP PET-CT Cirugía hepática Quimioterapia preoperatoria (? )
Cáncer de colon metastásico resecable Sospecha TAC de TAP PET-CT Cirugía hepática Quimioterapia postoperatoria Quimioterapia preoperatoria (? )

Conclusiones La metastasectomía hepática es una opción potencialmente curativa para un subgrupo de pacientes con metástasis de cáncer de colon y recto Las opciones de terapia sistémica incluyen: – Quimioterapia post-operatoria (Fluoruracilo) – Quimioterapia perioperatoria (FOLFOX) El papel de los biológicos (Bevacizumab / Cetuximab) por definir Si se hace quimioterapia preoperatoria, esta debe ser corta (aprox. 3 meses) para evitar daño hepático

TNM – Colon y Recto (AJCC 2010) M 0: No metástasis a distancia M 1: Metástasis a distancia – M 1 a: Sitio único de metástasis a distancia – M 1 b: Más de un sitio de metástasis a distancia
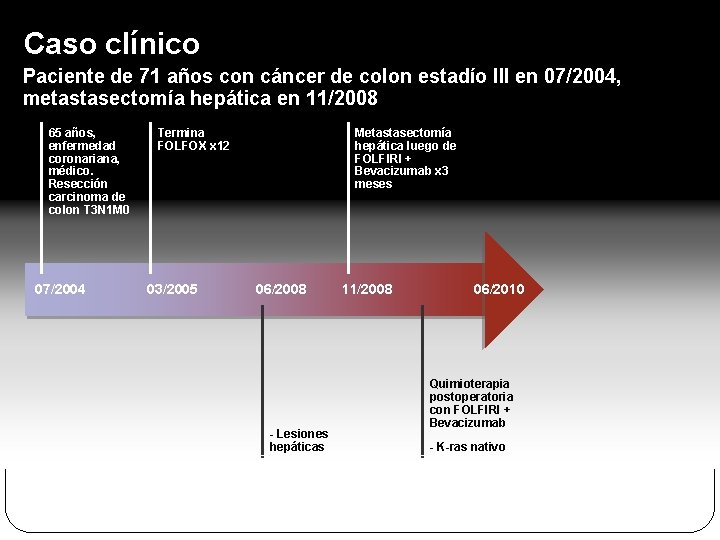
Caso clínico Paciente de 71 años con cáncer de colon estadío III en 07/2004, metastasectomía hepática en 11/2008 65 años, enfermedad coronariana, médico. Resección carcinoma de colon T 3 N 1 M 0 07/2004 Termina FOLFOX x 12 03/2005 Metastasectomía hepática luego de FOLFIRI + Bevacizumab x 3 meses 06/2008 - Lesiones hepáticas 11/2008 06/2010 Quimioterapia postoperatoria con FOLFIRI + Bevacizumab - K-ras nativo
• 16/06/2010
16/06/2010 PROSTATA

Terapia de mantenimiento en cáncer del pulmón de células no pequeñas Mauricio Lema, MD Oncología Clínica / Hematología Director Médico Clínica de Oncología Astorga Medellín, Colombia Oncología Clínica / Hematología Clínica SOMA Medellín, Colombia

Conflictos de Interés: Mauricio Lema Asesor y Speaker de Roche que manufacturan Capecitabina y Bevacizumab
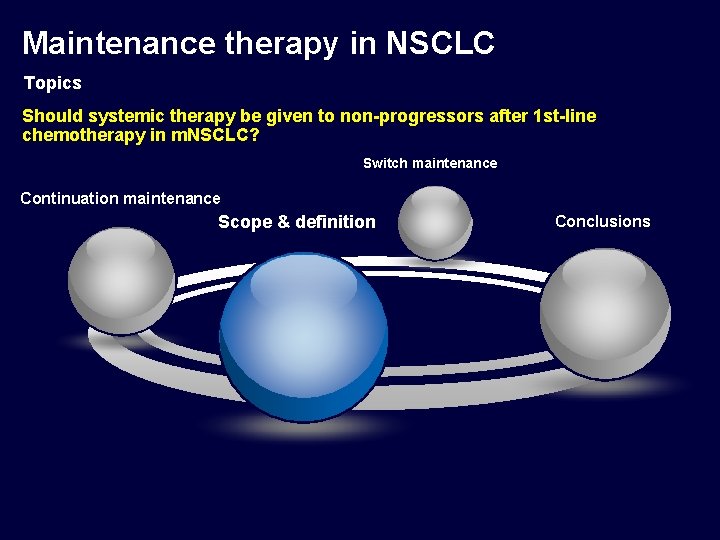
Maintenance therapy in NSCLC Topics Should systemic therapy be given to non-progressors after 1 st-line chemotherapy in m. NSCLC? Switch maintenance Continuation maintenance Scope & definition Conclusions
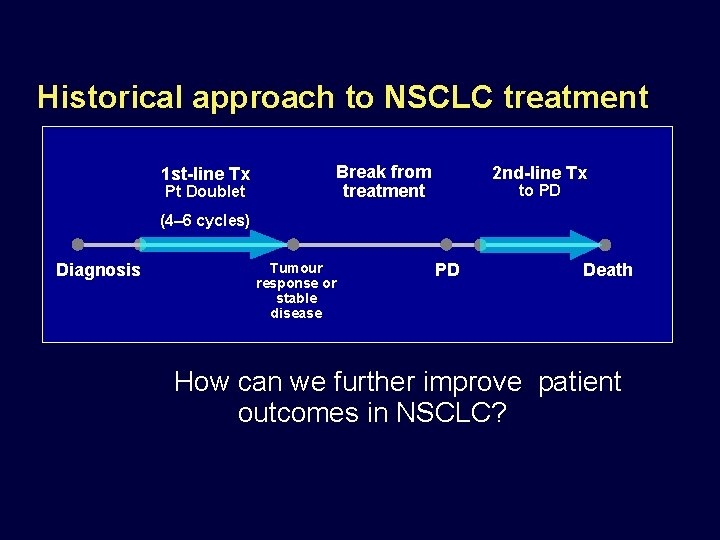
Historical approach to NSCLC treatment Break from treatment 1 st-line Tx Pt Doublet 2 nd-line Tx to PD (4– 6 cycles) Diagnosis Tumour response or stable disease PD Death How can we further improve patient outcomes in NSCLC?

Patients may not be eligible for furtherapy upon progression after first-line chemotherapy Socinski et al. 20021 Belani et al. 20032 Brodowicz et al. 20063 von Plessen et al. 20064 Barata et al. 20075 Park et al. 20076 Ciuleanu et al. 20087 Pirker et al. 20088 Scagliotti et al. 20089 Fidias et al. 200910 0 25 50 75 100 Patients receiving 2 nd-line therapy (%) In recent studies, approximately 50% of patients did not receive second-line therapy 1 J Clin Oncol 2002; 20: 1335– 43; 2 J Clin Oncol 2003; 21: 2933– 39; 3 Lung Cancer 2006; 52: 155– 63; 4 Br J Cancer 2006; 95: 966– 73; 5 J Thoracic Oncol 2007; 2(Suppl. 4): S 666 Abs. P 2 -235; 6 J Clin Oncol 2007; 25: 5233– 39; 7 J Clin Oncol 2008; 26(Suppl. 15 S): 426 s Abs. 8011; 8 J Clin Oncol 2008; 26(Suppl. 15 S): 6 s Abs. 3; 9 J Clin Oncol 2008; 26: 3543– 51; 10 J Clin Oncol 2009; 27: 591– 98

Maintenance therapy Continuation maintenance: the continued use of one of the agents given as 1 st line therapy after 4 -6 cycles of initial therapy in the absence of disease progression Switch maintenance: the initiation of a new agent not part of initial therapy after 4 -6 cycles of initial therapy the absence of disease progression. Kalemkarian et al, ASCO 2010
Revised approach to NSCLC treatment 2 nd-line Tx Active treatment 1 st-line Tx Pt Doublet to PD (4– 6 cycles) Diagnosis Tumour response or stable disease PD Patients with non-PD receive maintenance therapy deferring disease progression deferring symptom deterioration deferring death Death
Revised approach to NSCLC treatment 2 nd-line Tx Active treatment 1 st-line Tx Pt Doublet to PD (4– 6 cycles) Diagnosis Tumour response or stable disease PD Alternatives for active treatment following first-line chemotherapy continued cytotoxic doublet therapy continuation of agent used in first-line therapy (Avastin) different cytotoxic therapy (single agent, Alimta) targeted therapy (Tarceva) Death
Revised approach to NSCLC treatment 2 nd-line Tx Active treatment 1 st-line Tx Pt Doublet to PD (4– 6 cycles) Diagnosis Tumour response or stable disease PD Alternatives for active treatment following first-line chemotherapy continued cytotoxic doublet therapy continuation of agent used in first-line therapy (Avastin) different cytotoxic therapy (single agent, Alimta) targeted therapy (Tarceva) Death

Limited benefits and cumulative toxicity with extended cycles of chemotherapy Median no. of cycles (range) Overall survival, months (range) Socinski et al, Arm A (standard) 4 (0– 6) 6. 6 (5. 4– 9. 0) Socinski et al, Arm B (extended) 4 (0– 19) 8. 5 (6. 3– 10. 3) Park et al, Arm A (2 + 4 cycles) 6 (2– 6) 14. 9 (13. 0– 16. 8) Park et al, Arm B (2 + 2 cycles) 4 (2– 4) 15. 9 (12. 4– 19. 4) Patients who received additional cycles of chemotherapy had higher incidences of grade 3– 4 neurological and haematological toxicities Socinski MA, et al. J Clin Oncol 2002; 20: 1335– 43 Park JO, et al. J Clin Oncol 2007; 25: 5233– 9

Limited benefits and cumulative toxicity with extended cycles of chemotherapy Median no. of cycles (range) Overall survival, months (range) Socinski et al, Arm A (standard) 4 (0– 6) 6. 6 (5. 4– 9. 0) Socinski et al, Arm B (extended) 4 (0– 19) 8. 5 (6. 3– 10. 3) Park et al, Arm A (2 + 4 cycles) 6 (2– 6) 14. 9 (13. 0– 16. 8) Park et al, Arm B (2 + 2 cycles) 4 (2– 4) 15. 9 (12. 4– 19. 4) Patients who received additional cycles of chemotherapy had higher incidences of grade 3– 4 neurological and haematological toxicities Socinski MA, et al. J Clin Oncol 2002; 20: 1335– 43 Park JO, et al. J Clin Oncol 2007; 25: 5233– 9
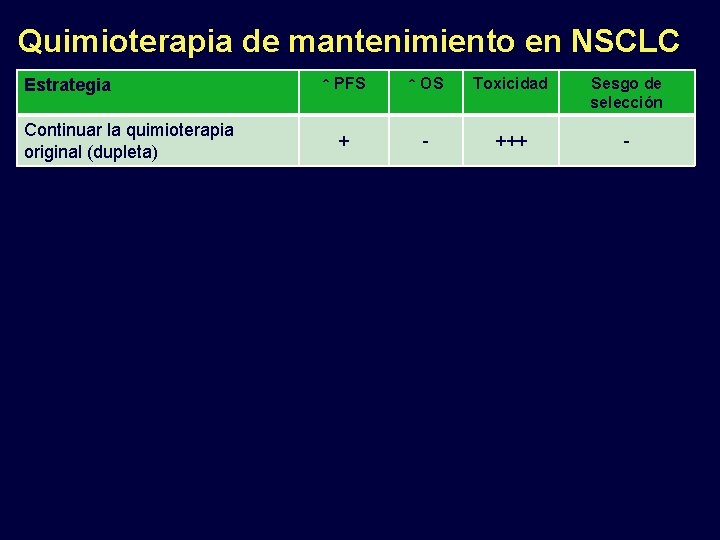
Quimioterapia de mantenimiento en NSCLC Estrategia Continuar la quimioterapia original (dupleta) ↑ PFS ↑ OS Toxicidad Sesgo de selección + - +++ -

Maintenance with cytotoxic chemotherapy Standard vs extended regimen (n) HR (95% CI) for PFS HR (95% CI) for OS Brodowicz, 2006 gemcitabine 68 vs 138 0. 69 (0. 56– 0. 86) 0. 84 (0. 52– 1. 38) Belani, 2003 paclitaxel 65 vs 65 NR 1. 02 (0. 66– 1. 57) Study Significantly longer PFS but modest improvement in OS Increased adverse events and impaired Qo. L Soon, Y et al. J Clin Oncol 2008; 26(Suppl. 15 Pt I): 427 s Abs. 8013
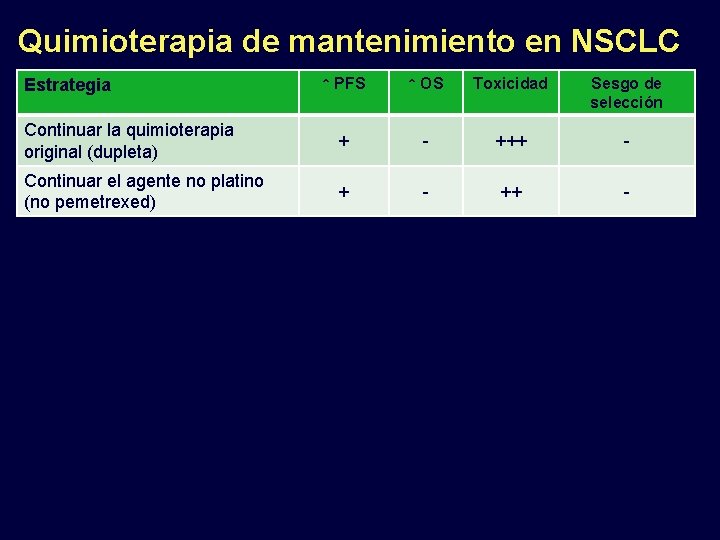
Quimioterapia de mantenimiento en NSCLC ↑ PFS ↑ OS Toxicidad Sesgo de selección Continuar la quimioterapia original (dupleta) + - +++ - Continuar el agente no platino (no pemetrexed) + - ++ - Estrategia
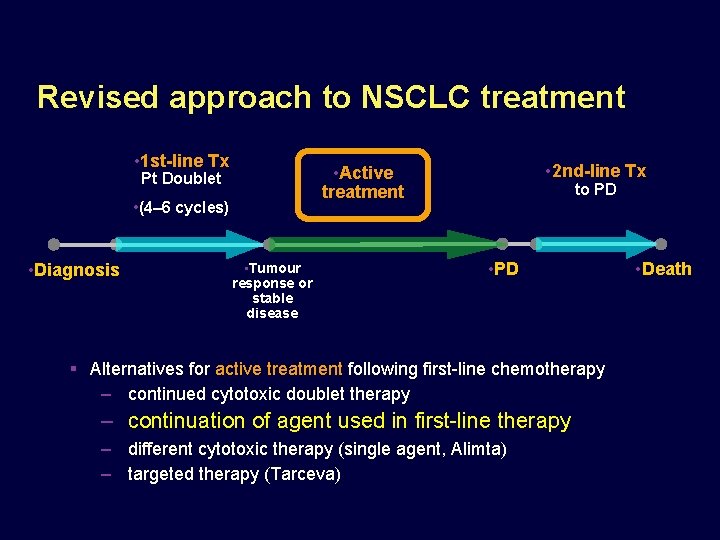
Revised approach to NSCLC treatment • 1 st-line Tx • (4– 6 cycles) • Diagnosis • 2 nd-line Tx • Active treatment Pt Doublet • Tumour response or stable disease to PD • PD Alternatives for active treatment following first-line chemotherapy – continued cytotoxic doublet therapy – continuation of agent used in first-line therapy – different cytotoxic therapy (single agent, Alimta) – targeted therapy (Tarceva) • Death

Phase III trial of bevacizumab in non-squamous NSCLC: ECOG 4599 (PC) Paclitaxel 200 mg/m 2 Carboplatin AUC 6 mg/m 2 q 3 wk) Eligibility Non-squamous NSCLC No crossover to bevacizumab permitted No Hx of hemoptysis No CNS metastases (PCB) PC x 6 cycles + bevacizumab (15 mg/kg q 3 wk) to PD Stratification variables RT vs no RT Stage IIIB or IV vs recurrent Wt loss < 5% vs ≥ 5% Measurable vs nonmeasurable Parameter PC PCB RR (%) 15 35 10. 3 12. 3 1 -year survival (%) 44 51 2 -year survival (%) 15 33 Median survival (months) Sandler A, et al. N Engl J Med. 2006; 355: 2542 -50. p value p = 0. 003
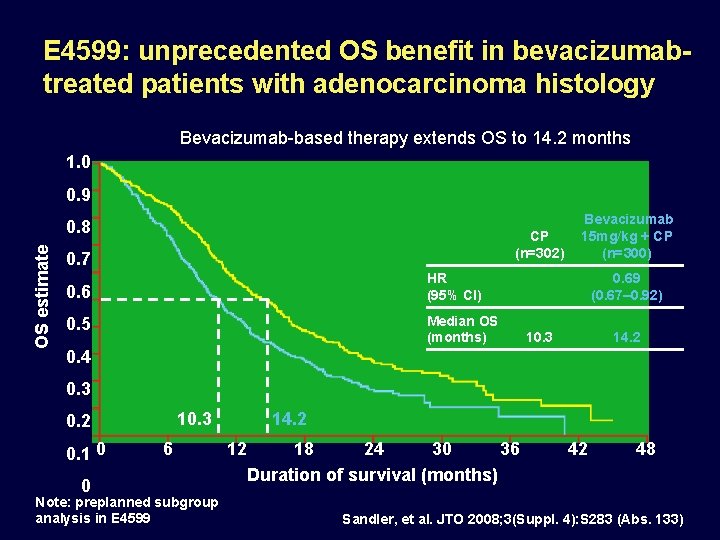
E 4599: unprecedented OS benefit in bevacizumabtreated patients with adenocarcinoma histology Bevacizumab-based therapy extends OS to 14. 2 months 1. 0 increase of 3. 9 months vs CP 0. 9 31% reduction in the risk of death OS estimate 0. 8 CP (n=302) 0. 7 0. 6 HR (95% CI) 0. 5 Median OS (months) Bevacizumab 15 mg/kg + CP (n=300) 0. 69 (0. 67– 0. 92) 10. 3 14. 2 0. 4 0. 3 10. 3 0. 2 0. 1 0 0 6 Note: preplanned subgroup analysis in E 4599 14. 2 12 18 24 30 36 Duration of survival (months) 42 48 Sandler, et al. JTO 2008; 3(Suppl. 4): S 283 (Abs. 133)
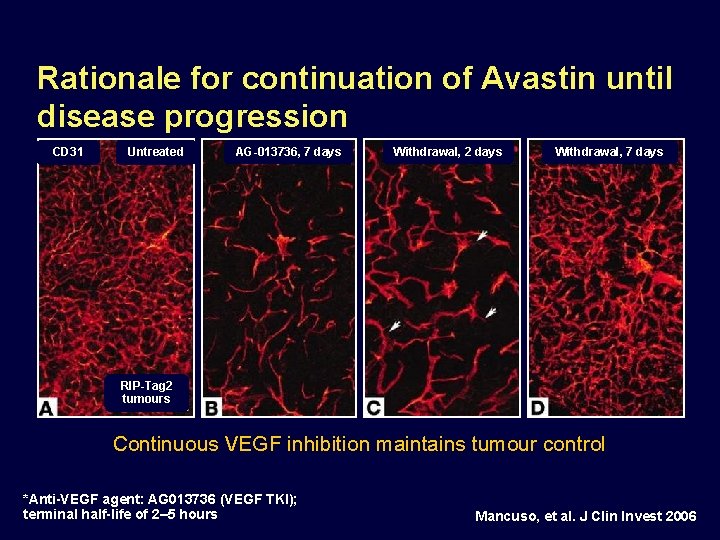
Rationale for continuation of Avastin until disease progression CD 31 Untreated AG-013736, 7 days Withdrawal, 2 days Withdrawal, 7 days RIP-Tag 2 tumours Continuous VEGF inhibition maintains tumour control *Anti-VEGF agent: AG 013736 (VEGF TKI); terminal half-life of 2– 5 hours Mancuso, et al. J Clin Invest 2006
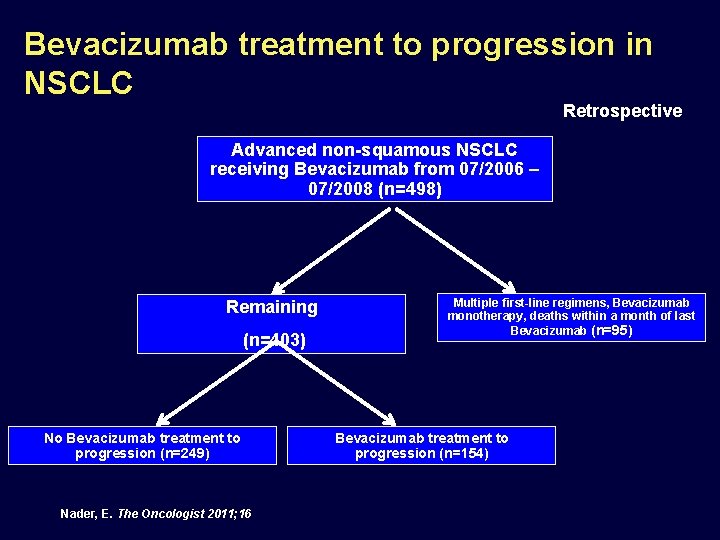
Bevacizumab treatment to progression in NSCLC Retrospective Advanced non-squamous NSCLC receiving Bevacizumab from 07/2006 – 07/2008 (n=498) Remaining (n=403) No Bevacizumab treatment to progression (n=249) Nader, E. The Oncologist 2011; 16 Multiple first-line regimens, Bevacizumab monotherapy, deaths within a month of last Bevacizumab (n=95) Bevacizumab treatment to progression (n=154)
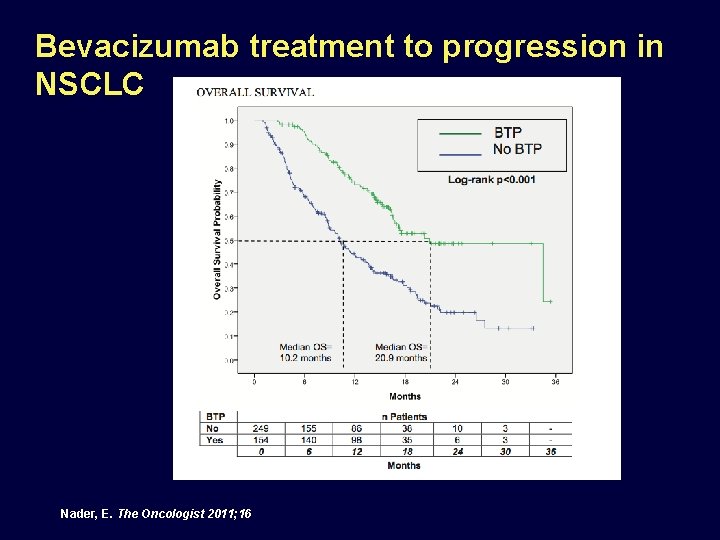
Bevacizumab treatment to progression in NSCLC Nader, E. The Oncologist 2011; 16
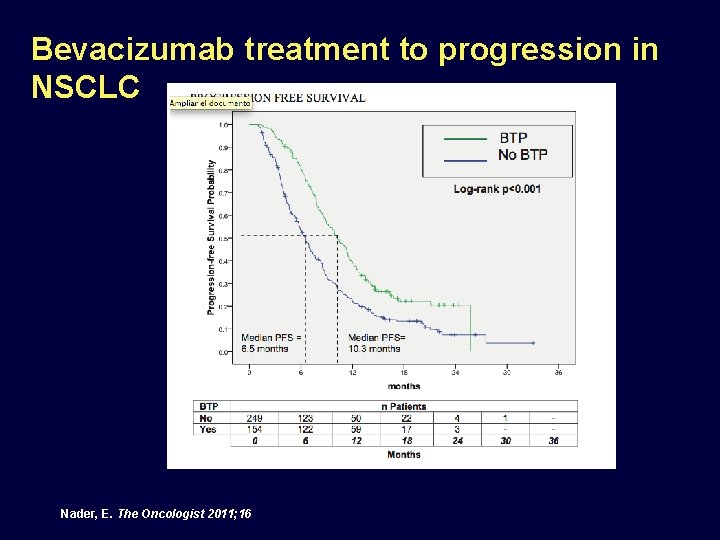
Bevacizumab treatment to progression in NSCLC Nader, E. The Oncologist 2011; 16

PARAMOUNT: Continuación de Pemetrexed (Pem) después de no progresión con Cisplatino + Pem Pacientes con cáncer del pulmón noescamoso avanzado, sin progresión después de 4 ciclos de Cisplatino + Pemetrexed*, y PS 0/1 Placebo (n=180) 1: 2 Pemetrexed** (n=359) * Cisplatino 75 mg/m 2/día 1, IV + Pemetrexed 500 mg/m 2/día 1, IV; **Pemetrexed: 500 mg/m 2/día 1, IV 939 pacientes participaron en la fase de inducción – No progresión en 539 (57. 4%) Desenlace Principal: Supervivencia Libre de Progresión (mediano, meses) – Placebo: 2. 6 meses – Pemetrexed: 3. 9 meses – HR: 0. 64 (p=0. 00025) Referencia: Paz-Ares LG, et al. J Clin Oncol 29: 2011 (suppl; CRA 7510)
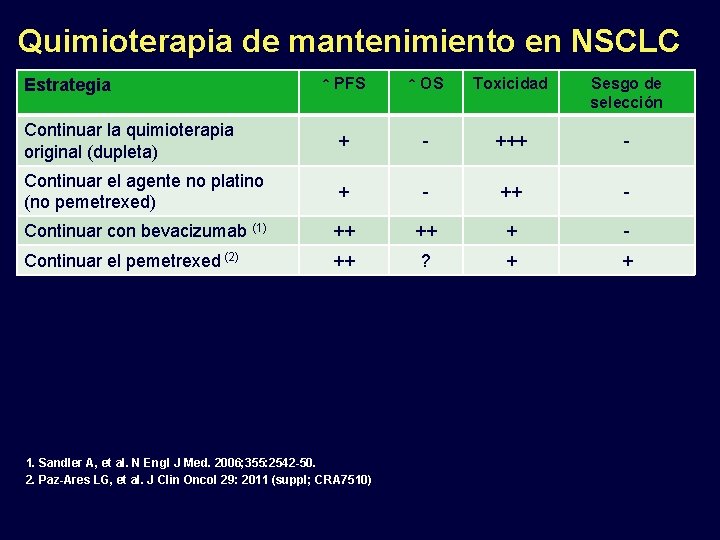
Quimioterapia de mantenimiento en NSCLC ↑ PFS ↑ OS Toxicidad Sesgo de selección Continuar la quimioterapia original (dupleta) + - +++ - Continuar el agente no platino (no pemetrexed) + - ++ - Continuar con bevacizumab (1) ++ ++ + - Continuar el pemetrexed (2) ++ ? + + Estrategia 1. Sandler A, et al. N Engl J Med. 2006; 355: 2542 -50. 2. Paz-Ares LG, et al. J Clin Oncol 29: 2011 (suppl; CRA 7510)
Revised approach to NSCLC treatment 2 nd-line Tx Active treatment 1 st-line Tx Pt Doublet to PD (4– 6 cycles) Diagnosis Tumour response or stable disease PD Alternatives for active treatment following first-line chemotherapy continued cytotoxic doublet therapy continuation of agent used in first-line therapy different cytotoxic therapy (single agent) targeted therapy Death
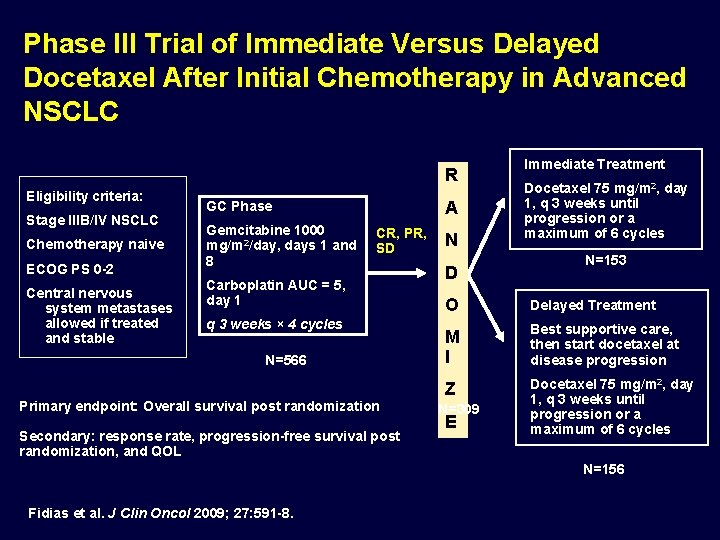
Phase III Trial of Immediate Versus Delayed Docetaxel After Initial Chemotherapy in Advanced NSCLC R Eligibility criteria: Stage IIIB/IV NSCLC Chemotherapy naive ECOG PS 0 -2 Central nervous system metastases allowed if treated and stable A GC Phase Gemcitabine 1000 mg/m 2/day, days 1 and 8 CR, PR, SD Carboplatin AUC = 5, day 1 q 3 weeks × 4 cycles N=566 Primary endpoint: Overall survival post randomization Secondary: response rate, progression-free survival post randomization, and QOL N D Immediate Treatment Docetaxel 75 mg/m 2, day 1, q 3 weeks until progression or a maximum of 6 cycles N=153 O Delayed Treatment M I Best supportive care, then start docetaxel at disease progression Z Docetaxel 75 mg/m 2, day 1, q 3 weeks until progression or a maximum of 6 cycles N=309 E N=156 Fidias et al. J Clin Oncol 2009; 27: 591 -8.
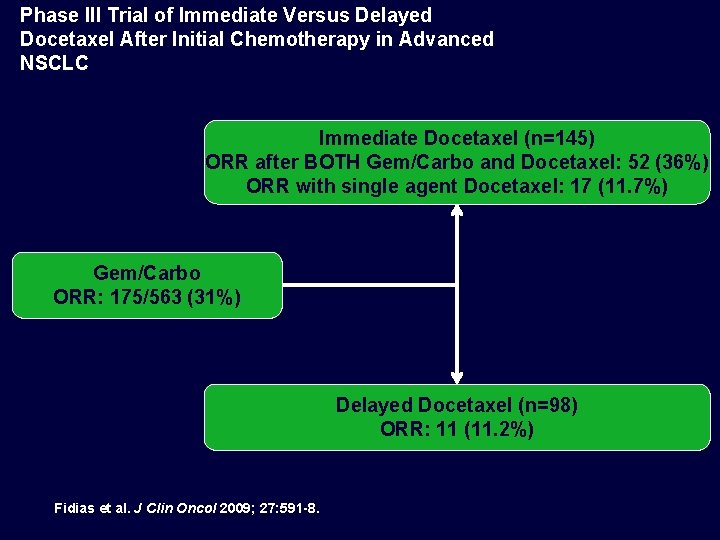
Phase III Trial of Immediate Versus Delayed Docetaxel After Initial Chemotherapy in Advanced NSCLC Immediate Docetaxel (n=145) ORR after BOTH Gem/Carbo and Docetaxel: 52 (36%) ORR with single agent Docetaxel: 17 (11. 7%) Gem/Carbo ORR: 175/563 (31%) Delayed Docetaxel (n=98) ORR: 11 (11. 2%) Fidias et al. J Clin Oncol 2009; 27: 591 -8.
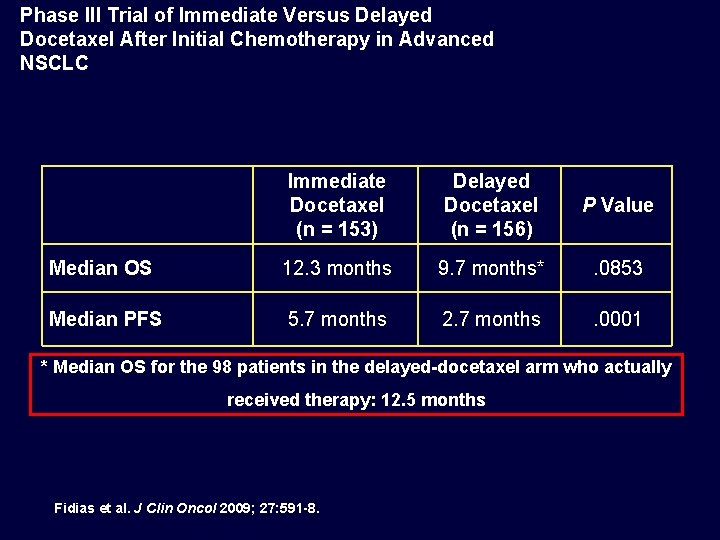
Phase III Trial of Immediate Versus Delayed Docetaxel After Initial Chemotherapy in Advanced NSCLC Immediate Docetaxel (n = 153) Delayed Docetaxel (n = 156) P Value Median OS 12. 3 months 9. 7 months* . 0853 Median PFS 5. 7 months 2. 7 months . 0001 * Median OS for the 98 patients in the delayed-docetaxel arm who actually received therapy: 12. 5 months Fidias et al. J Clin Oncol 2009; 27: 591 -8.
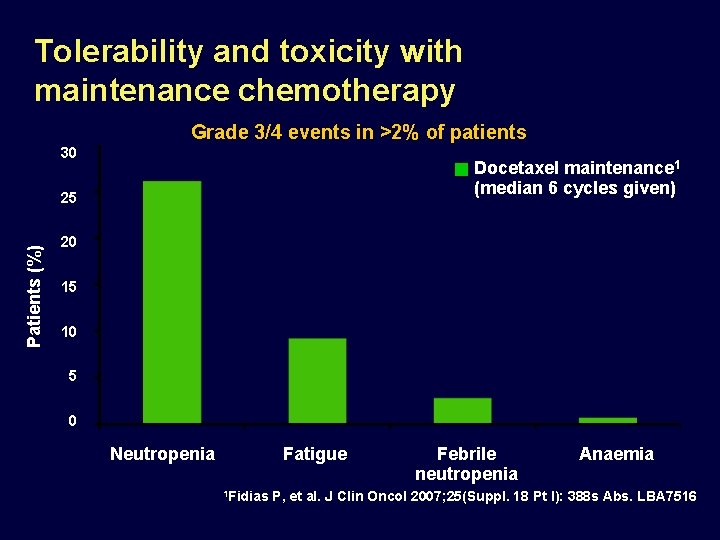
Tolerability and toxicity with maintenance chemotherapy Grade 3/4 events in >2% of patients 30 Docetaxel maintenance 1 (median 6 cycles given) Patients (%) 25 20 15 10 5 0 Neutropenia Fatigue 1 Fidias Febrile neutropenia Anaemia P, et al. J Clin Oncol 2007; 25(Suppl. 18 Pt I): 388 s Abs. LBA 7516
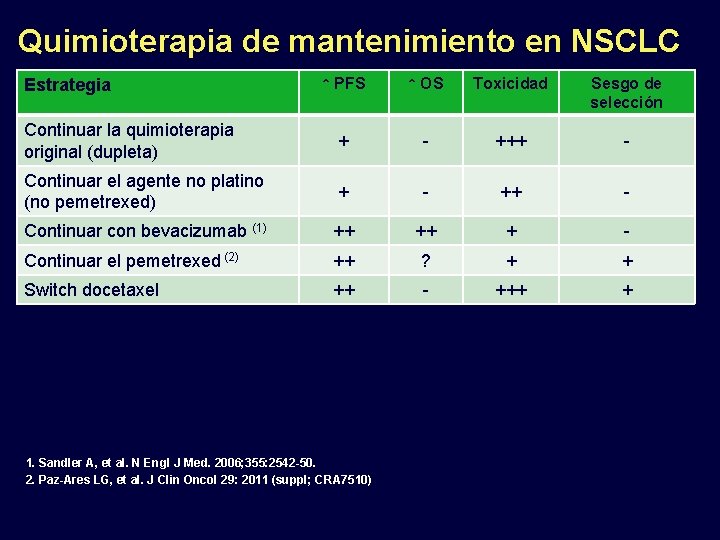
Quimioterapia de mantenimiento en NSCLC ↑ PFS ↑ OS Toxicidad Sesgo de selección Continuar la quimioterapia original (dupleta) + - +++ - Continuar el agente no platino (no pemetrexed) + - ++ - Continuar con bevacizumab (1) ++ ++ + - Continuar el pemetrexed (2) ++ ? + + Switch docetaxel ++ - +++ + Estrategia 1. Sandler A, et al. N Engl J Med. 2006; 355: 2542 -50. 2. Paz-Ares LG, et al. J Clin Oncol 29: 2011 (suppl; CRA 7510)
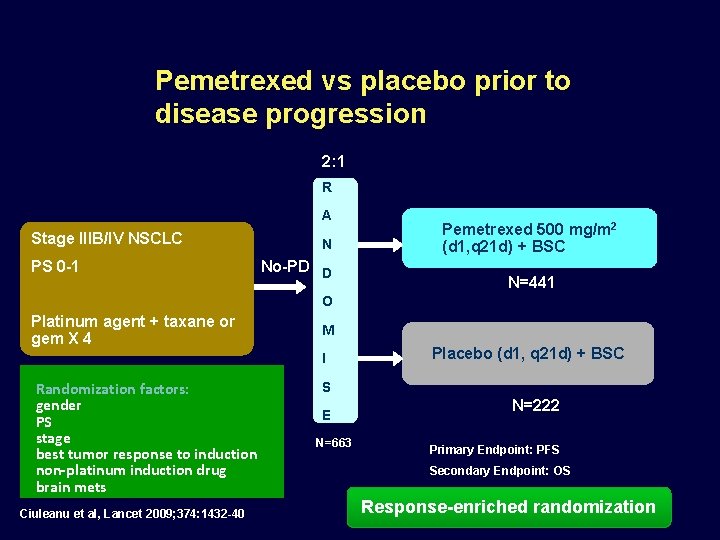
Pemetrexed vs placebo prior to disease progression 2: 1 R A Stage IIIB/IV NSCLC PS 0 -1 N No-PD D Pemetrexed 500 mg/m 2 (d 1, q 21 d) + BSC N=441 O Platinum agent + taxane or gem X 4 M I Randomization factors: gender PS stage best tumor response to induction non-platinum induction drug brain mets Ciuleanu et al, Lancet 2009; 374: 1432 -40 Placebo (d 1, q 21 d) + BSC S E N=663 N=222 Primary Endpoint: PFS Secondary Endpoint: OS Response-enriched randomization
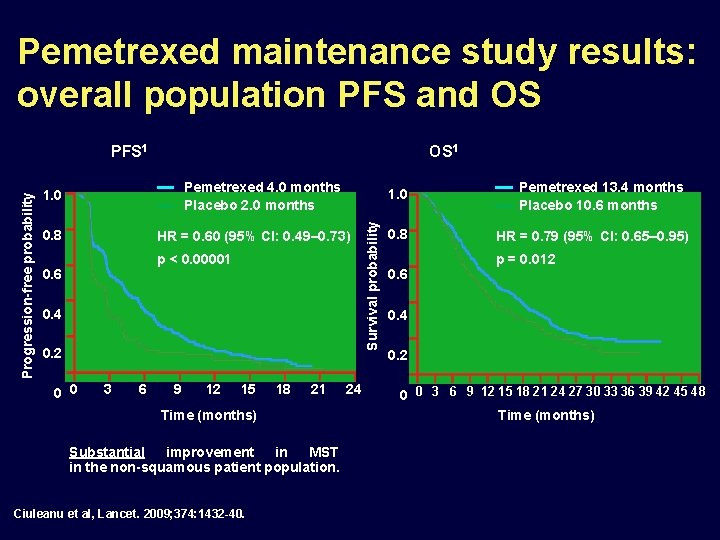
Pemetrexed maintenance study results: overall population PFS and OS OS 1 Pemetrexed 4. 0 months Placebo 2. 0 months 1. 0 0. 8 1. 0 HR = 0. 60 (95% CI: 0. 49– 0. 73) p < 0. 00001 0. 6 0. 4 0. 2 0 0 3 6 9 12 15 18 21 Time (months) Substantial improvement in MST in the non-squamous patient population. Ciuleanu et al, Lancet. 2009; 374: 1432 -40. 24 Survival probability Progression-free probability PFS 1 0. 8 Pemetrexed 13. 4 months Placebo 10. 6 months HR = 0. 79 (95% CI: 0. 65– 0. 95) p = 0. 012 0. 6 0. 4 0. 2 0 0 3 6 9 12 15 18 21 24 27 30 33 36 39 42 45 48 Time (months)
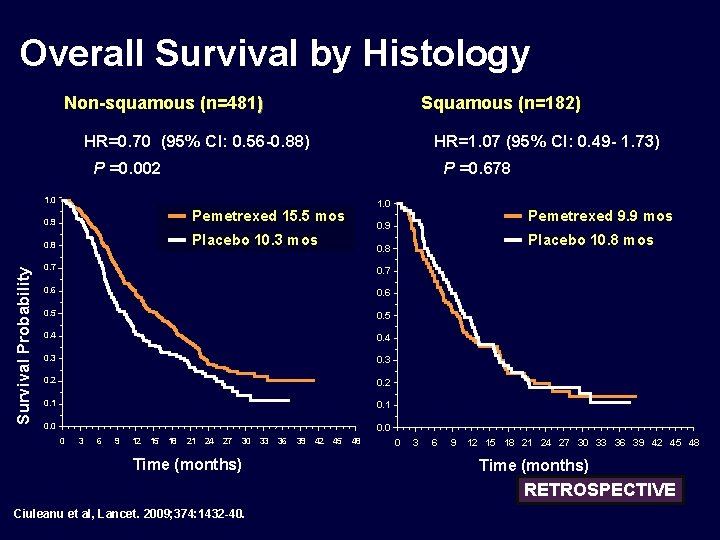
Overall Survival by Histology Non-squamous (n=481) Squamous (n=182) HR=0. 70 (95% CI: 0. 56 -0. 88) HR=1. 07 (95% CI: 0. 49 - 1. 73) P =0. 002 P =0. 678 Survival Probability 1. 0 0. 9 Pemetrexed 15. 5 mos 0. 8 Placebo 10. 3 mos 1. 0 0. 7 0. 6 0. 5 0. 4 0. 3 0. 2 0. 1 0. 0 3 6 9 12 15 18 21 24 27 30 Time (months) 33 36 39 42 Placebo 10. 8 mos 0. 8 0. 7 0 Pemetrexed 9. 9 mos 0. 9 45 48 0 3 6 9 12 15 18 21 24 27 30 33 36 39 42 45 48 Time (months) RETROSPECTIVE Ciuleanu et al, Lancet. 2009; 374: 1432 -40.
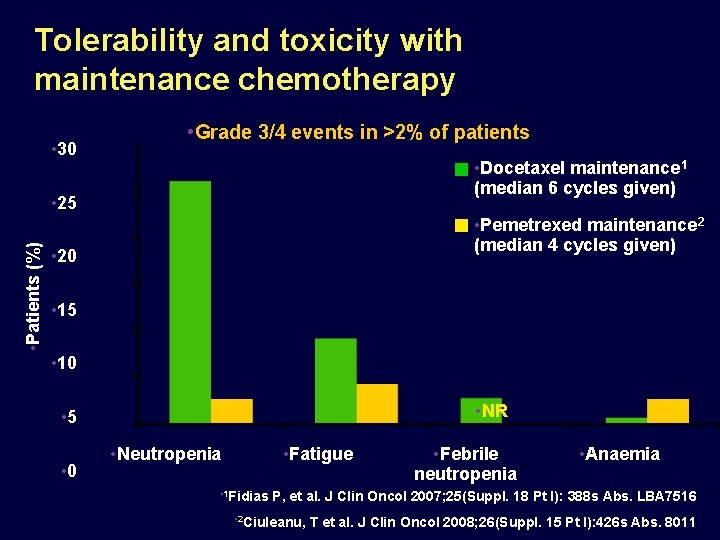
Tolerability and toxicity with maintenance chemotherapy • 30 • Grade 3/4 events in >2% of patients • Docetaxel maintenance 1 (median 6 cycles given) • Patients (%) • 25 • Pemetrexed maintenance 2 (median 4 cycles given) • 20 • 15 • 10 • NR • 5 • 0 • Neutropenia • Fatigue • 1 Fidias • Febrile neutropenia • Anaemia P, et al. J Clin Oncol 2007; 25(Suppl. 18 Pt I): 388 s Abs. LBA 7516 • 2 Ciuleanu, T et al. J Clin Oncol 2008; 26(Suppl. 15 Pt I): 426 s Abs. 8011
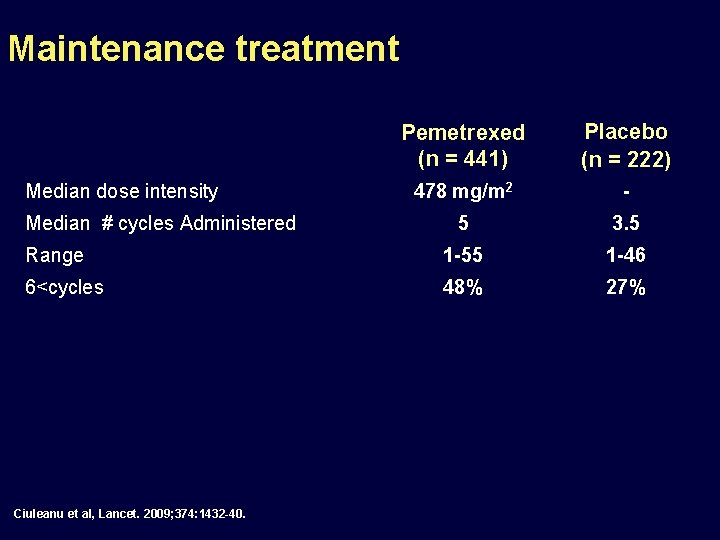
Maintenance treatment Pemetrexed (n = 441) Placebo (n = 222) 478 mg/m 2 - 5 3. 5 Range 1 -55 1 -46 6<cycles 48% 27% Median dose intensity Median # cycles Administered Ciuleanu et al, Lancet. 2009; 374: 1432 -40.
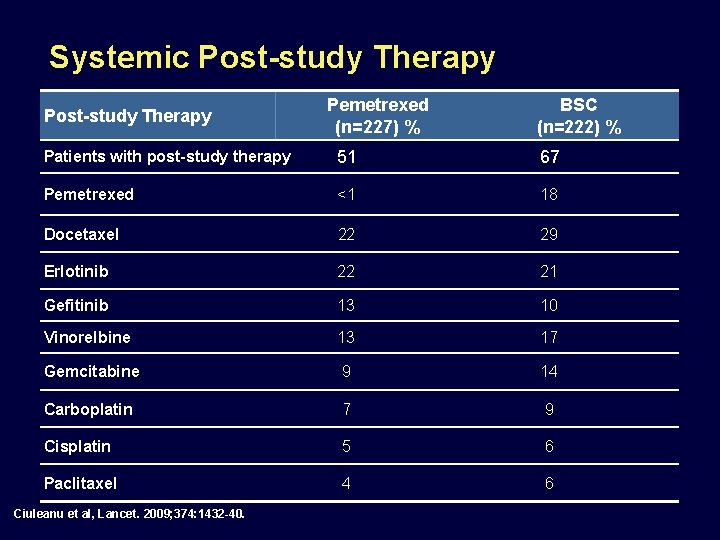
Systemic Post-study Therapy Pemetrexed (n=227) % BSC (n=222) % Patients with post-study therapy 51 67 Pemetrexed <1 18 Docetaxel 22 29 Erlotinib 22 21 Gefitinib 13 10 Vinorelbine 13 17 Gemcitabine 9 14 Carboplatin 7 9 Cisplatin 5 6 Paclitaxel 4 6 Ciuleanu et al, Lancet. 2009; 374: 1432 -40.
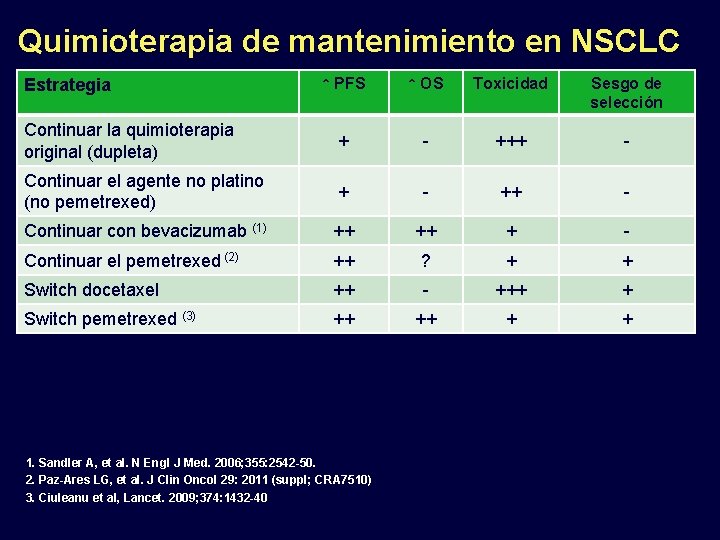
Quimioterapia de mantenimiento en NSCLC ↑ PFS ↑ OS Toxicidad Sesgo de selección Continuar la quimioterapia original (dupleta) + - +++ - Continuar el agente no platino (no pemetrexed) + - ++ - Continuar con bevacizumab (1) ++ ++ + - Continuar el pemetrexed (2) ++ ? + + Switch docetaxel ++ - +++ + Switch pemetrexed (3) ++ ++ + + Estrategia 1. Sandler A, et al. N Engl J Med. 2006; 355: 2542 -50. 2. Paz-Ares LG, et al. J Clin Oncol 29: 2011 (suppl; CRA 7510) 3. Ciuleanu et al, Lancet. 2009; 374: 1432 -40

Not all RANDOMIZATIONS are EQUAL. . . Arm A Inclusion criteria R Arm B • “Unselected” randomization Maintenance 2011
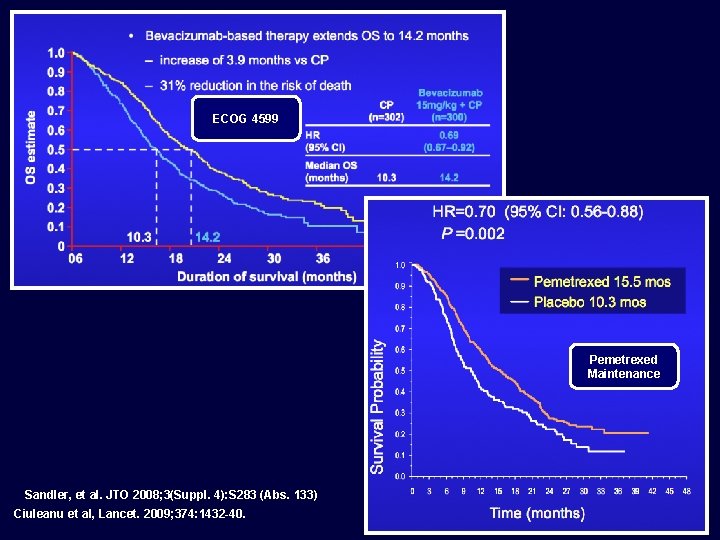
ECOG 4599 Pemetrexed Maintenance Sandler, et al. JTO 2008; 3(Suppl. 4): S 283 (Abs. 133) Ciuleanu et al, Lancet. 2009; 374: 1432 -40.
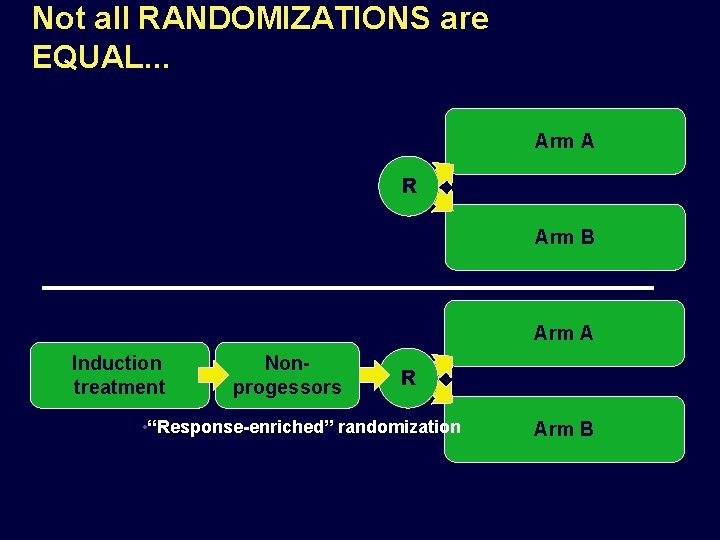
Not all RANDOMIZATIONS are EQUAL. . . Arm A R Arm B Arm A Induction treatment Nonprogessors R • “Response-enriched” randomization Arm B
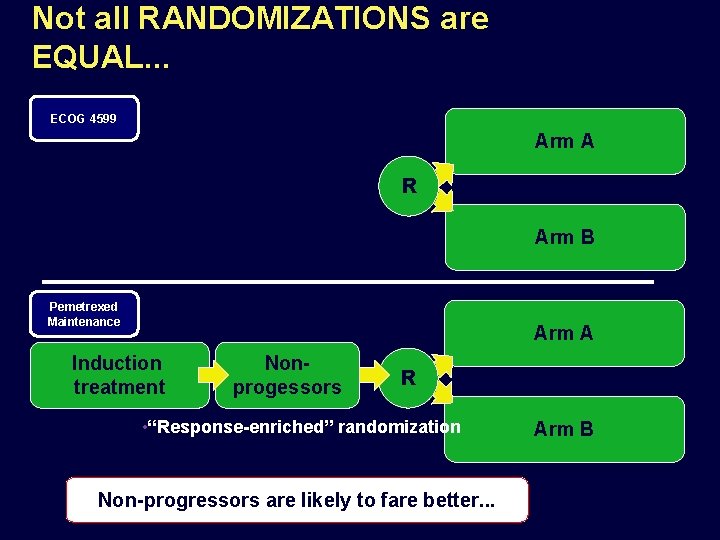
Not all RANDOMIZATIONS are EQUAL. . . ECOG 4599 Arm A R Arm B Pemetrexed Maintenance Arm A Induction treatment Nonprogessors R • “Response-enriched” randomization Non-progressors are likely to fare better. . . Arm B
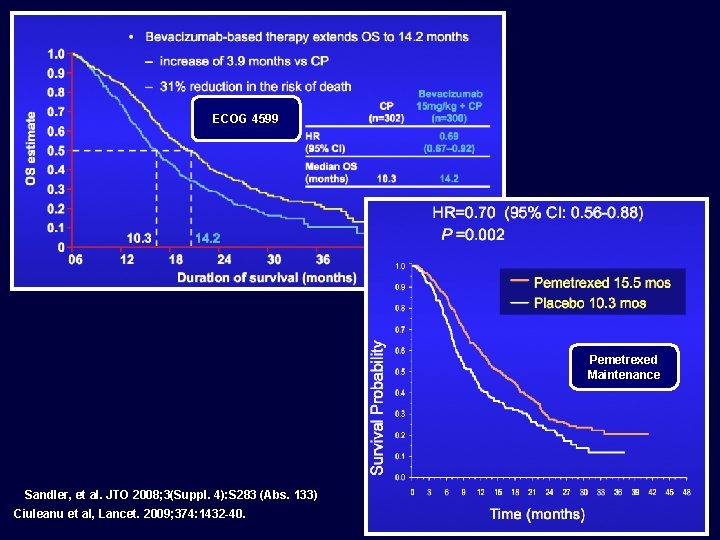
ECOG 4599 Pemetrexed Maintenance Sandler, et al. JTO 2008; 3(Suppl. 4): S 283 (Abs. 133) Ciuleanu et al, Lancet. 2009; 374: 1432 -40.

Pemetrexed continuation pitfalls Not suitable for patients with squamous-NSCLC Not applicable to patients treated with Bevacizumab + CT in 1 st line Comparison with Bevacizumab + CT continuation not possible due to randomization strategy – Unselected in Bevacizumab + CT trials – Response-enriched in Pemetrexed trial No evidence of continuation maintenance with pemetrexed – Pemetrexed likely benefit small or nil due to little evidence of benefit of pemetrexed after 5 cycles in ANY setting
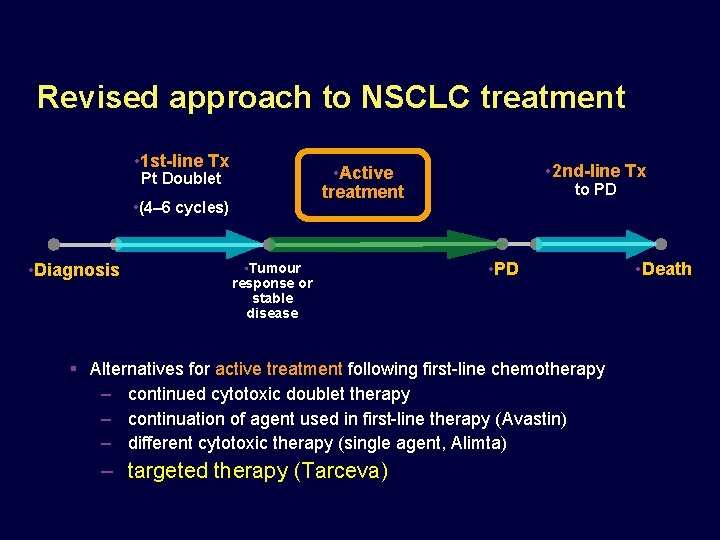
Revised approach to NSCLC treatment • 1 st-line Tx • (4– 6 cycles) • Diagnosis • 2 nd-line Tx • Active treatment Pt Doublet • Tumour response or stable disease to PD • PD Alternatives for active treatment following first-line chemotherapy – continued cytotoxic doublet therapy – continuation of agent used in first-line therapy (Avastin) – different cytotoxic therapy (single agent, Alimta) – targeted therapy (Tarceva) • Death
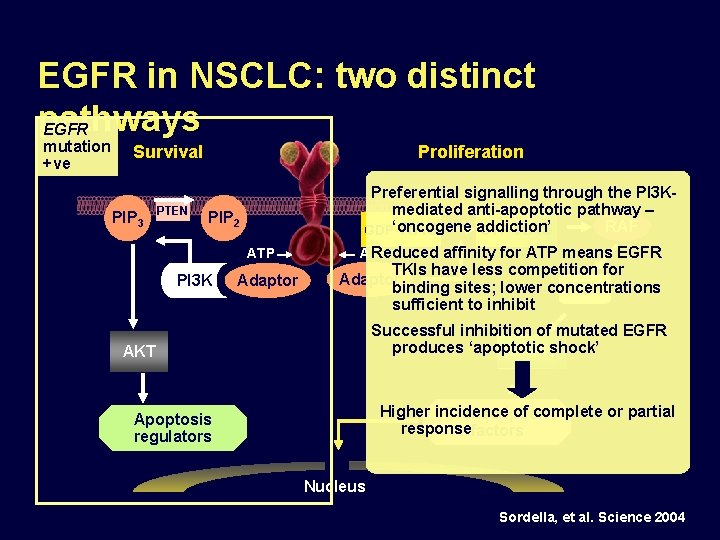
EGFR in NSCLC: two distinct pathways EGFR mutation +ve Proliferation Survival PIP 3 PTEN Preferential signalling through the PI 3 Kmediated anti-apoptotic pathway – RAF addiction’ GDP‘oncogene -RAS GTP-RAS PIP 2 ATP PI 3 K Adaptor ATP Reduced affinity for ATP means EGFR TKIs have less competition for Adaptor binding sites; lower concentrations MEK sufficient to inhibit Successful inhibition of mutated EGFR produces ‘apoptotic MAPKshock’ AKT Higher incidence of complete or partial Transcription responsefactors Apoptosis regulators Nucleus Sordella, et al. Science 2004
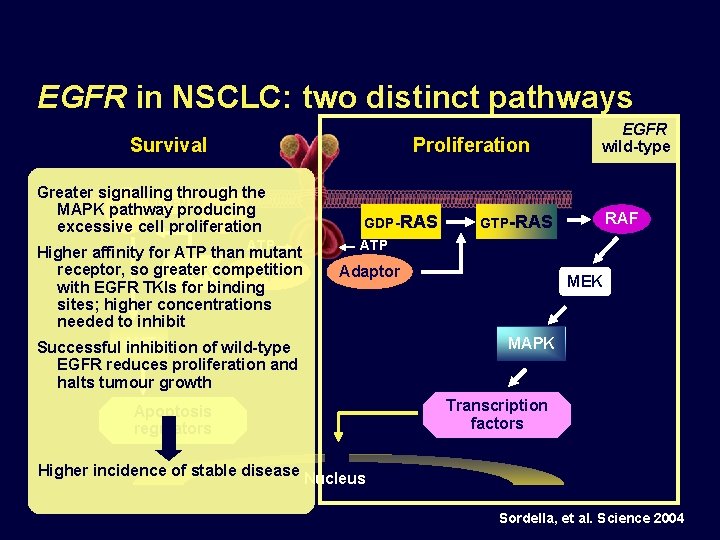
EGFR in NSCLC: two distinct pathways Proliferation Survival Greater signalling through the PTEN MAPK pathway producing PIP 3 PIP 2 excessive cell proliferation Higher affinity for ATP than ATP mutant receptor, so greater PI 3 Kcompetition Adaptor with EGFR TKIs for binding sites; higher concentrations needed to inhibit Successful AKT inhibition of wild-type EGFR reduces proliferation and halts tumour growth GDP-RAS EGFR wild-type RAF GTP-RAS ATP Adaptor Apoptosis regulators MEK MAPK Transcription factors Higher incidence of stable disease Nucleus Sordella, et al. Science 2004
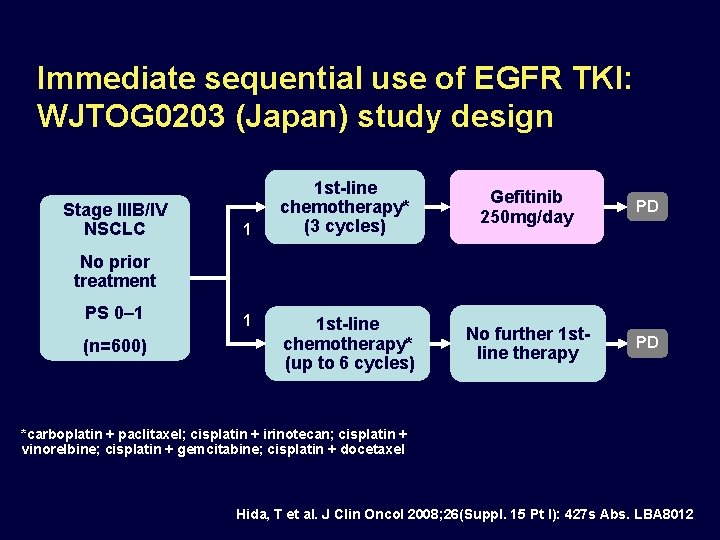
Immediate sequential use of EGFR TKI: WJTOG 0203 (Japan) study design Stage IIIB/IV NSCLC 1 1 st-line chemotherapy* (3 cycles) Gefitinib 250 mg/day PD 1 st-line chemotherapy* (up to 6 cycles) No further 1 stline therapy PD No prior treatment PS 0– 1 (n=600) 1 *carboplatin + paclitaxel; cisplatin + irinotecan; cisplatin + vinorelbine; cisplatin + gemcitabine; cisplatin + docetaxel Hida, T et al. J Clin Oncol 2008; 26(Suppl. 15 Pt I): 427 s Abs. LBA 8012
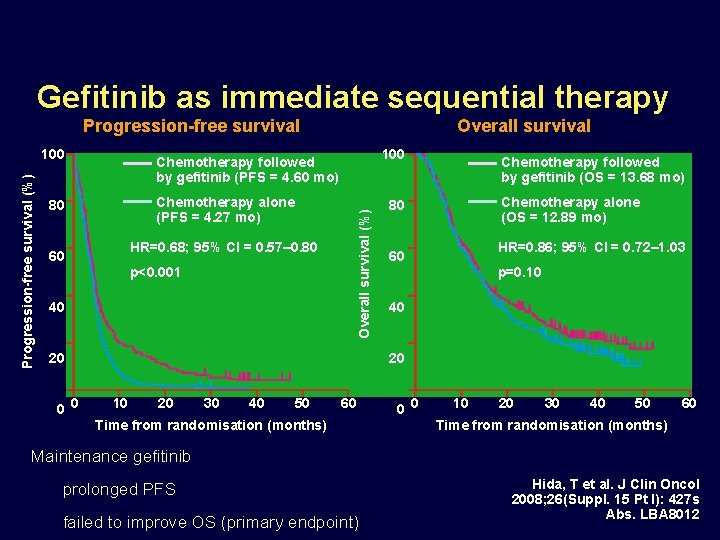
Gefitinib as immediate sequential therapy Progression-free survival 100 Chemotherapy followed by gefitinib (PFS = 4. 60 mo) Chemotherapy alone (PFS = 4. 27 mo) 80 HR=0. 68; 95% CI = 0. 57– 0. 80 60 p<0. 001 40 Overall survival (%) Progression-free survival (%) 100 Overall survival 20 0 0 Chemotherapy followed by gefitinib (OS = 13. 68 mo) Chemotherapy alone (OS = 12. 89 mo) 80 HR=0. 86; 95% CI = 0. 72– 1. 03 60 p=0. 10 40 20 10 20 30 40 50 60 Time from randomisation (months) 0 0 10 20 30 40 50 60 Time from randomisation (months) Maintenance gefitinib prolonged PFS failed to improve OS (primary endpoint) Hida, T et al. J Clin Oncol 2008; 26(Suppl. 15 Pt I): 427 s Abs. LBA 8012
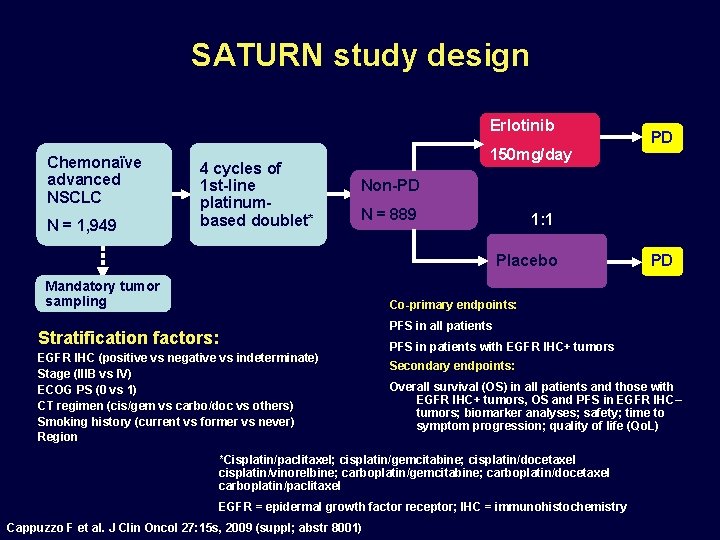
SATURN study design Erlotinib Chemonaïve advanced NSCLC N = 1, 949 4 cycles of 1 st-line platinumbased doublet* 150 mg/day PD Non-PD N = 889 1: 1 Placebo Mandatory tumor sampling PD Co-primary endpoints: PFS in all patients Stratification factors: EGFR IHC (positive vs negative vs indeterminate) Stage (IIIB vs IV) ECOG PS (0 vs 1) CT regimen (cis/gem vs carbo/doc vs others) Smoking history (current vs former vs never) Region PFS in patients with EGFR IHC+ tumors Secondary endpoints: Overall survival (OS) in all patients and those with EGFR IHC+ tumors, OS and PFS in EGFR IHC– tumors; biomarker analyses; safety; time to symptom progression; quality of life (Qo. L) *Cisplatin/paclitaxel; cisplatin/gemcitabine; cisplatin/docetaxel cisplatin/vinorelbine; carboplatin/gemcitabine; carboplatin/docetaxel carboplatin/paclitaxel EGFR = epidermal growth factor receptor; IHC = immunohistochemistry Cappuzzo F et al. J Clin Oncol 27: 15 s, 2009 (suppl; abstr 8001)
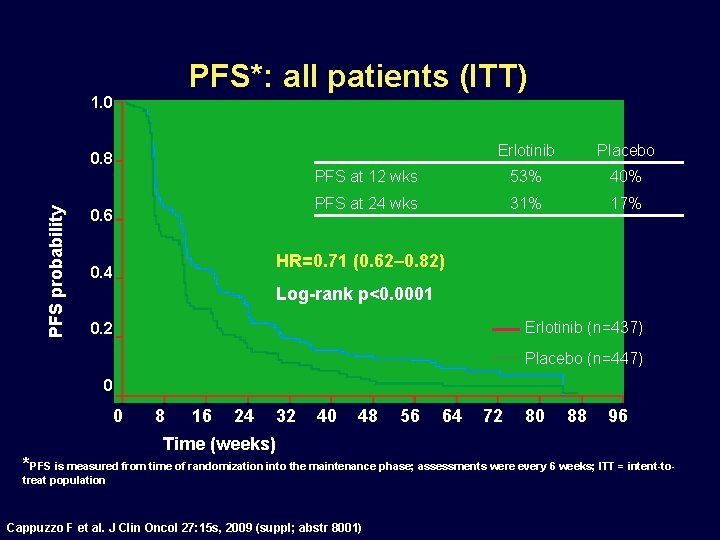
PFS*: all patients (ITT) 1. 0 Erlotinib Placebo PFS at 12 wks 53% 40% PFS at 24 wks 31% 17% PFS probability 0. 8 0. 6 HR=0. 71 (0. 62– 0. 82) 0. 4 Log-rank p<0. 0001 Erlotinib (n=437) 0. 2 Placebo (n=447) 0 0 8 16 24 32 40 48 56 64 72 80 88 96 Time (weeks) *PFS is measured from time of randomization into the maintenance phase; assessments were every 6 weeks; ITT = intent-totreat population Cappuzzo F et al. J Clin Oncol 27: 15 s, 2009 (suppl; abstr 8001)
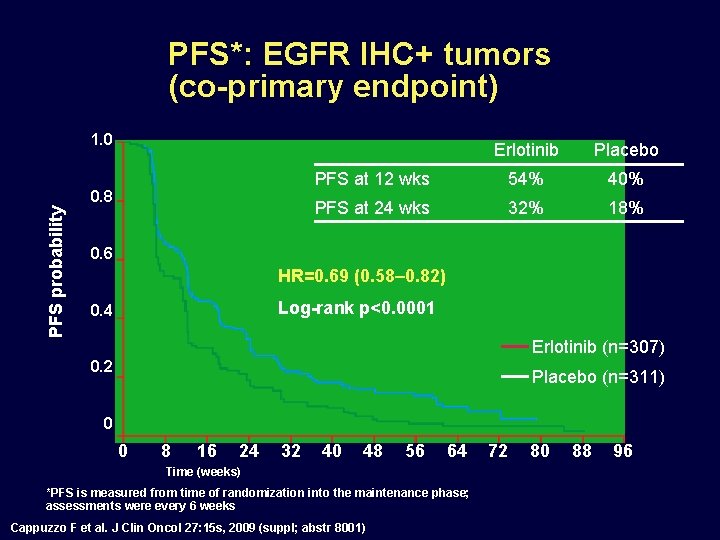
PFS*: EGFR IHC+ tumors (co-primary endpoint) 1. 0 PFS probability 0. 8 Erlotinib Placebo PFS at 12 wks 54% 40% PFS at 24 wks 32% 18% 0. 6 HR=0. 69 (0. 58– 0. 82) Log-rank p<0. 0001 0. 4 Erlotinib (n=307) 0. 2 Placebo (n=311) 0 0 8 16 24 32 40 48 56 64 Time (weeks) *PFS is measured from time of randomization into the maintenance phase; assessments were every 6 weeks Cappuzzo F et al. J Clin Oncol 27: 15 s, 2009 (suppl; abstr 8001) 72 80 88 96
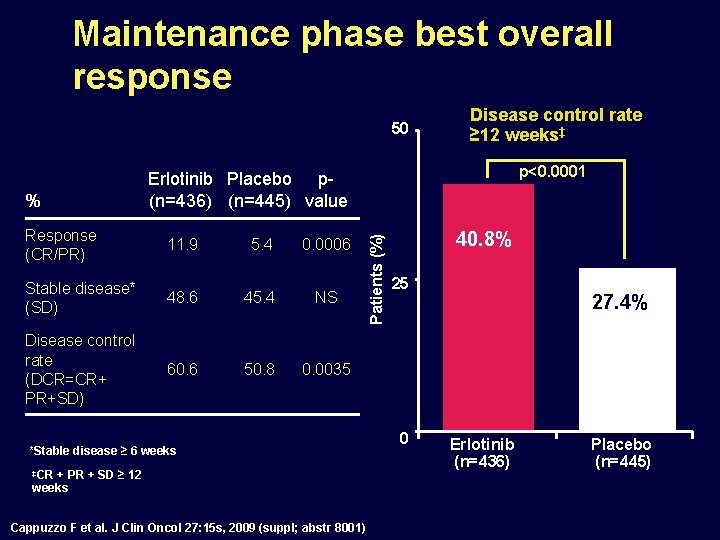
Maintenance phase best overall response 50 p<0. 0001 Erlotinib Placebo p(n=436) (n=445) value Response (CR/PR) 11. 9 5. 4 0. 0006 Stable disease* (SD) 48. 6 45. 4 NS Disease control rate (DCR=CR+ PR+SD) 60. 6 50. 8 0. 0035 *Stable disease ≥ 6 weeks ‡CR + PR + SD ≥ 12 weeks Cappuzzo F et al. J Clin Oncol 27: 15 s, 2009 (suppl; abstr 8001) 40. 8% Patients (%) % Disease control rate ≥ 12 weeks‡ 40. 8% 25 0 27. 4% 4% Erlotinib (n=436) Placebo (n=445)
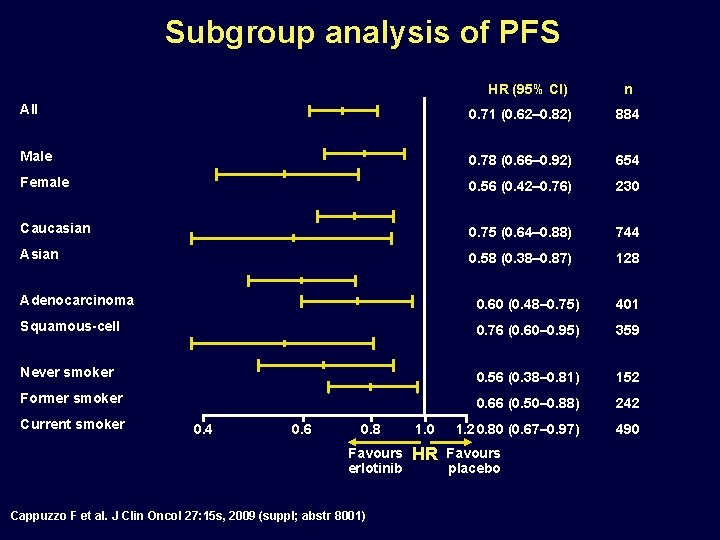
Subgroup analysis of PFS HR (95% CI) n All 0. 71 (0. 62– 0. 82) 884 Male 0. 78 (0. 66– 0. 92) 654 Female 0. 56 (0. 42– 0. 76) 230 Caucasian 0. 75 (0. 64– 0. 88) 744 Asian 0. 58 (0. 38– 0. 87) 128 Adenocarcinoma 0. 60 (0. 48– 0. 75) 401 Squamous-cell 0. 76 (0. 60– 0. 95) 359 Never smoker 0. 56 (0. 38– 0. 81) 152 Former smoker 0. 66 (0. 50– 0. 88) 242 1. 2 0. 80 (0. 67– 0. 97) 490 Current smoker 0. 4 0. 6 0. 8 1. 0 Favours erlotinib HR Cappuzzo F et al. J Clin Oncol 27: 15 s, 2009 (suppl; abstr 8001) Favours placebo
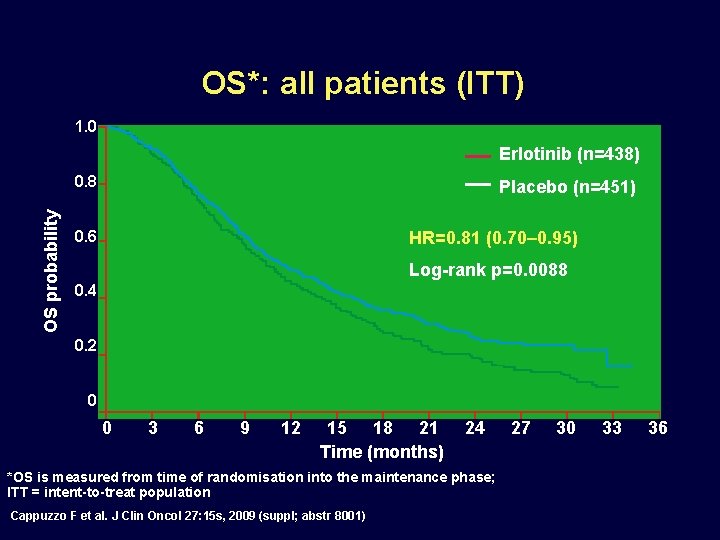
OS*: all patients (ITT) 1. 0 Erlotinib (n=438) OS probability 0. 8 Placebo (n=451) 0. 6 HR=0. 81 (0. 70– 0. 95) Log-rank p=0. 0088 0. 4 0. 2 0 0 3 6 9 12 15 18 21 Time (months) 24 *OS is measured from time of randomisation into the maintenance phase; ITT = intent-to-treat population Cappuzzo F et al. J Clin Oncol 27: 15 s, 2009 (suppl; abstr 8001) 27 30 33 36
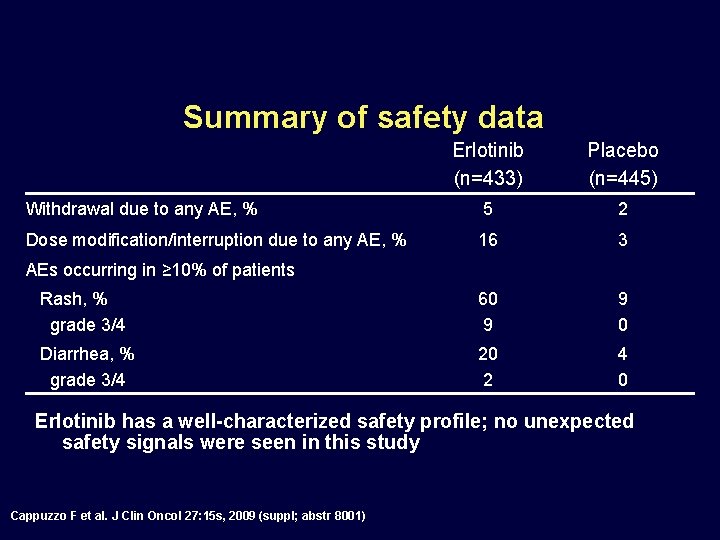
Summary of safety data Erlotinib (n=433) Placebo (n=445) Withdrawal due to any AE, % 5 2 Dose modification/interruption due to any AE, % 16 3 Rash, % grade 3/4 60 9 9 0 Diarrhea, % grade 3/4 20 2 4 0 AEs occurring in ≥ 10% of patients Erlotinib has a well-characterized safety profile; no unexpected safety signals were seen in this study Cappuzzo F et al. J Clin Oncol 27: 15 s, 2009 (suppl; abstr 8001)

Post-study treatment Erlotinib Placebo (n=438) (n=451) % with at least one treatment All classes 71 72 taxanes (including docetaxel) 30 31 antimetabolites (including pemetrexed) 24 23 antineoplastic agents 16 18 tyrosine-kinase inhibitors 11 21 platinum compounds 9 12 • Cappuzzo F et al. J Clin Oncol 27: 15 s, 2009 (suppl; abstr 8001)
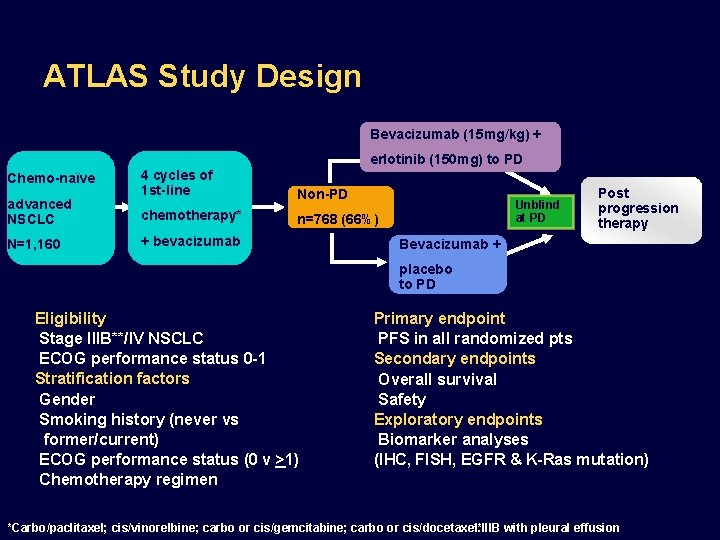
ATLAS Study Design Bevacizumab (15 mg/kg) + erlotinib (150 mg) to PD Chemo-naïve advanced NSCLC N=1, 160 4 cycles of 1 st-line chemotherapy* Non-PD n=768 (66%) + bevacizumab 1: 1 Unblind at PD Post progression therapy Bevacizumab + placebo to PD Eligibility Stage IIIB**/IV NSCLC ECOG performance status 0 -1 Stratification factors Gender Smoking history (never vs former/current) ECOG performance status (0 v >1) Chemotherapy regimen Primary endpoint PFS in all randomized pts Secondary endpoints Overall survival Safety Exploratory endpoints Biomarker analyses (IHC, FISH, EGFR & K-Ras mutation) *Carbo/paclitaxel; cis/vinorelbine; carbo or cis/gemcitabine; carbo or cis/docetaxel. **IIIB with pleural effusion
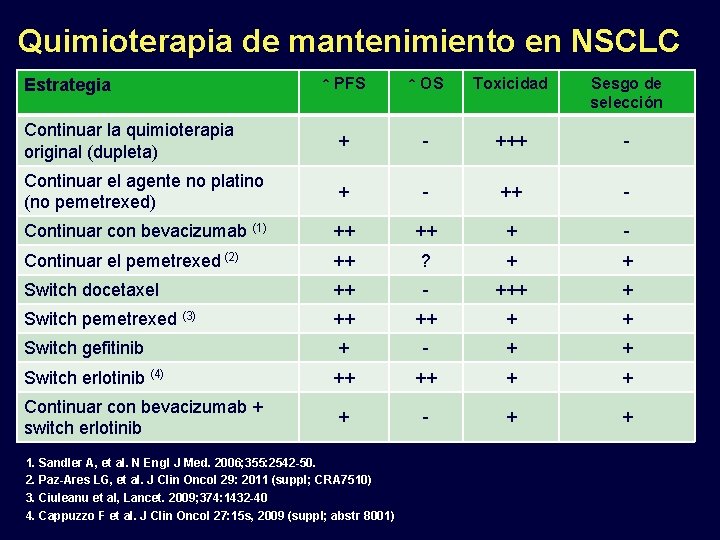
Quimioterapia de mantenimiento en NSCLC ↑ PFS ↑ OS Toxicidad Sesgo de selección Continuar la quimioterapia original (dupleta) + - +++ - Continuar el agente no platino (no pemetrexed) + - ++ - Continuar con bevacizumab (1) ++ ++ + - Continuar el pemetrexed (2) ++ ? + + Switch docetaxel ++ - +++ + Switch pemetrexed (3) ++ ++ + + Switch gefitinib + - + + Switch erlotinib (4) ++ ++ + + Continuar con bevacizumab + switch erlotinib + - + + Estrategia 1. Sandler A, et al. N Engl J Med. 2006; 355: 2542 -50. 2. Paz-Ares LG, et al. J Clin Oncol 29: 2011 (suppl; CRA 7510) 3. Ciuleanu et al, Lancet. 2009; 374: 1432 -40 4. Cappuzzo F et al. J Clin Oncol 27: 15 s, 2009 (suppl; abstr 8001)
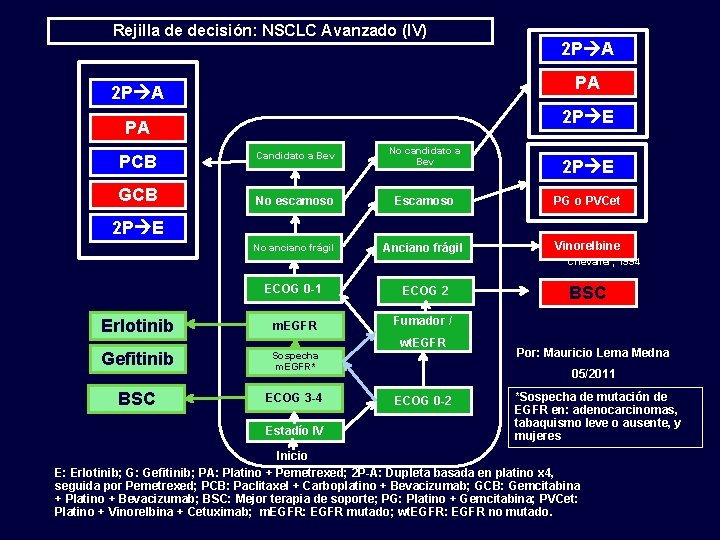
Rejilla de decisión: NSCLC Avanzado (IV) PA 2 P E PA PCB GCB 2 P A Candidato a Bev No candidato a Bev No escamoso Escamoso PG o PVCet No anciano frágil Anciano frágil Vinorelbine 2 P E Chevalier, 1994 ECOG 0 -1 ECOG 2 Erlotinib m. EGFR Fumador / Gefitinib Sospecha m. EGFR* BSC ECOG 3 -4 wt. EGFR Estadío IV BSC Por: Mauricio Lema Medna 05/2011 ECOG 0 -2 *Sospecha de mutación de EGFR en: adenocarcinomas, tabaquismo leve o ausente, y mujeres Inicio E: Erlotinib; G: Gefitinib; PA: Platino + Pemetrexed; 2 P-A: Dupleta basada en platino x 4, seguida por Pemetrexed; PCB: Paclitaxel + Carboplatino + Bevacizumab; GCB: Gemcitabina + Platino + Bevacizumab; BSC: Mejor terapia de soporte; PG: Platino + Gemcitabina; PVCet: Platino + Vinorelbina + Cetuximab; m. EGFR: EGFR mutado; wt. EGFR: EGFR no mutado.

Maintenance therapy in NSCLC Should systemic therapy be given to non-progressors after 1 st-line chemotherapy in m. NSCLC? In squamous-cell carcinoma Solid evidence with Erlotinib switch maintenance In bevacizumab-treated patients Non squamous histology Probably, YES Bevacizumab should be used until progression In non squamous-cell carcinoma, non bevacizumab -treated patientes Pemetrexed + P indicated in 1 st-line, no evidence of benefit with pemetrexed continuous maitenance Solid evidence with Erlotinib switch maintenance Less likely to benefit (personal opinion) Asymptomatic patient after inductionin nonbevacizumab induction chemotherapy Blurred distinction between 1 st- and 2 nd- line therapy
- Slides: 179