14 Skupina C Si Ge Sn Pb Skupinov
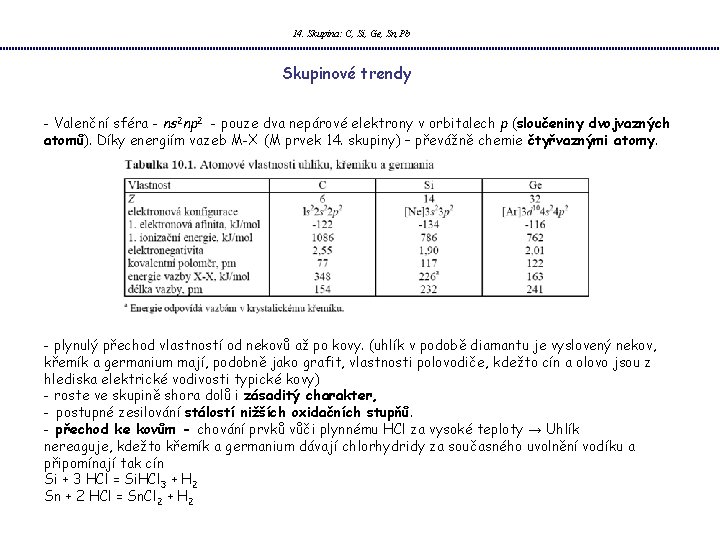
14. Skupina: C, Si, Ge, Sn, Pb Skupinové trendy - Valenční sféra - ns 2 np 2 - pouze dva nepárové elektrony v orbitalech p (sloučeniny dvojvazných atomů). Díky energiím vazeb M-X (M prvek 14. skupiny) – převážně chemie čtyřvaznými atomy. - plynulý přechod vlastností od nekovů až po kovy. (uhlík v podobě diamantu je vyslovený nekov, křemík a germanium mají, podobně jako grafit, vlastnosti polovodiče, kdežto cín a olovo jsou z hlediska elektrické vodivosti typické kovy) - roste ve skupině shora dolů i zásaditý charakter, - postupné zesilování stálostí nižších oxidačních stupňů. - přechod ke kovům - chování prvků vůči plynnému HCl za vysoké teploty → Uhlík nereaguje, kdežto křemík a germanium dávají chlorhydridy za současného uvolnění vodíku a připomínají tak cín Si + 3 HCl = Si. HCl 3 + H 2 Sn + 2 HCl = Sn. Cl 2 + H 2

14. Skupina: C, Si, Ge, Sn, Pb Skupinové trendy Křemík i germanium - vlastnosti, které zcela nezapadají do obecných trendů. - nepravidelný průběh elektronegativity - zvýrazňuje podoba mezi uhlíkem a germaniem a mezi křemíkem a cínem (redukce halogenidů zinkem v kyselém prostředí) křemik a cín - substituci nepodléhají. křemík a cínu - rozpustnost v roztocích hydroxidů alkalických kovů, kterou ještě navíc připomíná chování jiných elektropozitivních kovů (Al, Be) Germanium s roztoky hydroxidů nereaguje
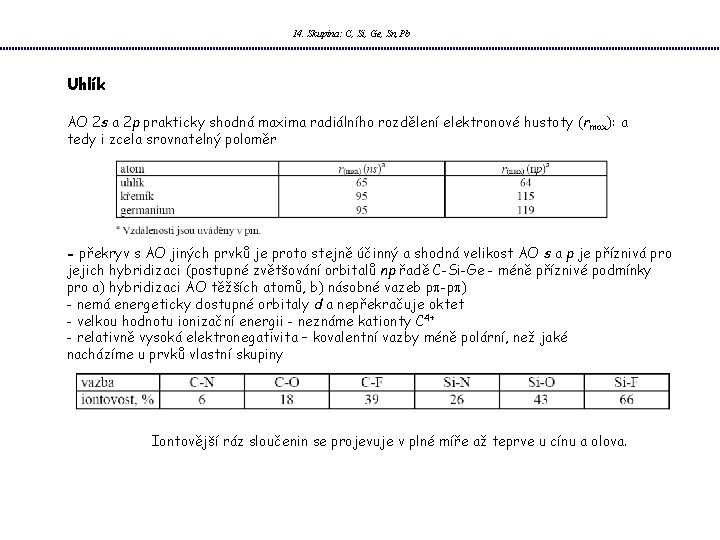
14. Skupina: C, Si, Ge, Sn, Pb Uhlík AO 2 s a 2 p prakticky shodná maxima radiálního rozdělení elektronové hustoty (rmax): a tedy i zcela srovnatelný poloměr - překryv s AO jiných prvků je proto stejně účinný a shodná velikost AO s a p je příznivá pro jejich hybridizaci (postupné zvětšování orbitalů np řadě C-Si-Ge - méně příznivé podmínky pro a) hybridizaci AO těžších atomů, b) násobné vazeb pp-pp) - nemá energeticky dostupné orbitaly d a nepřekračuje oktet - velkou hodnotu ionizační energii - neznáme kationty C 4+ - relativně vysoká elektronegativita – kovalentní vazby méně polární, než jaké nacházíme u prvků vlastní skupiny Iontovější ráz sloučenin se projevuje v plné míře až teprve u cínu a olova.
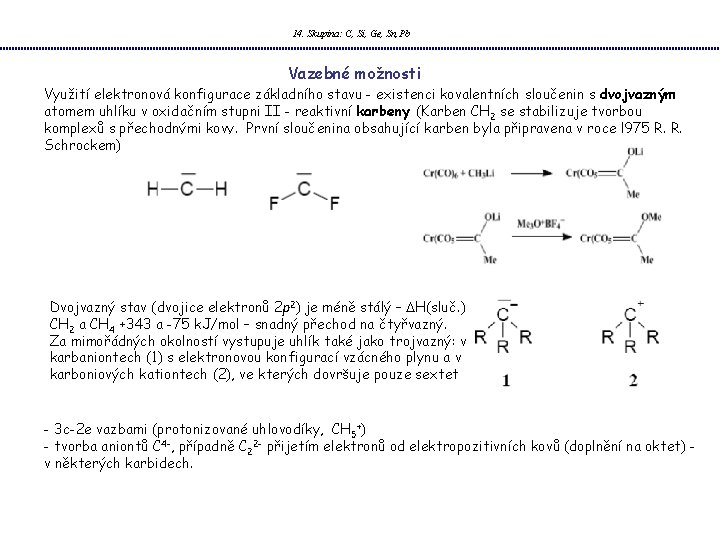
14. Skupina: C, Si, Ge, Sn, Pb Vazebné možnosti Využití elektronová konfigurace základního stavu - existenci kovalentních sloučenin s dvojvazným atomem uhlíku v oxidačním stupni II - reaktivní karbeny (Karben CH 2 se stabilizuje tvorbou komplexů s přechodnými kovy. První sloučenina obsahující karben byla připravena v roce l 975 R. R. Schrockem) Dvojvazný stav (dvojice elektronů 2 p 2) je méně stálý – DH(sluč. ) CH 2 a CH 4 +343 a -75 k. J/mol – snadný přechod na čtyřvazný. Za mimořádných okolností vystupuje uhlík také jako trojvazný: v karbaniontech (1) s elektronovou konfigurací vzácného plynu a v karboniových kationtech (2), ve kterých dovršuje pouze sextet - 3 c-2 e vazbami (protonizované uhlovodíky, CH 5+) - tvorba aniontů C 4 -, případně C 22 - přijetím elektronů od elektropozitivních kovů (doplnění na oktet) v některých karbidech.

14. Skupina: C, Si, Ge, Sn, Pb Vazebné možnosti Neomezené spojování atomů ( rovných, rozvětvených řetězců, kruhů či polyedrických útvarů) Stálost – energie vazby C-C, nemají zásadité vlastnosti (neobsahují volný el. pár), vazby C-H v nasycených uhlovodících nejsou příliš polarizovány – nejsou kyselé, energeticky nedostupné orbitaly d Větší kovalentní poloměry atomů křemíku a germania jsou příznivější pro vznik stálejších polyedrů obecného vzorce M 2 n. H 2 n (M = C, Si nebo Ge, n = 2, 3 a 4): Tvorba násobné vazby typu pp–pp - této snaze podřizuje i chování sloučenin - mnohé z nich podléhají změnám jež nakonec vedou k přeměně jednoduchých vazeb na násobné. Zisk vazebné energie

14. Skupina: C, Si, Ge, Sn, Pb Molekulové formy, alotropie uhlíku Uhlík - existuje v řadě alotropických modifikací, které se liší strukturou a mají proto i rozdílné chemické a fyzikální vlastnosti - grafitu, diamantu a jako molekula fulleren. Diamant. trojrozměrná struktura - výsledek tetraedrického uspořádání jednotlivých atomů uhlíku do šestičlenných kruhů židličkové konformace s délkou vazby C-C 154 pm (prostupuje celým krystalem) Každý takový krystal je pak vlastně obří molekulou. Tetraedrické uspořádání atomů a lokalizované vazby určují diamantu jeho známé vlastnosti, mezi které patří odolnost k chemickým činidlům a neobyčejná tvrdost, nevede el. proud Eg = 5. 47 e. V.
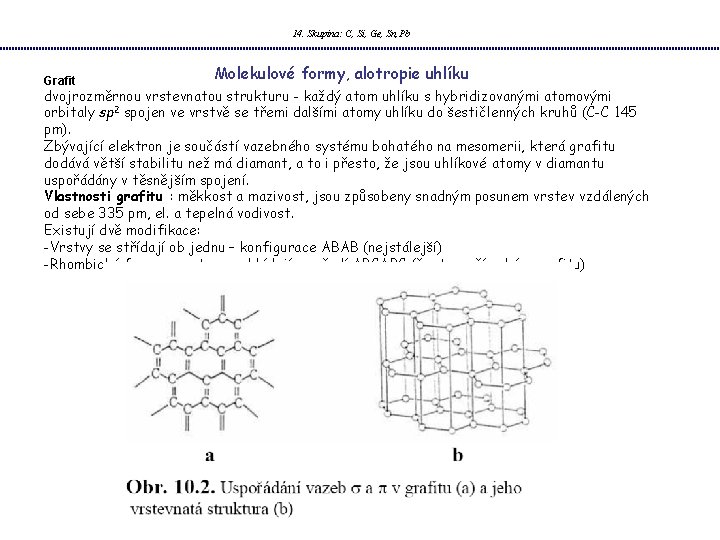
14. Skupina: C, Si, Ge, Sn, Pb Grafit Molekulové formy, alotropie uhlíku dvojrozměrnou vrstevnatou strukturu - každý atom uhlíku s hybridizovanými atomovými orbitaly sp 2 spojen ve vrstvě se třemi dalšími atomy uhlíku do šestičlenných kruhů (C-C 145 pm). Zbývající elektron je součástí vazebného systému bohatého na mesomerii, která grafitu dodává větší stabilitu než má diamant, a to i přesto, že jsou uhlíkové atomy v diamantu uspořádány v těsnějším spojení. Vlastnosti grafitu : měkkost a mazivost, jsou způsobeny snadným posunem vrstev vzdálených od sebe 335 pm, el. a tepelná vodivost. Existují dvě modifikace: -Vrstvy se střídají ob jednu – konfigurace ABAB (nejstálejší) -Rhombická forma – vrstvy se ukládají v pořadí ABCABC (často v přírodním grafitu)
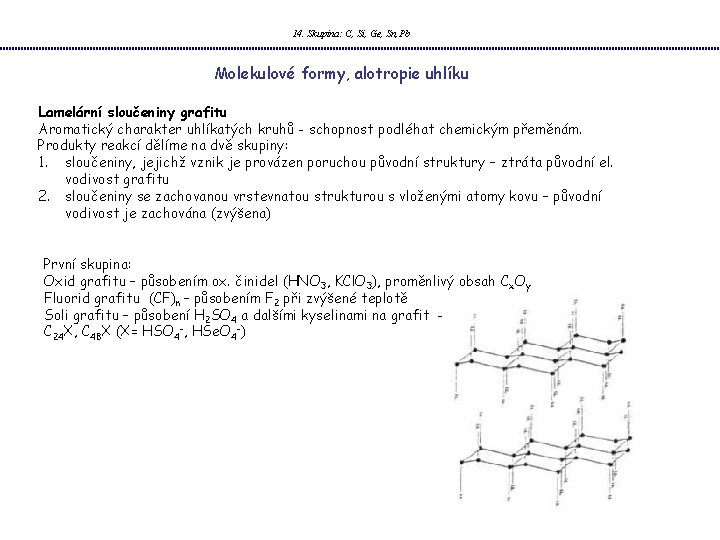
14. Skupina: C, Si, Ge, Sn, Pb Molekulové formy, alotropie uhlíku Lamelární sloučeniny grafitu Aromatický charakter uhlíkatých kruhů - schopnost podléhat chemickým přeměnám. Produkty reakcí dělíme na dvě skupiny: 1. sloučeniny, jejichž vznik je provázen poruchou původní struktury – ztráta původní el. vodivost grafitu 2. sloučeniny se zachovanou vrstevnatou strukturou s vloženými atomy kovu – původní vodivost je zachována (zvýšena) První skupina: Oxid grafitu – působením ox. činidel (HNO 3, KCl. O 3), proměnlivý obsah Cx. Oy Fluorid grafitu (CF)n – působením F 2 při zvýšené teplotě Soli grafitu – působení H 2 SO 4 a dalšími kyselinami na grafit C 24 X, C 48 X (X= HSO 4 -, HSe. O 4 -)

14. Skupina: C, Si, Ge, Sn, Pb Molekulové formy, alotropie uhlíku Lamelární sloučeniny grafitu Aromatický charakter uhlíkatých kruhů - schopnost podléhat chemickým přeměnám. Produkty reakcí dělíme na dvě skupiny: 1. sloučeniny, jejichž vznik je provázen poruchou původní struktury – ztráta původní el. vodivost grafitu 2. sloučeniny se zachovanou vrstevnatou strukturou s vloženými atomy kovu (interkaláty grafitu) – původní vodivost je zachována (zvýšena) Interkaláty grafitu: MCn – reakce grafitu s taveninou nebo parami alkalických kovů pro Li n = 6, 12, 18, Na n = 64 K n = 8, 10, 16, 24 sloučenina KC 8 – atom K vsunut mezi šestičlenné kruhy KC 8 + H 2 O = C 8 + KOH + H 2
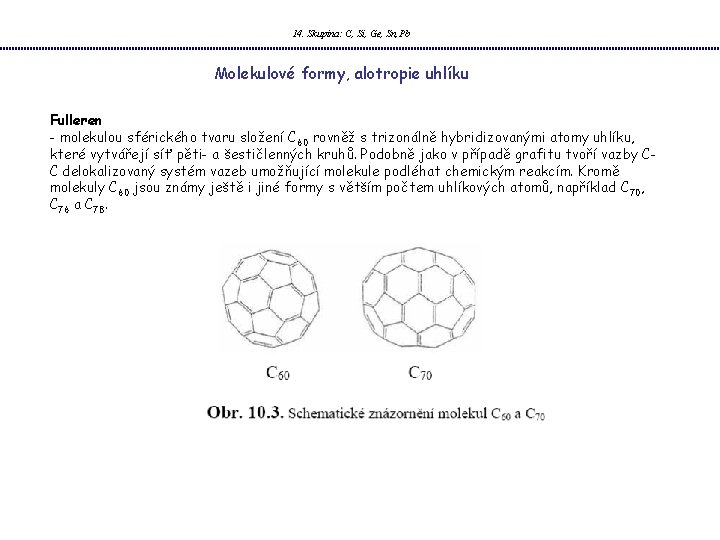
14. Skupina: C, Si, Ge, Sn, Pb Molekulové formy, alotropie uhlíku Fulleren - molekulou sférického tvaru složení C 60 rovněž s trizonálně hybridizovanými atomy uhlíku, které vytvářejí síť pěti- a šestičlenných kruhů. Podobně jako v případě grafitu tvoří vazby CC delokalizovaný systém vazeb umožňující molekule podléhat chemickým reakcím. Kromě molekuly C 60 jsou známy ještě i jiné formy s větším počtem uhlíkových atomů, například C 70, C 76 a C 78.
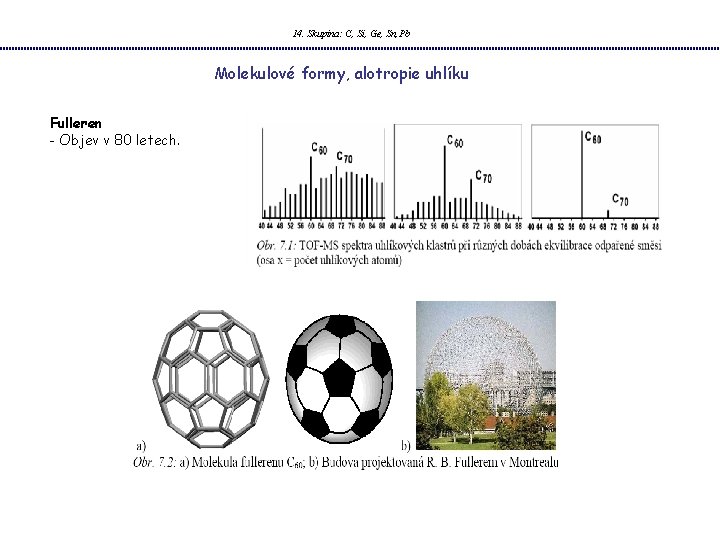
14. Skupina: C, Si, Ge, Sn, Pb Molekulové formy, alotropie uhlíku Fulleren - Objev v 80 letech.
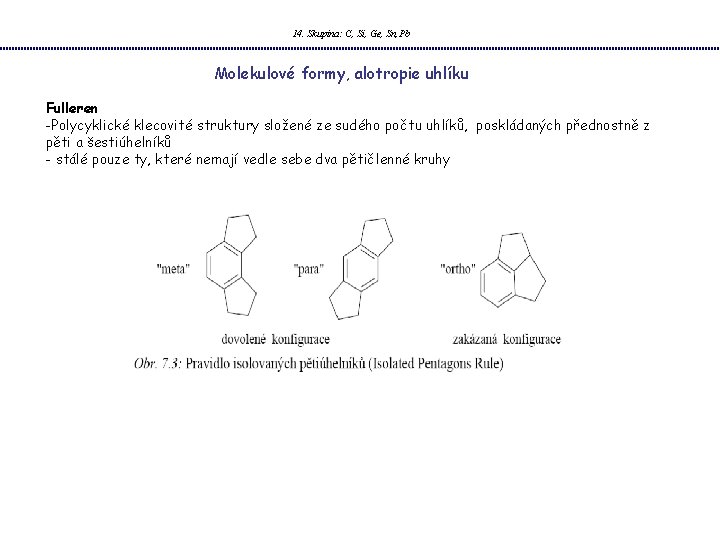
14. Skupina: C, Si, Ge, Sn, Pb Molekulové formy, alotropie uhlíku Fulleren -Polycyklické klecovité struktury složené ze sudého počtu uhlíků, poskládaných přednostně z pěti a šestiúhelníků - stálé pouze ty, které nemají vedle sebe dva pětičlenné kruhy
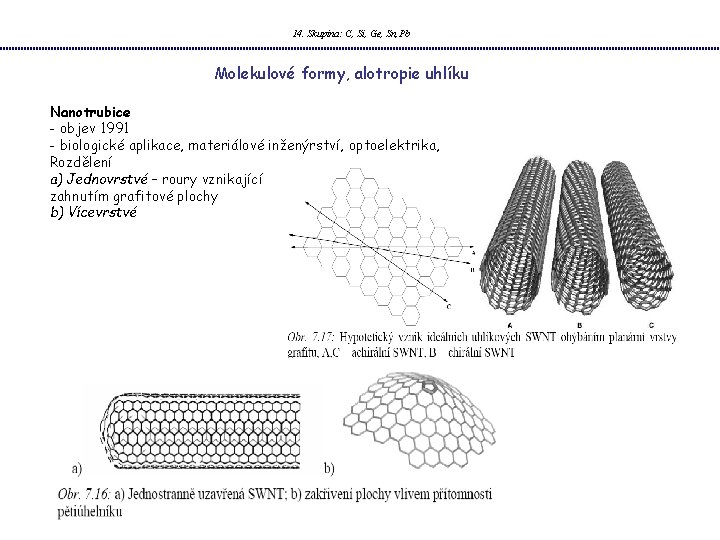
14. Skupina: C, Si, Ge, Sn, Pb Molekulové formy, alotropie uhlíku Nanotrubice - objev 1991 - biologické aplikace, materiálové inženýrství, optoelektrika, Rozdělení a) Jednovrstvé – roury vznikající zahnutím grafitové plochy b) Vícevrstvé

14. Skupina: C, Si, Ge, Sn, Pb Vybrané sloučeniny uhlíku Karbidy binární sloučeniny uhlíku s atomy elektropozitivních prvků nebo s atomy s elektronegativitou blízkou uhlíku. 1. iontové (solné) povahy 2. Kovalentní 3. Kovové 4. Karbidy přechodného typu Karbidy iontové - tvoří je většina elektropozitivních prvků - obsahují anionty C 4 -, C 22 -, HC 2 -, C 34 -, - tyty ionty ve vodě podléhají hydrolýze za vzniku příslušných uhlovodíků (Anion C 22 - poskytuje hydrolýzou ethyn C 2 H 2 a v případě karbidu s aniontem C 34 - vzniká reakcí s vodou propyn CH 3 -C CH)

14. Skupina: C, Si, Ge, Sn, Pb Vybrané sloučeniny uhlíku Karbidy kovalentní - řadíme např. karbid tetraboru B 4 C, křemíku Si. C, dikyan (CN)2 Kovalentní acetylidy - Cu 2 C 2, Ag 2 C 2 – acetylén + odpovídající sůl, - explosivní Kovové karbidy - Ti. C, Zr. C, VC, Ta. C, Mo. C – intersticiální sloučeniny proměnlivého složení, kde atomy C jsou v oktaedrických mezerách v nejtěsnějším uspořádáním kovu. - vysoké body tání, tvrdost, el. vodivost. Karbidy přechodného typu - přechod mezi iontovými a kovovými. - Cr 3 C 2, Mn 3 C, Fe 3 C, Co 3 C – deformovaná struktura s řetězci C - snadná hydrolýza za vzniku uhlovodíků - Fe 3 C – cementit (základní složka oceli)
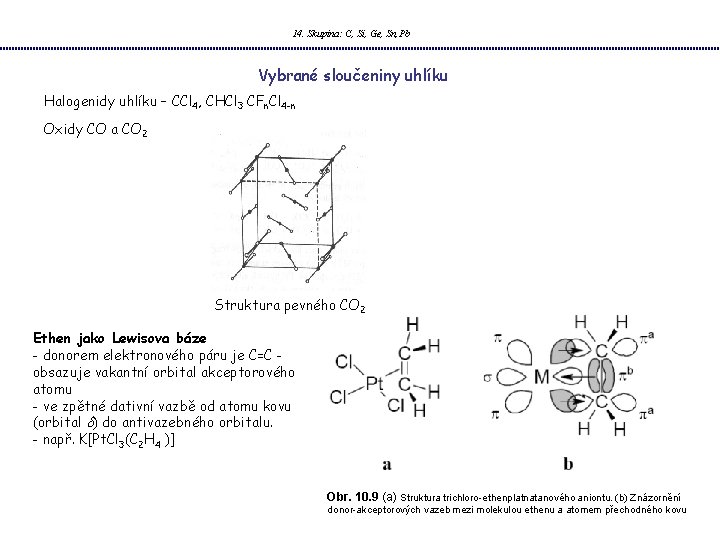
14. Skupina: C, Si, Ge, Sn, Pb Vybrané sloučeniny uhlíku Halogenidy uhlíku – CCl 4, CHCl 3 CFn. Cl 4 -n Oxidy CO a CO 2 Struktura pevného CO 2 Ethen jako Lewisova báze - donorem elektronového páru je C=C obsazuje vakantní orbital akceptorového atomu - ve zpětné dativní vazbě od atomu kovu (orbital d) do antivazebného orbitalu. - např. K[Pt. Cl 3(C 2 H 4 )] Obr. 10. 9 (a) Struktura trichloro-ethenplatnatanového aniontu. (b) Znázornění donor-akceptorových vazeb mezi molekulou ethenu a atomem přechodného kovu

14. Skupina: C, Si, Ge, Sn, Pb Těžší analoga uhlíku Oxidační stavy Elektronová konfigurace ns 2 np 2 - oxidačních stavů II a IV, -kovalentní sloučeniny typu MX 2 (kde X jednovazný atom) - dva elektrony využité k chemické vazbě méně stálé - stálost oxidačního stavu II se zažíná projevovat teprve až u germania → halogenidy Si. X 2 (X = F, Cl) se stabilizují polymerací x monomerní halogenidy germanaté Ge. X 2 (X = F, Cl, Br, I , Ge. X 4 + Ge = 2 Ge. Cl 2). - vztah energie uvolněné při vzniku kovalentní vazby a energie nezbytné k využití elektronové dvojice ns 2 k vazebným účelům – čím je vazebná energie větší - tím je větší podíl elektronů ns 2 na vazbě (sp 3 < sp 2 < sp). Vazebná energie s rostoucím protonovým číslem klesá - klesá podíl elektronů ns 2 na kovalentní vazbě. Postupně se stávají nevazebným párem. (např. experimentálně zjištěné struktury hydridů těžších prvků - vazebné úhly blízko 90 o) Vazebná energie klesá
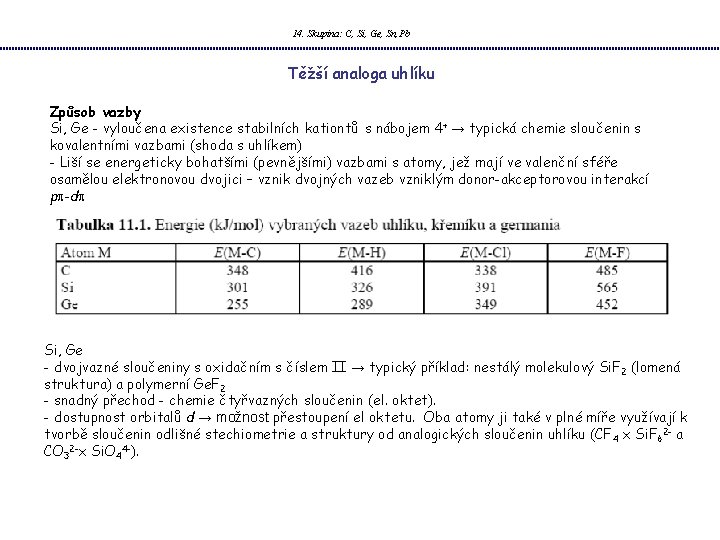
14. Skupina: C, Si, Ge, Sn, Pb Těžší analoga uhlíku Způsob vazby Si, Ge - vyloučena existence stabilních kationtů s nábojem 4+ → typická chemie sloučenin s kovalentními vazbami (shoda s uhlíkem) - Liší se energeticky bohatšími (pevnějšími) vazbami s atomy, jež mají ve valenční sféře osamělou elektronovou dvojici – vznik dvojných vazeb vzniklým donor-akceptorovou interakcí pp-dp Si, Ge - dvojvazné sloučeniny s oxidačním s číslem II → typický příklad: nestálý molekulový Si. F 2 (lomená struktura) a polymerní Ge. F 2 - snadný přechod - chemie čtyřvazných sloučenin (el. oktet). - dostupnost orbitalů d → možnost přestoupení el oktetu. Oba atomy ji také v plné míře využívají k tvorbě sloučenin odlišné stechiometrie a struktury od analogických sloučenin uhlíku (CF 4 x Si. F 62 - a CO 32 -x Si. O 44 -).
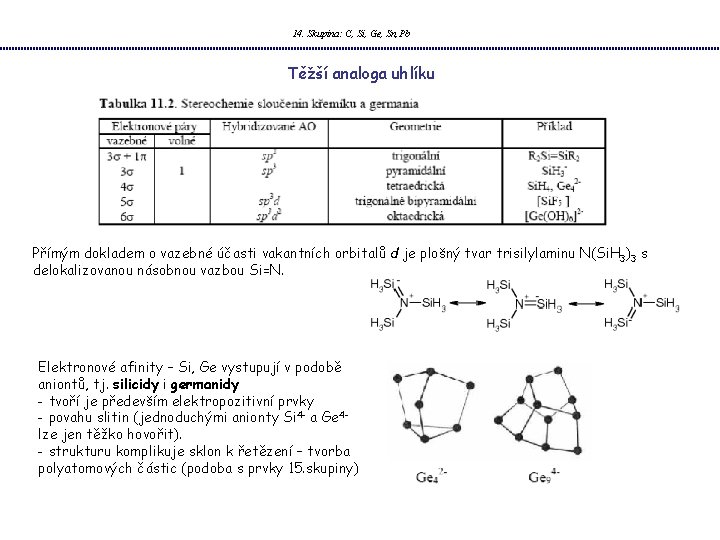
14. Skupina: C, Si, Ge, Sn, Pb Těžší analoga uhlíku Přímým dokladem o vazebné účasti vakantních orbitalů d je plošný tvar trisilylaminu N(Si. H 3)3 s delokalizovanou násobnou vazbou Si=N. Elektronové afinity – Si, Ge vystupují v podobě aniontů, tj. silicidy i germanidy - tvoří je především elektropozitivní prvky - povahu slitin (jednoduchými anionty Si 4 - a Ge 4 lze jen těžko hovořit). - strukturu komplikuje sklon k řetězení – tvorba polyatomových částic (podoba s prvky 15. skupiny)
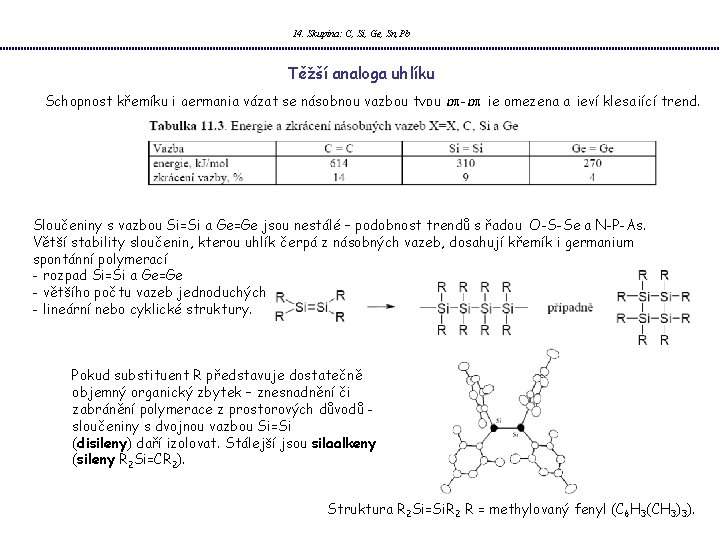
14. Skupina: C, Si, Ge, Sn, Pb Těžší analoga uhlíku Schopnost křemíku i germania vázat se násobnou vazbou typu pp-pp je omezena a jeví klesající trend. Sloučeniny s vazbou Si=Si a Ge=Ge jsou nestálé – podobnost trendů s řadou O-S-Se a N-P-As. Větší stability sloučenin, kterou uhlík čerpá z násobných vazeb, dosahují křemík i germanium spontánní polymerací - rozpad Si=Si a Ge=Ge - většího počtu vazeb jednoduchých - lineární nebo cyklické struktury. Pokud substituent R představuje dostatečně objemný organický zbytek – znesnadnění či zabránění polymerace z prostorových důvodů sloučeniny s dvojnou vazbou Si=Si (disileny) daří izolovat. Stálejší jsou silaalkeny (sileny R 2 Si=CR 2). Struktura R 2 Si=Si. R 2 R = methylovaný fenyl (C 6 H 3(CH 3)3).

14. Skupina: C, Si, Ge, Sn, Pb Těžší analoga uhlíku Odpor Si, Ge k dvojným vazbám – např. geminální dioly: uhlík (1) přecházejí snadno na ketony s dvojnou vazbou C=O (E(C-O) = 358, E(C=O) = 745 k. J/mol), kdežto v křemíkových diolů (2) vznikají polymery s vazbou -Si-O-Si- Přes sklon k tvorbě rozsáhlejších řetězců s jednoduchou vazbou - řízené spojování atomů do dlouhých řetězců -Si-Si-Si- (-Ge-Ge-Ge-) předem definované délky se nedaří - nedostatek vhodných experimentálních postupů (termodynamická překážka neexistuje) Omezená schopnost vytvářet homogenní řetězce s větším počtem atomů se týká sloučenin s vodíkem (silany a germany). hydridy obecného vzorce Sin. H 2 n+2 (Gen. H 2 n+2) pouze po Si 8 (Ge 5). Substitucí H za Me, F vazby Si-Si se natolik stabilizují, že je možné získat sloučeniny i s delšími řetězci Si-C: prostorový vliv alkylových (arylových) skupin Si-F: donor-akceptorová vazba pp(F)-dp(Si)

14. Skupina: C, Si, Ge, Sn, Pb Těžší analoga uhlíku - Výroba Křemík se získává z Si. O 2 redukcí za vysoké teploty uhlíkem, a aby se potlačil vznik karbidu Si. C, musí být oxid v nadbytku Si. O 2 + 2 C = Si + 2 CO Si. O 2 + 2 Si. C = 3 Si + 2 CO Výroba germania stejná, navíc je možné k redukci Ge. O 2 využít také vodík. Tato připravený Si - 97 – 99 %. Pro účely elektronického průmyslu Si – o čistotě minimálně 99, 9999 %, Zonální tavení - dlouhé tenké tyče ve speciální pícce se postupně přetavují. Tavená zóna se posunuje od jednoho konce ke druhému a nečistoty přítomné v materiálu se koncentrují v roztavené zóně a postupně se dostávají ke konci tyče. Výroba Si: těkavá sloučenina (HSi. Cl 3, Si. Cl 4) - vedou se přes vrstvu vysoce čistého křemíku o teplotě přes 1 100 °C kdy dochází k jejich rozkladu a vzniklý vysoce čistý křemík se ukládá v krystalické podobě na původní křemíkovou podložku. 2 HSi. Cl 3 → Si + 2 HCl + Si. Cl 4 Uvedeným postupem vzniká křemík který vyhovuje požadavkům pro výrobu elektronických polovodičových součástek. křemíkové čipy

14. Skupina: C, Si, Ge, Sn, Pb Sloučeniny s vodíkem, silany a halogensilany Křemík i germania tvoří hydridy (silany a germany) - Mn. H 2 n+2 (M je Si nebo Ge). Oproti uhlovodíkům jsou omezenou délkou řetězce (Si 8 H 18 a Ge 5 H 12). Nenasycené hydridy (H 2 Si=Si. H 2 , HSi Si. H) nejsou známy. Příprava - kyselá hydrolýza silicidů, slitin germania (analogie s hydrolýzou karbidů) - nevýhodou je vznik směs vyšších hydridů Výměnná reakce - bezvodé prostředí (silany i germany) - nestálé, samozápalné, podléhají hydrolýze vodou za nezbytné přítomnosti hydroxidových iontů. Si 4 H 10 + 13/2 O 2 = 4 Si. O 2 + 5 H 2 O Reaktivita kontrastuje se stálými uhlovodíky standardních slučovacích entalpií (CH 4 = -75; Si. H 4 = +33, 5; Ge. H 4 = +92 k. J/mol) energeticky dostupné orbitaly 3 d atomu Si (Ge) pro el. pár Lewisovy báze, rozdělení náboje v molekule (C-0, 10 v CH 4 a Si+0, 13 v Si. H 4).

14. Skupina: C, Si, Ge, Sn, Pb Sloučeniny s vodíkem, silany a halogensilany Další vlastnosti – krakování, rce. s alkoholy, halogenovodíky Halogenderiváty – snadná hydrolýza + intramolekulární kondenzace - disiloxan Organokřemičité sloučeniny. Silanoly, siloxany, silikony Největší význam mají halogenderiváty Rn. Si. X 4 -n (n = 1 -3) - výroba silikonů. Získávají se působením alkylchloridů na elementární křemík nebo na jeho slitiny s mědí. Vazby Si-X (X = Cl, Br) - snadná hydrolýza – vznik silanolů (obdoba alkoholů) Jejich kondenzací v závislosti na počtu skupin OH přítomných v molekule vznikají siloxany (např. hexamethyldisiloxan),
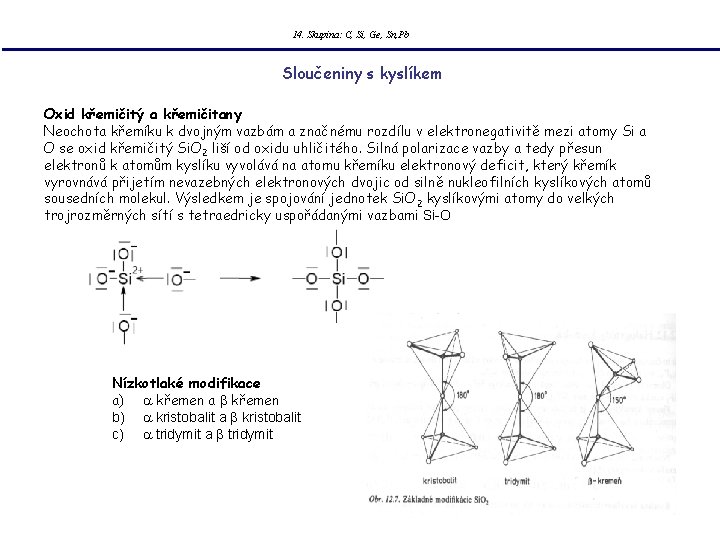
14. Skupina: C, Si, Ge, Sn, Pb Sloučeniny s kyslíkem Oxid křemičitý a křemičitany Neochota křemíku k dvojným vazbám a značnému rozdílu v elektronegativitě mezi atomy Si a O se oxid křemičitý Si. O 2 liší od oxidu uhličitého. Silná polarizace vazby a tedy přesun elektronů k atomům kyslíku vyvolává na atomu křemíku elektronový deficit, který křemík vyrovnává přijetím nevazebných elektronových dvojic od silně nukleofilních kyslíkových atomů sousedních molekul. Výsledkem je spojování jednotek Si. O 2 kyslíkovými atomy do velkých trojrozměrných sítí s tetraedricky uspořádanými vazbami Si-O Nízkotlaké modifikace a) a křemen a b křemen b) a kristobalit a b kristobalit c) a tridymit a b tridymit

14. Skupina: C, Si, Ge, Sn, Pb Sloučeniny s kyslíkem - spojení přes kyslík - tetraedrické jednotky Si. O 4 se liší pouze natočením tetraedrů - vzájemné přeměny forem a a b jsou vratné Křemen - díky struktuře (úhel 150°) není střed souměrnosti – optická aktivita - piezoelektrický jev - účinkem mechanické síly se indukuje el. náboj - roztavením jakékoliv modifikace – amfoterní Si. O 2 - křemenné sklo - s teplotou nemění koeficient tepelné roztažnosti Kyselina křemičitá - okyselením křemičitanů, - nestálá – kondenzace na polymerní produkty – koloidní roztoky se po delší době přemění na gely jehož vysušením – amfoterní pevná látka silikagel Křemičitany -strukturní jednotky Si. O 4 s vazbami Si-O-Si Silikátové sklo: amfoterní tavenina křemičitanů, - tavením oxidů(uhličitanů) kovů s Si. O 2. Na 2 CO 3 + Ca. CO 3 + 6 Si. O 2 = Na 2 O. Ca. O. 6 Si. O 2 + 2 CO 2
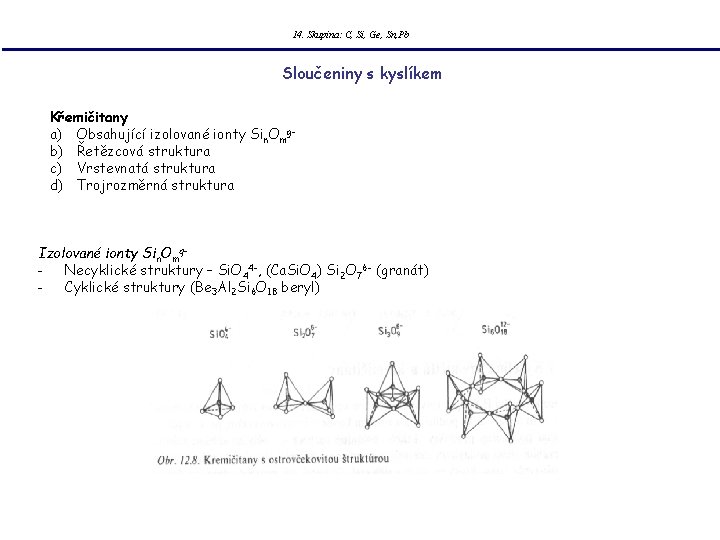
14. Skupina: C, Si, Ge, Sn, Pb Sloučeniny s kyslíkem Křemičitany a) Obsahující izolované ionty Sin. Omgb) Řetězcová struktura c) Vrstevnatá struktura d) Trojrozměrná struktura Izolované ionty Sin. Omq- Necyklické struktury – Si. O 44 -, (Ca. Si. O 4) Si 2 O 76 - (granát) - Cyklické struktury (Be 3 Al 2 Si 6 O 18 beryl)

14. Skupina: C, Si, Ge, Sn, Pb Sloučeniny s kyslíkem Řetězová struktura - Pyroxény – jednoduché nekonečné řetezce (spodument Li. Al(Si. O 3)2) - Amfiboly - zdvojené nekonečné řetězce Azbesty – jsou tvořené z těchto křemičitanů
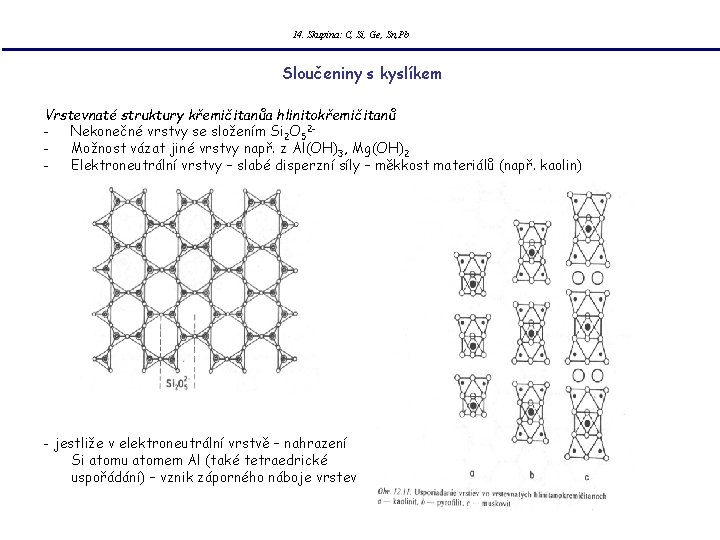
14. Skupina: C, Si, Ge, Sn, Pb Sloučeniny s kyslíkem Vrstevnaté struktury křemičitanůa hlinitokřemičitanů - Nekonečné vrstvy se složením Si 2 O 52 - Možnost vázat jiné vrstvy např. z Al(OH)3, Mg(OH)2 - Elektroneutrální vrstvy – slabé disperzní síly – měkkost materiálů (např. kaolin) - jestliže v elektroneutrální vrstvě – nahrazení Si atomu atomem Al (také tetraedrické uspořádání) – vznik záporného náboje vrstev

14. Skupina: C, Si, Ge, Sn, Pb Sloučeniny s kyslíkem Hlinitokřemičitany s trojrozměrnou strukturou - Trojrozměrná kostra tvořená Si. O 4 jednotkami, část je nahrazena Al – převládá záporný náboj, který je kompenzován kationty (Na+, K+, Ca 2+) Živce - Kompaktní minerály M(Al. O 2)(Si. O 2)3 , MII(Al. O 2)2(Si. O 2)2 - Neobsahují a nepřijímají vodu Ultramaríny - Kromě {(Si. Al)O 2} obsahují také Cl-, SO 42 - Barevné – používají se jako pigmenty Zeolity - základem je jednotka (Si. O 4)24 – spojené do vyšších celků - ve struktuře jsou dutiny – pro kompenzující kation, nebo jiné malé molekuly, např. v zeolitu typu A - H 2 O lze reverzibilně zachycovat a vypuzovat Použití: Adsorbenty molekul – selektivní oddělování plynů a kapalin, plynové chromatografii Katalyzátory – např. krakování uhlovodíků Imobilizátory některých komplexů Měniče iontů, změkčovače vody v pracích prostředcích
- Slides: 30