1 VNITN PROSTED Biochemick stav LF MU V

1

VNITŘNÍ PROSTŘEDÍ © Biochemický ústav LF MU (V. P. ) 2009 2

Vnitřní prostředí: Claude Bernard, 1878: „Co je vnitřní prostředí ? Je to krev, ve skutečnosti však nikoliv celá, nýbrž tekutá část krve, krevní plazma, všechny intersticiální tekutiny, zdroj a výslednice všech základních změn. “ 3

Vnitřní prostředí = ECT (extracelulární tekutina) zevní prostředí ECT buňka stálost vnitřního prostředí 4
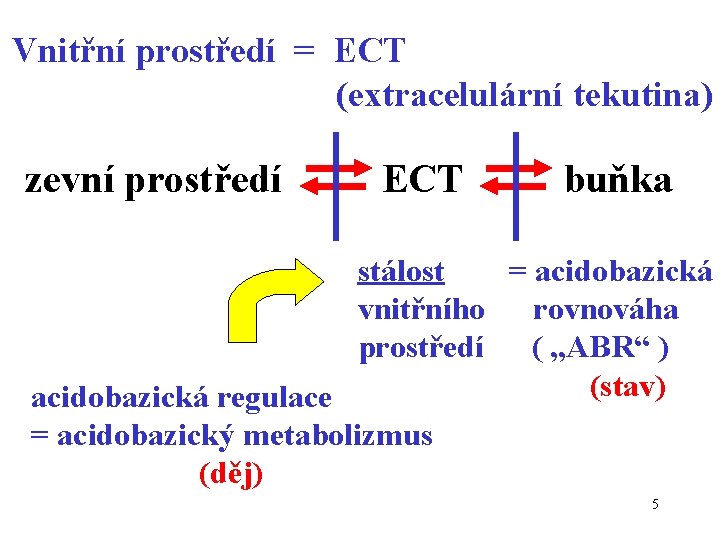
Vnitřní prostředí = ECT (extracelulární tekutina) zevní prostředí ECT buňka stálost = acidobazická vnitřního rovnováha prostředí ( „ABR“ ) (stav) acidobazická regulace = acidobazický metabolizmus (děj) 5
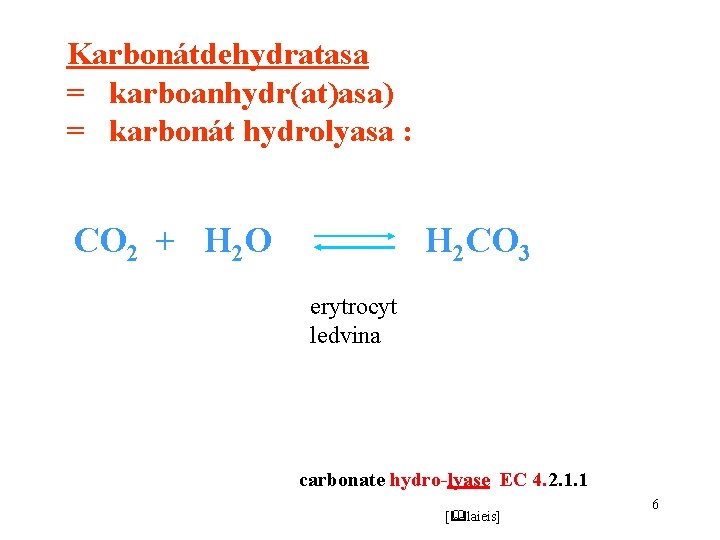
Karbonátdehydratasa = karboanhydr(at)asa) = karbonát hydrolyasa : CO 2 + H 2 O H 2 CO 3 erytrocyt ledvina carbonate hydro-lyase EC 4. 2. 1. 1 [ laieis] 6

PUFRY 7
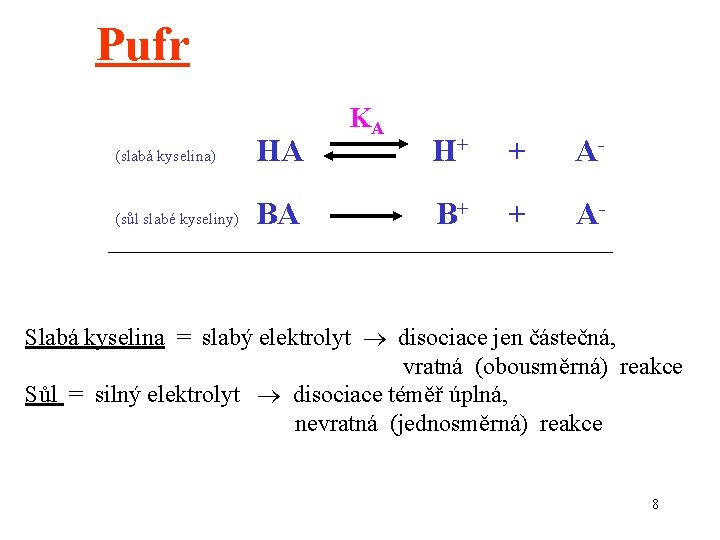
Pufr (slabá kyselina) HA (sůl slabé kyseliny) BA KA H+ + A- B+ + A- Slabá kyselina = slabý elektrolyt disociace jen částečná, vratná (obousměrná) reakce Sůl = silný elektrolyt disociace téměř úplná, nevratná (jednosměrná) reakce 8

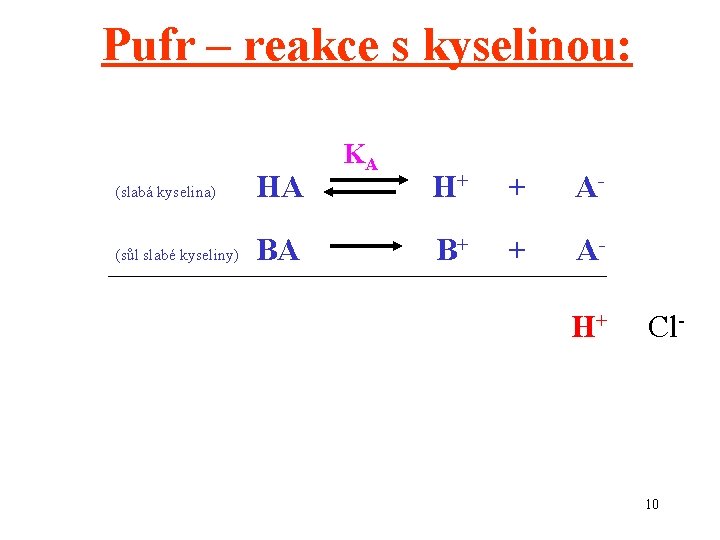
Pufr – reakce s kyselinou: (slabá kyselina) HA (sůl slabé kyseliny) BA KA H+ + A- B+ + AH+ Cl- 10
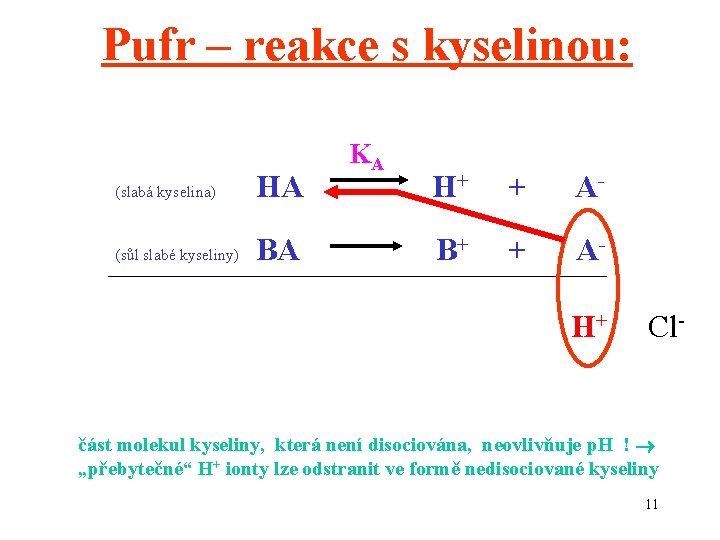
Pufr – reakce s kyselinou: (slabá kyselina) HA (sůl slabé kyseliny) BA KA H+ + A- B+ + AH+ Cl- část molekul kyseliny, která není disociována, neovlivňuje p. H ! „přebytečné“ H+ ionty lze odstranit ve formě nedisociované kyseliny 11

Pufr - reakce se zásadou: (slabá kyselina) HA (sůl slabé kyseliny) BA KA H+ + A- B+ + A- Na+ OH 12
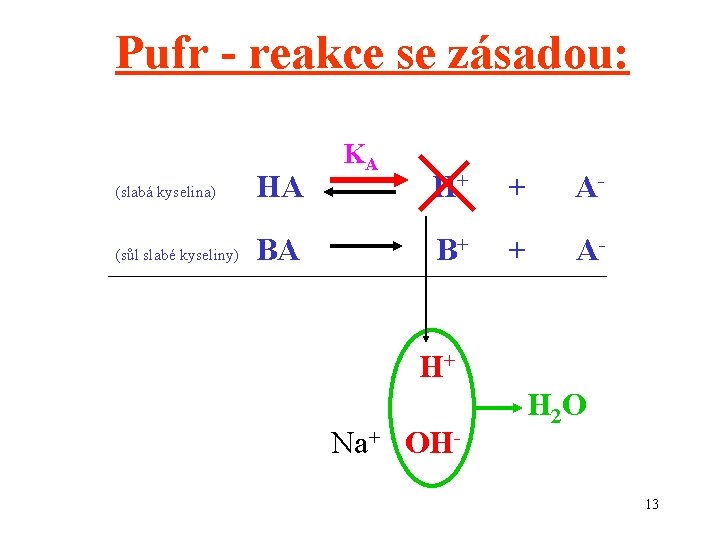
Pufr - reakce se zásadou: (slabá kyselina) HA (sůl slabé kyseliny) BA KA H+ + A- B+ + A- H+ Na+ OH- H 2 O 13
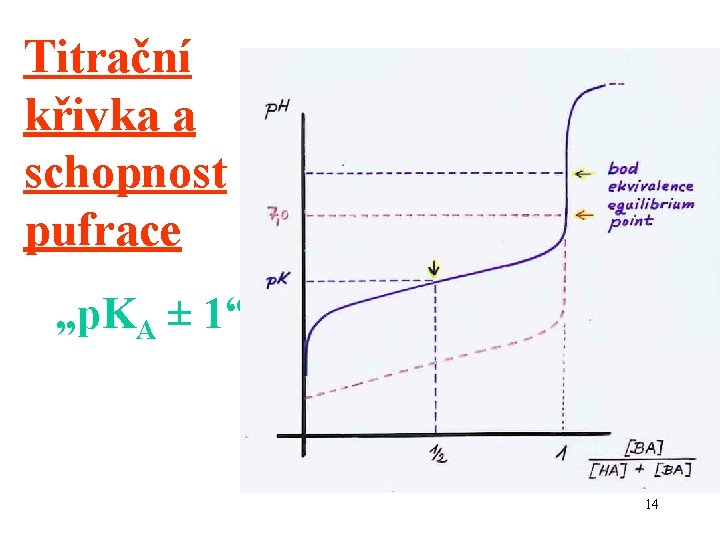
Titrační křivka a schopnost pufrace „p. KA ± 1“ 14
![Hraniční hodnoty p. H (plná krev) p. H = 7, 40 [H+] 40 nmol. Hraniční hodnoty p. H (plná krev) p. H = 7, 40 [H+] 40 nmol.](http://slidetodoc.com/presentation_image/60ab6abebc203af62144ea5bab71f43b/image-15.jpg)
Hraniční hodnoty p. H (plná krev) p. H = 7, 40 [H+] 40 nmol. l-1 p. H = 6, 80 [H+] 160 nmol. l-1 p. H = 7, 70 [H+] 20 nmol. l-1 15
![Poznámka: [H+] jsou zde v nmol. l-1 (tj. 10 – 9 mol. l-1) , Poznámka: [H+] jsou zde v nmol. l-1 (tj. 10 – 9 mol. l-1) ,](http://slidetodoc.com/presentation_image/60ab6abebc203af62144ea5bab71f43b/image-16.jpg)
Poznámka: [H+] jsou zde v nmol. l-1 (tj. 10 – 9 mol. l-1) , - nezaměňujte s mmol. l-1 , které představují miliónkrát vyšší koncentraci !!! [H+] (nmol. l-1) = 10 (9 – p. H) p. H = 9 – log [H+] (nmol. l-1) 16
![Hraniční hodnoty p. H (plná krev) p. H = 7, 40 [H+] 40 nmol. Hraniční hodnoty p. H (plná krev) p. H = 7, 40 [H+] 40 nmol.](http://slidetodoc.com/presentation_image/60ab6abebc203af62144ea5bab71f43b/image-17.jpg)
Hraniční hodnoty p. H (plná krev) p. H = 7, 40 [H+] 40 nmol. l-1 normální hodnota p. H = 6, 80 p. H = 7, 70 [H+] 160 nmol. l-1 [H+] 20 nmol. l-1 4 násobek normy [H+] ½ normy [H+] 17

Krajní hodnoty p. H slučitelné se životem p. H = 6, 80 p. H = 7, 70 [H+] 160 nmol. l-1 [H+] 20 nmol. l-1 4 násobek normy [H+] ½ normy [H+] tolerance k acidémii (acidóze) je značně vyšší, alkalémie (alkalózy) proto představují větší nebezpečí 18
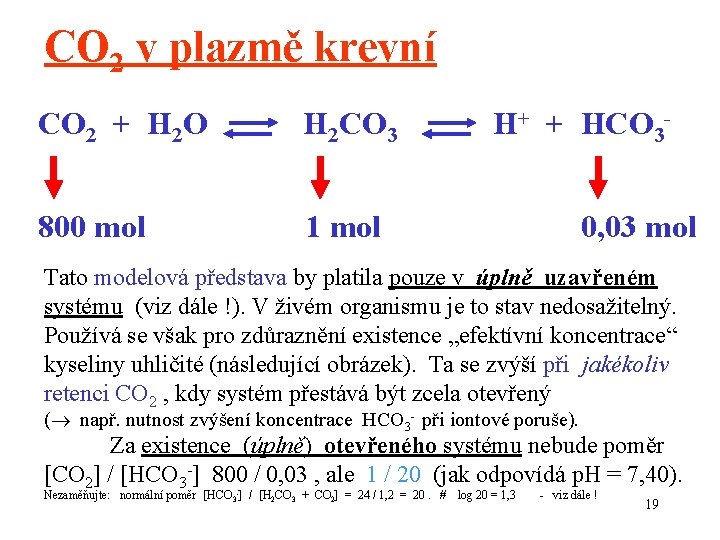
CO 2 v plazmě krevní CO 2 + H 2 O H 2 CO 3 800 mol 1 mol H+ + HCO 30, 03 mol Tato modelová představa by platila pouze v úplně uzavřeném systému (viz dále !). V živém organismu je to stav nedosažitelný. Používá se však pro zdůraznění existence „efektívní koncentrace“ kyseliny uhličité (následující obrázek). Ta se zvýší při jakékoliv retenci CO 2 , kdy systém přestává být zcela otevřený ( např. nutnost zvýšení koncentrace HCO 3 - při iontové poruše). Za existence (úplně) otevřeného systému nebude poměr [CO 2] / [HCO 3 -] 800 / 0, 03 , ale 1 / 20 (jak odpovídá p. H = 7, 40). Nezaměňujte: normální poměr [HCO 3 -] / [H 2 CO 3 + CO 2] = 24 / 1, 2 = 20. # log 20 = 1, 3 - viz dále ! 19

Kyselina uhličitá v plazmě: CO 2 = fyzikálně rozpuštěný CO 2 (chemicky nezreagovaný) H 2 CO 3 = CO 2 zreagovaný na kyselinu CO 2 + H 2 CO 3 = „efektivní koncentrace kyseliny uhličité“ ( Efektivní ve smyslu „účinná“ koncentrace vyjadřuje, že jako kyselina uhličitá budou působit také její molekuly, doplňované z přebytku CO 2 ) 20
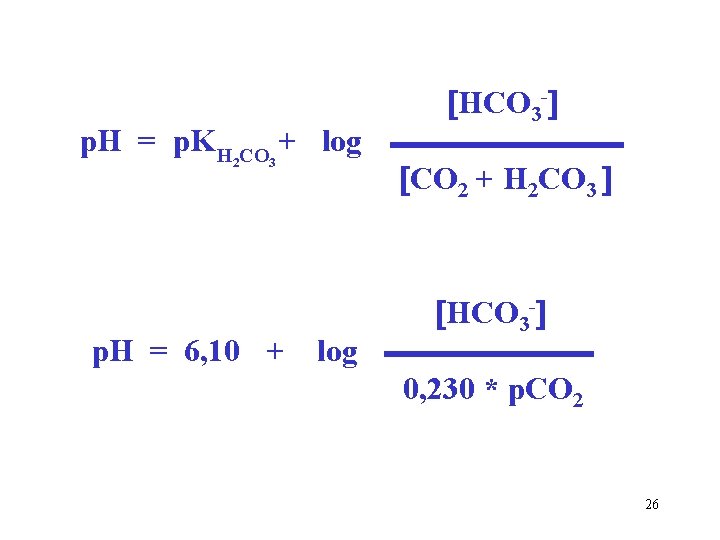
p. H = p. K H 2 CO 3 + log p. H = 6, 10 + log HCO 3 - CO 2 + H 2 CO 3 HCO 3 - 0, 230 * p. CO 2 26
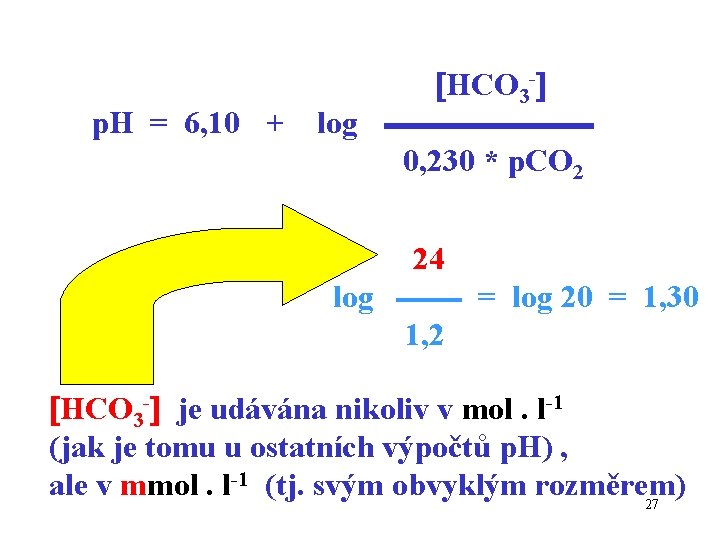
p. H = 6, 10 + log HCO 3 - 0, 230 * p. CO 2 24 log = log 20 = 1, 30 1, 2 HCO 3 - je udávána nikoliv v mol. l-1 (jak je tomu u ostatních výpočtů p. H) , ale v mmol. l-1 (tj. svým obvyklým rozměrem) 27
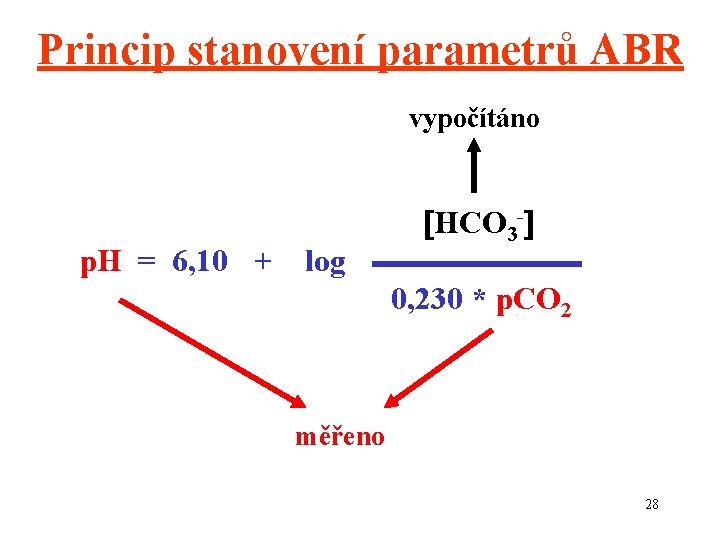
Princip stanovení parametrů ABR vypočítáno p. H = 6, 10 + log HCO 3 - 0, 230 * p. CO 2 měřeno 28

p. CO 2 a p. O 2 článek („elektroda“) METODY „PŘÍMÉHO MĚŘENÍ“ (nikoliv Astrupova metoda!) p. CO 2 silikonová membrána měří se změna p. H (kombinovaná skleněná a Ag /Ag. Cl elektroda v roztoku bikarbonátu) p. O 2 polypropylenová membrána kyslík redukován na O 22 - (vznik peroxidu, polarografický princip: měří se průchod el. proudu mezi Pt katodou a Ag / Ag. Cl anodou ve fosfátovém pufru) 29

PARAMETRY ABR 30

Základní parametry ABR: p. H = 7, 40 0, 05 p. CO 2 = 5, 33 0, 5 k. Pa BE 3 mmol. l-1 = 0 __________________________ BE = base excess [beis ik´ses] = „výchylka nárazníkových bazí“, „výchylka pufrových bazí“ - původní význam „nadbytek bazí“ zanikl spolu s pojmem 31 „base deficit“, BD

Parametry ABR: 1/ p. H je rozhodujícím parametrem metabolismus v buňkách je určen enzymy, které mají svoje p. H optima naše veškeré snahy o úpravu ABR musí směřovat k normalizaci p. H (~ 7, 40) 2/ p. CO 2 a BE jsou základními parametry informují o tom, jak bylo výsledného p. H dosaženo spolu s p. H umožňují posoudit typ poruchy ABR 3/ všechny ostatní parametry jsou pomocné - některé mohou být tzv. „aktuální“, jiné „korigované“ !! 32

Parametry ABR akt HCO 3 std BE = = = aktuální / standardní 24 3 mmol. l-1 0 3 mmol. l-1 (Za shodných podmínek [HCO 3 -] = 24 mmol. l-1 odpovídá hodnotě BE = 0 mmol. l-1 ) 33

Parametry ABR aktuální: „akt“ = aktuální tj. za daného stavu, který neodpovídá standardu Zjednodušeně: v praxi je to hodnota nějakého parametru ABR při p. CO 2 , které se odchyluje od své normální hodnoty (p. CO 2 5, 33 k. Pa !!) Některé standardní podmínky (p. O 2 a teplotu vzorku plné krve) zajišťuje při měření analyzátor. - Standardní způsob odběru a 34 zacházení se vzorkem musí být vždy striktně dodržen !!

Parametry ABR standardní: „std“ = standardní = korigované, vztahující se ke standardním podmínkám standardní podmínky: 1/ p. CO 2 = 5, 33 k. Pa (normální) 2/ p. O 2 (krev saturována kyslíkem) 3/ t = 37, 0 °C 4/ vzorek plné krve („anaerobní odběr“) 35

Parametry ABR korigované: jsou přepočítány pro normální p. CO 2 36

Doplňující údaje: • p. O 2 = 9 – 15 k. Pa (věková závislost) • saturace Hb kyslíkem = 0, 95 – 0, 98 • formy Hb nepřenášející kyslík 37

Dřívější údaje: BBb = buffer base (blood) 48 mmol. l-1 ´bafә beis blad souhrn konjugovaných pufrových bazí (plné krve) BBp = buffer base (plasma) 42 mmol. l-1 ´bafә beis plaezmә souhrn konjugovaných pufrových bazí (plazmy) 38
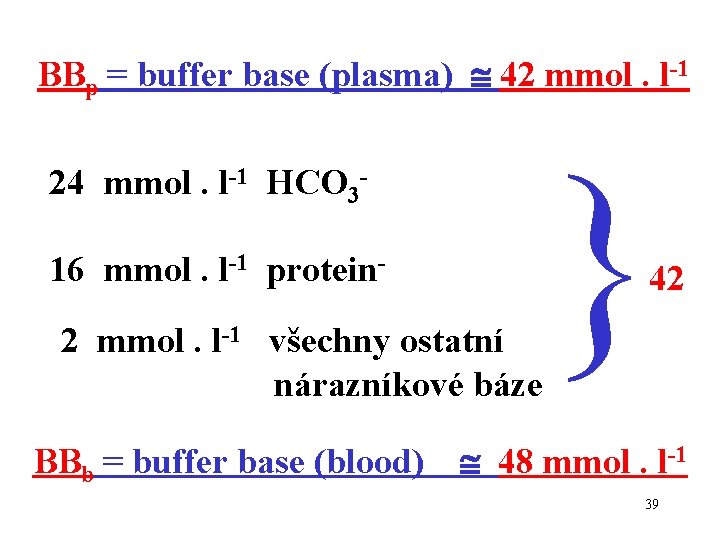
BBp = buffer base (plasma) 42 mmol. l-1 24 mmol. l-1 HCO 316 mmol. l-1 protein 2 mmol. l-1 všechny ostatní nárazníkové báze BBb = buffer base (blood) } 42 48 mmol. l-1 39

Hb - koncentrace a pufrová kapacita MHb = 64. 458 g. mol-1 ( 4 Fe) [Hb] = 140 g. l-1 140 / 64. 458 = 0, 002 17 mol. l-1 = 2, 2 mmol. l-1 Hb se chová jako vícesytná konjugovaná báze: má 38 His. Při p. H plazmy jsou karboxyly a aminoskupiny vedlejších řetězců plně ionizovány a nepufrují. Pufrová kapacita Hb je tak vytvářena imidazolovými jádry His. (K výpočtu podílu pufrové kapacity Hb v krvi je nutno znát hematokrit a event. i hustotu erytrocytů). 40
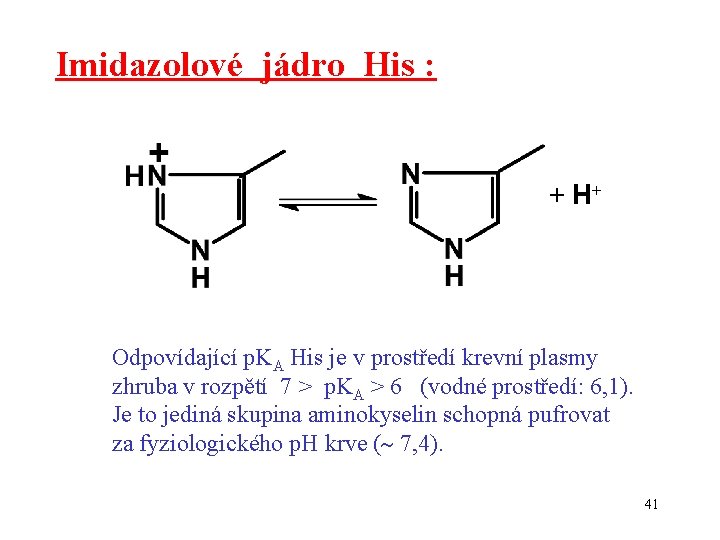
Imidazolové jádro His : + H+ Odpovídající p. KA His je v prostředí krevní plasmy zhruba v rozpětí 7 > p. KA > 6 (vodné prostředí: 6, 1). Je to jediná skupina aminokyselin schopná pufrovat za fyziologického p. H krve ( 7, 4). 41

Poznámka: Současné metody „přímého měření“ parametrů ABR neumožňují analyzátorům vyčíslit BBb a BBp (lze je však vypočítat doplněním některých dalších hodnot - [Hb], iontogramu *) ). Údaje BBb a BBp pocházejí z dob používání tzv. „ekvilibračních metod“ dle Astrupa (přibližně do konce 70. let, kdy byly uváděny mezi parametry ABR spolu s ostatními výsledky). Oba pojmy i dnes představují užitečnou informaci o pufračních vlastnostech krve resp. plasmy. *) BBp = [Na+] + [K+] - [Cl-] 42
nepřímá měření od 70. /80. let UŽ NE !! 43

Hydrogenuhličitan sodný („bikarbonát“) je zásaditý Na. HCO 3 + H 2 O H 2 CO 3 + Na+ + OH- (Kyselina uhličitá v elipse symbolizuje slabý, tedy prakticky nedisociovaný elektrolyt. Hydroxid sodný je silný, tj. téměř zcela disociovaný elektrolyt - ve vodném roztoku vzniká přebytek OH- iontů, podmíňující zásaditou reakci. ) 44
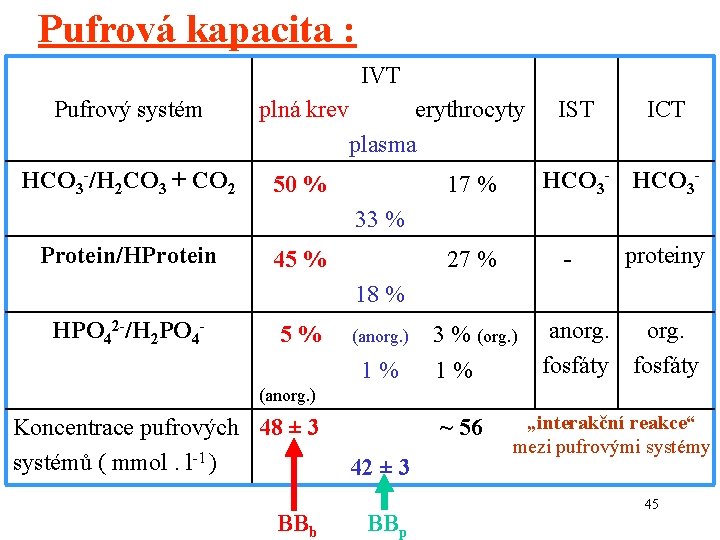
Pufrová kapacita : IVT Pufrový systém plná krev HCO 3 -/H 2 CO 3 + CO 2 50 % erythrocyty plasma IST ICT HCO 3 - 17 % 33 % Protein/HProtein 45 % - 27 % proteiny 18 % HPO 42 -/H 2 PO 4 - 5% (anorg. ) 1% 3 % (org. ) 1% anorg. fosfáty (anorg. ) Koncentrace pufrových 48 ± 3 systémů ( mmol. l-1 ) BBb ~ 56 42 ± 3 BBp „interakční reakce“ mezi pufrovými systémy 45

Poznámka Při posuzování podílu BBp (= 42 mmol. l-1) a pufrační kapacity erythrocytů ( 56 mmol. l-1) na BBb (tj. na celkové pufrační kapacitě krve) je nutno vzít v úvahu alespoň hematokrit ( 0, 45): 0, 45 objemu je pro erythrocyty, jejich podíl na BBb je: 56 · 0, 45 = 25, 2 25 mmol. l-1 0, 55 objemu je pro plasmu, její podíl na BBb je: 42 · 0, 55 = 23, 1 23 mmol. l-1 celkem ( BBb ) 48 mmol. l-1 46
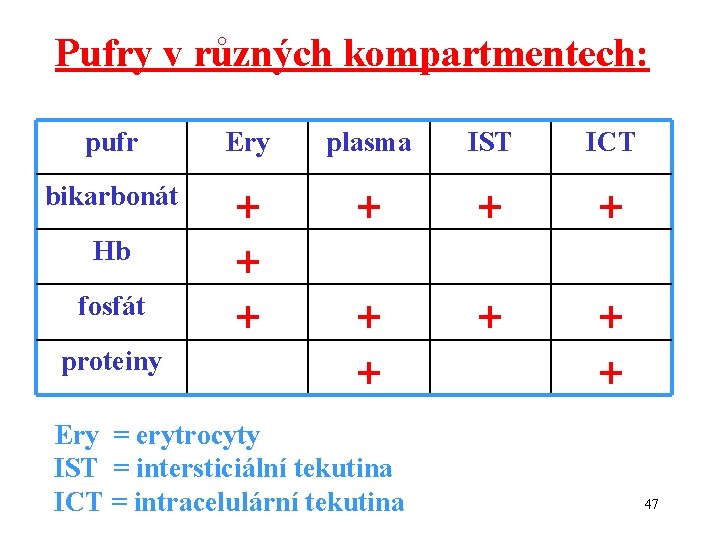
Pufry v různých kompartmentech: pufr Ery plasma IST ICT bikarbonát Hb fosfát proteiny Ery = erytrocyty IST = intersticiální tekutina ICT = intracelulární tekutina 47
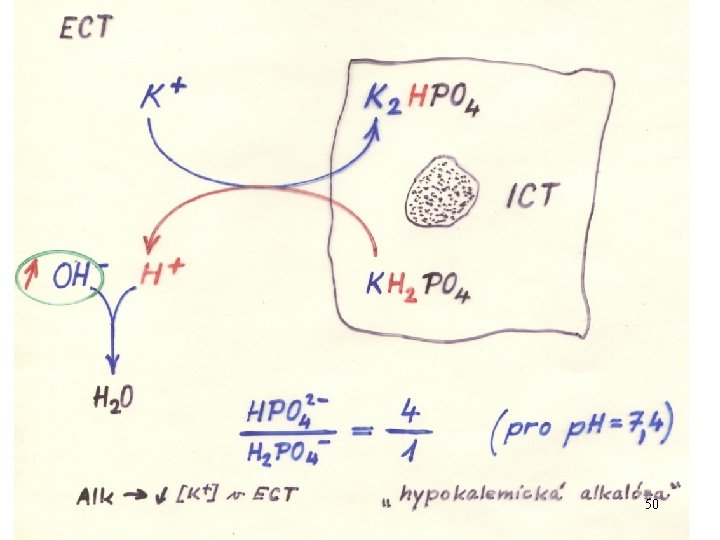
50

PORUCHY ABR 51
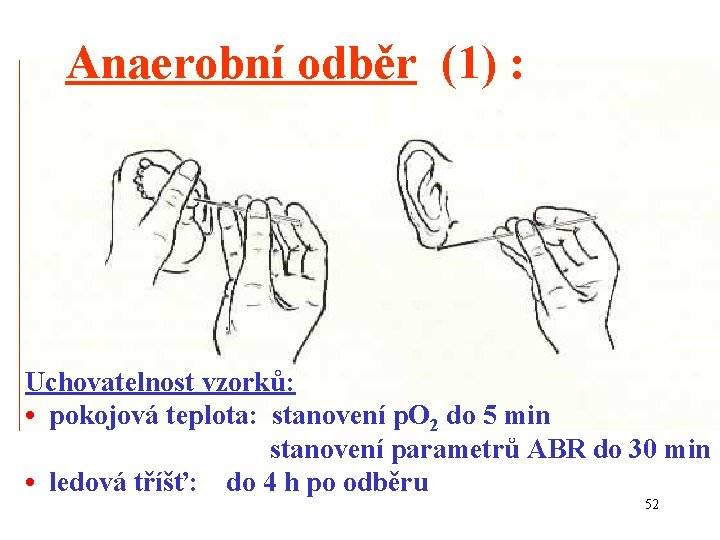
Anaerobní odběr (1) : Uchovatelnost vzorků: • pokojová teplota: stanovení p. O 2 do 5 min stanovení parametrů ABR do 30 min • ledová tříšť: do 4 h po odběru 52
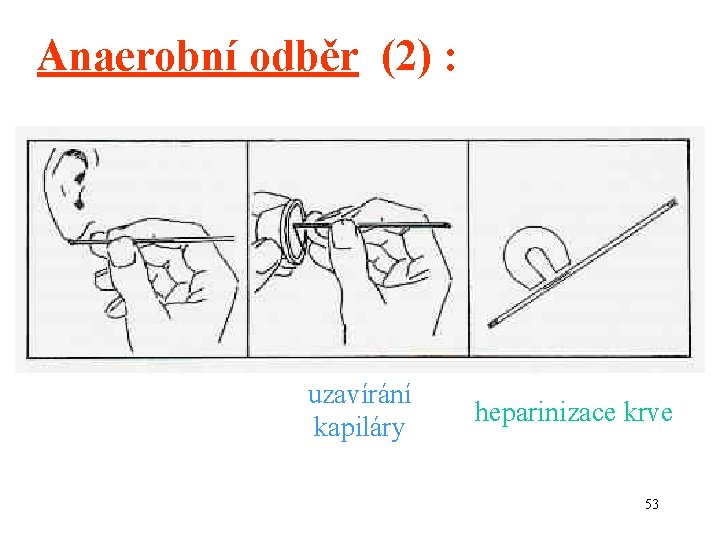
Anaerobní odběr (2) : uzavírání kapiláry heparinizace krve 53

Základní pojmy: odchylky od normálního p. H: acidémie (p. H 7, 36) alkalémie (p. H 7, 44) děje vyvolávající tyto odchylky: acidóza („Ac“) alkalóza („Alk“) respirační děj („R“): prvotní porucha je ve změně p. CO 2 metabolický děj („M“): prvotní porucha je ve změně [HCO 3 -] nebo [H+] 54
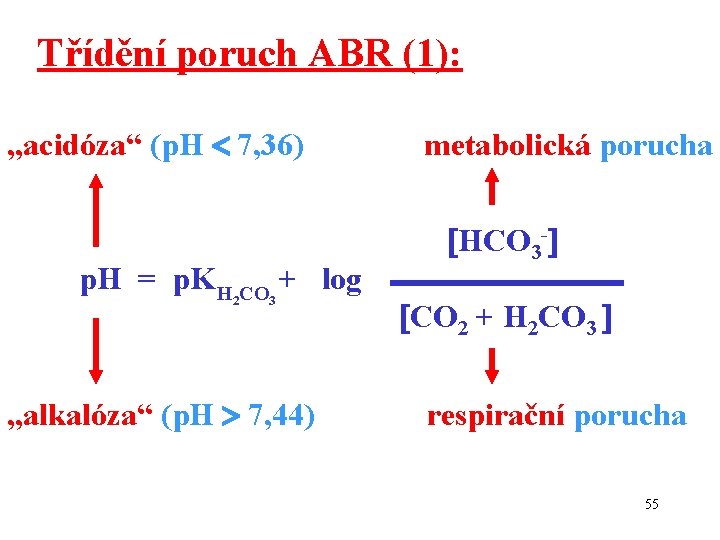
Třídění poruch ABR (1): „acidóza“ (p. H 7, 36) p. H = p. K H 2 CO 3 + log „alkalóza“ (p. H 7, 44) metabolická porucha HCO 3 - CO 2 + H 2 CO 3 respirační porucha 55

Třídění poruch ABR (2): - podle časového projevu: akutní (dekompenzované) ustálené (kompenzované) - zcela čisté metabolické poruchy nebo zcela čisté respirační poruchy (tj. izolované akutní poruchy) prakticky neexistují, protože kompenzační děje začínají téměř okamžitě, ale ustálení může trvat i několik dnů (v závislosti na typu poruchy) 57

Záznamový list acidobazické regulace souhrnné hodnocení (p. H, p. CO 2 a p. H)*) - dle Astrupa + Siggaard-Andersena [sigurd] *) 58 z toho pouze p. CO 2 je nezávisle proměnnou veličinou, rozhodující o stavu ABR
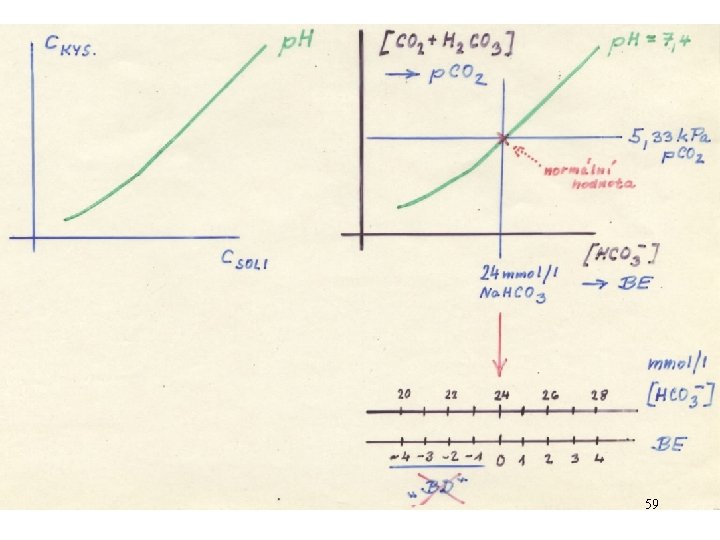
59
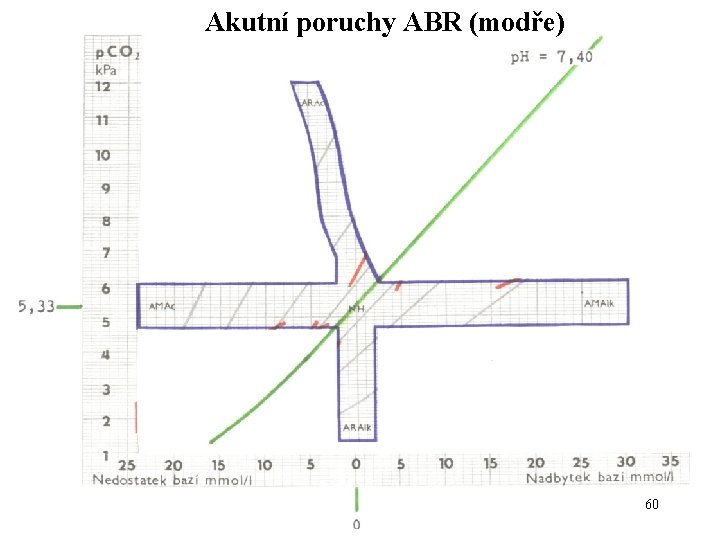
Akutní poruchy ABR (modře) 60
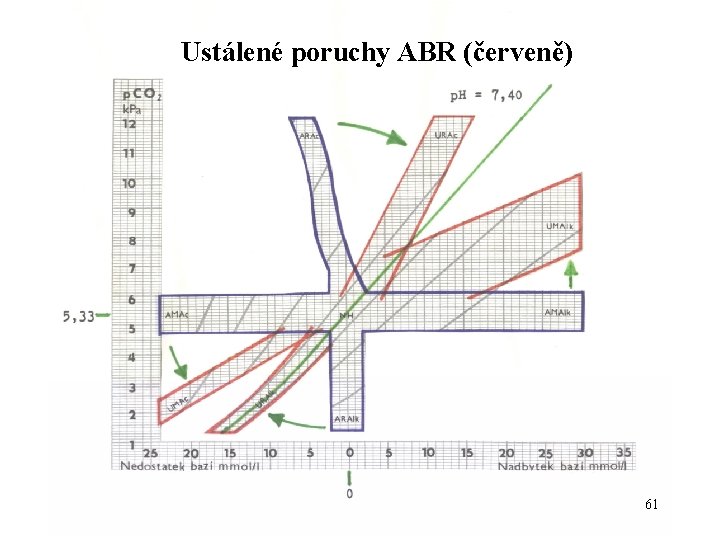
Ustálené poruchy ABR (červeně) 61
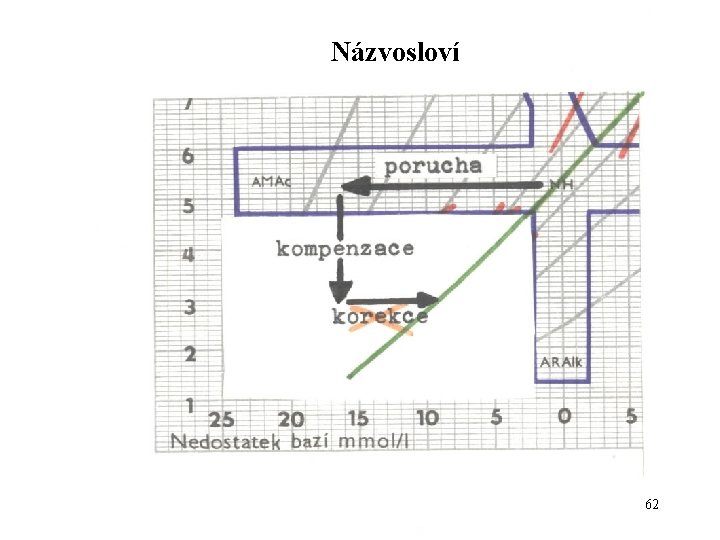
Názvosloví 62
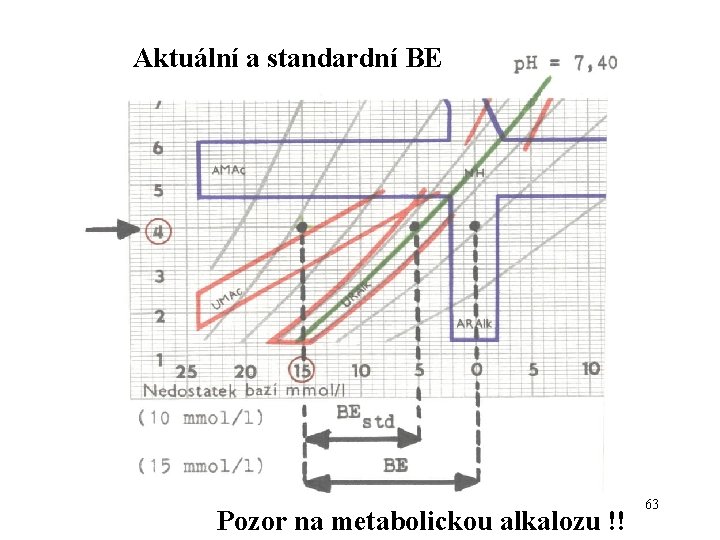
Aktuální a standardní BE Pozor na metabolickou alkalozu !! 63

Časové hledisko úpravy poruch ABR : „setrvačnost !!“ 64

Játra a ABR : 1/ acidemie: NH 3 glutamin (Gln) (transport do ledvin, uvolnění NH 4+ glutaminasou. . . ) 2/ alkalemie: NH 3 močovina 65
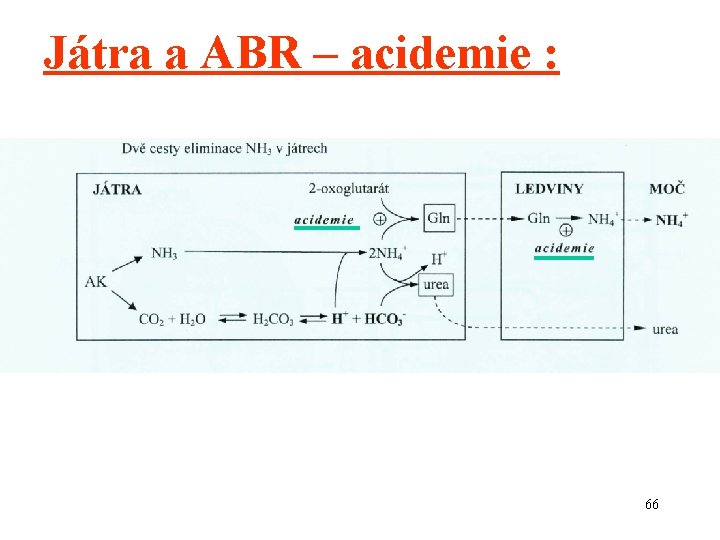
Játra a ABR – acidemie : 66

Játra a ABR - alkalemie (1) ( Naopak, za acidemie organismus (zásaditými) hydrogenuhličitany šetří: za acidemie bude tedy syntéza močoviny omezena. ) 67
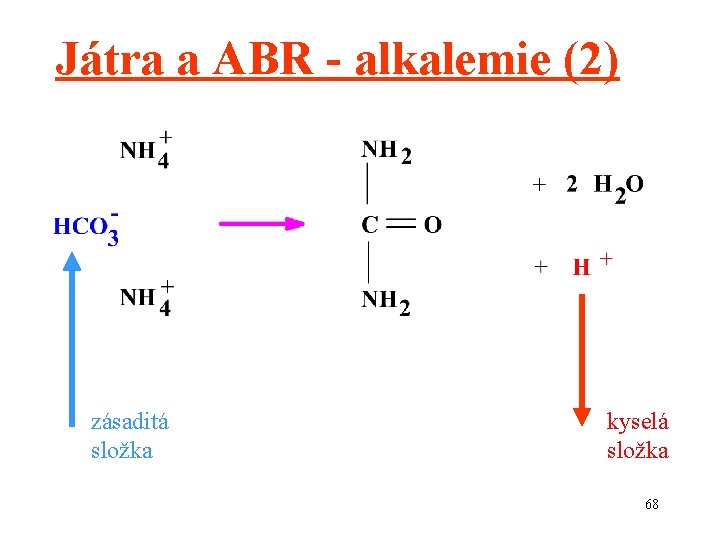
Játra a ABR - alkalemie (2) zásaditá složka kyselá složka 68
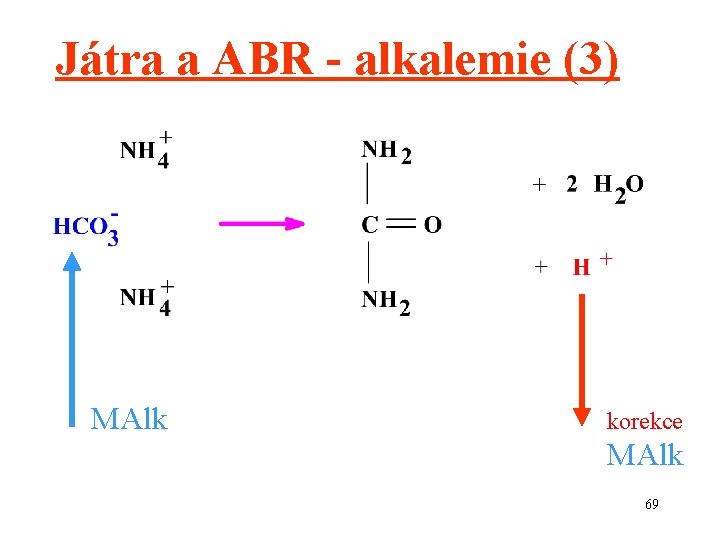
Játra a ABR - alkalemie (3) MAlk korekce MAlk 69
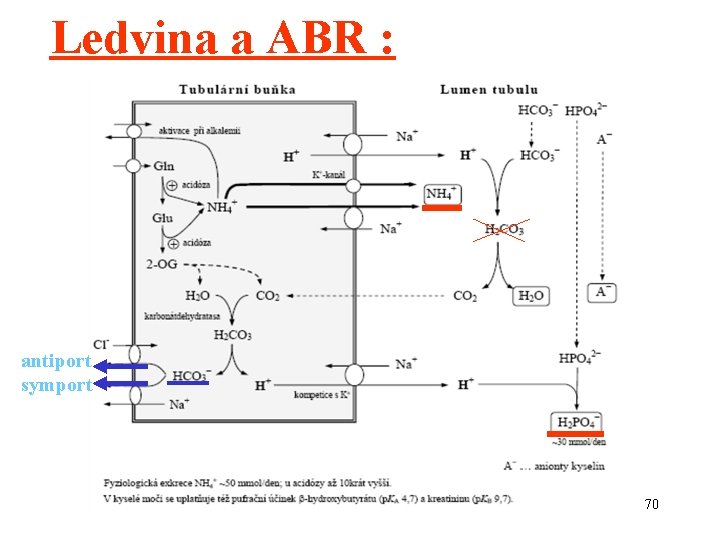
Ledvina a ABR : antiport symport 70
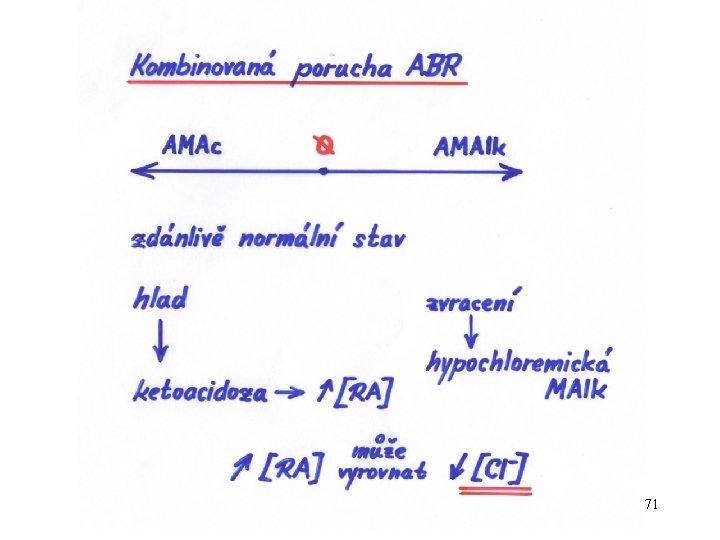
71
![Parametry ABR a ionty Stanovení parametrů ABR zpravidla vždy doplňujeme stanovením koncentrace iontů: [Na+] Parametry ABR a ionty Stanovení parametrů ABR zpravidla vždy doplňujeme stanovením koncentrace iontů: [Na+]](http://slidetodoc.com/presentation_image/60ab6abebc203af62144ea5bab71f43b/image-64.jpg)
Parametry ABR a ionty Stanovení parametrů ABR zpravidla vždy doplňujeme stanovením koncentrace iontů: [Na+] [K+] [Cl-] (~ 140 mmol. l-1 ) (~ 4, 4 mmol. l-1 ) (~ 100 mmol. l-1 ) Odchylka chloridů od normy má základní význam pro rozpoznání kombinované poruchy ABR. Dokonalejší systém představuje rozšířené hodnocení dle Stewarta a Fencla (uveden je jednoduchý postup bez počítače) 72

ZDOKONALENÉ HODNOCENÍ KOMBINOVANÝCH PORUCH ABR (dle Stewarta a Fencla) 73

Nezávisle proměnné veličiny určující stav ABR : p. CO 2 SID netěkavé slabé kyseliny = [Alb-] + [Pi-] Závisle proměnné veličiny určující stav ABR : p. H , [H+] [HCO 3 -] , BE 76
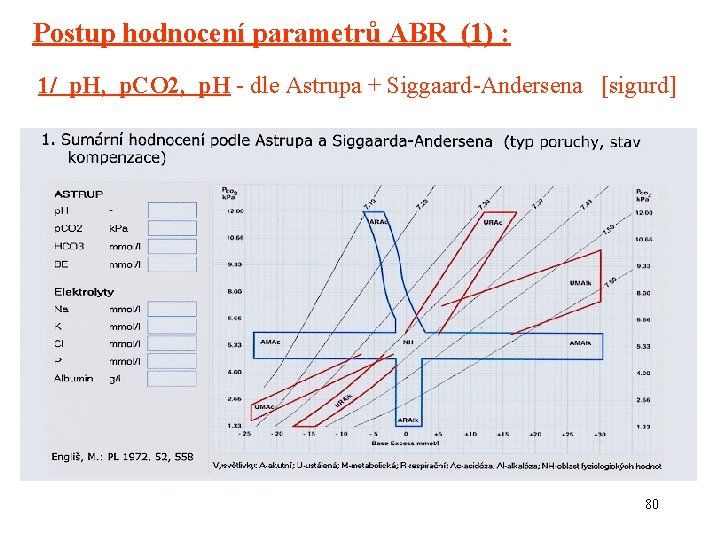
Postup hodnocení parametrů ABR (1) : 1/ p. H, p. CO 2, p. H - dle Astrupa + Siggaard-Andersena [sigurd] 80
![Referenční hodnoty : mmol. l-1 [Na+] [Cl-]korig 140 100 [UA-]korig 8 [Pi-] [Alb-] 2 Referenční hodnoty : mmol. l-1 [Na+] [Cl-]korig 140 100 [UA-]korig 8 [Pi-] [Alb-] 2](http://slidetodoc.com/presentation_image/60ab6abebc203af62144ea5bab71f43b/image-68.jpg)
Referenční hodnoty : mmol. l-1 [Na+] [Cl-]korig 140 100 [UA-]korig 8 [Pi-] [Alb-] 2 12 83

Hodnocení pacienta (1) : odchylky koncentrací jednotlivých ukazatelů od referenčních hodnot zařadíme do sloupců acidóza / alkalóza (dle svých znamének: „+“ pro zvýšení, „ “ pro snížení) mmol. l-1 acidóza alkalóza [Na+] [Cl-]korig 140 100 + + [UA-]korig 8 + [Pi-] [Alb-] 2 12 + + 84
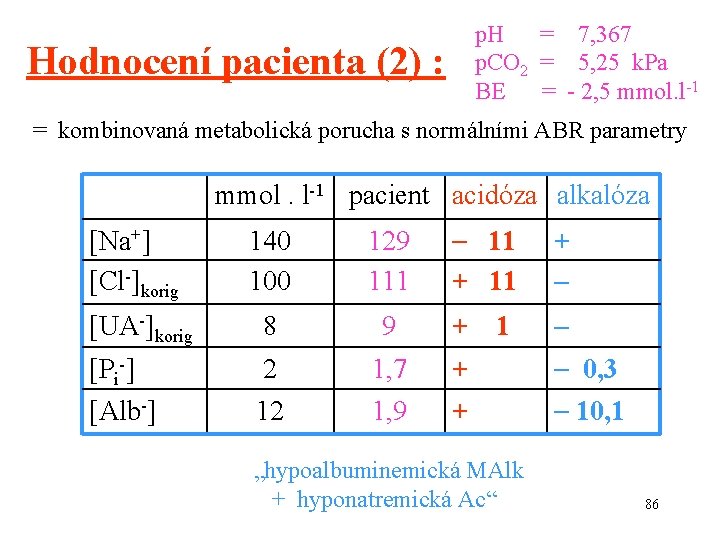
p. H = 7, 367 p. CO 2 = 5, 25 k. Pa BE = - 2, 5 mmol. l-1 Hodnocení pacienta (2) : = kombinovaná metabolická porucha s normálními ABR parametry mmol. l-1 pacient acidóza alkalóza 11 + 9 + 1, 7 1, 9 + + [Na+] [Cl-]korig 140 100 129 111 [UA-]korig 8 [Pi-] [Alb-] 2 12 1 „hypoalbuminemická MAlk + hyponatremická Ac“ 0, 3 10, 1 86

Proč „hypoalbuminemická MAlk + hyponatremická Ac“ ? hypoalbuminémie = úbytek jedné z „netěkavých slabých kyselin“ úbytek je obvykle pokryt zvýšením koncentrace (alkalického) hydrogenuhličitanu MAlk hyponatrémie = důsledek zředění (diluce) jsou zředěny pufrační systémy snížila se pufrační kapacita vztažená na objem neustálá metabolická produkce kyselin MAc (hyponatremická Ac = diluční Ac) 87

Co je obsahem jednotlivých údajů odvozených z iontogramu plazmy ? SID = [HCO 3 -] + [Alb-] + [Pi-] „netěkavé slabé kyseliny“ AG = [UA-] + [Alb-] + [Pi-] „netěkavé slabé kyseliny“ [UA-] anionty (převážně) org. kyselin, zcela disociované 88
![[UA-] anionty (převážně) org. kyselin, zcela disociované hypoxie laktát ketoacidóza acetoacetát β-hydroxybutyrát ledvinová insuficience [UA-] anionty (převážně) org. kyselin, zcela disociované hypoxie laktát ketoacidóza acetoacetát β-hydroxybutyrát ledvinová insuficience](http://slidetodoc.com/presentation_image/60ab6abebc203af62144ea5bab71f43b/image-73.jpg)
[UA-] anionty (převážně) org. kyselin, zcela disociované hypoxie laktát ketoacidóza acetoacetát β-hydroxybutyrát ledvinová insuficience sulfát intoxikace formiát salicylát …. . 89

94
- Slides: 74